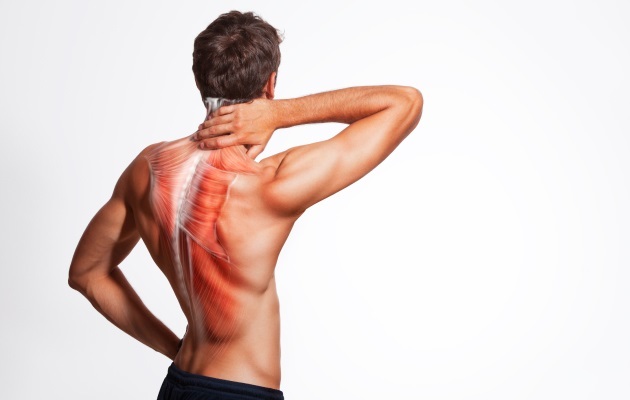
Дефанс паравертебральных мышц что это
Мышечно-тонический синдром
Специалисты реабилитационного центра “Лаборатория движения” помогут в восстановлении функций опорно-двигательного аппарата
Самым частым проявлением дегенеративных патологий позвоночника является мышечно тонический синдром. Длительное и стойкое напряжение мышц, отвечающих за поддержание стабильности позвоночных сегментов, приводит к формированию болезненных «триггерных точек». И только комплексное лечение, направленное на оптимизацию различных звеньев двигательной системы, позволяет существенно облегчить состояние пациента.
Рассказывает специалист ЦМРТ
Дата публикации: 29 Июня 2021 года
Дата проверки: 30 Ноября 2021 года
Содержание статьи
Причины мышечно-тонических болевых синдромов
Чрезмерные статические нагрузки и микротравмирование позвоночных структур влечет за собой рефлекторное напряжение мышц, ограничение их подвижности и формирование неоптимального двигательного стереотипа. Основной причиной мышечно-тонического синдрома являются дегенеративно-дистрофические заболевания позвоночника (остеохондроз, межпозвонковые грыжи) и нарушения осанки, связанные с врожденными аномалиями развития и деформацией спинного хребта.
Спровоцировать болезненный мышечный спазм может:
Под воздействием провоцирующих факторов в мышцах происходят биохимические процессы с выделением медиаторов воспаления, вызывающих рефлекторное сокращение мышц.
Симптомы мышечно-тонического синдрома
Основным признаком миотонического синдрома являются глубокие ноющие вертеброгенные боли. Болезненные спазмы, сопровождающиеся уплотнением и отечностью одной или нескольких мышц, существенно ограничивают подвижность. Из-за взаимодействия с нервными рецепторами развивается стойкая болезненность. Та, в свою очередь, усиливает сокращение мышц и замыкает порочный круг: спазм – отек – боль – спазм.
Мышечно-тонический синдром пояснично-крестцового отдела чаще всего становится следствием тяжелых физических нагрузок. Напряжение грушевидной мышцы может повлечь за собой боль в области ягодицы, тазобедренного сустава. В случае сдавливания седалищного нерва возможно онемение одной из конечностей.
Мышечно-тонический синдром шейного отдела проявляется цервикальными болями, болевыми ощущениями в шее, усиливающимися при разгибании и поворотах головы, гиперстезией 4-го и 5-го пальцев руки.
Для мышечно-тонического синдрома грудного отдела характерна болезненность между лопаток и по ходу ребер. Иногда может наблюдаться ощущение жжения и сдавленности в груди, имитирующих проявления сердечных проблем.
Классификация мышечно-тонических синдромов
Существует несколько разновидностей мышечно-тонических болевых синдромов. Они классифицируются в зависимости от локализации:
Помимо вышеперечисленных, патологическим изменениям нередко подвергается трапециевидная, широчайшая грудная, квадратная мышца поясницы, подниматель лопатки. Болевой синдром может быть первичным (охватывающим только спазмированные ткани) и вторичным, локализованным вне зоны повреждения.
Диагностика
Комплекс диагностических мероприятий включает:
Самым информативным, безопасным и безболезненным методом нейровизуализации признана магнитно-резонансная томография. Она дает максимально точную оценку состоянию позвоночника и спинного мозга, позволяет выявить протрузии и межпозвонковые грыжи, определить их размеры и локализацию.
Дегенеративные изменения позвоночника
Специалисты ЦМРТ более 15 лет специализируются на диагностике и лечении заболеваний позвоночника. Читайте подробнее на странице Лечение позвоночника.
Дегенеративно-дистрофические заболевания позвоночника проявляются структурными и функциональными изменениями системы элементов позвоночных двигательных сегментов. В процесс могут быть вовлечены межпозвонковые диски, концевые пластины, фасеточные суставы, а в запущенных стадиях — позвоночный канал и спинной мозг. Симптомы вариативны, зависят от локализации, стадии заболевания. Диагностика подразумевает проведение КТ, МРТ. Лечение консервативное, в сложных случаях при деструкции позвонков, образовании грыж — оперативное.
Рассказывает специалист ЦМРТ
Дата публикации: 19 Мая 2021 года
Дата проверки: 30 Ноября 2021 года
Содержание статьи
Причины дегенеративных изменений позвоночника
Дегенеративно-дистрофические изменения позвоночного столба всегда вторичны и являются реакцией на механическую травму или нарушение обмена веществ. Дистрофия позвоночника может быть вызвана метаболическими причинами:
Симптомы дегенеративных изменений позвоночника
Клинические проявления поражения позвоночно-двигательных сегментов многообразны, зависят от отдела позвоночника, вовлечения нервно-сосудистых пучков. Симптомы включают:
Стадии развития дегенеративных изменений позвоночника
Остеохондроз — наиболее часто встречающаяся форма дегенеративного поражения позвоночного столба. На начальной стадии болезни изменения развиваются в пульпозном ядре. Структура утрачивает эластичность, теряет воду, что приводит к травматизации гиалиновых пластинок и прилегающих участков тел позвонков. По мере прогрессирования дегенерации появляются трещины, разрывы пластинок (узелки Шморля) и фиброзного кольца (протрузии и грыжи дисков). Другие компоненты — тела позвонков, связки, суставы — со временем вовлекаются в процесс с развитием остеосклероза.
Суставные поверхности смещаются, постепенно появляются подвывихи фасеточных суставов — остеоартроз (реберно-поясничный артроз). Дистрофические изменения в телах позвонков и последующее разрушение в терминальной стадии заболевания инициируют искривление позвоночного столба, стеноз канала.
Как диагностировать
После оценки жалоб и анамнеза дегенеративные изменения позвоночника подтверждают с помощью тестов визуализации, проводят:
Компьютерную томографию. КТ показывает патологию костных структур:
Магнитно-резонансное сканирование. МРТ визуализирует изменения мягких тканей и помогает обнаруживать:
Нейромиографию. НМГ назначают для исключения неврологической природы симптомов
БОЛИ В СПИНЕ: болезненный мышечный спазм и его лечение миорелаксантами
Боли в спине — одна из наиболее распространенных жалоб, которые пациенты предъявляют в общемедицинской практике. Часто они вызываются остеохондрозом позвоночника — дегенеративным поражением хряща межпозвонкового диска и реактивными изменениями со стороны
Боли в спине — одна из наиболее распространенных жалоб, которые пациенты предъявляют в общемедицинской практике. Часто они вызываются остеохондрозом позвоночника — дегенеративным поражением хряща межпозвонкового диска и реактивными изменениями со стороны тел смежных позвонков. Поражение межпозвонкового диска развивается вследствие его повторных травм (подъем тяжести, избыточная статическая и динамическая нагрузка, падения и др.) и возрастных дегенеративных изменений. Студенистое ядро, центральная часть диска, высыхает и частично утрачивает амортизирующую функцию. Фиброзное кольцо, расположенное по периферии диска, истончается, в нем образуются трещины, к которым смещается студенистое ядро, образуя выпячивание (пролапс), а при разрыве фиброзного кольца — грыжу. В настоящее время созданы препараты, оказывающие структурно-модифицирующее действие на хрящевую ткань (старое название — хондропротекторы). Типичным представителем группы является препарат хондро, назначаемый курсом по 4 месяца (эффект сохраняется 2 месяца после отмены). В пораженном позвоночном сегменте возникает относительная нестабильность позвоночника, развиваются остеофиты тел позвонков (спондилез), повреждаются связки и межпозвонковые суставы (спондилоартроз). Грыжи межпозвонковых дисков наиболее часто наблюдаются в нижних поясничных дисках, реже — в нижних шейных и верхних поясничных, крайне редко — в грудных. Грыжи диска в тело позвонка (грыжи Шморля) клинически не значимы, грыжи диска в заднем и заднебоковом направлении могут вызвать сдавление спинно-мозгового корешка (радикулопатию), спинного мозга (миелопатию на шейном уровне) или их сосудов.
Кроме компрессионных синдромов возможны рефлекторные (мышечно-тонические), которые обусловлены импульсацией из рецепторов в ответ на изменения в дисках, связках и суставах позвоночника — болезненный мышечный спазм. Рефлекторное напряжение мышц вначале имеет защитный характер, поскольку приводит к иммобилизации пораженного сегмента, однако в дальнейшем этот фактор становиться причиной возникновения боли. В отличие от компрессионных синдромов остеохондроза позвоночника, которые встречаются относительно редко, болевые мышечные спазмы возникают в течение жизни практически у каждого второго человека.
Классический пример болезненного мышечного спазма представляет люмбаго (поясничный прострел), который характеризуется резкой, простреливающей болью в пояснице, развивающейся, как правило, при физической нагрузке (подъем тяжести и др.) или неловком движении. Больной нередко застывает в неудобном положении, попытка движения приводит к усилению боли. При обследовании выявляют напряжение мышц спины, обычно сколиоз, уплощение поясничного лордоза или кифоз.
Люмбалгия — боль в спине — и люмбоишиалгия — боль в спине и по задней поверхности ноги — развиваются чаще после физической нагрузки, неловкого движения или переохлаждения, реже — без каких-либо причин. Боли носят ноющий характер, усиливаются при движениях в позвоночнике, определенных позах, ходьбе. Для люмбоишиалгии характерна боль в ягодице, в задненаружных отделах ноги, не достигающая пальцев. При обследовании выявляют болезненность, напряжение мышц спины и задней группы мышц ноги, ограничение подвижности позвоночника, часто сколиоз, симптомы натяжения (Ласега, Вассермана и др.).
На шейном уровне могут возникать рефлекторные мышечно-тонические синдромы: цервикалгия и цервикобрахиалгия, которые чаще развиваются после физической нагрузки или неловкого движения шеи. Цервикалгия — боль в шейной области, которая нередко распространяется на затылок (цервикокраниалгия). Цервикобрахиалгия — боль в шейной области, распространяющаяся на руку. Характерно усиление болей при движениях в шее или, наоборот, при длительном статическом положении (в кино, после сна на плотной высокой подушке и др.). При обследовании выявляют напряжение шейных мышц, часто наблюдается ограничение движений в шейном отделе, болезненность при пальпации остистых отростков и межпозвонковых суставов на стороне боли.
При компрессии нервного корешка (радикулопатии) кроме болезненного мышечного спазма и ограничений подвижности в позвоночнике и конечностях выявляются чувствительные, рефлекторные и (или) двигательные нарушения в зоне пораженного корешка. На поясничном уровне чаще поражаются пятый поясничный (L5) и первый крестцовый (S1) корешки, реже — четвертый поясничный корешок и очень редко — верхние поясничные корешки. Радикулопатии нижних шейных корешков встречаются значительно реже.
Важно помнить, что боли в спине могут быть единственным симптомом при опухоли спинного мозга, сирингомиелии и других заболеваниях спинного мозга. Боли возникают при деструкции позвонков и поражении нервных корешков вследствие инфекционных процессов (туберкулезный спондилит, спинальный эпидуральный абсцесс), новообразованиях (первичные и метастатические опухоли позвоночника, миеломная болезнь), дисметаболических нарушениях (остеопороз, гиперпаратиреоз, болезнь Педжета). Боль в спине может быть следствием перелома позвоночника, его врожденных или приобретенных деформаций (сколиоза и др.), стеноза позвоночного канала, спондилолистеза, анкилозирующего спондилоартрита.
Она возможна при различных соматических заболеваниях (сердца, желудка, поджелудочной железы, почек, органов малого таза и др.) по механизму отраженных болей.
Обследование пациента с болью в спине требует тщательности. Нельзя любые боли в спине списывать на «остеохондроз» — состояние, которое при рентгенологическом исследовании выявляется у большинства людей среднего и пожилого возраста. Для неврологических проявлений остеохондроза позвоночника и миофасциальных болей характерны болезненный мышечный спазм и ограничение подвижности позвоночника.
Диагноз рефлекторных и компрессионных осложнений остеохондроза основывается на клинических данных и требует исключения других возможных причин болей в спине. Рентгенографию позвоночника используют, в основном, для исключения врожденных аномалий и деформаций, воспалительных заболеваний (спондилитов), первичных и метастатических опухолей. Рентгеновская КТ или МРТ позволяет выявить грыжу диска, определить ее размеры и локализацию, а также обнаружить стеноз позвоночного канала, опухоль спинного мозга.
Диагноз миофасциальных болей основывается на клинических данных (выявление болезненного мышечного напряжения одной или нескольких мышц) и требует исключения других возможных причин боли; дифференциальный диагноз с рефлекторными синдромами (мышечно-тоническими синдромами) вследствие остеохондроза позвоночника часто вызывает сложности; возможно сочетание этих заболеваний.
Лечение рефлекторных синдромов и радикулопатий вследствие остеохондроза основывается в остром периоде на обеспечении покоя — больному рекомендуется избегать резких наклонов и болезненных поз. Предписаны постельный режим в течение нескольких дней до стихания резких болей, жесткая постель (щит под матрац), прием миорелаксантов центрального действия, при необходимости — также дополнительно анальгетиков, нестероидных противовоспалительных средств. Для облегчения передвижения в этот период следует надеть шейный или поясничный корсет (фиксирующий пояс). Можно использовать физиотерапевтические анальгезирующие процедуры, втирание обезболивающих мазей, компрессы с 30–50-процентным раствором димексида и новокаином, новокаиновые и гидрокортизоновые блокады. При ослаблении болей рекомендуют постепенное увеличение двигательной активности и упражнения на укрепление мышц.
При хроническом течении рефлекторных синдромов и радикулопатий могут быть эффективны мануальная терапия, рефлексотерапия, физиотерапевтическое лечение, санаторно-курортное лечение. Хирургическое лечение (удаление грыжи диска) необходимо в тех редких случаях, когда возникает сдавление спинного мозга или корешков конского хвоста. Хирургическое лечение также показано при дискогенной радикулопатии, сопровождающейся выраженным парезом, и при длительном (более трех-четырех месяцев) отсутствии эффекта от консервативного лечения и наличии большой грыжи диска. Для профилактики обострений остеохондроза рекомендуют избегать провоцирующих факторов (подъем больших грузов, ношение тяжелой сумки в одной руке, переохлаждение и др.), регулярно заниматься лечебной гимнастикой.
При миофасциальных болях необходимо, чтобы мышца находилась в покое в течение нескольких дней. В качестве лечения можно назначать упражнения на растяжение мышц (постизометрическая релаксация), физиотерапию, рефлексотерапию или местное введение анестетиков в триггерные зоны, компрессы с димексидом и анестетиками.
Как уже было отмечено, и при острых болях, и при хронических болевых синдромах большое значение имеет лечение болезненного мышечного спазма. Тоническое напряжение мышц может не только само по себе быть причиной боли, но и способно вызвать деформацию и ограничивать подвижность позвоночника, а также обуславливать компрессию проходящих вблизи нервных стволов и сосудов. Для его лечения помимо нестероидных противовоспалительных средств, анальгетиков, (например, нимулид в форме трансдермального геля для местной терапии или в форме лингвальных таблеток при остром болевом синдроме), физиотерапии и лечебной гимнастики в качестве препаратов первого ряда применяют миорелаксанты — препараты, способные разорвать «порочный круг» болевого синдрома [2].
Для лечения болезненного мышечного спазма миорелаксанты используются внутрь или парентерально. Снижая рефлекторное мышечное напряжение, миорелаксанты уменьшают боль, улучшают двигательные функции и облегчают проведение лечебной физкультуры. Лечение миорелаксантами начинают с обычной терапевтической дозы и продолжают до тех пор, пока сохраняется болевой синдром; как правило, курс лечения составляет несколько недель. В ходе целого ряда исследований удалось доказать, что при болезненном мышечном спазме добавление к стандартной терапии (нестероидные противовоспалительные средства, анальгетики, физиотерапия, лечебная гимнастика) миорелаксантов приводит к более быстрому регрессу боли, мышечного напряжения и улучшению подвижности позвоночника.
В качестве миорелаксантов применяются мидокалм, баклофен и сирдалуд. Миорелаксанты обычно не комбинируют друг с другом. Для снятия болезненных мышечных спазмов можно также использовать диазепам (седуксен, реланиум) в индивидульно подобранной дозе.
Сирдалуд (тизанидин) — агонист α-2 адренергических рецепторов. Препарат снижает мышечный тонус вследствие подавления полисинаптических рефлексов на уровне спинного мозга, что может быть вызвано угнетением высвобождения возбуждающих аминокислот и активацией глицина, снижающего возбудимость интернейронов спинного мозга; сирдалуд обладает также умеренным центральным анальгезирующим действием. При приеме внутрь максимальная концентрация сирдалуда в крови достигается через час, прием пищи не влияет на его фармакокинетику. Начальная доза препарата составляет 6 мг в сутки в три приема, средняя терапевтическая доза — 12—24 мг в сутки, максимальная доза — 36 мг в сутки. В качестве побочных эффектов отмечаются сонливость, головокружение, незначительное снижение артериального давления; требуется осторожность при приеме препарата больными пожилого возраста.
Мидокалм (толперизон) в течение длительного времени широко используется при лечении рефлекторных и компрессионных осложнений дегенеративно-дистрофических изменений позвоночника (остеохондроз, спондилез, спондилоартроз) и миофасциальных болей [3]. Мидокалм оказывает преимущественно центральное миорелаксирующее действие. Снижение мышечного тонуса при приеме препарата связывается с угнетающим влиянием на каудальную часть ретикулярной фармации и подавлением спинно-мозговой рефлекторной активности. Препарат обладает умеренным центральным анальгезирующим действием и легким сосудорасширяющим влиянием. Прием мидокалма начинают с 150 мг в сутки три раза в день, постепенно увеличивая дозу до получения эффекта, у взрослых обычно до 300—450 мг в сутки. Для быстрого эффекта препарат вводится внутримышечно по 1 мл (100 мг) два раза в сутки или внутривенно по 1 мл один раз в сутки.
Эффективность и безопасность применения мидокалма при болезненном мышечном спазме доказана в ходе двойного слепого плацебо-контролируемого исследования [4]. В восьми исследовательских центрах 110 больных в возрасте от 20 до 75 лет методом рандомизации получали мидокалм в дозе 300 мг в сутки или плацебо в сочетании с физиотерапией и реабилитацией в течение 21 дня. В качестве объективного критерия эффективности лечения рассматривают болевой порог давления, измеряемый с помощью специального прибора (Pressure Tolerance Meter) в 16 симметричных точек туловища и конечностей. Кроме того, пациенты субъективно оценивали свое состояние по интенсивности боли, ощущению напряжения мышц и подвижности позвоночника; врач также оценивал напряжение мышц и подвижность позвоночника. Перед началом лечения и после его окончания проводилось развернутое клиническое и лабораторное обследование, включая ЭКГ, измерение артериального давления, биохимический анализ крови по 16 показателям.
Согласно результатам исследований, применение мидокалма достоверно снижает болезненный мышечный спазм, измеряемый объективно инструментальным методом. Различие между группами лечения и плацебо, которое отмечалось уже на четвертый день, постепенно увеличивалось и становилось статистически достоверным на 10-й и 21-й дни лечения, которые были выбраны в качестве конечных точек для доказательного сравнения. Анализ субъективной оценке результатов лечения, данной врачами и пациентами после его окончания (через 21 день), показал, что в группе больных, получавших мидокалм, достоверно чаще результаты лечения оценивались как очень хорошие, тогда как в группе плацебо эффект существенно чаще отсутствовал. Согласно субъективной оценке результатов лечения, данной больными после его окончания (через 21 день), каких-либо значимых различий, касающихся переносимости мидокалма и плацебо, выявлено не было. У подавляющего большинства больных отмечалась хорошая переносимость мидокалма. Результаты ЭКГ, биохимические и гематологические показатели в группе пациентов, принимавших как мидокалм, так и плацебо, также не различались.
Важно отметить, что более половины (62%) пациентов, включенных в исследование, получали другие виды терапии до начала исследования, и у большинства из них (68%) при этом не отмечалось улучшения. Это свидетельствует об эффективности мидокалма в лечении болезненного мышечного спазма, резистентного к другим видам терапии.
Введение мидокалма парентерально позволяет быстро снять боль и уменьшить мышечное напряжение. При вертеброгенном мышечно-тоническом синдроме внутримышечное введение 100 мг мидокалма ослабляет боль уже через 1,5 ч, а лечение мидокалмом в течение недели по 200 мг/сут в/м, а затем на протяжении двух недель по 450 мг/сут перорально имеет достоверное преимущество над стандартной терапией; при этом терапия мидокалмом не только позволяет уменьшить боль, но и снимает тревожность, повышает умственную работоспособность [1].
При болезненном мышечном спазме достоинствами мидокалма помимо эффективного миорелаксирующего и обезболивающиего эффекта являются отсутствие побочных эффектов и хорошее взаимодействие с нестероидными противовоспалительными средствами, что во многих случаях позволяет уменьшить дозу последних и вследствие этого ослабить или даже полностью устранить их побочные эффекты, не снижая эффективности лечения.
Важным преимуществом мидокалма перед другими миорелаксантами является отсутствие седативного эффекта и мышечной слабости при его приеме. Это преимущество доказано в ходе двойного слепого плацебо-контролируемого исследования [5]. В исследовании вошли 72 здоровых добровольца в возрасте от 19 до 27 лет (средний возраст — 21,7 лет). Исследование проводилось в течение восьми дней, все это время добровольцы методом рандомизации получали 150 или 450 мг мидокалма в сутки в три приема либо плацебо — также в три приема. Нейропсихологические исследования осуществляются утром в первый и последний (восьмой) дни исследования до и после приема мидокалма через 1,5, 4 и 6 ч либо плацебо. Результаты исследования не показали каких-либо существенных различий в скорости сенсомоторных реакций и быстроте выполнения различных психологических тестов через 1,5, 4 и 6 ч после приема мидокалма в дозе 50 или 150 мг либо плацебо. Аналогичные исследования, проведенные на восьмой день с начала приема мидокалма, также не показали существенных различий в сравнении с группой плацебо. Это свидетельствует о хорошей переносимости мидокалма и возможности назначения его в тех случаях, когда по роду деятельности пациенту требуется сохранить быстроту реакций и способность концентрировать внимание, в том числе при вождении автомобиля.
Таким образом, болезненный мышечный спазм представляет собой одну из наиболее распространенных причин болей в спине (вследствие рефлекторных синдромов остеохондроза или миофасциальных болей). В таких случаях рекомендуется применение миорелаксантов в комбинации с различными лекарственными средствами, физиотерапией и лечебной гимнастикой. В последние годы доказана эффективность и безопасность миорелаксанта мидокалма, который не вызывает седативного эффекта и выпускается в форме для парентерального введения с целью быстрого купирования болевого синдрома.
Литература.
В. А. Парфенов, доктор медицинских наук, профессор ММА им. И. М. Сеченова
Т. Т. Батышева, кандидат медицинских наук Поликлиника восстановительного лечения №7 Москвы
Недифференцированный спондилит
Междисциплинарное взаимодействие неврологов и ревматологов позволило выявить редкую причину болевого синдрома.
Одной из самых частых жалоб, с которой сталкиваются в клинической практике врачи-неврологи, являются жалобы на боли в спине. Согласно статистическим данным, до 80% населения хотя бы раз в своей жизни сталкивались с подобным синдромом. В большинстве случаев боль является вертеброгенной и обусловлена остеохондрозом позвоночника. Однако встречаются и редкие причины, диагностика которых требует более длительного и тщательного обследования пациентов.
Одной из редких причин болевого синдрома является спондилоартропатия.
К спондилоартропатиям относят:
Распространённость спондилоартропатии составляет 5—12 на 1000 населения. Данная группа заболеваний является одной из редких причин болевого синдрома в спине, поэтому не всегда специалистам удаётся установить правильный диагноз и назначить лечение.
Пример из клинической практики нашего отделения.
Пациент М., 53 года, 18.03.2019 экстренно госпитализирован в 1 неврологическое отделение КБ№1 с жалобами на интенсивные боли в нижне-грудном и поясничном отделах позвоночника с иррадиацией по задней поверхности левой ноги до большого пальца (до 10 баллов по ВАШ), невозможность стоять и ходить из-за болей.
Состояние при поступлении: Общее состояние: удовлетворительное. Кожные покровы: обычной окраски, влажность нормальная. Отеки отсутствуют. Дыхание через нос свободное. Аускультативно везикулярное. Пульс: 72 уд. в мин., удовлетворительного наполнения, ритмичный. АД 140/90 мм рт.ст. Тоны сердца: ритмичны. Язык чистый. Пальпация живота безболезненна. Дизурических расстройств нет.
Неврологический статус: В сознании, контактен, ориентирован. Тревожен, фиксирован на собственных ощущениях. Менингеальных знаков нет. Глазные щели D=S. Зрачки D=S. Фотореакции живые. Движения глазных яблок не ограничены. Нарушений чувствительности на лице нет. Лицо симметрично. Нистагма нет. Слух не нарушен. Глотание, фонация не нарушены. Язык по средней линии. Парезов нет. Сухожильные рефлексы живые, S=D. Патологических рефлексов не выявляется. Чувствительность не нарушена. Дефанс, болезненность при пальпации паравертебральных мышц в грудном и поясничном отделах. Симптом Ласега отрицательный с 2-х сторон.
Лабораторные обследования:
В анализах крови – повышение уровня С-реактивного белка (43.43 мг/л), СОЭ (50 мм/час).
Анализ мочи – без патологии.
Инструментальные обследования:
На МРТ поясничного отдела позвоночника выявлены дегенеративные изменения, малая грыжа межпозвонкового диска L5-S1 4 мм, спондилоартроз в дугоотростчатых суставах, выраженный на уровне L4-L5 с периартикулярной кистой слева и признаками воспалительного процесса в периартикулярных мягких тканях, спондилез.
На МРТ грудного отдела позвоночника выявлены умеренные дегенеративные изменения, артроз реберно-позвоночных суставов, протрузии межпозвонковых дисков TH7-Th9, TH4- TH5, спондилез.
Обращало на себя внимание несоответствие клинической картины (выраженные боли до 10 баллов по ВАШ) и изменений на МРТ (малая грыжа L5-S1 4мм), неэффективность стационарного лечения в предыдущую госпитализацию, повышение показателей воспаления (С-РБ, СОЭ).
Пациент был консультирован ревматологом. Предположен воспалительный генез заболевания. Зачастую спондилоартропатии ассоциированы с урогенитальной инфекцией, однако выявить специфического возбудителя по анализам крови и при исследовании простатического сока в данном случае не удалось. Анализ на HLA-B27 – отрицательный.
Начата гормональная терапия глюкокортикостероидами (Дексазон 12 мг в сутки), и антибактериальная терапия Ципрофлоксацином 500 мг х 2 раза/сут. На фоне гормональной и антибактериальной терапии отмечалась положительная динамика в виде уменьшения болевого синдрома до 1-2 баллов по ВАШ. Пациент выписан с улучшением и рекомендациями по продолжению антибактериальной терапии сроком до 3-х месяцев с последующей консультацией ревматолога.
Таким образом, междисциплинарное взаимодействие неврологов и ревматологов позволило выявить редкую причину болевого синдрома, установить правильный диагноз и назначить лечение.