Дефект фолатного цикла что это
Гены фолатного цикла. Где миф, а где реальность?
Разбираемся, что такое фолатный цикл, зачем он нужен, какие в нем участвуют гены и почему о них можно не беспокоиться.
Фолатный цикл, или обмен витаминов В9 и В12, влияет на многие жизненно важные процессы, включая строительство ДНК и работу генов. Сбои в работе фолатного цикла связывают с целым рядом болезней: от инфаркта или инсульта до анемии и осложнений при беременности.
В этом сложном процессе участвует целый ряд ферментов, а также производные фолиевой кислоты или витамина В9. Гены, кодирующие эти ферменты, часто называют генами фолатного цикла. В них могут быть варианты, которые меняют активность и устойчивость ферментов. Анализ генов фолатного цикла может выявить эти варианты и указать на возможные проблемы. Однако связь между вариантами генов и развитием болезней до сих пор не доказана.
Содержание:
Эта статья носит исключительно образовательный и информационный характер и не может быть использована для диагностики или лечения, а также для замены профессиональных рекомендаций.
Зачем нужны гены фолатного цикла

Что можно узнать из генетического теста
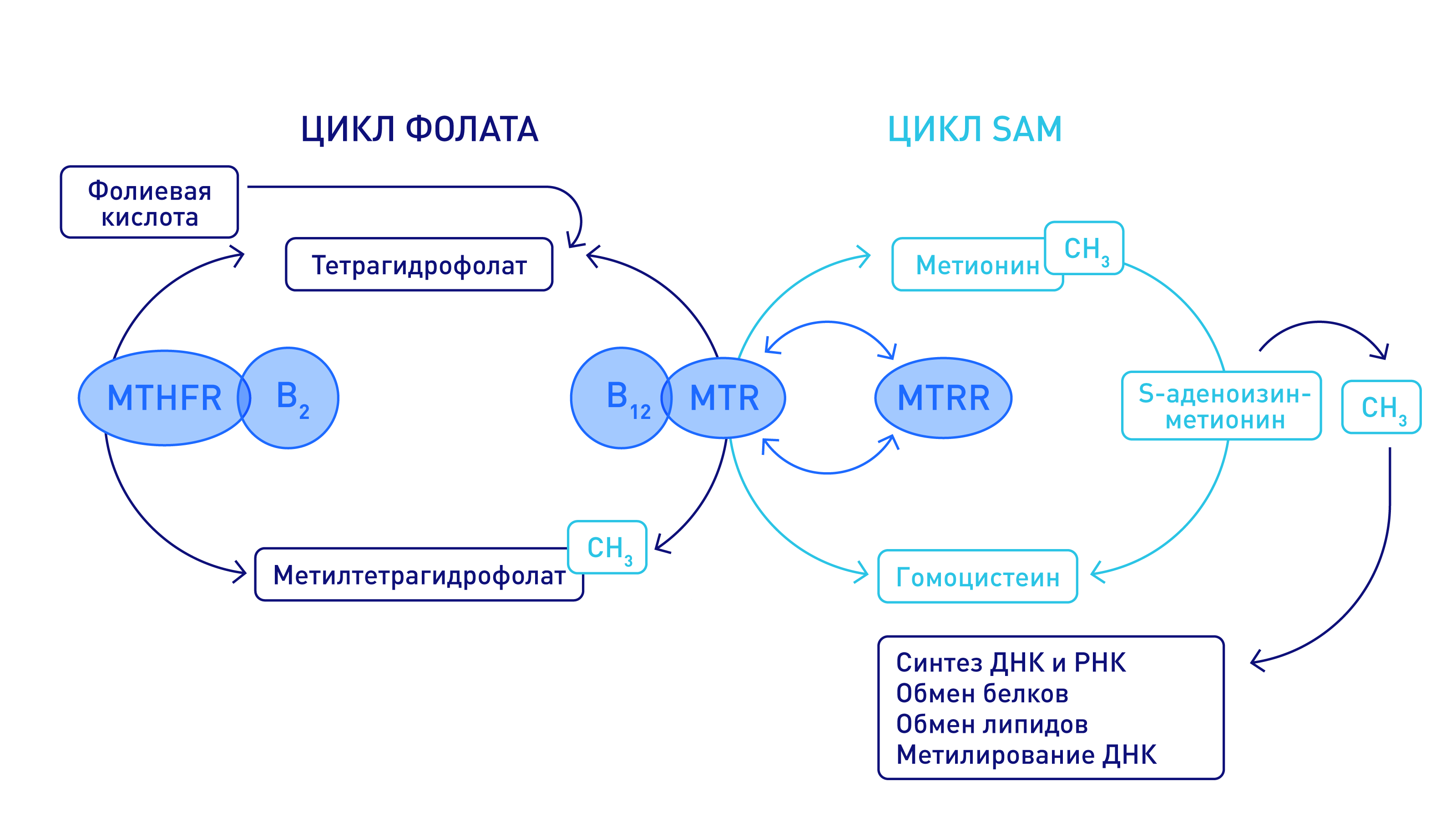
Эти ферменты участвуют на разных этапах реакции восстановления фолатов, к которым относятся, например, витамины В9 и В12. Главная цель этой реакции — получить от фолатов как можно больше СН3 метильных групп и обезвредить гомоцистеин.
Это промежуточный продукт обмена фолатов и метионина — исходного материала для реакций метилирования или переноса метильной группы (СН3). Этот процесс очень важен для работы организма: метилирование ДНК регулирует работу генов, а фолатный цикл как бы расставляет «выключатели» в нужных местах генома.
За счет этого генетическая информация сохраняется и считывается лучше, а разные клетки организма синтезируют не все белки подряд, а только те, которые нужны им сейчас. Например, клетки слизистой оболочки желудка синтезируют пищеварительные ферменты. А вот у меланоцитов в коже геном тот же, но гены пищеварительных ферментов выключены и вместо них синтезируется меланин, который дает нам загар.
Основные функции трех генов фолатного цикла:
| Название гена | Название фермента | Функция |
|---|---|---|
| MTHFR | Метилентетрагидрофо-латредуктаза | Участвует в подготовке кофактора — активной формы фолиевой кислоты В9 для синтеза метионина из гомоцистеина |
| MTR | Метионин-синтаза | Участвует в реакции синтеза метионина из гомоцистеина с помощью В12 |
| MTRR | Метионин-синтаза-редуктаза | Поддерживает активность метионин-синтазы и обеспечивает непрерывную утилизацию гомоцистеина |
Откуда про эти гены столько мифов
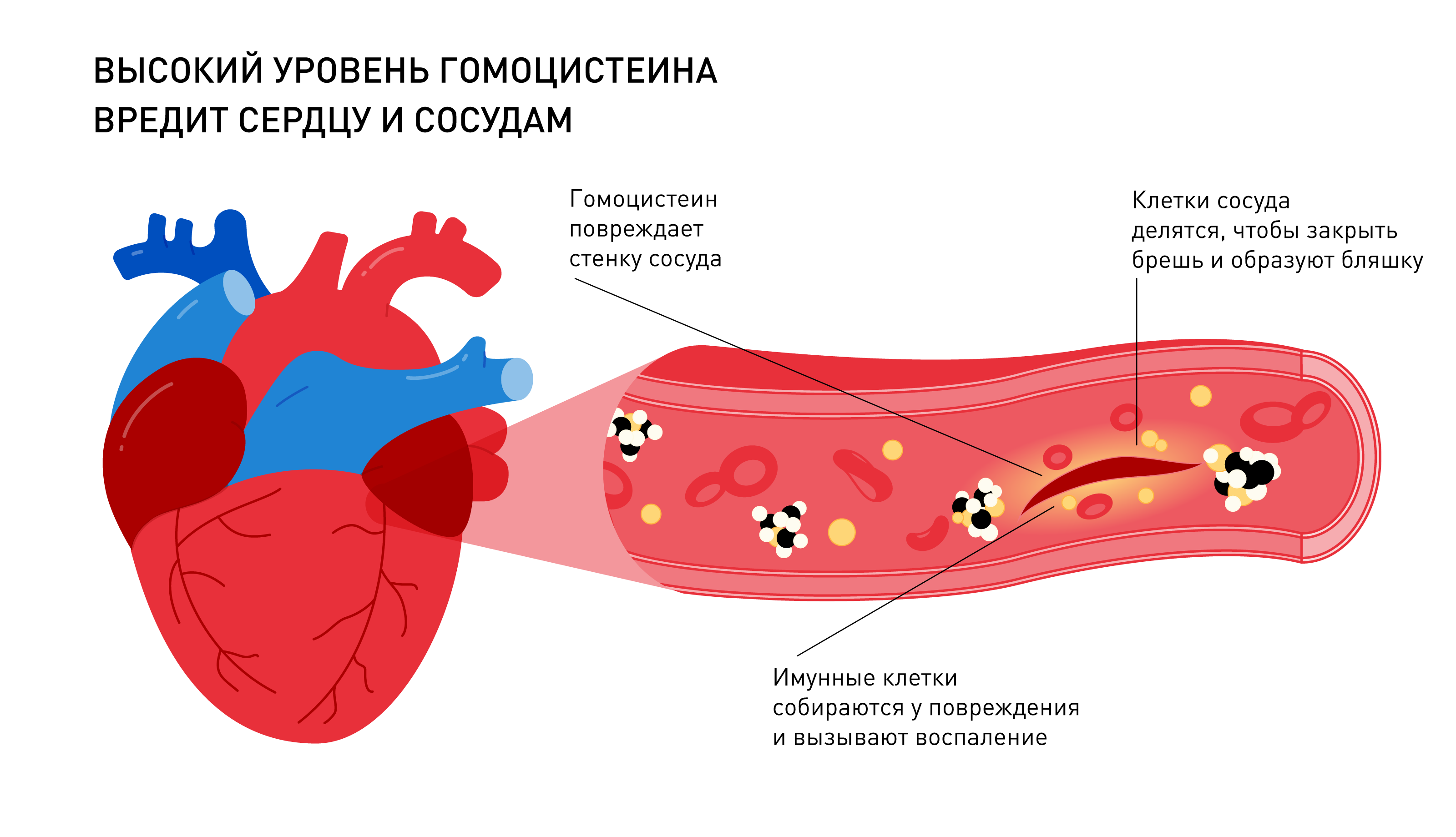
Из-за нарушений в работе фолатного цикла в организме может накапливаться гомоцистеин — производное метионина. В концентрации сильно выше лабораторных норм гомоцистеин повреждает сосуды и нейроны. Его высокое содержание в крови связывают со многими патологиями: ишемической болезнью сердца, инфарктом, атеросклерозом, болезнью Альцгеймера, анемией, тромбозом.

Как генетическое тестирование помогает при планировании семьи
Первые данные о влиянии гомоцистеина на здоровье появились в 1962 году, когда было описано редкое наследственное заболевание гомоцистинурия. Для этого состояния характерен высокий уровень гомоцистеина, который вызывает серьезную задержку в психическом развитии из-за неправильной работы гена СВS. Впервые повышение уровня гомоцистеина и развитие тромбоза в детстве было связано со сбоями в работе фермента MTHFR в 1991 году. А в 1995 были обнаружены варианты в гене MTHFR, которые влияют на активность фермента.
В итоге родилась теория о том, что варианты генов фолатного цикла могут приводить к высокому уровню гомоцистеина из-за нарушений в работе ферментов. Следовательно, наличие таких вариантов могло оказаться ценным маркером для диагностики и предотвращения различных заболеваний: от бесплодия до рака.
Сотни ученых искали взаимосвязь между патологиями и разными вариантами генов, и такая корреляция была найдена. Без достаточных доказательств клинического значения, на основании этой взаимосвязи анализ генов фолатного цикла стали предлагать пациентам.
Правда о генах фолатного цикла
Анализ генов фолатного цикла не входит в рекомендации большинства мировых генетических сообществ и клинических организаций. А если внимательно присмотреться к его научной базе, оказывается, что доказательств связи между вариантами этих генов и заболеваниями недостаточно.
Основная проблема в том, что полиморфизмы или варианты генов — далеко не единственная причина повышения уровня гомоцистеина в крови. Это справедливо только для редких случаев гомоцистинурии, а в остальном нельзя не учитывать диету, образ жизни и целый ряд других показателей обмена веществ.
Комплексных исследований, доказывающих связь болезней помимо гомоцистинурии с мутациями, пока нет. А опубликованные результаты не всегда согласуются друг с другом.
В 2018 году вышел большой критический обзор исследований, посвященных гену MTHFR. Авторы обзора пришли к выводу, что клинического значения мутаций генов фолатного цикла недостаточно, чтобы руководствоваться этим при ведении серьезных заболеваний. Сравнивая различные статьи по этой теме, ученые обнаружили методологические ошибки и нестыковки в данных.
Например, большинство исследований рассматривает небольшие выборки жителей Азии. При этом в других популяциях похожие связи не прослеживаются. Кроме того, публикаций с опровержением этого мифа может быть мало из-за академической предвзятости к негативным результатам исследований. Похожая ситуация и с другими двумя генами: MTRR и MTR.
Рекомендации
Профессиональные ассоциации генетиков и ключевые клинические организации в мире советуют обходиться без тестирования генов фолатного цикла при постановке диагноза и выборе лечения.
| Организация | Рекомендации | Документ |
|---|---|---|
| American Heart Association | Гомоцистеин не следует использовать в оценке риска сердечно-сосудистых заболеваний. | Greenland et al. (2010). |
| American Congress of Obstetricians and Gynecologists | Из-за недостаточной связи между C677T полиморфизмом в гене MTHFR и любыми осложнениями беременности, включая риск венозной тромбоэмболии, скрининг мутаций MTHFR не рекомендуется. | American Congress of Obstetricians and Gynecologists (2013). |
| American College of Medical Genetics | Генетический анализ MTHFR не следует включать в клиническую оценку риска тромбоза или рецидивирующей потери беременности. | Hickey et al. (2013). |
Анализ генов фолатного цикла не помогает вылечить или предотвратить сердечно-сосудистые заболевания, психические расстройства и осложнения при беременности.
С Генетическим тестом Атлас можно узнать, какие из ваших генов действительно влияют на предрасположенность к заболеваниям. Анализ вариантов в гене MTHFR или других генах “фолатного цикла” (MTR, MTRR) намеренно не включен в интерпретацию результатов генетического теста.
Фолатный цикл: анализ
Фолатный цикл, метилирование, метилфолат… В этой статье вы найдете много новых полезных слов, а, главное, узнаете, зачем нам нужен витамин B 9, как он влияет на уровень гомоцистеина и как контролировать свой фолатный цикл.
Витамин B 9 – это водорастворимый витамин, отвечающий за грамотную работу иммунной, сердечно-сосудистой и нервной систем. Витамин снижает образование гомоцистеина – вещества, которое в избытке провоцирует сердечно-сосудистые патологии.
Дефицит В9 приводит к:
· усталости, слабости и раздражительности;
· риску развития патологий нервной системы, включая шизофрению и аутизм;
· риску осложнений беременности: задержке роста плода, дефекту нервной трубки, отслойке плаценты.
К снижению витамина В9 ведет:
· частое употребление кофе и кофеинсодержащих напитков;
· воспалительные заболевания кишечника;
· применение противосудорожных препаратов;
· прием противовоспалительных средств (аспирин, ибупрофен);
· прием противозачаточных таблеток.
У витамина В9 есть две формы :
1. Фолат – витамин, который существует в природе и присутствует в продуктах питания.
2. Фолиевая кислота – синтетическая форма B 9, основа добавок. Прежде, чем организм сможет ее использовать, она должна быть преобразована в активную форму. Но некоторые генетические мутации могут замедлить этот процесс.
В9 содержится в фруктах и их соках, темно-зеленых листовых овощах, орехах, горохе, фасоли, морепродуктах, мясе, птице, яйцах, молочных продуктах и зерне. Шпинат, спаржа, печень и брюссельская капуста имеют самый высокий уровень фолатов.
Суточная доза потребления витамина В9 составляет 400 мкг, для беременных и кормящих женщин – 600 мкг.
Нарушение фолатного цикла приводит к накоплению гомоцистеина и повышению его уровня в крови. Он обладает токсическим действием, повышает риск развития атеросклероза и тромбоза. Гипергомоцистеинемия может стать причиной серьезных осложнений беременности. У женщин с нарушенным фолатным циклом чаще рождаются дети с дефектом нервной трубки и синдромом Дауна.
Для нормальной работы фолатного цикла требуется, чтобы гены, которы е кодируют ферменты, не имели нарушений. Из-за генетических вариаций организм некоторых людей может недостаточно эффективно использовать витамин В9, в результате чего может выявляться его недостаточность даже при нормальном его поступлении. Например, нарушение работы фермента MTHFR приводит к неэффективному превращению витамина В9 в активную форму, что в дальнейшем аукнется дефицитом витамина.
Людям с дефектами в генах фолатного цикла лучше избегать употребления большого количества фолиевой кислоты и выбирать добавки, которые содержат активный метилфолат (5-MTHF). Это связано с тем, что прием добавок, содержащих активную форму витамина B9, гарантирует, что фолат может сразу использоваться организмом.
Как узнать, есть ли у вас дефекты генов, отвечающих за усвоение витамина B 9?
Он может называться по-разному: фолатный цикл анализ, витамин б9 анализ, мутации фолатного цикла анализ, анализ генов фолатного цикла, анализ полиморфизмов фолатного цикла, нарушения фолатного цикла анализ, генетический анализ фолатного цикла… Но суть одна: это анализ, который исследует гены, отвечающие за метаболизм витамина В9.
Вам необходимо это исследование, если:
После анализа вы узнаете:
Дефект фолатного цикла что это
Генетика фолатного цикла
Генетика фолатного цикла
Ф олатный цикл – каскадный процесс, контролируемый ферментами, которые в качестве коферментов имеют производные фолиевой кислоты. Ключевым этапом в данном процессе является синтез метионина из гомоцистеина. Это достигается в процессе превращения фолатов: восстановления 5,10-метилентетрагидрофолата до 5-метилтетрагидрофолата, несущего метильную группу, которая необходима для превращения гомоцистеина в метионин. Восстановление фолатов происходит при участии фермента метилентетрагидрофолатредуктаза (MTHFR). Метильная группа переносится на витамин B12, который затем отдает ее гомоцистеину, образуя метионин с помощью фермента метионин-синтазы (MTR). Однако в некоторых случаях В12 может окисляться, что приводит к подавлению метионин-синтазы. Для поддержания активности фермента необходимо восстановительное метилирование с помощью фермента метионин-синтаза-редуктазы (MTRR).
Нарушение фолатного цикла приводит к накоплению гомоцистеина в клетках и повышению общего уровня гомоцистеина в плазме. Гомоцистеин обладает выраженным токсическим, атерогенным и тромбофилическим действием, что обусловливает повышенный риск развития ряда патологических процессов.
Причины нарушений фолатного цикла:
Генетические дефекты ферментов фолатного цикла MTHFR, MTR и MTRR.
Дефицит фолиевой кислоты.
Дефицит витаминов В6 и В12.
Назначение: Позволяет определить генетические дефекты ферментов фолатного цикла MTHFR, MTR и MTRR.
Стоимость услуги: 2500.
Материал исследования/ Подготовка к проведению анализа:
венозная кровь с ЭДТА (Не требуется специальная подготовка).
буккальный (защечный) эпителий/ не рекомендуется прием пищи в течение 2 часов до взятия соскоба.
Противопоказания к проведению анализа: отсутствуют.
Срок исполнения: 10 рабочих дней (без учёта доставки).
Показания к назначению исследования:
Повышенный уровень гомоцистеина в крови (гипергомоцистеинемия);
Невынашивание беременности, гибель плода во 2 и 3 триместрах беременности;
Рождение ребенка с изолированными пороками нервной трубки, сердца или урогенитального тракта;
Плановая подготовка к беременности;
Наличие ИБС, артериальной гипертонии, атеросклероза или атеротромбоза;
Семейная предрасположенность к онкологическим заболеваниям;
Назначение оральных контрацептивов и гормональной заместительной терапии.
Метод исполнения: Исследование «Генетика фолатного цикла» выполняется методом ПЦР в реальном времени, включающий анализ 4 локусов генов MTHFR, MTR, MTRR.
Возможность проведения качественного и количественного анализа.
Высокая специфичность реакции за счет использования высокоспецифичных флуоресцентных зондов.
100% соответствие результатам «золотого стандарта».
Быстрый и точный метод определения генотипа.
Анализ на наличие мутаций достаточно провести 1 раз в жизни.
Высокая прогностическая значимость выявляемых факторов риска.
Генетический полиморфизм, ассоциированный с риском развития нарушений обмена гомоцистеина (фолатный цикл)
Фолиевая кислота – водорастворимый витамин B9, необходимый для роста и развития кровеносной и иммунной систем. Недостаток фолиевой кислоты может вызвать мегалобластную анемию у взрослых, а при беременности повышает риск развития дефектов нервной
трубки. Производные фолиевой кислоты называются фолатами. Животные и человек не синтезируют фолиевую кислоту, получая ее в основном вместе с пищей. Фолиевая кислота в больших количествах содержится в зеленых овощах с листьями, бобовых, в хлебе из муки грубого помола, дрожжах, печени. Во многих странах законодательство обязывает производителей мучных продуктов обогащать зерна фолиевой кислотой.
Группа соединений фолатов играет ведущую роль в широком спектре жизненно важных процессов:
Данные функции реализуются в процессе метаболизма фолатов, который составляет основу фолатного цикла.
Фолатный цикл – каскадный процесс, контролируемый ферментами, которые в качестве коферментов имеют производные фолиевой кислоты. Ключевым этапом в данном процессе является синтез метионина из гомоцистеина. Это достигается в процессе превращения фолатов: восстановления 5,10-метилентетрагидрофолата до 5-метилтетрагидрофолата, несущего метильную группу, которая необходима для превращения гомоцистеина в метионин. Восстановление фолатов происходит при участии фермента метилентетрагидрофолат-редуктазы (MTHFR). Метильная группа переносится на B12, который затем отдает ее гомоцистеину, образуя метионин с помощью фермента метионин-синтазы (MTR). Однако в некоторых случаях В12 может окисляться, что приводит к подавлению метионин-синтазы. Для поддержания активности фермента необходимо восстановительное метилирование с помощью фермента метионин-синтаза-редуктазы (MTRR).
Нарушение фолатного цикла приводит к накоплению гомоцистеина в клетках и повышению общего уровня гомоцистеина в плазме крови. Главной формой фолата в плазме является 5-метилтетрагидрофолат, несущий на себе метильную группу, которая необходима для превращения гомоцистеина в метионин. Поскольку кобаламин (витамин B12) служит акцептором метильной группы 5-метилтетрагидрофолата, дефицит этого витамина приводит к «ловушке для фолата». Это тупиковый путь метаболизма, поскольку метилтетрагидрофолат не может восстанавливаться до тетрагидрофолата и возвращаться в фолатный пул.
Это приводит к истощению запаса метионина и выбросу в кровь избытка гомоцистеина, который
обладает атерогенным действием, гипертензивными свойствами, повышает гиперагрегацию тромбоцитов.
Кроме того, гомоцистеин свободно проходит через плаценту и оказывает тератогенное и фетотоксическое действие.
Нарушение метаболизма фолатов и повышение уровня гомоцистеина обусловливают повышенный
риск развития патологических процессов:
Нарушения фолатного цикла не оказывают изолированного влияния на возникновение венозных тромбозов при применении гормональной заместительной терапии и оральных контрацептивов, однако при наличии других тромбофилических полиморфизмов (особенно лейденской мутации и мутации гена протромбина: 20201 G>A) многократно усиливают их действие.
Причины нарушения фолатного цикла:
Анализ полиморфизмов в генах фолатного цикла позволяет определить предрасположенность
к указанным выше патологическим процессам и дает возможность своевременного принятия мер
посредством назначения корректирующей терапии.
П оказания к назначению профиля «Генетика метаболизма фолатов» :
Полиморфизм гена метионинсинтазы MTR(A2756G)
П оказания к назначению: повторные эпизоды венозных тромбоэмболий в анамнезе, эпизоды тромбоэмболий во время беременности, в послеродовом периоде и во время приёма оральных контрацептивов, необъяснимая гибель плода во 2 или 3 триместрах беременности, мегалобластная анемия, мутация MTRR.
Биологический материал для анализа : цельная кровь, стабилизированная ЭДТА
Полиморфизм гена метилентетрагидрофолатредуктазы MTHFR(A1298C) (тератогенный фактор)
Показания к назначению: повторные эпизоды венозных тромбоэмболий в анамнезе, эпизоды тромбоэмболий во время беременности, в послеродовом периоде и во время приёма оральных контрацептивов, необъяснимая гибель плода во 2 или 3 триместрах беременности, дефект невральной трубки у плода в анамнезе.
Биологический материал для анализа : цельная кровь, стабилизированная ЭДТА
Полиморфизм гена метилентетрагидрофолатредуктазы MTHFR(С677Т) (наследственная гипергомоцистеинемия)
Частота встречаемости гомозиготного носительства по данной мутации среди белого населения планеты составляет от 5 до 12 %. Гетерозиготная мутация С677Т наблюдается у 50% в популяции. Полиморфизм C677T связан, по крайней мере, с четырьмя группами многофакторных заболеваний: сердечно-сосудистыми заболеваниями (атеросклеротическое поражение сосудов, атеротромбоза и его осложнений), дефектами развития плода (дефект развития нервной трубки), колоректальной аденомой и раком молочной железы и яичника.
Показания к назначению: гипергомоцистеинемия, ИБС и инфаркт миокарда, атеросклероз и атеротромбоз, антифосфолипидный синдром, полипоз кишечника, колоректальная аденома и рак, мутации генов BRCA, цервикальная дисплазия, особенно в сочетании с папилломавирусной инфекцией.
Биологический материал для анализа : цельная кровь, стабилизированная ЭДТА
Полиморфизм гена редуктазы метионинсинтазы MTRR(A66G) (тератогенный фактор)
Ген MTRR кодирует фермент метионинсинтазу редуктазу, участвующий в большом количестве биохимических реакций, связанных с переносом метильной группы. Одной из функций МСР является обратное превращение гомоцистеина в метионин. В качестве кофактора в этой реакции принимает участие витамин В12 (кобаламин). Полиморфизм I22M A>G связан с аминокислотной заменой в молекуле фермента МСР. В результате этой замены функциональная активность фермента снижается, что приводит к повышению риска нарушений развития плода – дефектов невральной трубки. Влияние полиморфизма усугубляется дефицитом витамина В12. При сочетании полиморфизма I22M A>G гена MTRR с полиморфизмом 677C-> T в гене MTHFR риск увеличивается. Полиморфизм I22M A->G гена MTRR также усиливает гипергомоцистеинемию, вызываемую полиморфизмом 677C-> T в гене MTHFR.
Показания к назначению: повторные эпизоды венозных тромбоэмболий в анамнезе, эпизоды тромбоэмболий во время беременности, в послеродовом периоде и во время приёма оральных контрацептивов, необъяснимая гибель плода во 2 или 3 триместрах беременности.
Биологический материал для анализа : цельная кровь, стабилизированная ЭДТА
Генетика метаболизма фолатов
Поскольку метаболизм фолатов является важным звеном базовых биологических процессов, то его нарушения, в том числе генетически обусловленные, рассматриваются как фактор высокого риска развития патологических состояний: сердечно-сосудистых заболеваний (ССЗ), онкологических заболеваний, нарушений репродуктивных функций и патологий развития плода. Своевременное выявление генетической мутации, нарушающей выработку ферментов фолатного цикла, дает возможность эффективно контролировать и корректировать уровень фолиевой кислоты у пациентов, что благотворно сказывается на их здоровье.
Группа соединений фолатов играет ведущую роль в широком спектре жизненно важных процесов:
Фолатный цикл – каскадный процесс превращения фолиевой кислоты в доступное для усваивания организмом производное – 5-метилтетрагидрофолат. Процесс контролируется ферментом метилентетрагидрофолатредуктазой (MTHFR). Обмен фолатов является источником одноуглеродных фрагментов (метильной группы –СН3) для жизненно важных клеточных процессов: биосинтеза пуриновых нуклеотидов и превращения уридинионофосфата в тимидилат; митилирования ДНК и РНК.
С фолатным циклом сопряжён цикл образования метионина из гомоцистеина, который проходит при участии витамина В12 и двух ферментов: метионин-синтазы (MTR) и метионин-синтаза-редуктазы (MTRR).
Нарушения метаболизма фолатов влияют на стабильность ДНК двумя основными способами:
Поскольку метаболизм фолатов является важным звеном базовых биологических процессов, то его нарушения, в том числе генетически обусловленные, рассматриваются как фактор высокого риска развития патологических состояний: сердечно-сосудистых заболеваний (ССЗ), онкологических заболеваний, нарушений репродуктивных функций и патологий развития плода.
С точки зрения вклада в развитие ССЗ рассматриваются два процесса, связанные с фолатным циклом: накопление гомоцистеина и нарушение процессов метилирования ДНК.
Основным повреждающим эффектом повышения уровня гомоцистеина является активация атеротромбоза за счёт многочисленных механизмов. Установлено, что у больных с повышенным уровнем гомоцистеина риск смерти от всех сердечно-сосудистых причин был выше в 1,7 раза, от инфаркта миокарда – в 3,4 раза, от инсульта – в 4,3 раза, чем у больных с нормальным уровнем гомоцистеина. Кроме того, гомоцистеин является частичным агонистом рецепторов глицина. При таких состояниях, как инфаркт и травма мозга, когда концентрация глицина возрастает, даже незначительные концентрации гомоцистеина начинают оказывать выраженное нейротоксическое воздействие. Эффективность метаболизма гомоцистеина напрямую зависит от достаточности фолатов в организме и полноценного функционирования фермента MTHFR.
Роль генетически обусловленных нарушений метаболизма фолатов была доказана для пациентов с инфарктом миокарда и ишемическим инсультом: наличие полиморфизма MTHFR C667T было ассоциировано с тромботическими событиями. Тем не менее следует отметить, что само по себе носительство условно «неблагоприятных» аллельных вариантов генов ферментов фолатного цикла повышает риск ССЗ в случае отсутствия коррекции уровня фолатов в организме. Исследования показали, что носительство полиморфных аллелей MTHFR C667T не влияло на прогноз больных с нормальным уровнем фолиевой кислоты, в то время как при низком фолатном статусе риск основных коронарных событий был повышен на 32% у гетерозиготных носителей и на 44% у гомозиготных носителей аллели 667TT, а также была отмечена тенденция к повышению сердечно-сосудистых осложнений у носителей потенциально благоприятного «дикого» генотипа, имевших сопутствующий дефицит фолиевой кислоты.
Регулярный приём фолиевой кислоты (под контролем врача) значительно снижает содержание в крови гомоцистеина и сокращает ежегодную смертность от ССЗ.
Особую актуальность генетические дефекты фолатного цикла имеют с точки зрения развития репродуктивных проблем и пороков развития плода. Ассоциация генетических полиморфизмов ферментов фолатного цикла доказана при осложнениях беременности: фетоплацентарной недостаточности, преэклампсии, преждевременной отслойке нормально расположенной плаценты, замершей беременности, внутриутробной гибели плода, развитии гестоза. Была установлена связь с высокой частотой аномальных гинекологических и акушерских кровотечений. Примечательно, что дефекты генов ферментов фолатного цикла ассоциированы и с бесплодием у мужчин, необструктивной азооспермией и олигозооспермией.
Важно знать, что при наследственных дефектах генов ферментов фолатного цикла избыток синтетической фолиевой кислоты может ещё больше нарушить равновесие и привести к таким же последствиям для плода, как и дефицит этого витамина.
Показания к генетическому анализу:
При проведении генетического исследования метаболизма фолатов определяют следующие полиморфизмы: