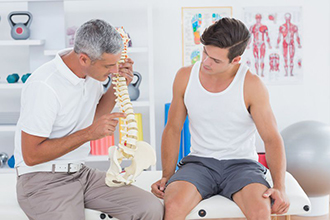
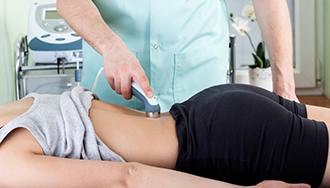
Дексаметазон или дипроспан при остеохондрозе что лучше
Дексаметазон или дипроспан при остеохондрозе что лучше
Смоленская государственная медицинская академия
Кафедра клинической фармакологии и антимикробной химиотерапии
ГЛЮКОКОРТИКОИДНЫЕ ПРЕПАРАТЫ
ХАРАКТЕРИСТИКА ОТДЕЛЬНЫХ ПРЕПАРАТОВ
В зависимости от структуры глюкокортикоиды различаются по длительности действия, выраженности противовоспалительной, минералокортикоидной, метаболической и иммуносупрессивной активности (табл. 5). Причем, нет прямой корреляции между их иммуносупрессивным и противовоспалительным действием. Например, дексаметазон обладает мощным противовоспалительным эффектом и относительно низкой иммуносупрессивной активностью.
КОРТИЗОН
Препарат природного глюкокортикоида, биологически неактивен. Активируется в печени, превращаясь в гидрокортизон. Обладает кратковременным действием. По сравнению с другими глюкокортикоидами имеет более выраженную минералокортикоидную активность, то есть оказывает существенное влияние на водно-электролитный обмен.
Особенности применения
В основном используется для заместительной терапии надпочечниковой недостаточности у больных с нормальной функцией печени.
Формы выпуска:
ГИДРОКОРТИЗОН
Природный глюкокортикоид, по глюкокортикоидной активности в 4 раз слабее преднизолона, по минералокортикоидной несколько превосходит его. Как и при применении кортизона, высока вероятность развития отеков, задержки натрия и потери калия.
Особенности применения
Гидрокортизон так же, как и кортизон, не рекомендуется применять для фармакодинамической терапии, особенно у больных с отеками, гипертензией, сердечной недостаточностью.
Применяется, главным образом, для заместительной терапии при первичной и вторичной надпочечниковой недостаточности. При острой надпочечниковой недостаточности и других неотложных состояниях препаратом выбора является гидрокортизона гемисукцинат.
Формы выпуска:
ПРЕДНИЗОЛОН
Синтетический глюкокортикоид, наиболее часто используется в клинической практике для фармакодинамической терапии и рассматривается как стандартный препарат. По глюкокортикоидной активности в 4 раза сильнее гидрокортизона, а по минералокортикоидной активности уступает ему. Относится к глюкокортикоидам со средней продолжительностью действия.
Формы выпуска:
ПРЕДНИЗОН
По активности и другим параметрам близок к преднизолону. Исходно преднизон является метаболически неактивным препаратом (пролекарством). Активируется в печени путем гидроксилирования и превращения в преднизолон. Поэтому при тяжелых заболеваниях печени использовать его не рекомендуется. Основным преимуществом преднизона является его более низкая стоимость.
Формы выпуска:
МЕТИЛПРЕДНИЗОЛОН
По сравнению с преднизолоном обладает несколько большей (на 20%) глюкокортикоидной активностью, минимальным минералокортикоидным действием, реже вызывает нежелательные реакции (особенно изменения психики, аппетита, ульцерогенное действие). Имеет более высокую стоимость, чем преднизолон.
Особенности применения
Так же, как и преднизолон, используется в основном для фармакодинамической терапии. Предпочтителен у больных с психическими нарушениями, ожирением, язвенной болезнью, а также при проведении пульс-терапии.
Формы выпуска:
ТРИАМЦИНОЛОН
Является фторированным глюкокортикоидом. Обладает более сильным (на 20%) и длительным глюкокортикоидным действием, чем преднизолон. Не имеет минералокортикоидной активности. Чаще вызывает нежелательные реакции, особенно со стороны мышечной ткани («триамцинолоновая» миопатия) и кожи (стрии, кровоизлияния, гирсутизм).
Формы выпуска:
ДЕКСАМЕТАЗОН
Так же, как и триамцинолон, является фторированным препаратом. Один из наиболее мощных глюкокортикоидов: в 7 раз сильнее преднизолона по глюкокортикоидной активности. Не обладает минералокортикоидным действием. Вызывает сильное угнетение гипоталамо-гипофизарно-надпочечниковой системы, выраженные нарушения углеводного, жирового, кальциевого обмена, психостимулирующее действие, поэтому не рекомендуется назначать его на длительный срок.
Особенности применения
Препарат имеет некоторые особые показания к применению: бактериальный менингит; отек мозга; в офтальмологии (кератит, увеит и другие); профилактика и лечение тошноты и рвоты при химиотерапии; лечение тяжелого абстинентного синдрома при алкоголизме; профилактика синдрома дыхательных расстройств у недоношенных (дексаметазон стимулирует синтез сурфактанта в альвеолах легких); лейкоз (замена преднизолона на дексаметазон при остром лимфобластном лейкозе значительно снижает частоту поражения центральной нервной системы).
Формы выпуска:
БЕТАМЕТАЗОН
Формы выпуска:
Таблица 5. Сравнительная активность глюкокортикоидов для системного введения
| ||||||||||||||||||||||||||||||||||||||||||||||||||
* ГК глюкокортикоидная активность
** МК минералкортикоидная активность
Лечебные блокады
Лечебно-медикаментозная блокада — это инъекция обезболивающих препаратов в нервные сплетения, избавляющая от мышечных болей и спазмов в короткий срок.
Содержание статьи:
Лечебная блокада – медикаментозный метод купирования болевого синдрома, а также другой неврологической симптоматики. Такая техника обезболивания применяется более века, за который доказала высокую эффективность. Медикаментозная блокада позволяет избавиться от боли в очень короткий срок и существенно улучшить качество жизни и самочувствие.
Каноны современной медицины диктуют как можно более быстрое купирование боли. Иначе ухудшается психологическое состояние пациента. Это накладывается на имеющуюся симптоматику, многократно ухудшая клиническую картину. Иногда хроническая боль приводит к суициду. Поэтому лечебная блокада получила очень широкое распространение. Она устраняет причину боли с минимальными побочными эффектами и без интоксикации организма.
Медикаментозная блокада имеет непродолжительное обезболивающее действие. Однако, благодаря снятию мышечного спазма и иных симптомов, общее самочувствие улучшается на более долгий срок. Блокады проводят курсами от 2 до 15 уколов, перерыв – 3-4 дня.
Лечебная блокада – это инъекция (укол) лекарственного препарата в очаг боли, в том числе эпидурально.
Медикаментозная блокада обеспечивает трехфазное избавление от боли. Сначала из-за раздражения болевых рецепторов иглой боль усиливается. Затем она стихает до минимального уровня. На третьей фазе достигается терапевтический эффект – боль уходит. Когда препарат перестает действовать, боль возвращается. Однако ее интенсивность снижается вплоть до 50%.
После лечебно-медикаментозной или диагностической блокады рекомендуется снизить двигательную активность области воздействия. Иногда нужна иммобилизация, например, шейным корсетом. В некоторых случаях показан постельный режим.
Преимущества лечебных блокад
Показания к проведению лечебной блокады
Виды лечебно-диагностических блокад
Локальные
Инъекция делается в зону поражения, под очаг или вокруг него, в область измененных тканевых реакций, в воспаление и др. Разделяются на периартикулярные (в ткани около суставов) и периневральные (в нервные каналы).
Сегментарные
Уколы в различные сегменты, к ним относятся паравертебральные блокады, которые делаются в проекцию сегментов позвоночника. Каждому спинномозговому нерву и сегменту позвоночника соответствует дерматом (участок кожного покрова, соединительной ткани), склеротом (область костной системы), миотом (часть мышечной системы). Вводя препарат внутрикожно в какой-либо дерматом, можно влиять на соответствующий участок позвоночника и/или внутренний орган. Самое частое показание – миотонические реакции паравертебральных мускулов при остеохондрозе.
Вертебральные
Такая лечебная блокада объединяет в неврологии несколько техник. Применяется при боли в спине. Анестетик может вводиться внутрикожно, между остистыми позвонковыми отростками на глубину 2-4 см, в зону тела позвонка. В последнем случае от линии остистых отростков отступают на 3-4 см вбок. Иглу направляют под углом 35° и вводят на 8-10 см в глубину.
Блокады позвоночника
Сильная боль в позвоночнике связана с ущемлением спинномозговых нервов. Блокада действует направленно и нормализует самочувствие. Это не простая процедура, поэтому проводится в крайнем случае.
При блокаде на время отключается нервная проводимость определенных волокон. Для этого используют местные анестетики, которые блокируют клеточное проведение путем ингибирования потенциалзависимых натриевых ходов.
Процедуры показаны при протрузии диска, остеохондрозе, невралгии, межпозвонковой грыже, миозите, спондилоартрозе. Блокады позвоночника бывают шейными, грудными, торако-люмбальными, сакро-люмбальными, копчиковыми, паравертебральными. Последние разделяются на внутрикожные и подкожные (обезболивают кожу около позвоночника), внутримышечные (снимают спазм и воспаление мышц), периневральные («выключают» пораженный нерв).
Эффект наступает за несколько минут. Параллельно снижается сосудистый спазм, ускоряется восстановление тканей, нормализуется обмен веществ, проходит отек от воспаления.
Блокады пяточной шпоры
Применяются для снятия воспаления пяточной фасции. Инъекция делается в пяточный шип, в самый центр. Используются лекарственные средства на основе гормонов. Эффект мгновенный. Трудность заключается в костно-солевой структуре шипа, что затрудняет процесс. Врач должен обладать высокой квалификацией и опытом. Стероиды не только снимают воспаление, но и «разгоняют» метаболизм. За счет последнего происходит рассасывание костного нароста. Чаще всего используется один из трех глюкокортикостероидов: «Гидрокортизон», «Дипроспан» или «Кеналог». Эффективность метода на 90% зависит от правильности инъекции. Поэтому процедура проводится под контролем УЗИ. Она крайне болезненна, поэтому предварительно обеспечивается местная анестезия «Ультракаином», «Новокаином» или другим аналогичным лекарством. После укола 30-60 минут нельзя наступать на пятку. Далее, чтобы снизить давление на пяточные фасции, используют специальные стельки.
Блокады суставов
Применяются для мелких и крупных суставов, когда болевой синдром является следствием дегенеративного процесса или воспаления. Анестетик вводится в суставную капсулу. После этого боль устраняется полностью. Если же случай запущенный, то она значительно снижается. Основные показания – это бурсит, остеоартроз суставов, периартрит, артрит неинфекционной природы, тендовагинит. Процедура не требует подготовки, проводится под местной анестезией. Длительность – 20 минут. Эффект наступает через несколько минут. Сразу после введения препарата можно двигаться. Длительность эффекта зависит от степени поражения сустава. Она составляет в среднем 21 день. Затем делают повторные блокады. Иногда инъекции делают не в сустав, а в мышцу. Это нужно, чтобы снизить спазм, вызывающий боль. Также к этой группе относятся паравертебральные блокады. По такой технологии лечат следующие суставы: голеностопный, тазобедренный, лучезапястный, коленный, плечевой, локтевой.
Блокады нерва
Анестетик вводится в область, по которой идет периферический нерв. Таким образом устраняются боль, сосудистый спазм, мышечное напряжение, воспаление и отек. Показания: неврит, невралгия, онкология, суставные патологии, мышечно-тонический и туннельный синдромы. Процедура может проходить под ультразвуковым контролем. Длительность – до 10 минут. Обезболивающий эффект наступает через несколько минут и сохраняется до 21 дня. Могут проводиться повторные процедуры, кроме случаев, когда эффект не наступает после 1-2 введений.
Препараты, которые применяют при лечебных блокадах
Сначала рассмотрим наиболее часто применяемые местные анестетики.
«Новокаин»
Может вводиться в нервы и ткани, обезболивает, снимает спазм. В патологическом очаге проходит сильное раздражение, отключается периферическая иннервация. Препарат улучшает трофику тканей, а также:
Считается наиболее безопасным средством подавления боли, характеризуется минимумом побочных эффектов. Имеет определенную степень токсичности.
«Лидокаин»
Местный анестетик, обеспечивающий более интенсивный и длительный эффект, по сравнению с «Новокаином». Применяется в форме гидрохлорида. Блокирует потенциалзависимые натриевые каналы, что прекращает генерацию импульсов в нервных окончаниях и блокирует проведение импульсов по нервам. Блокирует не только болевые импульсы, но и другие. Расширяет сосуды, не имеет местнораздражающего эффекта. Через несколько минут после введения «Лидокаина» пропадает боль, расслабляются мышцы. Токсичность ниже, чем у «Новокаина».
«Бупивакаин»
Препарат амидного ряда. Эффект от него развивается медленно, но сохраняется длительно. Это препарат, примерно в 16 раз более мощный, чем «Новокаин». Вся группа амидных анестетиков более стабильна, по сравнению со сложноэфирными (тот же «Новокаин»). Их длительный эффект объясняется тем, что они имеют более долгий период полувыведения. Это связано с тем, что препараты перерабатываются не плазмой, а печенью. «Бупивакаин» предотвращает распространение болевого импульса по нервам, блокируя натриевые каналы мембраны нейронов. Блокада – последовательная, в зависимости от размера нервных волокон (мелкие более чувствительны, по сравнению с крупными), степени активации (большая частота импульсов открывает больше каналов для блокировки), степени миелинизации (волокна с миелиновой оболочкой блокируются лучше). Эффект от процедуры наступает через 5-10 минут.
Теперь перейдем к самым популярным глюкокортикостероидам. Препараты этой группы призваны усилить эффективность блокады, снять воспаление, аллергическую реакцию. Могут применяться также самостоятельно.
«Гидрокортизон»
Относится к группе препаратов с короткой продолжительностью действия. Содержит искусственные гормоны, которые аналогичны вырабатываемым надпочечниками. Применяется для лечения пяточной шпоры курсом из 3-5 инъекций. Активное вещество препарата накапливается в тканях, снимая воспаление. Основное преимущество – низкая цена. Однако он проигрывает «Дипроспану» по эффективности.
При введении в суставы совместно с «Лидокаином» эффект развивается в течение суток и длится до нескольких недель. Способен повышать артериальное давление, одновременно снижая концентрацию лимфоцитов. Благодаря первому, увеличивается объем кровообращения, а второму – снижается интенсивность иммунного ответа. Препарат подходит для неврологических блокад. При около- или внутрисуставных блокадах обязательно смешивание микрокристаллической суспензии с местным анестетиком, чтобы предупредить некроз.
«Дексаметазон»
Глюкокортикостероид длительного действия. Один из самых мощных препаратов. Имеет выраженный противовоспалительный, противоаллергический, иммунодепрессивный и десенсибилизирующий эффект. Особенно хорошо проявляет себя при совместном применении с анестетиком при дегенеративно-дистрофических патологиях. Снижает неадекватную реакцию на анестезирующий препарат. Действует быстро, подходит для блокад мягких тканей и суставов. По сравнению с «Гидрокортизоном», «Дексаметазон» в 25-30 раз активнее. Случаи некроза при его применении не известны, на обмен электролитов влияет мало.
«Депо-медрол»
Метилпреднизолона ацетат – форма метилпреднизолона, обладающая пролонгированным воздействием. Это объясняется худшей растворимостью и меньшей активностью метаболизации. Используется для блокад мягких тканей и суставов. Для эпидуральных блокад – с осторожностью, потому что может спровоцировать воспаление паутинной спинномозговой оболочки.
Используется для лечения всех суставов, за исключением труднодоступных и не имеющих синовиальной полости. При введении в тазобедренный сустав необходимо исключить попадание в крупные сосуды. Инъекции в окружающие сустав ткани могут быть мало- или неэффективными. Если с первого укола не наступает положительного эффекта, процедуру не повторяют.
«Дипроспан»
Препарат на основе бетаметазона. Применяется для лечения пяточной шпоры. Обеспечивает быстрый обезболивающий и противовоспалительный эффект. Снимает аллергическую реакцию. Обычно позволяет вылечить шпору за 1-2 сеанса. Существенный недостаток – разрушительное влияние на надпочечники и гипофиз. Однако вероятность осложнений в этом препарате резко снижена, по сравнению с аналогами. От других подобных лекарственных средств отличается микрокристаллической структурой. Может применяться для эпидуральных блокад, а также блокад спинномозговых нервов, мускулатуры и др. Эффективен при деструктивно-дистрофических заболеваниях позвоночника, в частности поясничного отдела.
Возможные осложнения и меры их профилактики
Лечебные блокады отличаются крайне низким процентом осложнений – 0,5%. Это могут быть реакции на препараты, симптомы интоксикации (рвота, головокружение, сердцебиение), повреждения сосудов в местах инъекций. Чтобы профилактировать осложнения, вводят дополнительные препараты, а после процедуры пациенту рекомендуется 1-2 часа полежать. Не рекомендовано сразу сильно нагружать себя физически, что часто бывает, потому что люди избавляются от боли. Если не проявлять осторожность в плане двигательной активности, симптоматика вернется и будет более сильной.
При блокадах позвоночника возможны кровотечения, инфицирование прокола, повреждение внутренних оболочек, мягких тканей. Последнее обычно связано с неопытностью врача. Также может развиться анафилактический шок. Поэтому процедуру проводят только в медицинском учреждении. Для предупреждения осложнений делают пробную инъекцию.
При блокаде пяточной шпоры у 15-20% людей бывают осложнения. Чаще всего они случаются из-за неправильного введения глюкокортикостероидов и индивидуальной реакции на них. Это может быть отмирание мягких тканей, нагноение, разрыв пяточной фасции. Нужно каждый день после процедуры самостоятельно осматривать пятку, чтобы вовремя заметить негативную реакцию. Ее первые признаки – это боль, почернение и/или покраснение кожи, онемение. Осложнения могут быть отсроченными и возникать даже через несколько недель после процедуры. Это объясняется пролонгированным действием глюкокортикостероидов.
Инъекции гормонов в сустав при артрозе: соглашаться или нет?
В последние годы ортопеды и ревматологи все чаще назначают пациентам уколы в сустав. Метод привлекает тем, что действующее вещество быстро попадает «по адресу» – в суставную полость. Внутрь можно доставить лекарства, которые снимут боль и воспаление, восстановят хрящевую ткань и синовиальную жидкость. Иногда в назначениях фигурируют гормоны. Стоит ли соглашаться на такое лечение?
Инъекции гормонов в сустав быстро снимают боль
Какие препараты вводят в сустав
В зависимости от нужного эффекта, от стадии гонартроза или коксартроза, от диагноза назначают препараты с таким действием:
Препарат для инъекций выбирает врач в зависимости от целей и клинической картины
В каких случаях назначают гормоны
На поздних стадиях артроза тазобедренного сустава или любого другого, когда боли беспокоят пациента почти всегда и обезболивающие таблетки не помогают, могут назначить более сильное средство. Это экстренная мера терапии, способная быстро снять боль и улучшить самочувствие. К сожалению, есть у этой медали и обратная сторона, особенно если прибегать к такому методу чаще, чем это необходимо.
Частые инъекции гормональных препаратов не выдержит ни один организм
Каких правил нужно придерживаться, если вам назначили уколы гормонов в сустав
Если без инъекций гормонов не обойтись, помните вот о чем:
Инъекции гормонов – это крайняя мера при артрозе
В видео вы увидите, как в условиях медкабинета делают укол протеза синовиальной жидкости в коленный сустав:
Есть ли альтернатива?
Инъекции гормонов уменьшают боль при артрозе голеностопа, колена, бедра, но оказывают и негативное влияние на организм. Особенно опасны они при сахарном диабете, артериальной гипертензии, язве желудка, а также если у пациента нарушена работа почек. К тому же кортикостероиды лишь на время избавляют от боли, значит, человеку с каждым разом будет необходима все бОльшая доза.
Вместо вредных для здоровья кортикостероидов, которые к тому же не лечат, можно выбрать другие терапевтические методы:
Курс инъекций протеза синовиальной жидкости составляет 2-5 процедур. После этого об артрозе можно будет забыть на 1-1,5 года. Препарат на основе гиалуроновой кислоты или синтетический Noltrex безопасен для ЖКТ и других систем организма, не нанесет вреда диабетикам и людям с повышенным артериальным давлением.
Если вас беспокоят сильные боли в суставе, не спешите купировать их гормонами. Рассмотрите вариант лечения с перспективой на будущее, вместо того чтобы долго травить свой организм кортикостероидами.
Современные подходы к ведению больных с болью в спине
Российский государственный медицинский университет, Москва
Одним из наиболее распространенных клинических синдромов является боль в пояснично-крестцовой области (боль в спине), обусловленная вертеброгенной патологией. Боль в спине встречается у 60–80% взрослой популяции и является одной из наиболее частых причин временной утраты трудоспособности. Эпизоды болей в спине ежегодно развиваются у половины трудоспособного населения, при этом наиболее часто поражаются лица в возрасте 35–55 лет. Число таких пациентов исключительно высоко, особенно в условиях амбулаторного неврологического приема. Считается, что в подавляющем большинстве случаев (около 90%) длительность болевого синдрома не превышает 6 нед, вместе с тем у остальных пациентов боль приобретает хронический характер. Регистрируется тенденция к росту частоты заболеваний опорно-двигательного аппарата. Так, в Российской Федерации число таких больных за последние 10 лет (1988–1997 гг.) выросло с 7,7 до 11,2 млн (более чем на 40%). Следует учитывать, что реальная распространенность этих заболеваний, вероятно, значительно выше.
Основными причинами боли в спине являются дегенеративные изменения позвоночника, в частности остеохондроз, дисфункция фасеточных суставов, частичный надрыв фиброзного кольца, пролабирование межпозвонковых дисков, в ряде случаев осложненный формированием грыжи диска, спондилолистез, стеноз спинального канала, остеопороз. Необходимо учитывать, что у ряда пациентов источником болевых ощущений могут являться воспалительные изменения позвонков или прилегающих тканей (спондилит, остеомиелит, эпидуральный абсцесс), в том числе обусловленные воздействием специфического возбудителя (например, палочки Коха). Причиной болевого синдрома может явиться первичная или метастатическая опухоль позвонков, мозговых оболочек или спинальных корешков. Наконец, боль в спине может быть не связана с патологией позвоночника, а носить отраженный характер при широком спектре соматических заболеваний, поражающих органы малого таза, тазобедренный сустав, нисходящий отдел аорты и пр. Разнообразие причин болевого синдрома требует исключительной тщательности при постановке диагноза и выработке лечебной тактики. Помимо детального анализа клинической картины заболевания и проведения радиологического исследования (включая использование компьютерной томографии – КТ и магнитно-резонансной томографии – МРТ) нередко возникает необходимость в углубленном соматическом обследовании больного.
Значимыми факторами риска развития поражения межпозвонковых дисков являются малоподвижный образ жизни с отсутствием физических нагрузок или, наоборот, повышенные физические нагрузки с повторной микротравматизацией позвоночника, воздействие вибрации, избыточная масса тела, высокий рост, повторные беременности. Большую роль играют производственные факторы – длительное пребывание в автотранспорте, частые переохлаждения, несоответствие между физическими возможностями индивидуума и объемом испытываемых нагрузок. Врожденные особенности строения скелета (асимметрия длины ног, аномалии строения тазобедренных суставов, люмбализация или сакрализация и пр.) также могут рассматриваться в качестве факторов, предрасполагающих к возникновению дегенеративных поражений позвоночника. Имеются сведения о генетической детерминированности поражения межпозвонковых дисков, в частности, обусловленной нарушением выработки коллагена 1Х типа.
Наличие длительно существующего хронического болевого синдрома в области спины или поясницы тесно ассоциировано с развитием депрессии, тревожных нарушений, при этом частота депрессивных расстройств среди больных со спондилогенными дорсопатиями в 3–4 раза выше, чем в популяции в целом. Имеется зависимость выраженности и длительности болевого синдрома и тяжести последующих нарушений двигательного стереотипа и эмоциональных расстройств. Наличие депрессивных и тревожных расстройств, в особенности в сочетании с болевым синдромом, способно не только вызывать снижение качества жизни пациентов, но и приводить к стойкой утрате трудоспособности. Даже при купировании острых болей эмоциональные расстройства могут персистировать на протяжении достаточно длительного времени, обусловливая дезадаптацию пациента.
Ведение больного в остром периоде
Основными задачами ведения больного в остром периоде болевого синдрома в рамках спондилогенной дорсопатии являются купирование болевого синдрома, восстановление нормальной биомеханики позвоночника, создание условий для проведения полноценного курса реабилитационных мероприятий. Максимально раннее и полное купирование болевого синдрома способно предупредить фиксацию патологического двигательного стереотипа, обеспечить возможность раннего проведения реабилитационных мероприятий. Кроме того, своевременное устранение болевых ощущений обеспечивает, с одной стороны, возможность для раннего подключения двигательной терапии и его активизации, а с другой – предупреждает становление эмоциональных расстройств. В настоящее время целесообразность выбора терапевтической тактики, препятствующей хронизации патологического процесса, не вызывает сомнений.
С целью устранения патогенных физических факторов, способных вызвать усиление болевого синдрома, показано обеспечение щадящего двигательного режима, полное исключение или ограничение физических нагрузок («лучше три дня лежать, чем неделю лечиться»). Желательно обеспечение щадящего режима в домашних условиях или неврологическом стационаре. Пациент должен избегать флексорных или ротационных движений в поясничном отделе позвоночника, в особенности выполняемых в быстром темпе или с дополнительными физическими нагрузками. При невозможности госпитализации следует обеспечить иммобилизацию соответствующего отдела позвоночника при помощи ортезов, фиксирующих поясов (корсетов), снабженных вертикальными ребрами жесткости. В острой стадии заболевания, характеризующейся наличием выраженного болевого синдрома, как правило, нецелесообразно проведение активных гимнастических упражнений, ручного массажа, а также применение тепловых процедур, сеансов мануальной терапии. В то же время при относительно нетяжелых обострениях, в случае умеренно выраженного болевого синдрома, при преобладании мышечно-тонических расстройств, можно достичь положительного эффекта проведением постизометрической релаксации.
НПВП и анальгетики
На сегодняшний день не вызывает сомнения целесообразность применения нестероидных противовоспалительных препаратов (НПВП) для лечения пациентов с спондилогенной дорсопатией. Эффективность такого подхода установлена в ходе целого ряда клинических исследований. Характерной особенностью фармакологического действия этих препаратов является способность угнетать активность циклооксигеназы-2 (ЦОГ-2) – ключевого фермента синтеза простагландинов, простациклинов и тромбоксанов. Известна роль ЦОГ-2 в качестве важнейшего катализатора в процессе метаболизма арахидоновой кислоты, который сопровождается образованием медиаторов отека и воспаления. Оказывая влияние на болевые окончания в очаге повреждения, простагландины повышают их чувствительность к брадикинину – пептиду, образующемуся в тканях при воспалении и одновременно являющемуся стимулятором болевых окончаний.
Вместе с тем торможение активности ЦОГ-2 при болевых синдромах, связанных с различной степени выраженности воспалительным процессом, не является единственным анальгетическим механизмом НПВП. Различная выраженность способности подавлять синтез простагландинов, наблюдающаяся у препаратов этой группы, диссоциация между противовоспалительным и анальгетическим эффектами НПВП позволяют предполагать существование иных механизмов реализации обезболивающих эффектов при спондилогенных дорсопатиях. Кроме того, не выявлено прямой зависимости между степенью подавления синтеза медиаторов воспаления, с одной стороны, и анальгетической активностью препаратов – с другой.
Несомненными преимуществами фармакокинетики лекарственных средств данной группы являются короткий период полувыведения, отсутствие аккумуляции и энтеропеченочной рециркуляции, длительное накопление в области воспаления. Благодаря этим качествам лекарства имеют хорошее соотношение польза/риск. Быстрота наступления обезболивающего действия служит основанием для назначения этих средств в первую очередь для купирования острых болевых синдромов различной интенсивности. Наиболее распространенными препаратами этой группы являются диклофенак, кеторолак, производные оксикамов (пироксикам, лорноксикам), производные пропионовой кислоты (ибупрофен, флурбипрофен, кетопрофен, напроксен).
Широко применяемый диклофенак характеризуется хорошей переносимостью, сочетающейся с выраженным обезболивающим эффектом. В клинической практике удобно использование пролонгированной формы диклофенак-ретард, содержащей 100 мг активного вещества. Прием пищи не оказывает клинически значимого влияния на всасывание активного вещества из таблеток ретард и его системную биодоступность. Степень абсорбции находится в прямой зависимости от дозы препарата. Среднее значение максимальной концентрации препарата в плазме достигается в среднем через 4 ч и сохраняется в течение 24 ч.
Производные пропионовой кислоты имеют малый период полувыведения, составляющий порядка 4 ч, и характеризуются хорошей переносимостью при относительно низком риске побочных эффектов. Эти препараты быстро всасываются в кишечнике и быстро элиминируются, не кумулируются при нарушении метаболических процессов. Они обладают умеренной ингибирующей активностью на синтез простагландинов, поэтому по своему противовоспалительному действию уступают диклофенаку, индометацину и фенилбутазону. В связи с этим целесообразно их применение при относительно нетяжелых дорсопатиях с умеренным болевым синдромом.
К сожалению, подавляющее большинство НПВП обладает ульцерогенным действием, что заставляет в каждом индивидуальном случае решать вопрос о целесообразности их применения и способе введения в организм. Отсутствие заболеваний желудочно-кишечного тракта допускает возможность перорального приема. Считается, что риск возникновения гастропатии, обусловленной приемом НПВП, достоверно выше у лиц в возрасте старше 65 лет, при длительном (более 3 мес) приеме НПВП, в особенности при применении двух препаратов и более из этой группы, одновременном приеме кортикостероидов и непрямых антикоагулянтов и, соответственно, у больных язвенной болезнью желудка в анамнезе. Вероятными факторами риска являются женский пол, курение, злоупотребление алкоголем, наличие хеликобактерной инфекции. В качестве профилактических мероприятий, снижающих риск поражения слизистой оболочки желудка, могут быть использованы ингибиторы протонной помпы (омепразол по 20 мг 1 раз в сутки) или блокаторы Н2-гистаминовых рецепторов (ранитидин по 300 мг в сутки), а также антацидные препараты.
При плохой переносимости НПВП, наличии хронического гастрита, перенесенной язвенной болезни применение таблетированных лекарственных форм исключено. В этом случае возможно их парентеральное (внутримышечное) или ректальное (в виде свечей) введение. Использование ректальных суппозиториев характеризуется высокой скоростью всасывания (она может соответствовать таковой при пероральном приеме или быть незначительно ниже ее). Так, после ректального введения 50 мг диклофенака максимальная концентрация его в плазме достигается в среднем в пределах 1 ч. К сожалению, угроза обострения желудочно-кишечной патологии полностью не исключается и в этой ситуации.
В последнее время широкое распространение получили трансдермальные формы НПВП (мази, кремы, гели). Необходимо четко представлять, что биодоступность препаратов при локальном введении, как правило, на порядок ниже, чем при пероральном применении. Серьезным недостатком трансдермальных лекарственных форм является малая концентрация действующего вещества и ограниченность прохождения препарата непосредственно к патологическому очагу. Большинством исследователей признается целесообразность применения трансдермальных форм при умеренно выраженных болевых синдромах, тогда как при выраженном болевом синдроме их эффективность явно недостаточна. Выраженный обезболивающий эффект проводимого лечения может быть достигнут при многократном (не менее 4–6 раз в сутки) нанесении препарата.
Большое внимание привлекают селективные ингибиторы ЦОГ-2, обеспечивающие ингибирование синтеза медиаторов воспаления и не оказывающие влияния на продукцию простаноидов (целекоксиб, нимесулид). Несомненным достоинством этих препаратов является относительно низкий риск поражения слизистой оболочки желудка и двенадцатиперстной кишки. Вместе с тем их обезболивающий эффект в острой стадии спондилогенной дорсопатии не всегда достаточен, что требует продления курса терапии или повышения доз препаратов.
Сроки применения НПВП и анальгетиков определяются интенсивностью болевого синдрома, курс их приема прекращается по мере достижения эффекта. Следует отметить нецелесообразность «профилактического» применения НПВП у больных со спондилогенными дорсопатиями при отсутствии болевого синдрома – убедительных подтверждений превентивного эффекта не получено, тогда как риск осложнений возрастает значительно.
Повышение эффективности применения НПВП может быть достигнуто за счет комбинирования лекарственных препаратов, воздействующих на различные звенья патогенеза болевого синдрома. Наблюдающаяся при этом потенциация эффекта позволяет использовать относительно низкие дозы препаратов и минимизировать фармакологическую нагрузку на организм пациента. С этой целью у некоторых пациентов может быть использовано внутривенное капельное введение смеси из обезболивающих препаратов, седативных, мочегонных средств. Помимо взаимно потенцирующего действия адекватно подобранных компонентов «коктейля», нельзя исключить психотерапевтического действия указанного способа лечения.
Миорелаксанты
Хорошим терапевтическим эффектом обладает комбинация обезболивающих средств с миорелаксантами, уменьшающими выраженность мышечно-тонических проявлений. Указанный комплекс может быть эффективным как при компрессионных, так и при рефлекторных синдромах. В качестве препаратов, снижающих повышенный мышечный тонус, используются производные бензодиазепинов (диазепам, тетразепам), толперизон, тизанидин. Тизанидин помимо расслабляющего действия на поперечнополосатую мускулатуру обладает умеренным гастропротективным действием. Механизм подобного эффекта не вполне ясен, хотя имеются данные о том, что препарат, оказывая влияние через центральные альфа-адренергические пути, тормозит выработку желудочного секрета, предотвращает изменения гликопротеинов, обусловленные действием ацетилсалициловой кислоты или НПВП, и повреждение слизистой оболочки желудка. Учитывая то, что практически все миорелаксанты в той или иной степени обладают седативным эффектом, следует информировать пациента о возможных побочных эффектах – сонливости, снижении концентрации внимания, заторможенности. Нередко выраженность этих эффектов ограничивает применение данной группы препаратов в амбулаторных условиях.
Противоотечная терапия
В ряде случаев компрессионный синдром сопровождается локальным венозным полнокровием, отеком корешка и окружающих его тканей, что делает целесообразным включение в терапевтический комплекс диуретиков (салуретиков или осмотических) и, в отдельных тяжелых случаях, кортикостероидов. Из гормональных препаратов обычно используются преднизолон (40–60 мг в сутки) или дексаметазон (4–8 мг в сутки) на протяжении 3–5 дней с последующей быстрой отменой. Необходимо учитывать повышенный риск осложнений со стороны желудочно-кишечного тракта при одновременном применении кортикостероидов и НПВП. В ряде стран применяется эпидуральное введение кортикостероидов. Получены данные об эффективности данного способа лечения у пациентов с остро развившимся болевым синдромом. Менее обосновано эпидуральное введение препаратов при умеренно выраженных болях в пояснице и нижней части спины, а также при их хроническом или подостром характере заболевания.
Комбинированные препараты
Удачной комбинацией лекарственных средств, обладающих обезболивающим и противоотечным действием, положительным образом влияющих на обмен веществ в периферическом нерве и окружающих тканях, является препарат «Амбене». Выпускается в виде готового для употребления двухкамерного шприца для инъекций, первая камера которого содержит 2 мл раствора фенилбутазона (375 мг) и 3,5 мг дексаметазона, вторая – 1 мл цианокобаламина (2,5 мг). Кроме того, в состав амбене входит лидокаин, добавление которого обеспечивает уменьшение болевых ощущений непосредственно в месте введения. Растворы смешиваются непосредственно перед употреблением. Лечебное воздействие компонентов, входящих в состав амбене, потенцируются, за счет чего обеспечивается быстрый и стойкий обезболивающий эффект.
Фенилбутазон представляет собой НПВП пиразолонового ряда, который за счет ингибирования активности ЦОГ уменьшает продукцию простагландинов и оказывает обезболивающее и противовоспалительное действие. Выраженный анальгетический эффект сочетается с хорошей переносимостью, благодаря чему суточная доза может составлять до 1200–1600 мг. Дексаметазон является синтетическим глюкокортикоидом с мощным противовоспалительным, противоаллергическим, десенсибилизирующим, а также противоотечным действием. Основные клинические эффекты реализуются вследствие угнетения высвобождения медиаторов воспаления эозинофилами, мембраностабилизирующего действия, уменьшения количества тучных клеток. Цианокобаламин (витамин В12) участвует в метаболизме целого ряда биологически активных веществ, обладает высокой биологической активностью, в том числе в отношении метаболических процессов в периферической нервной системе.
Амбене оказывает выраженный обезболивающий эффект у больных со спондилогенной дорсопатией, при этом отличается хорошей переносимостью. Препарат вводится внутримышечно 1 раз в сутки не чаще 1 раза в 2–3 дня. Следует учитывать, что отдельные компоненты препарата способны вызывать нежелательные побочные эффекты. Как и прочие НПВП, фенилбутазон оказывает ульцерогенное действие, относительно редко наблюдаются кожные проявления (крапивница, сухая экзема). Дексаметазон характеризуется низкой частотой возникновения побочных эффектов, вместе с тем необходимо иметь в виду возможность снижения толерантности к глюкозе, повышение риска развития эрозивно-язвенных поражений желудка и двенадцатиперстной кишки. Исходя из этого, амбене не следует применять у больных с острыми заболеваниями желудка и двенадцатиперстной кишки, нарушением обмена углеводов (снижение толерантности к глюкозе), индивидуальной непереносимости его отдельных компонентов.
Купирование как компрессионных, так и рефлекторных болевых синдромов может быть достигнуто применением блокады болезненных мышечных групп или триггерных точек. Технически правильно выполненные, эти манипуляции обладают достаточной эффективностью и не вызывают значимых осложнений. Требуется аккуратность при выполнении паравертебральных блокад во избежание травматизации спинальных корешков. Используются комбинации раствора анестетика (новокаин, лидокаин) и небольшой дозы кортикостероида (суспензия гидрокортизона, бетаметазона дипропионат). Локальное введение препаратов, обладающих системным, а не местным действием (антиагреганты, вазоактивные препараты, миорелаксанты и пр.), а также не обладающих способностью к депонированию в ткани, нецелесообразно. К сожалению, эффект, оказываемый блокадами в отношении болевого синдрома, не носит стойкого характера, в связи с чем возникает необходимость повторных манипуляций.
В ряде случаев применение НПВП, даже в комбинации с миорелаксантами, не оказывает должного положительного эффекта. Хронизация болевого синдрома сопровождается эмоциональными расстройствами, в частности с преобладанием депрессивных реакций, что диктует необходимость расширения фармакотерапевтического арсенала. Исследования последних лет убедительно продемонстрировали, что хронизация боли у пациентов с поясничными болями обусловлена причинами скорее психологическими, чем биомеханическими (т.е. связанными непосредственно с патологией позвоночника и корешков). Следствием этого является увеличение сроков процесса выздоровления, резкое ограничение возможности двигательной реабилитации больных, нарушение взаимодействия в системе «врач–пациент». Причинами, затрудняющими процесс восстановления, являются убежденность пациента в наличии прогрессирующего органического поражения позвоночника, в необходимости полного ограничения физических нагрузок, нарушения социальных функций, связанных с заболеванием, ориентация на пассивное (лекарственное, физиотерапевтическое), но не активное лечение (дозированные физические нагрузки, специальные упражнения). Мощным лечебным инструментом в этой ситуации является проведение разъяснительной психотерапии, формирование у больного оптимистических взглядов на перспективы лечения, выработка стратегии поведения на будущее (оптимальный объем и характер трудовых и бытовых нагрузок, проведение профилактических мероприятий и пр.).
Антидепрессанты и антиконвульсанты
В этой ситуации к лечению могут быть подключены антидепрессанты, причем желательно использовать препараты, оказывающие седативный и миорелаксирующий эффект (например, амитриптилин). Противоболевым эффектом обладает карбамазепин – эффективный антиконвульсант из группы производных иминостильбена. Препарат инактивирует натриевые каналы, угнетает высвобождение возбуждающих нейротрансмиттеров в синаптическую щель, вызывая снижение синаптической передачи. Помимо основного противосудорожного и обезболивающего действия препарат обладает антипсихотическим и антиманиакальным эффектами. Высказывается предположение о том, что положительный эффект карбамазепина у пациентов со спондилогенными дорсопатиями может быть опосредован воздействием на центральные ноцицептивные механизмы, нормализацией мышечного тонуса. Дозирование препарата осуществляется индивидуально, в зависимости от переносимости, а также от характера двигательного режима. Побочные эффекты (в первую очередь сонливость, нарушение концентрации внимания) требуют аккуратности в подборе дозы препарата, в особенности в амбулаторных условиях. Вероятность указанных расстройств возрастает при одновременном назначении седативных средств, антидепрессантов, некоторых миорелаксантов. Убедительных данных о целесообразности применения прочих антиконвульсантов не получено, хотя исследования такого рода проводятся.
В комплекс терапевтических мероприятий должны быть включены и немедикаментозные методы лечения – физиотерапия (фоно- или электрофорез лекарственных препаратов, воздействие электрическими токами специально подобранной конфигурации, частоты и напряжения, низкоэнергетическое лазерное излучение). Обезболивающим эффектом обладает рефлексотерапия в различных модификациях (традиционная акупунктура, электро- и лазеропунктура). Следует отметить значительные трудности при сравнении результатов применения различных физиотерапевтических методов лечения, явную недостаточность исследований их эффективности, удовлетворяющих требованиям доказательной медицины.
Имеющиеся на сегодняшний день данные свидетельствуют о существовании значительного арсенала фармакотерапевтических и нелекарственных способов купирования болевого синдрома у больных спондилогенными дорсопатиями. Представляется желательным индивидуальный выбор терапевтической тактики с использованием комбинации различных препаратов, их дозировок и способов введения. Сочетанное применение различных способов лечения позволяет повысить эффективность лечения и уменьшить фармакологическую нагрузку на организм. По мере купирования болевого синдрома абсолютно необходимым является использование методов восстановительной терапии, лечебной гимнастики, направленной на формирование мышечного корсета, укрепление мускулатуры брюшной стенки и спины. Не менее важным является обучение больного навыкам повседневной двигательной активности – формирование двигательного стереотипа, предупреждающего возникновение болевых ощущений.