Дексаметазон перед химиотерапией для чего
Дексаметазон перед химиотерапией для чего
Тошнота и рвота, обусловленная химиотерапией, относится к числу наиболее тяжело переносимых осложнений для больного. К высокоэметогенным режимам относятся комбинации на основе цисплатина и доксорубицина (АС или FAC), которые широко используются при проведении адъювантной терапии у больных раком молочной железы. Для профилактики острой тошноты и рвоты (в первые 24 часа после введения препаратов) рекомендуется использовать комбинацию антагонистов рецепторов серотонина (например, ондансетрон) и нейрокинина-1 (апрепитант) совместно с дексаметазоном. Эта тройная комбинация успешно справляется с острой тошнотой и рвотой у большинства больных. Проблемой остается отсроченная тошнота и рвота, возникающая на вторые сутки и далее после введения препаратов.
Исторически для купирования отсроченной тошноты и рвоты использовали дексаметазон. В 2006 году Международная организация по сопроводительной терапии при злокачественных опухолях (MASCC) рекомендовала назначение дексаметазона или апрепитанта для купирования отсроченной тошноты и рвоты. Включение апрепитанта было обосновано его способностью уменьшать частоту развития отсроченной тошноты и рвоты по сравнению с ондансетроном при профилактике острой рвоты у больных, получавших цисплатин-содержащие режимы. С учетом того, что ондансетрон оказывает минимальное влияние на профилактику отсроченной тошноты и рвоты, реальная эффективность апрепитанта не была установлена.
Это послужило основанием для проведения исследования для оценки способности апрепитанта в сравнении с дексаметазоном предотвращать развитие отсроченной тошноты и рвоты у больных раком молочной железы, которые получали комбинацию доксорубицина и циклофосфамида (60/600 мг/м 2 ). Все больные получали одинаковую профилактику острой тошноты и рвоты, которая подразумевала назначение апрепитанта в дозе 125 мг внутрь за час до введения химиотерапии, палоносетрона 0,25 мг в/в струйно и дексаметазон 8 мг в/в капельно за 30 минут до введения. В дальнейшем пациенты были рандомизированы в две группы, одна из которых получала дексаметазон 4 мг внутрь 3 раза в день 2-3 дни, а другая апрепитант 80 мг внутрь на 2 и 3 дни. Лечение было двойным слепым. Основным критерием эффективности была частота отсутствия тошноты и рвоты на 2-5 дни после проведения терапии.
В исследование была включена 551 больная, из которых 273 получали дексаметазон, а 278 – апрепитант. Частота полного контроля острой тошноты и рвоты составила 87,6% и 84,9% в группе дексаметазона и апрепитанта соответственно. Частота отсутствия тошноты и рвоты в период 2-5 дней лечения составила 79,5% для обеих групп. Одновременно отмечена тенденция возникновения более выраженной тошноты и рвоты большей продолжительностью с большим числом эпизодов рвоты в группе апрепитанта по сравнению с дексаметазоном. В группе дексаметазона достоверно чаще отмечали развитие бессонницы и сердцебиений, а в группе апрепитанта – потерю аппетита и сонливость. Качество жизни в обеих группах существенно не отличалось.
Результаты исследования убедительно демонстрируют равную эффективность дексаметазона и апрепитанта для профилактики отсроченной тошноты и рвоты у больных, получивших комбинацию доксорубицина и циклофосфамида. Важным итогом данного исследования является изменение рекомендаций MASCC по профилактике отсроченной тошноты и рвоты. Вместо прежней рекомендации использовать дексаметазон либо апрепитант следует использовать дексаметазон. Несмотря на равную частоту полного контроля тошноты и рвоты в обеих группах, в группе дексаметазона отмечено меньшее число эпизодов рвоты с меньшей продолжительностью. Другим преимуществом дексаметазона является цена, которая примерно в 10 раз ниже, чем у апрепитанта. Остается неизвестным, способна ли комбинация дексаметазона и апрепитанта улучшить частоту контроля отсроченной тошноты и рвоты по сравнению с только дексаметазоном.
Ключевые слова: тошнота и рвота, дексаметазон, апрепитант, рак молочной железы.
Библиотека
ПРОФИЛАКТИКА РВОТЫ, ОБУСЛОВЛЕННОЙ ПРОВЕДЕНИЕМ ХИМИОТЕРАПИИ
И РАДИОТЕРАПИИ: РЕЗУЛЬТАТЫ ПЕРУДЖИЙСКОЙ МЕЖДУНАРОДНОЙ
ПРОТИВОРВОТНОЙ КОНСЕНСУСНОЙ КОНФЕРЕНЦИИ
The Antiemetic Subcommittee of the Multinational Association of Supportive Care in Cancer (MASCC)
Annals of Oncology 17: 20–28, 2006
Перевод – Жуков Н.В.
СТЕПЕНЬ ЭМЕТОГЕННОСТИ ХИМИОПРЕПАРАТОВ
Под степенью эметогенности понимается риск развития рвоты у больных, получающих тот или иной цитостатик без противорвотной терапии. Например, высокая степень эметогенности подразумевает, что более 90% больных, получающих терапию данным препаратом, будет иметь тошноту и рвоту в отсутствие адекватной противорвотной терапии.
Определение эметогенности химиопрепаратов имеет как минимум две цели. Во-первых, это позволяет систематизировать рекомендации по противорвотной терапии для различных видов цитостатиков. Во-вторых, более рационально организовывать последующие исследования по противорвотной терапии. До настоящего времени было предложено несколько классификаций эметогенности химиопрепаратов, разделявших их на несколько групп (от 3 до 5). [1, 2].
К сожалению, существовавшие до настоящего времени классификации были не лишены ряда существенных недостатков. Большинство классификаций не делали различия между различными типами рвоты: острой, отсроченной и предшествующей. Ни в одной из классификаций не оценивалась тошнота, и лишь некоторые из них обращали внимание на важность факторов, связанных с режимом лечения и/или специфическими особенностями пациента (доза химиопрепаратов, скорость введения, путь назначения, пол и возраст пациента, потребление алкоголя в анамнезе и т.д.)[1, 2].
Новую проблему для оценки степени эметогенности представляют и бурно развивающиеся в настоящее время направления – пероральная цитостатическая терапия и целевая (target) терапия, обычно предусматривающие длительное назначение препаратов. В такой ситуации (если препарат назначается перорально на протяжении нескольких дней или недель) различие между острой и отсроченной рвотой теряются. Hesketh et al. [3] предложили определять степень эметогенности исходя из риска развития острой рвоты после использования цитостатиков в монотерапии (с учетом дозы препаратов и пути их введения). Данная классификация с определенными изменениями была принята консенсусной конференцией в качестве рабочей.
По классификации, принятой консенсусной конференцией, внутривенные цитостатики разделены на 4 группы по риску развития рвоты: высокоэметогенные, среднеэметогенные, низкоэметогенные и минимально эметогенные (Таблица 1). Отдельно указываются препараты для перорального приема, которые также разделены на 4 группы (Таблица 2). В связи с тем, что пероральные препараты чаще назначаются в течение нескольких дней или даже недель, определение их эметогенности указано только по отношению к начальному периоду приема. Степень эметогенности и, соответственно, противорвотные режимы для пероральных цитостатиков могут различаться с рекомендованными для однократного внутривенного их использования.
Таблица 1.
Эметогенность внутривенных противоопухолевых препаратов при назначении в виде монотерапии однократно.
Правила проведения химиотерапии: что нужно знать пациенту
Лекарственную противоопухолевую терапию получают практически все пациенты, болеющие злокачественными новообразованиями. Особенностью этого лечения является его длительность и повторяемость. Отдельные курсы введения препарата проводятся на протяжении нескольких лет, иногда в течение всей жизни больного. Какие правила необходимо соблюдать при получении этого вида лечения, чтобы сохранить качество жизни, рассказала кандидат медицинских наук Елена Викторовна Ткаченко – онколог, химиотерапевт, заведующая отделением краткосрочной химиотерапии НМИЦ онкологии имени Н.Н. Петрова.
– Елена Викторовна, когда применяют химиотерапевтическое лечение?
– Химиотерапию применяют на разных стадиях онкологического заболевания: на начальной стадии проводят предоперационную (неоадъювантную) и послеоперационную (адъювантную) терапию, также на более поздних стадиях, когда оперативное вмешательство по каким-то причинам уже невозможно. Противоопухолевая лекарственная терапия проводится и тогда, когда заболевание вернулось после радикального лечения. Поэтому многие наши пациенты получают это лечение и месяцы, и годы. И в этом нет ничего страшного или удивительного. Например, пациенты с сахарным диабетом, гипертонической или ишемической болезнями постоянно соблюдают определенные условия жизни и принимают специальные препараты. Так и онкологическое заболевание является хроническим, и, к сожалению, нередко даже после завершения лечения, через некоторое время вновь приходится его возобновлять.
– Какие побочные действия у химиотерапии?
– Побочные действия свойственны всем видам противоопухолевого лечения, даже если оно проводится по современным стандартам. Это связано с механизмом действия противоопухолевых препаратов. Осложнения бывают четырех степеней: побочные эффекты первой и второй степени больше тревожат самих пациентов, но врачи к ним относятся спокойно, потому что эти осложнения часто неизбежны и угрозы для жизни не представляют. В основном это изменения самочувствия пациента и лабораторных показателей, нетребующие лечения, например, выпадение волос или некоторое снижение лейкоцитов по результатам анализов. К третьей и четвертой степеням относятся так называемые жизнеугрожающие осложнения, они требуют серьезного внимания со стороны лечащего врача.
– Лекарственное противоопухолевое лечение пациент в основном получает через вену. Есть ли способы подготовить вены, чтобы избежать возможных побочных эффектов?
– Да, существует ряд рекомендаций, выполняя которые пациент может научиться тренировать свои вены перед введением препаратов.
– Какие побочные эффекты от введения препаратов бывают?
– При внутривенном введении цитостатиков нередко развиваются воспалительно– склеротические реакции со стороны вен. Они проявляются разнообразно: от выраженной боли по ходу сосудов уже во время инъекции до подострых флебитов, тромбофлебитов, флеботромбозов с исходом в облитерацию вен, иначе говоря, зарастание вены. При длительном введении фторурацила стенки сосудов пропитываются препаратом. Этот побочный эффект возникает практически в 100% случаев при применении некоторых препаратов. Зуд и эритема кожи по ходу вены во время введения цитостатиков отмечаются примерно в 3% инфузий, они проходят в течение 30 минут без осложнений и не свидетельствуют о подтекании препарата. Попадание под кожу раздражающих препаратов (цисплатин, дакарбазин, этопозид, фторурацил, паклитаксел, винорельбин) может вызвать жгучую боль и покраснение в месте инъекции, но если принять правильные меры, то к некрозу это не приведет.
– Существуют способы избежать осложнений или их облегчить?
– Медицинский персонал знает, как профилактировать осложнения со стороны вен. Полезно это знать и пациентам. Дело в том, что инъекции растворов цитостатиков вводятся только в минимально допустимых концентрациях. Капельные инфузии с большим количеством жидкости служат лучшим способом предупреждения повреждений стенки вен (только в случаях, когда это рекомендовано как способ введения цитостатика). Если препарат необходимо вводить струйно, то его разводят в 20-30 мл рекомендуемого растворителя, а после инъекции промывают вены изотоническим раствором NaCl. При попадании некоторых препаратов под кожу возникает гиперемия, воспаление. В трети случаев может возникнуть некроз, который без вмешательства не заживет. В этом случае необходимо обратиться за хирургической помощью.
– Что нужно делать, если химиопрепарат всё-таки попал под кожу?
– Подачу препарата необходимо остановить, но иглу или катетер вытаскивать из вены не нужно, через них медсестра извлечет попавший под кожу препарат. Для некоторых химиопрепаратов существуют антидоты (противоядия), но, к сожалению, есть они не для всех препаратов. Антидотом медсестра обколет место инъекции, а затем уже удалит из вены иглу или катетер. Пораженной конечности следует придать приподнятое положение на 48 часов, чтобы уменьшить риск воспаления и отека. Для этого достаточно закрепить руку в согнутом положении с помощью перевязки или косынки.
При попадании под кожу таких препаратов как винкристин, винбластин, винорельбин, этопозид прикладывают теплый компресс на 15-20 минут не менее четырех раз в сутки в течение 24- 48 часов. При воспалительной реакции возможна аппликация гидрокортизоновой мази.
Если развился флебит (т.е. воспаление вены), то он лечится по таким же принципам, как и обычные флебиты вне химических ожогов: применяются низкомолекулярные гепарины, антикоагулянты непрямого действия, антиагреганты.
– Почему лекарственное противоопухолевое лечение можно получать только в специализированных клиниках?
– Дело в том, что у каждого препарата свой срок и скорость введения, и для дробного и длительного введения применяется специальное оборудование. Именно поэтому ни в коем случае нельзя капать химиотерапию дома или в поликлинике, где не знают, что такое противоопухолевая лекарственная терапия. Давно уже, по крайней мере, в Санкт-Петербурге, комитетом по здравоохранению врачам, медсестрам запрещено капать противоопухолевые препараты на дому после смерти нескольких пациентов. Вы можете проводить химиотерапию только в специализированной клинике, где можно быть уверенным, что врач и медсестра понимают, что делают. Препараты должны определенным образом разводиться, капаться, храниться, их нельзя смешивать. Есть только пара препаратов, которые смешивают в одном флаконе. Все остальные должны капаться поочередно, да еще и между препаратами необходимо промывать систему физраствором. Каждый препарат должен разводиться определенным раствором: глюкозой, раствором Рингера, водой для инъекций или физраствором. Это сложная наука.
– Какое оборудование для введения препаратов сегодня используется?
– Существует несколько типов медицинского оборудования для длительного и дробного введения препаратов. Например, перфузоры – это устройства, позволяющие вводить медикаментозные препараты и растворы с исключительно высокой точностью. Порой счёт идет на десятые доли миллилитров в час (особенно часто это применяется в отделении реанимации, где скорости введения медикаментов, как правило, 1 мл/час, 5.6 мл/час и т.д.). Перфузоры могут быть механическими или электронными. Они имеют несколько названий: инфузоматы, линеаматы, шприцевые насосы, шприцевые дозаторы и др. Есть микроинфузионная помпа (инфузор) – безопасное и эффективное медицинское изделие, предназначенное для длительного, дозированного, контролируемого введения лекарственных препаратов, используемых в медикаментозной терапии (в том числе и химиотерапии). Как правило, такие помпы называют инфузор или инфузомат. Так же можно встретить названия: шприцевой насос, дозатор медицинский, инфузионный насос и др.
При использовании микроинфузионной помпы обеспечивается постепенное поступление препарата в организм за счет механизма сокращения резервуара и трубки инфузора.
– Какие правила введения противоопухолевых препаратов должен знать пациент?
– Введение противоопухолевых препаратов должно выполняться только в отделениях, специализирующихся на цитотоксической химиотерапии исключительно под наблюдением компетентного врача. Этот метод лечения требует специальной подготовки, тщательности при приготовлении растворов препаратов и соблюдения всех правил их введения, указанных в инструкциях. Поэтому к выполнению работ с цитостатиками должны допускаться медицинские сестры, прошедшие специальную подготовку, обученные безопасным методам и приемам работы. Также необходимо соблюдать последовательность и скорость введения препаратов, учитывать химические свойства при использовании оборудования для их введения. Соблюдать правила и сроки хранения препаратов как в аптечной упаковке, так и после их приготовления. Ни в коем случае нельзя смешивать препараты «в одном флаконе», если в инструкции по применению данных препаратов нет для этого особых указаний. Необходимо знать и соблюдать все условия хранения препарата и его транспортировки, если он приобретается и доставляется в клинику самим пациентом. Это очень важно. Потому что многие пациенты говорят: «Я куплю, привезу, а вы мне прокапайте!» Если вы купите, например, герцептин в аптеке и привезете его к нам не в холодильнике, а в обычной упаковке, что мы получим? В лучшем случае – воду. В случае личного приобретения препаратов уточните правила хранения и транспортировки у своего врача.
– Какие способы внутривенной доставки препаратов сегодня используются?
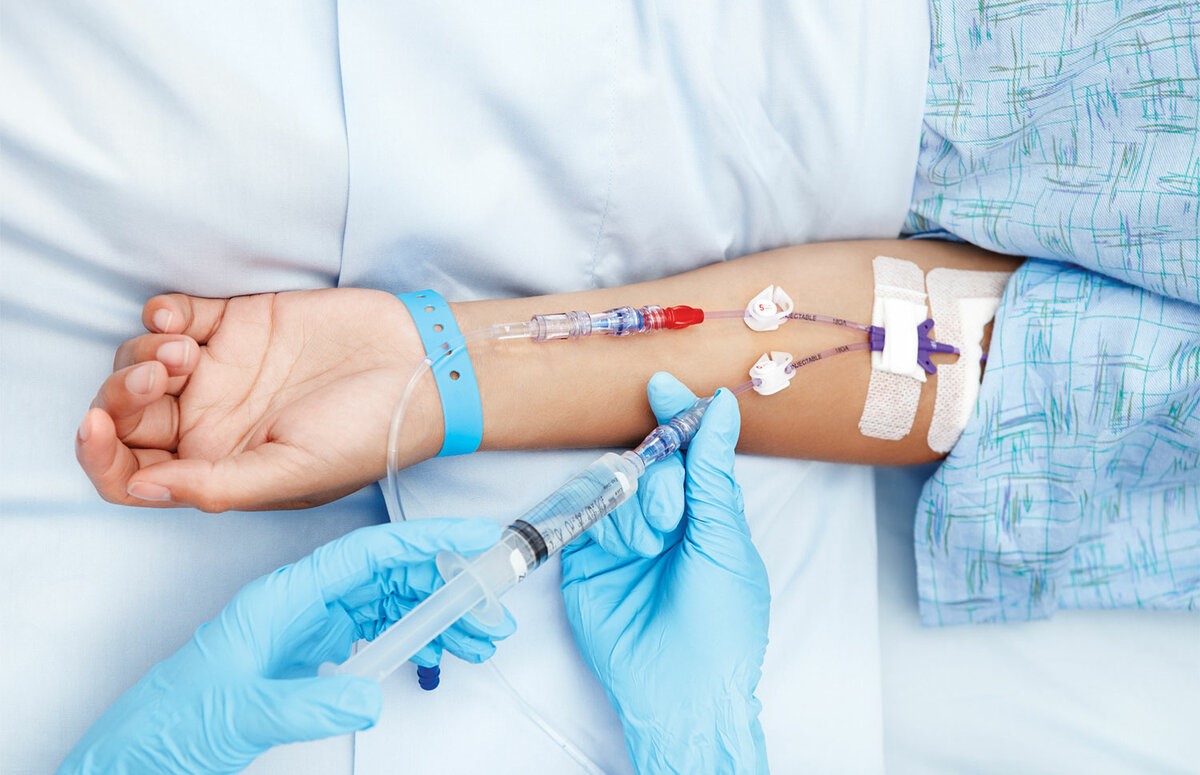
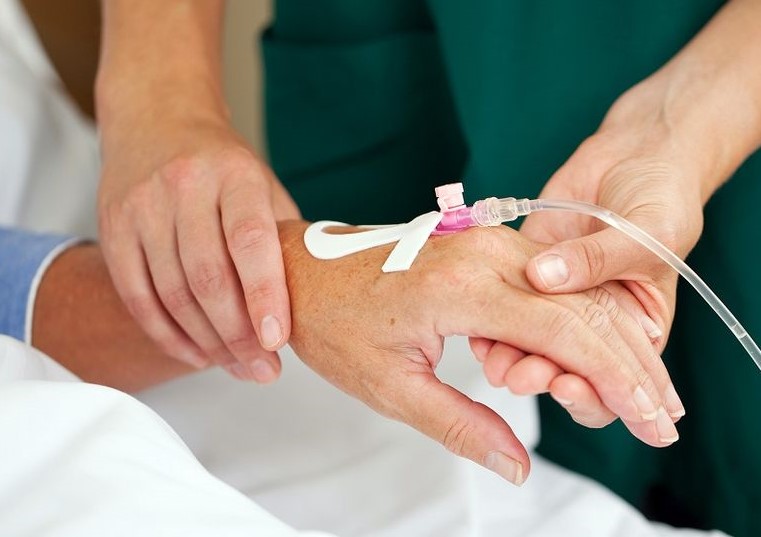
– На сегодняшний день существует несколько способов: через иглу, переферический венозный катетер, центральный венозный катетер и имплантируемый порт. Вы знаете, когда я начала работать в медицине, мы работали еще многоразовыми иглами. Они были тупые, поэтому могли долго стоять в вене. А как только появились одноразовые иглы, стали возникать сложности. Они же острые, чуть пациент шевельнулся, она прокалывает вену моментально. Поэтому если необходимо вводить препарат долго, то делать это лучше через переферический венозный катетер. Если его устанавливать в асептических условиях, правильно ухаживать, то до 10 дней им можно пользоваться.
Для более длительного венозного доступа используют центральный венозный катетер, особенно в тех случаях, когда необходимо обеспечить полное парентеральное питание у хронических больных. Край центрального венозного катетера вводится в пустотелую вену. У этих катетеров много преимуществ. Но неправильный уход за ними может привести и к серьезным осложнениям. Поскольку если возникнет воспаление, то оно будет не местным, а общим. Поэтому центральный венозный катетер требует профессионального использования и тщательного ухода.
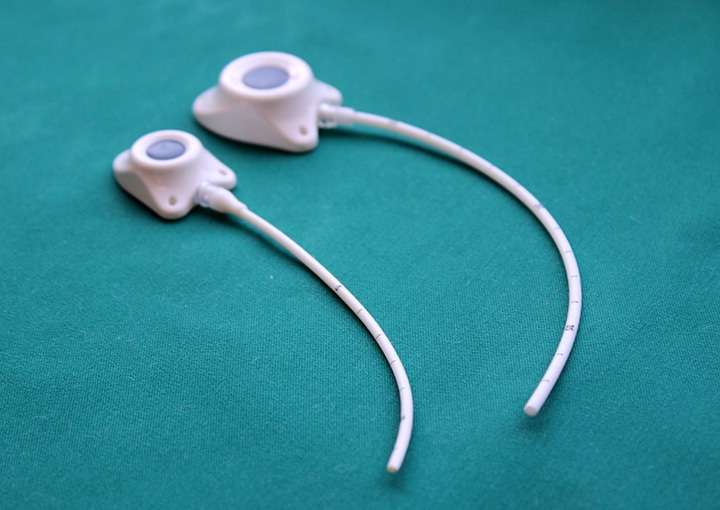
Еще существует порт-система. Это инвазионный порт, который представляет собой титановый резервуар в виде толстой монеты диаметром около 4-4,5 см и толщиной около 1 см, который покрыт изнутри биоинертным полимером. На верхней плоской части установлена мембрана из многослойного силикона, через которую вводят лекарственные препараты. Порт имеет тонкую трубочку-катетер длиной до 10-15 см, которая пропускается в яремную вену и реже в артерию.
Показания к применению порт-системы:
Есть свои противопоказания, но они все относительны, и доктора сами принимают решение, учитывать их или нет.
– Какие очевидные преимущества у порт-системы?
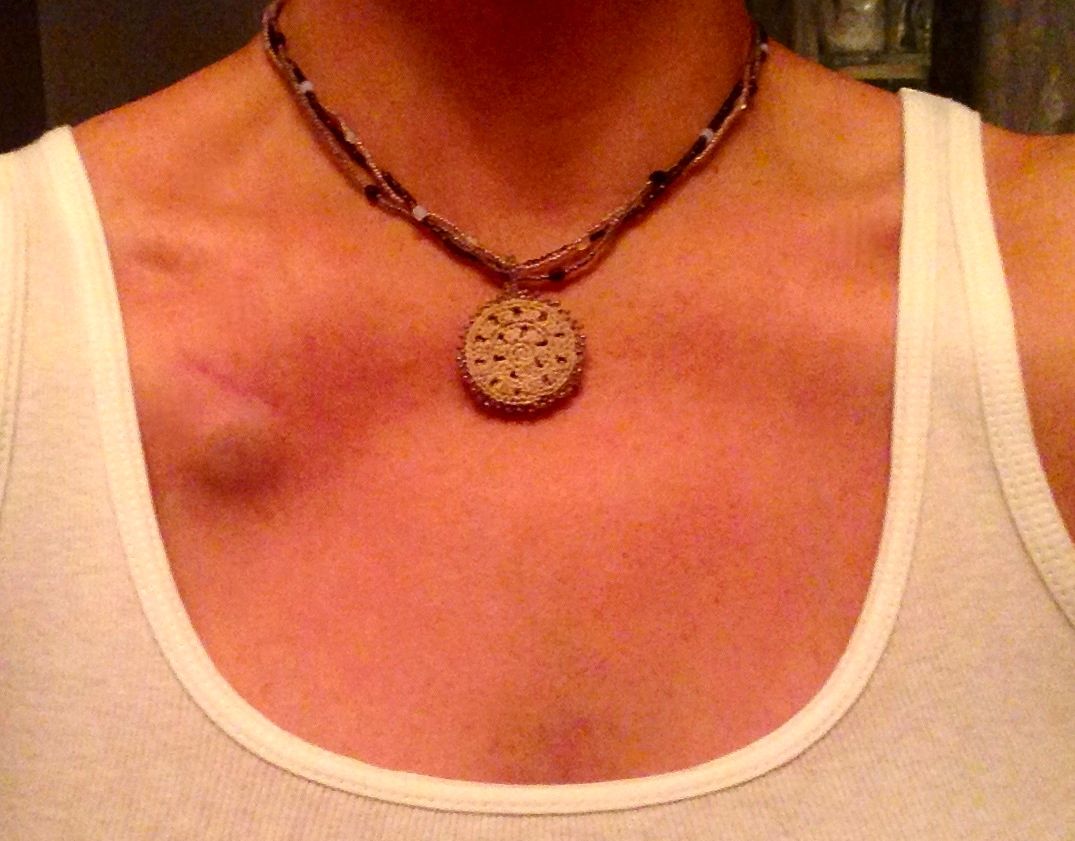
– Их много. Главное, что человек может вести привычный образ жизни. Венозный порт имплантируется под кожу пациента, он не виден снаружи, поэтому не может быть задет одеждой, инфицироваться при приеме ванны, «выскочить» из вены. Люди с установленными портами могут заниматься спортом, выполнять физическую нагрузку, плавать, путешествовать, отдыхать заграницей и т.д. Им можно проходить МРТ и КТ исследования, он совместим с магнитным полем. При правильной эксплуатации порт-система может работать 5-7 лет. Существуют наблюдения, что если за порт-системой правильно ухаживать, то фактически она может использоваться пожизненно. В некоторых странах установка порт-системы является неотъемлемой частью «золотого стандарта» лечения. В Западной Европе порты широко применяются у пациентов с впервые выявленным онкологическим заболеванием, которым планируется проведение множественных сеансов химиотерапии, особенно цитостастическими препаратами, которые вызывают повреждение периферических вен. Кроме того, инфузионные порты устанавливаются пациентам с тонкими периферическими венами на верхних и нижних конечностях. В отечественной онкологической практике порты пока используются редко.
– Как происходит установка инфузионного порта?
– Процедура имплантации порта проводится под местной анестезией и абсолютно безболезненна. Порт, как правило, имплантируется в правую подключичную область, хотя место может быть любым, главное, чтобы рядом была проходимая вена. Процедура занимает от 10 до 30 минут и не требует длительной госпитализации. Пациент находится в стационаре около часа после установки, а потом самостоятельно может ехать домой. Врач предоставляет ему необходимую информацию о правилах поведения после операции и о лекарствах, которые необходимо принимать в течение нескольких дней после процедуры.
– Как ухаживать за порт-системой?
– О каких «сигналах тревоги» должен знать пациент с установленным портом?
– Надо понимать, что при использовании порт-системы бывают и осложнения. Пациент должен насторожиться и обратиться к врачу в случае:
Источники
Материал подготовила:
НАТАЛЬЯ СУББОТИНА
специалист по связям с общественностью
НМИЦ онкологии им Н.Н. Петрова,
Кемеровский государственный университет, факультет филологии и журналистики, отделение журналистики
Материал подготовила:
ЮЛИЯ КОБЛЯКОВА
специалист по связям с общественностью
НМИЦ онкологии им Н.Н. Петрова,
Санкт-Петербургский политехнический университет Петра Великого
Кафедра рекламы и связей с общественностью
Дексаметазон Ферейн : инструкция по применению
Что такое препарат и для чего его применяют
Дексаметазон содержит действующее вещество дексаметазона фосфат, в виде дексаметазона натрия фосфата.
Фармакотерапевтическая группа
Кортикостероиды для системного применения. Глюкокортикостероид.
Код АТХ: Н02АВ02.
Дексаметазон вводят внутривенно или внутримышечно в неотложных случаях, а также при невозможности перорального применения препарата при таких состояниях:
Эндокринные нарушения: заместительная терапия первичной или вторичной (гипофизарной) недостаточности надпочечников (гидрокортизон, или кортизон являются препаратами выбора, при необходимости синтетические аналоги могут применяться вместе с минералокортикоидами; в Педиатрической практике совместное применение с минералокортикоидами чрезвычайно важно); острая недостаточность. надпочечников (гидрокортизон или кортизон являются препаратами выбора; может оказаться необходимым совместное применение с минералокортикоидами, особенно в случае применения синтетических аналогов); перед операциями и в случаях серьезных травм или заболеваний у пациентов с установленной надпочечниковой недостаточностью или при неопределенном адренокортикальном запасе; шок, устойчивый к традиционной терапии, при наличной или подозреваемой недостаточности надпочечников; врожденная гиперплазия надпочечников; негнойное воспаление щитовидной железы; гиперкальциемия, вызванная раковым поражением.
Ревматические заболевания: как вспомогательная терапия для. кратковременного применения (для выведения пациента из острого состояния или при обострении болезни) при: посттравматическом остеоартрозе; синовите при остеоартрозе; ревматоидном артрите, включая ювенильный ревматоидный артрит (в некоторых случаях может потребоваться низкодозовая поддерживающая терапия); эпикондилите; остром неспецифическом тендосиновите; остром подагрическом артрите; псориатическом артрите; анкилозирующем спондилите.
Коллагенозы: в период обострения или в отдельных случаях как поддерживающая терапия при: системной красной волчанке; остром ревматическом миокардите.
Заболевания кожи: пузырчатка; тяжелая мультиформная эритема (синдром Стивенса-Джонсона); эксфолиативный дерматит; буллезный герпетиформный дерматит; тяжелый себорейный дерматит; тяжелый псориаз; фунгоидный микоз.
Аллергические заболевания: контроль тяжелых или инвалидизирующих аллергических состояний, не поддающихся традиционному лечению: бронхиальная астма; контактный дерматит; атопический дерматит; сывороточная болезнь; хронический или сезонный аллергический ринит; аллергия на лекарства; крапивница после переливания крови; острый неинфекционный отек гортани (препаратом выбора является эпинефрин).
Глазные заболевания: тяжелые острые и хронические аллергические и воспалительные процессы с поражением глаз: поражение глаз, вызванное Herpes zoster; ирит, иридоциклит; хориоретинит; диффузный задний увеит и хориоидит; неврит зрительного нерва; симпатическая офтальмия; воспаление переднего сегмента; аллергический конъюнктивит кератит; аллергическая краевая язва роговицы, тяжелые воспалительные процессы после травм глаз и операций.
Желудочно-кишечные заболевания: для выведения пациента из критического периода при: язвенном колите (системная терапия); болезни Крона (системная терапия).
Заболевания дыхательных путей: саркоидоз; бериллиоз; очаговый или диссеминированный туберкулез легких (вместе с соответствующей противотуберкулезной химиотерапией); синдром Леффлера, не поддающийся терапии другими методами; аспирационный пневмонит.
Гематологические заболевания: приобретенная (аутоиммунная) гемолитическая анемия; идиопатическая тромбоцитопеническая пурпура у взрослых (НЕ ВВОДИТЬ ВНУТРИМЫШЕЧНО. ); вторичная тромбоцитопения у взрослых; эритробластопения (эритроцитарная анемия); врожденная (эритроидная) гипопластическая анемия.
Онкологические заболевания: паллиативное лечение лейкемии и лимфомы у взрослых; острая лейкемия у детей.
Состояния, сопровождающиеся отеком: стимулирование диуреза или. уменьшение протеинурии при идиопатическом нефротическом синдроме (без уремии) и нарушение функции почек при системной красной волчанке.
Диагностические испытания гиперфункции надпочечников
Отек головного мозга: при первичных или метастатических опухолях мозга, черепно-мозговой травме, нейрохирургическом вмешательстве, кровоизлиянии в мозг, энцефалите, менингите.
Другие показания: туберкулезный менингит с субарахноидальной блокадой или угрозой блокады (вместе с соответствующей противотуберкулезной терапией); трихинеллез с неврологическими симптомами или трихинеллез миокарда.
Показания для внутрисуставного введения или введения в мягкие ткани: как вспомогательная терапия для кратковременного применения (с целью выведения Пациента из острого состояния или при обострении болезни) при: ревматоидном артрите (тяжелое воспаление отдельного сустава); синовите при остеоартрите; остром и подостром бурсите; остром подагрическом артрите; эпикондилите; остром неспецифическом тендосиновите; посттравматическом остеоартрите.
Местное введение (введение в место поражения): келоидные поражения; локализованные гипертрофические, воспалительные и инфильтрированы поражения при опоясывающем лишае, псориазе, кольцевидном гранулеме; дисковый красный волчий лишай; липоидный атрофический дерматит Оппенгейма; локализованная алопеция.
Не применяйте препарат
Если у Вас:
острые вирусные, бактериальные или системные, грибковые инфекции (если не применяется надлежащая терапия), синдром Кушинга, вакцинация живой вакциной, амебные инфекции, глаукома, инфекционные поражения суставов и околосуставных мягких тканей, острая гнойная глазная инфекция (ретробульбарное введение), а также при кормлении грудью (за исключением неотложных случаев). Внутримышечное введение противопоказано пациентам с тяжелыми нарушениями свертывающей системы крови. Гиперчувствительность к действующему веществу или к любому из вспомогательных веществ, перечисленных в разделе 6.1.
Меры предосторожности
Применение в период беременности или кормления грудью.
Глюкокортикоиды проходят через плаценту и достигают высоких концентраций в плоде. По некоторым данным, даже фармакологические дозы глюкокортикоидов могут повысить риск недостаточности плаценты, олигогидрамниоза, замедленного развития плода или его внутриутробной смерти, повышение количества лейкоцитов (нейтрофилов) у плода и недостаточности надпочечников.
Во время беременности введение дексаметазона допустимо только по жизненным показаниям.
Детей, рожденных матерями, которым назначали ГКС во время беременности, нужно тщательно проверять на наличие недостаточности надпочечников.
Небольшие количества глюкокортикоидов находят в молоке. Поэтому кормление грудью не рекомендуется во время терапии дексаметазоном. Возможное влияние заключается в замедлении роста ребенка и уменьшении секреции эндогенных глюкокортикоидов.
Дети. Применяют детям с периода новорбжденности. Во время лечения дексаметазоном необходимо тщательное наблюдение за ростом и развитием детей.
Особые меры безопасности. У пациентов, которые длительное время лечатся дексаметазоном, может, наблюдаться синдром отмены (также без видимых признаков недостаточности надпочечников) при прекращении лечения (повышенная температура тела, насморк, покраснение конъюнктивы, головная боль, головокружение, сонливость или раздражительность, боль в мышцах и суставах, рвота, снижение массы тела, слабость, часто еще и конвульсии). Поэтому дозу дексаметазона надо снижать постепенно. Внезапное прекращение лечения может иметь летальные последствия,
Особенности применения. Во время Парентерального лечения ГКС в редких случаях могут наблюдаться реакции гиперчувствительности, поэтому надо принять надлежащие меры перед началом лечения дексаметазоном, несмотря на возможность аллергических реакций (особенно у пациентов с аллергическими реакциями на любые другие лекарства в анамнезе).
Если пациент находится в состоянии тяжелого стресса (из-за травмы, операции или тяжелое заболевание) в течение терапии, дозу дексаметазона следует увеличить, а если это происходит во время прекращения лечения, следует применять гидрокортизон или кортизон.
Пациентам, которым вводили дексаметазон продолжительное время и которые испытывают тяжелый стресс после прекращения терапии, следует восстановить применение дексаметазона, поскольку вызванная им недостаточность надпочечников может длиться в течение нескольких месяцев после прекращения лечения.
Лечение дексаметазоном или природными глюкокортикоидами может скрыть симптомы существующей или новой инфекции, а также симптомы кишечной перфорации. Дексаметазон может обострить системную грибковую инфекцию, латентный амебиаз и туберкулез легких.
Пациенты с туберкулезом легких в активной форме должны получать дексаметазон (вместе со средствами против туберкулеза) только при мимолетном или сильно рассеянном туберкулезе легких. Пациенты с неактивной формой туберкулеза легких, которые лечатся дексаметазоном, или пациенты, которые реагируют на туберкулин, должны получать химические профилактические средства.
Осторожность и медицинское наблюдение рекомендованы больным остеопорозом, гипертонией, сердечной недостаточностью, туберкулезом, глаукомой, печеночной или почечной недостаточностью, сахарным диабетом, активной пептической язвой, недавним кишечным анастомозом, язвенным колитом и эпилепсией. Особого ухода требуют пациенты в течение первых недель после инфаркта миокарда, пациенты с тромбоэмболией, тяжелой миастенией, гипотиреозом, психозом или психоневрозом, а также пациенты пожилого возраста.
Во время лечения может наблюдаться обострение сахарного диабета или переход от латентной фазы до клинических проявлений сахарного диабета.
При длительном лечении следует контролировать уровень калия в сыворотке. Вакцинация живой вакциной противопоказана при лечении дексаметазоном. Вакцинация убитой вирусной или бактериальной вакциной не приводит к ожидаемому синтезу антител и не дает ожидаемого защитного эффекта. Дексаметазон обычно не назначают за 8 недель до вакцинации и не начинают применять ранее, чем через 2 недели после вакцинации.
Пациенты, длительно лечившиеся высокими дозами дексаметазона и никогда не болевшие корью, должны избегать контакта с инфицированными лицами, при случайном контакте рекомендовано профилактическое лечение иммуноглобулином.
Рекомендуется проявлять осторожность пациентам, которые выздоравливают после операции или перелома костей, поскольку дексаметазон может замедлить заживление ран и образование костной ткани.
Действие глюкокортикоидов усиливается у больных циррозом печени или гипотиреозом.
Внутрисуставное назначение дексаметазона может привести к системным эффектам. Частое применение может вызвать поражение хряща или некроз кости.
Перед внутрисуставным введением следует удалить из сустава синовиальную жидкость и исследовать ее (проверить на наличие инфекции). Следует избегать введения ГКС в инфицированные суставы. Если инфекция сустава развивается после инъекции, следует начать надлежащую терапию антибиотиками.
Пациентам следует сообщить о том, чтобы они избегали физической нагрузки на пораженные суставы до времени, когда воспаление будет излечено.
Следует избегать введения препарата в неустойчивые суставы.
ГКС могут искажать результаты кожных аллергических тестов.
Специальная информация о некоторых ингредиентах: препарат содержит менее 1 ммоль (23 мг) натрия в дозе, то есть практически «свободен от натрия».
Другие лекарственные средства и данный препарат
Сообщите лечащему врачу о том, что вы применяете, недавно применяли или можете начать применять какие-либо другие препараты.
Одновременное применение дексаметазона и НПВП повышает риск желудочно- кишечного кровотечения и образование язв.
Эффективность дексаметазона уменьшается, если одновременно принимать рифампицин, карбамазепин, фенобарбитал, фенитоин (дифенилгидантоин), примидон, эфедрин или аминоглутетимид, поэтому доза дексаметазона в таких комбинациях должна увеличиваться.
Совместное применение дексаметазона и препаратов, ингибирующих CYP ЗА4 ферментативную активность, таких как кетоконазол, антибиотики-макролиды, может вызывать увеличение концентрации дексаметазона в сыворотке и плазме. Дексаметазон является умеренным индуктором CYP ЗА4. Совместное применение с препаратами, которые метаболизируются CYP ЗА4, такими как индинавир, эритромицин, может повышать их клиренс, что приводит к снижению концентрации в сыворотке.
Кетоконазол может подавлять синтез глюкокортикоидов корой надпочечников, таким образом, вследствие снижения концентрации дексаметазона может случаться надпочечниковая недостаточность.
Дексаметазон уменьшает терапевтический эффект препаратов для лечения сахарного диабета, артериальной гипертензии, антикоагулянтов кумаринового, празиквантела и натрийуретиков (поэтому дозу этих лекарств следует увеличить), он повышает активность гепарина, альбендазола и калийуретиков (дозу этих препаратов следует уменьшить в случае необходимости).
Дексаметазон может изменить действие антикоагулянтов кумаринового ряда, поэтому при применении такой комбинации лекарств следует более часто контролировать протромбиновое время.
Одновременное применение дексаметазона и высоких доз других ГКС или агонистов а2-адренорецепторов повышает риск развития гипокалиемии. У пациентов с гипокалиемией сердечные гликозиды большей степени способствуют нарушению ритма и имеют большую токсичность.
Глюкокортикоиды усиливают почечный клиренс салицилатов, поэтому иногда трудно получить терапевтические концентрации салицилатов в сыворотке. Надо проявлять осторожность пациентам, которым постепенно снижают дозу ГКС, поскольку при этом может наблюдаться повышение концентрации салицилата в сыворотке и интоксикация.
Если параллельно применяются оральные контрацептивы, период полувыведения глюкокортикоидов может удлиняться, что усиливает их биологическое действие и может повысить риск побочных эффектов.
Одновременное применение ритордина и дексаметазона противопоказано во время родов, это может привести к отеку легких. Сообщалось о смерти роженицы из-за развития такого состояния.
Одновременное применение дексаметазона и талидомида может вызвать токсический эпидермальный некролиз.
Виды взаимодействия, которые имеют терапевтические преимущества: параллельное назначение дексаметазона и метоклопрамида, дифенгидрамина, прохлорперазина или антагонистов рецепторов 5-НТЗ (рецепторов серотонина или 5-гидрокси-триптамина, тип 3, таких как ондансетрон или гранисетрон) эффективно для профилактики тошноты и рвоты, вызванных химиотерапией цисплатином, циклофосфамидом, метотрексатом, фторурацилом.