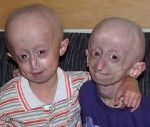
Детская прогерия что такое
Прогерия
Общие сведения
Прогерия – это генетическое заболевание, которое считается одним из редчайших, за всю историю человечества зафиксировано примерно 350 случаев. Самыми известными людьми с прогерией считаются диджей Леон Бота и мотиватор Сэм Бернс. Прогерия в России не очень распространена – зарегистрировано всего около 80 случаев.
Главной особенностью этого генетического дефекта является преждевременное старение организма, которое сопровождается существенными изменениями кожных покровов и работы внутренних органов. С греческого progeros переводится как «преждевременно постаревший».
Как указывает Википедия заболеванию присвоен код МКБ-10: Е34.8 и относится к другим уточненным эндокринным расстройствам.
Патогенез
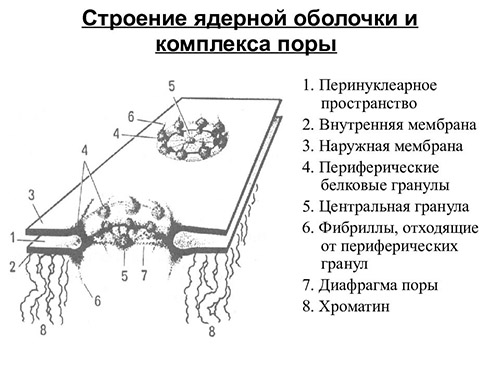
Классификация
Различают детскую прогерию — синдром Хатчинсона Гилфорда и взрослую — синдром Вернера.
В отличие от детской, проявляющейся в 5-8-месячном возрасте, у взрослых симптомокомплекс преждевременного старения развивается примерно в 20-30 лет, начинаясь в период полового развития. Тело и лицо начинает меняться как на картинке ниже (прогерия — фото) с разницей в 33 года: приобретает заостренные черты, нос становится похожим на птичий, рот узким, голос высоким и хриплым, кожа бледной, конечности тонкими, нет подкожной клетчатки. При этом происходит атрофия мышц, образование трофических язв, гипогонадизм, прогрессия глаукомы, катаракты, атеросклероза, облысения и поседения, выпадение зубов, снижение интеллекта.
Синдром Вернера, пациентке 15 и 48 лет
Прогерия: причины заболевания
Заболевание наследственное и передается по аутосомно-рецессивному типу, поэтому единичные случаи братьев и сестер с прогерией объясняются тем, что родители были достаточно близкими родственниками, например, кузенами и заболевание стало результатом кровосмешения. Однако, называют и другие причины заболевания, например:
Также предполагается, что синдром Хатчинсона Гилфорда возникает в результате спорадической – внезапной мутации в сперматозоиде или яйцеклетке еще до момента зачатия.
Симптомы
Как синдром преждевременного старения, болезнь прогерия вовлекает в патогенетический процесс различные системы и органы:
Анализы и диагностика
Благодаря работе исследовательских фондов изучения прогерии на сегодняшний день есть возможность идентифицировать генные мутации программами диагностического тестирования и помочь больным на более ранних стадиях развития заболевания.
Чтобы узнать есть ли генетические отклонения у ребенка достаточно посетить квалифицированного врача, который изучит внешний вид, данные анамнеза и направит на анализ крови, выявляющий генетические дефекты.
Лечение
Помощь особам, подверженным преждевременному старению должна быть комплексной, включая симптоматическое лечение, а также:
Ученые выдвигают предположение, что ингибиторы фарнезилтрансферазы (FTIs), которые помогают в борьбе с раком, также способны обратить процессы образования структурных аномалий.
Обычная медикаментозная терапия включает прием:
Процедуры и операции
Детская прогерия
Детская прогерия начинается внезапно в 5-8 месяцев либо реже в 3-4 года и проявляется в виде резкого замедления темпов физического развития.
При таком страшном летальном диагнозе очень важно выявить недуг на ранних стадиях, когда в организме еще не произошли необратимые процессы. Не смотря на то, что лекарство еще не изобрели, очень важно ребенку своевременно получить симптоматическое лечение, правильно выстроить его режим и питание с учетом особенностей организма.
Диета при прогерии
Омолаживающая диета против старения организма
Питание для предотвращения преждевременного старения должно быть калорийно ограниченным и качественно полноценным. Помимо этого диета должна быть:
Прогноз
Считается крайне неблагоприятным, так как единой стратегии лечения до сих пор не разработано и продолжительность жизни не превышает 27 лет, в среднем составляет 13 лет. Причинами летального исхода чаще всего становится истощение, инфаркт миокарда, злокачественные новообразования, интеркуррентные заболевания – случайно присоединившиеся и осложняющие течение самой прогерии. Особы с взрослой прогерией обычно доживают до 40-50 лет.
Список источников
Образование: Окончила Николаевский национальный университет им. В. А. Сухомлинского, получила диплом специалиста с отличием по специальности «Эмбриолог, цитолог, гистолог». Также, окончила магистратуру по специальности «Физиология человека и животных, преподаватель биологии». С отличием пройден курс по дисциплине «Фармакология».
Опыт работы: Работала старшим лаборантом кафедры Физиологии и биохимии Николаевского национального университета им. В. А. Сухомлинского в 2010 — 2011 гг.
Прогерия
Прогерия – редкое генетическое заболевание, характеризующееся преждевременным старением организма, соответствующими изменениями внутренних органов. Проявляется гиперпигментацией, истончением и утратой эластичности кожи, поседением и выпадением волос, увеличением размеров черепа, уменьшением его лицевой части, экзофтальмом, развитием атеросклероза сосудов, инфаркта и фиброза миокарда, остеопороза, сахарного диабета, формированием злокачественных опухолей. Диагностика основана на сборе клинических данных, лабораторном исследовании ДНК. Лечение направлено на устранение симптомов заболевания: профилактику и терапию атеросклероза, инфаркта миокарда, диабета, остеопороза, рака.
МКБ-10
Общие сведения
Термин «прогерия» в переводе с древнегреческого языка означает «преждевременное старение». Детская форма прогерии называется синдромом Хатчинсона-Гилфорда согласно фамилиям исследователей, которые впервые независимо друг от друга описали данную патологию: британский врач Дж. Хатчинсон – в 1889 году, его соотечественник Х. Гилфорд – в 1897 году. Взрослая форма носит название «синдром Вернера», так как в 1904 году немецкий врач О. Вернер первым официально наблюдал симптомы старения у подростков 14-19 лет. Оба варианта болезни являются крайне редкими. Распространенность детской прогерии составляет 1 случай на 7-8 млн. человек, с момента начала исследований патологии выявлено около 150 больных детей. Взрослая прогерия встречается чаще, средние эпидемиологические показатели – 1 больной на 100 тыс. населения.
Причины прогерии
В основе заболевания лежит генетическая мутация. Причиной детского типа прогерии является дефект гена LMNA, который кодирует особый белок ламин A, выстраивающий оболочку ядра клетки. Как правило, мутация происходит спорадически – во время созревания половых клеток у родителей или при зачатии. Однако исследователи выявили несколько случаев патологии у родных братьев и сестер, часть из которых входила в семьи с близкородственными браками. Это свидетельствует о возможности наследования мутации по аутосомно-рецессивному типу (родители являются носителями дефектного гена, но не болеют и способны к деторождению).
Прогерия взрослых – наследственное заболевание. Оно развивается при наличии дефекта в гене RECQL2, который ответственен за производство белка WRN, поддерживающего стабильность генома, целостность и структуру ДНК. Передача мутации происходит аутосомно-рецессивным способом, болезнь проявляется у людей, получивших два дефектных гена в одной аллели (от матери и от отца).
Патогенез
При детском варианте прогерии генетический дефект приводит к нарушению синтеза структурно правильного белка ламина А, образующего внутренний каркас ядерной оболочки. В результате мутации налаживается производство укороченного белка-предшественника преламина А, а строение созревшего конечного белка отличается от нормального. Молекулы белка встраиваются в ядерную мембрану, изменяют ее форму и повышают хрупкость. Ядро не может сохранять свою целостность, клетка гибнет раньше времени.
При болезни Вернера возникает недостаточность WRN-белка, определяется генетически детерминированная нестабильность хромосом. Их структура очень часто изменяется спонтанно или под воздействием некоторых факторов. В итоге ухудшается способность клеток к делению, пролиферативный потенциал становится в 3-5 раз меньше, чем должен быть в норме. В 10 раз увеличивается частота спонтанных мутаций, аномально укорачиваются теломеры – концевые участки хромосом, защищающие гены от повреждений.
Симптомы прогерии
Прогерия Хатчинсона дебютирует после периода нормального развития в возрасте от 6 месяцев до 2 лет. Изменяется внешность детей: замедляется рост, увеличиваются размеры черепа, но лицевая часть остается маленькой, нижняя челюсть – недоразвитой. Формируется клювовидный тонкий нос и экзофтальм (выпячивание глаз). Тотально выпадают волосы – на голове и теле, ресницы и брови. При алопеции разрушаются волосяные фолликулы, поэтому дальнейший рост волос становится невозможным. На волосистой части головы выбухают вены. Дерма и подкожная клетчатка подвергаются атрофическим изменениям: кожа истончается, иссушается, покрывается морщинами. Развивается липодистрофия – заметное снижение количества подкожного жира. Относительно сохранным он остается на щеках и лобке.
На туловище образуются склеродермоподобные очаги – уплотнения в нижней части живота, на ягодицах и бедрах. На открытых участках кожи появляются пигментные пятна. Ногти недоразвитые, ломкие, утолщенные, округло выпуклые – имеют форму «часовых стекол». К 2 годам развивается фиброз органов и околосуставных тканей. Пассивные движения в локтевых и коленных суставах ограничены (контрактуры), формируется характерное положение костей ног – «поза всадника». Скелет подвергается гипоплазии, дисплазии и дегенеративным изменениям. Молочные и постоянные зубы прорезываются с опозданием, частично отсутствуют, скученные, искривленные, подвержены кариесу. К 5-6 годам диагностируется атеросклероз сосудов, сердечные шумы, гипертрофия левого желудочка, помутнение хрусталика, резистентность к инсулину. Половые органы остаются недоразвитыми. Уровень умственного развития обычно выше, чем у сверстников.
Клинические проявления синдрома Вернера обнаруживаются с 14 до 18 лет. Подросток начинает отставать в росте, его волосы седеют и выпадают. К 20 годам пациенты лысеют. Кожа лица и конечностей бледнеет, истончается, натягивается. Под ней видна сеть кровеносных сосудов. Мышечная и жировая ткани атрофируются, руки и ноги становятся непропорционально тонкими, кожа над суставными выступами изъязвляется. К 30 годам появляется катаракта, голос слабеет и хрипнет, на ногах образуются язвы, на подошвах – мозоли, сосудистые звездочки, кератоз. Внешний вид пациентов специфичен: низкий рост, лунообразное лицо, выступающий подбородок, суженное ротовое отверстие, псевдоэкзофтальм.
Сальные и потовые железы атрофируются. Костно-суставные изменения включают метастатическую кальцификацию, явления генерализованного остеопороза, эрозивных остеоартритов, ограниченную подвижность и деформацию пальцев рук, сгибательные контрактуры, боли в конечностях, артрит и остеомиелит. Отмечаются атеросклеротические изменения сосудов, медленно прогрессирует катаракта, снижаются интеллектуальные способности. После 30 лет проявляются эндокринные заболевания – сахарный диабет, гипогонадизм, тиреопатии. У 5-10% больных обнаруживаются злокачественные опухоли различных органов, костей и кожи. Причиной смерти становится онкопатология или тяжелое сердечно-сосудистое заболевание.
Диагностика
Диагноз прогерии устанавливается на основании клинико-анамнестических данных. В зависимости от имеющейся симптоматики в диагностике могут принимать участие эндокринологи, неврологи, дерматологи, терапевты, врачи-генетики. Детскую и взрослую прогерию необходимо дифференцировать с системной склеродермией, пойкилодермией, синдромом Ротмунда-Томсона, синдромом Видемана-Раутенштрауха. К основным методам обследования больных относятся:
Лечение прогерии
Специфические методы терапии прогерии не разработаны. Медицинская помощь пациентам заключается в облегчении симптомов болезни. Проводится лечение атеросклероза, остеопороза, остеомиелита, катаракты, диабета, патологий сердца и онкологических заболеваний. Известен случай, когда состояние больного заметно улучшилось на несколько лет после операции трансплантации сердца.
Научные исследования ведутся в области генной инженерии – совершаются попытки выделить мутационный ген из ДНК и заменить его здоровым. Параллельно разрабатывается метод этиотропной терапии. Ученые из Швеции нашли способ нейтрализации дефектных молекул ламина A, которые проникают в мембрану клеточных ядер и способствуют гибели клетки. Положительные результаты получены на экспериментах с мышечной тканью крыс, на людях препарат пока не опробован. В США с 2012 года ведется изучение эффективности применения ингибитора фарнезилтрансферазы (лекарственного средства, разработанного для лечения рака). После терапии дети из экспериментальной группы чувствовали себя лучше, повысилась жесткость и эластичность артерий, плотность костей, снизились случаи транзиторных ишемических атак, сердечных патологий, утраты зрения и слуха. Продолжительность жизни увеличилась на 1,6-6 лет.
Прогноз и профилактика
В среднем больные детской прогерией доживают до 13 лет, зарегистрированы случаи смерти в 7 и 27 лет. Продолжительность жизни при взрослом типе заболевания составляет 30-40 лет. Причиной летального исхода становятся атеросклеротические осложнения и злокачественные новообразования. Профилактические меры отсутствуют. Предупредить рождение больного ребенка можно при наследственном характере болезни – при синдроме Вернера, в отдельных случаях синдрома Хатчинсона, когда патология выявлена в семье, будущие родители отнесены к группе высокого риска. Таким парам назначается медико-генетическое консультирование.
Прогерия

Прогерией называют старение преждевременного характера. Для этого патологического состояния характерен комплекс изменений кожных покровов и внутренних органов. Прогерия представлена детской и взрослой формами.
Виды и клиническая картина заболевания
С детской прогерией сталкиваются очень редко. Об этиологии и патогенезе данной формы болезни до конца неизвестно. По мнению некоторых специалистов, в основе развития заболевания лежит мутация гена LNMA. Этот ген осуществляет кодирование ламина А. Данный белок является компонентом оболочки ядра клетки. Как правило, ее развитие носит спорадический характер. Установлено, что дети с такой проблемой могут рождаться в кровнородственных браках. Это считается свидетельством возможного аутосомно-рецессивного наследования прогерии. В эпидермисе больных обнаружены расстройства восстановления ДНК, а также его атрофия. Иногда исчезает подкожно-жировая клетчатка. У большинства больных появление детской прогерии приходится на трехлетний возраст. Отмечается резкое замедление роста ребенка, развитие атрофических изменений кожи на конечностях и лице. Наблюдается истончение кожи. Она приобретает сухость, морщинистость. Возможно появление очагов гиперпигментации. Внешне заболевание проявляется большой головой, небольшими размерами лица, недоразвитием нижней челюсти. Кроме того, возможна атрофия мышечного аппарата, дистрофия зубов и ногтей, недоразвитие половых органов. Заболевание может стать причиной расстройства обмена жиров и атеросклероза.
Возникновение прогерии взрослых связано с нарушением обмена в соединительной ткани. Кроме того, большое значение уделяется расстройству репарации ДНК. Гистологически выявляется уплощенный эпидермис, склерозированная соединительная ткань, атрофичная подкожная клетчатка и пр. Проявление этой формы заболевания происходит во время полового созревания. Отмечается замедление роста и появление признаков гипогонадизма. В большинстве случаев, к 30 годам такие больные теряют волосы на голове. Довольно часто происходит нарушение зрения в виде катаракты. По мере прогрессирования прогерии руки и ноги становятся тонкими. Это связано с истончением кожи и атрофий подкожной клетчатки. На стопах, кистях и лице появляются очаги уплотнения. На местах, которые подвергаются давлению, происходит развитие гиперкератоза и плохо заживающих язв. Характерно обнаружение остеопороза, метастатической кальцификации мягких тканей. В наиболее тяжелых случаях имеет место быть возникновение остеомиелита. Часто прогерия сопровождается развитием сахарного диабета. Его признаки обнаруживаются после 40 лет. Кроме того, возможно появление злокачественных новообразований. Речь идет, к примеру, о раке кожи, саркоме, аденокарциноме и т.д.
Основой выявления прогерии является характерная клиническая картина болезни и анамнез. Данную патологию необходимо отличать от врожденной пойкилодермии и склеродермии.
Лечение прогерии
Синдром Гетчинсона-Гилфорда (прогерия)
Полный текст:
Аннотация
Синдром Гетчинсона-Гилфорда или прогерия (сенильный нанизм) — исключительно редкое генетическое заболевание детей с клиническими чертами преждевременного старения. Частота заболевания составляет 1 на 8 млн новорожденных (De Busk. 1972). К настоящему времени в мировой литературе описано около 70 пациентов с этим синдромом. Этиология прогерии неясна. Генетическая модель наследования неизвестна в связи с крайней редкостью встречаемости синдрома и отсутствием потомства у больных. Однако исследования зарубежных ученых позволяют говорить о спорадической доминантной мутации как генетической основе данного синдрома. Клиническая картина прогерии представлена симптомами прогрессирующего преждевременного старения. Характерен вид лица: с экзофтальмом, тонким клювовидным носом, большим мозговым и малым лицевым черепом, голос тонкий, имеются скелетные аномалии. Пубертат обычно не наступает, наружные гениталии гипоплазированы. Интеллект средний или выше среднего. Для данного синдрома характерны распространенный атеросклероз с поражением коронарных и мезентериальных сосудов, аорты, сосудов головного мозга, с гиперлипидемией. Прогерия как модель преждевременного старения изучается в разных аспектах: метаболическом, гормональном, гистологическом, иммунологическом, молекулярном.
Ключевые слова
Для цитирования:
Фофанова О.В. Синдром Гетчинсона-Гилфорда (прогерия). Проблемы Эндокринологии. 1995;41(4):24-26. https://doi.org/10.14341/probl11459
For citation:
Fofanova O.V. Syndrome Hutchinson-Gilford (progeria). Problems of Endocrinology. 1995;41(4):24-26. (In Russ.) https://doi.org/10.14341/probl11459
Синдром Гетчинсона-Гилфорда (Hutchinson-Gilford Progeria Syndrome), или прогерия (сенильный папизм) — исключительно редкое генетическое заболевание детей с клиническими чертами преждевременного старения.
Частота заболевания составляет 1 на 8 млн новорожденных (De Busk. 1972). К настоящему времени в мировой литературе описано около 70 пациентов с этим синдромом.
Этнология прогерии неясна.
Генетическая модель наследования неизвестна в связи с крайней редкостью встречаемости синдрома и отсутствием потомства у бальных. Однако исследования зарубежных ученых [2-4, 7] позволяют говорить о спорадической доминантной мутации как генетической основе данного синдрома. Отмечается влияние возраста отца как возможной причины новых мутаций. Так, средний возраст отцов составляет 35-37 лет.
Аутосомно-рецессивный тип наследования синдрома также обсуждается в литературе [7, 8, И]. Этот тип наследования был впервые предположен Gabr и соавт. в 1960 г. при описании двух моиозиготных сестер, а впервые сообщил о семейном случае прогерии Paterson в 1922 г., хотя описание двух больных братьев было неполным и без фотографий.
Клиническая картина прогерии представлена симптомами прогрессирующего преждевременного старения.
Дети рождаются нормальными, но к 1-му году жизни наблюдается выраженная задержка роста и массы тела. Конечный рост в среднем достигает 100 см. В первые годы жизни развивается тотальная алопеция. Кожа топкая, лоснящаяся, сухая, тугонатянутая (па кистях и стопах, наоборот, морщинистая). В нижней части живота и бедрах кожные изменения напоминают склеродермию. С возрастом появляются коричневые пигментные пятна. Потовые и сальные железы атрофируются.
Подкожный жировой слой полностью отсутствует, за исключением лобковой области. На черепе выражена подкожная венозная сеть. Нощи дистрофичные, влоть до аплазии. Зубы прорезываются с задержкой, аномально расположены, с ранним разрушением как молочных, так и постоянных зубов.
Характерен вид лица: с экзофтальмом, гонким клювовидным носом, большим мозговым и малым лицевым черепом. Голос тонкий.
Скелетные аномалии включают резорбцию ключицы с замещением фиброзной тканью, резорбцию конечных фаланг кистей (акроостеолиз), истончение длинных трубчатых костей и ребер, тугоподвижность сутавов пальцев, увеличение локтевых и коленных суставов. Часты асептические некрозы головки бедренной кости и вывих тазобедренного сустава.
Пубертат обычно не наступает, наружные гениталии ги- поплазированы.
Интеллект средний или выше среднего.
Для данного синдрома характерны распространенный атеросклероз с поражением коронарных и мезентериальных сосудов, аорты, сосудов головного мозга, с гиперлипидемией. Следует отметить, что заболевания, характерные для нормального процесса старения (катаракта, опухоли, сахарный диабет), встречаются при прогерии крайне редко.
Прогерия как модель преждевременного старения изучается в разных аспектах: метаболическом, гормональном, гистологическом, иммунологическом, молекулярном.
Гормональные исследования у детей [4] выявляют нормальную ночную секрецию соматотропного гормона гипофиза, но крайне низкий уровень инсулиноподобного фактора роста (ИФР-1) в плазме крови. Это позволяет предполагать наличие у данных больных бионеактивпого пула СТГ в крови, либо периферическую резистентность к эндогенному СТГ. либо выраженный дефицит питания. Трехмесячный период высококалорийного питания не увеличивает уровень ИФР-1 в крови, но ускоряет линейный рост.
Прогерия считается состоянием, связанным с ннсулиноре- зистентностыо умеренной степени. В 1983 г.[9] впервые была описана девочка, у которой в 2-легнсм возрасте уровень инсулина в крови натощак составлял 20-40 мкг/дл. В 4 года через 3 мес после удаления кисты яичника развилась гипергликемия натощак (до 250 мкг/дл) с высоким уровнем инсулина (более 2200 мкЕД/мл) и С-пептида (32,4 нг/мл) в крови. Уровень гемоглобина А1 достигал 10%. Связывание инсулина с рецепторами эритроциов было в пределах нормальных значений.
Иммунологический аспект в патогенезе прогерии впервые был выдвинут Walford в 1970 г. В 1973-1976 г. Singal и Goldstein выявили отсутствие либо резкое снижение экспрессии HLA культурой фибробластов кожи у детей с прогерией. Вместе с тем другие исследователи, анализируя экспрессию HLA у детей с прогерией и их здоровых родственников [2], нс выявили ни количественного, ни качественного дефицита в экспрессии HLA в фибробластах кожи. Различие в частоте встречаемости ряда HLA-антнгенов у больных прогерией и здоровых людей не дает право в настоящее время говорить о специфической ассоциации HLA и прогерии в связи с малым числом исследуемого материала.
Цитогенетический анализ выявил инвертированную вставку хромосомы 1 в 70% клеток биоптата кожи у 8-летиего мальчика с прогерией. Это первая описанная аномалия в изучаемой группе из 10 детей [4].
Биохимическими исследованиями показано, что одним из биомаркеров старения является мочевая экскреция гиалуроновой кислоты. В норме у детей и подростков содержание ее составляет менее 1% от уровня общих гликозаминогликанов и увеличивается с возрастом до 5-6%. У детей с прогерией выявлено значительное повышение (до 10-20%) экскреции гиалуроновой кислоты с мочой по сравнению со здоровыми людьми [4]. Данное повышение не наблюдается ни при одном генетическом заболевании, кроме синдрома Вернера, или “прогерии взрослых” [4]. Считается, что гиалуроновая кислота является ключевым фактором антиангиогенеза в процессе созревания и старения.
Изучение культуры фибробластов кожи от пациентов с прогерией выявляет значительное снижение клеточного роста вследствие подавления митотической активности. С другой стороны, отмечается нормальное распределение типов коллагена в коже, характерное для детей, а именно, преобладание коллагена 3-го типа над коллагеном 1-го типа [8].
Имеются данные, что в основе прогерии лежит дефицит метаболизма витамина Е [7].
Ряд исследователей связывают прогерию с генетически обусловленной ошибкой в синтезе внутриклеточных белков. Так, показано, что эритроциты больных детей содержат повышенную термолабильную фракцию ферментов: глюкозо-6- фосфатдегидрогепазу и б-фосфоглюконатдегидрогепазу |6]. Другие работы не подтверждают эту концепцию [3].
Данные олене или детей с прогерией крайне малочисленны.
Имеются сообщения об успешном использовании рекомбинантного гормона роста, в результате чего было достигнуто увеличение скорости роста [4].
Патогенетически оправданными считаются терапия витамином Е для восполнения его дефицита (Лугез и МШап, 15974) и усиленное белковое питание.
Значительный интерес представляет единственное в литературе сообщение об аортокоронарном шунтировании и транслюминальной ангиопластике у 14-летней девочки с прогерией [5]. В 7-летнем возрасте она перенесла 2 эпизода трапзиторпой правосторонней гемиплегии. Ангиография выявила полную окклюзию внутренней сонной артерии слева. Первые Приступы стенокардии появились у нее в 7-летнем возрасте, а в 11 лет девочка перенесла инфаркт миокарда. В 14 лет, на фоне’ 20-30 эпизодов стенокардии в сутки, корона- роангио(рафия выявила 60-100% атеросклероз коронарных артерий. Через 2 нед после операции аортокоронарного шунтирования приступы стенокардии пообносились. При коро- пароаигиографии отмечалась 90% обструкция дистального анастомоза. В связи с этим у девочки произведена транслюминальная балонная катетеризация места стеноза, с положительным эффектом.
Приводим описание собственного клинического случая.
Боль пая Н., 3 лет 9 мес., поступила в детское отделение ЭНЦ РАМН с жалобами на отставание в росте и массе, сниженный аппетит, облысение, резкую головную боль.
Перенесенные заболевания: дисплазия тазобедренный суставов (в 1 мес жизни), двусторонний врожденный вывих бедер (диагностирован в 6 мес жизни), стоматит, легкая форма (в 3 года).
Аллергологический анамнез не отягощен.
Область сердца визуально не изменена. Тоны сердца ясные, ритмичные. Часота сердечных сокращений 104 удара в минуту, АД 80/50 мм рт.ст. Дыхание везикулярное, хрипов нет. Зев чистый. Живот мягкий, безболезненный. Печень не увеличена, селезенка не пальпируется. Стул регулярный. Дизурических расстройств нет. Симптом Пастернацкого отрицательный с обеих сторон. Эндокринный статус: щитовидная железа не увеличена, симптомов нарушения функции нет. Симптомы гипокортицизма отсутствуют. Половой статус препубертатный: Ах 0, Р 0, Ма 0, Me 0.
Гормональное исследование мочи: свободный кортизол 1115,0 нмоль/л на 1 г креатинина (креатинин 0,24 г/л). Дс- гидроэпиандростерон-сульфат — следы.
Показатели гуморального аутоиммунитета: у больного ребенка не выявлено антител пи к тиреоглобулину человека, ни к микросомальному антигену тиреоцигов, ни к поверхностным антигенам клеток аденогипофиза и клеток коры надпочечников крысы.
Рентгенографическое исследование: на рентгенограмме черепа и кистей структура костей не изменена. Форма и размеры турецкого седла обычные. Сосудистый рисунок костей свода усилен. Дифференцирование скелета соответствует 12- 15 мес. Ногтевые фаланги деформированы, треугольной формы. На рентгенограмме стоп отмечается небольшое уплотнение стенок arteria dorsalis pedis.
Компьютерная томография головного мозга: на серии компьютерных томограмм изменения плотности мозговой ткани не выявлено. Желудочковая система не изменена. Хиазмальная цистерна расширена. Несколько расширена межполушарная щель. Данных, свидетельствующих об объемном процессе головного мозга, не выявлено.
ЭКГ: ЧСС 120 в минуту, ритм синусовый. Электроэнцефалограмма: на фоне умеренных диффузных изменений биоритмики с признаками диэнцефальной заинтересованности отмечаются признаки ирригации стволово-диэнцефальных структур с легким акцентом справа, в теменно-затылочной области. Эхоэнцефалограмма: эхо-пульсация неустойчиво усилена до 55%, смещения срединных структур нет, легкое расширение 111 желудочка (до 6 мм), вентрикулярный индекс умеренно выше нормы. Заключение: смещения срединных структур не выявлено. Расширение боковых желудочков.
Консультация окулиста: моторно-зрачковых нарушений не выявлено. Передний отрезок и среды без патологии. Глазное дно: диски бледно-розовые, сосуды умеренно расширены, полнокровны, извиты по всей протяженности сетчатки. Сетчатка на периферии разряжена, небольшие отеки. Заключение: повышение внутричерепного давления.
Консультация невропатолога: субкомпепсированпая гидроцефалия на фоне скудной церебральной симптоматики.
Консультация дерматолога: Alopecia totalis. Рекомендованы курсы лечения препаратами, улучшающими микроциркуляцию (трептал, троксевазип), поливитамины (Bj, В2, В(„ В15, А, Е); наружно — втирание с массажем головы геля актовегина, геля троксевазина, димексида, 01. Ricini.
Лечение рекомендовано проводить под контролем гликемии и суточной глюкозурии.
Помимо гормона роста, девочке назначено лечение, рекомендованное дерматологом, и полноценное белковое питание.
Таким образом, представленный материал, основанный на данных анамнеза, жалоб, результатах клинического обследования и лабораторно-инструментальных исследований, подтверждает наличие у ребенка классического синдрома Гетчинсона-Гилфорда (прогерии).