Дгпж предстательной железы что
Доброкачественная гиперплазия предстательной железы — разрастание железистой ткани и стромы переходной зоны простаты, приводящее к увеличению органа. Аденома простаты может вызывать нарушения мочевыделения: слабую струю мочи, чувство неполного опорожнения мочевого пузыря, частые или ночные позывы, парадоксальную ишурию. Диагноз устанавливают по данным уровня ПСА, ТРУЗИ, урофлоуметрии и опросника оценки симптомов IPSS. Лечение коррелирует с объемом железы, возрастом, сопутствующей патологией и выраженностью симптомов: применяют тактику ожидания, медикаментозную терапию, оперативные вмешательства, включая малоинвазивные методики.
МКБ-10
Общие сведения
Доброкачественная гиперплазия предстательной железы (аденома простаты, ДГПЖ, ДГП) — общая мировая проблема, с которой сталкивается одна треть мужчин старше 50 лет и 90% пациентов, доживших до 85 лет. По статистике, около 30 млн. мужчин имеют мочеполовую дисфункцию, связанную с ДГПЖ, и эта цифра с каждым годом увеличивается. Патология чаще встречается у афроамериканцев с изначально более высоким уровнем тестостерона, активностью 5-альфа-редуктазы, ростовых факторов и экспрессии рецепторов андрогенов (популяционная особенность). У жителей восточных стран аденому простаты регистрируют реже, что, по-видимому, связано с употреблением в пищу большого количества продуктов, содержащих фитостеролы (рис, соя и ее производные).
Причины ДГПЖ
Патогенез
Тестостерон в организме мужчины содержится в различных концентрациях: в крови его уровень больше, в простате — меньше. У возрастных мужчин происходит снижение уровня тестостерона, но уровень дигидротестостерона остается высоким. Значимая роль принадлежит специфичному для простаты ферменту 5-альфаредуктазе, благодаря которой тестостерон переходит в 5-альфа-дигидротестостерон. К его действию максимально чувствительны андрогенные рецепторы и ДНК ядер клеток простаты, которые стимулируют синтез факторов роста и тормозят апоптоз (нарушение программируемых процессов естественного отмирания). В результате старые клетки живут дольше, а новые активно делятся, вызывая пролиферацию ткани и рост аденомы.
Увеличенная простата способствует затруднению мочеиспускания на фоне сужения простатической части уретры (особенно, если рост аденомы направлен внутрь мочевого пузыря) и повышению тонуса гладкомышечных волокон стромы. На начальной стадии патологии состояние компенсируется за счет усиленной работы детрузора, который напрягаясь, позволяет моче эвакуироваться полностью.
По мере прогрессирования появляются морфологические изменения стенки мочевого пузыря: часть мышечных волокон заменяется соединительнотканными. Емкость органа постепенно увеличивается, а стенки становятся тоньше. Слизистая оболочка также претерпевает изменения: типичны гиперемия, трабекулярная гипертрофия и дивертикулы, эрозивные изъязвления и некроз. При присоединении вторичной инфекции развивается цистит. Доброкачественная гиперплазия простаты и застой мочи приводят к обратному току урины, цистолитиазу, гидронефротической трансформации почек и ХПН.
Классификация
В андрологии принято несколько классификаций ДГПЖ. В зависимости от объема железы (его определяют с помощью УЗИ и измеряют в кубических сантиметрах) выделяют малую (до 25 см³), среднюю (26-80 см³), крупную (более 80 см³) и гигантскую аденому (свыше 250 см³). Классификация Гюйона выделяет три клинических стадии ДГПЖ:
Симптомы ДГПЖ
Симптомы зависят от степени обструкции мочеиспускательного канала. Если увеличенная простата сдавливает уретру, появляются жалобы на учащенное мочеиспускание малыми порциями, особенно, в ночные часы, вялую струю, ощущение неполного опорожнения, независимо от частоты мочеиспускания. По мере роста аденоматозных узлов изменяется иннервация, в результате чего возникают ургентные позывы — неконтролируемое желание помочиться с последующим неудержанием мочи.
На продвинутой стадии развивается парадоксальная ишурия — невозможность полностью помочиться с одновременным подтеканием мочи по каплям, что связано с атонией стенок мочевого пузыря, а также с детрузорно-сфинктерной диссинергией — отсутствием синхронной работы между мышцей, ответственной за изгнание урины, и расслаблением сфинктера мочеиспускательного канала. Чтобы опорожнить мочевой пузырь, некоторые мужчины вынуждены мочиться по женскому типу ‒ сидя. Клинические проявления доброкачественной гиперплазии предстательной железы непатогномоничны и могут сопровождать любую обструкцию, включая стриктуру уретры, дивертикул, опухоль и пр., поэтому только на основании оценки симптомов установить диагноз невозможно.
Осложнения
Осложнения гиперплазированной простаты могут включать ряд состояний. На фоне ДГП в 35% проявляется острая задержка мочеиспускания. Остаточная моча имеет свойство кристаллизироваться, в этом случае в мочевом пузыре формируются конкременты с вторичным воспалением. Повышенное внутрипузырное давление способствует образованию пузырно-мочеточниковых рефлюксов, гидронефроза и ХПН. Если рассматривать осложнения терапии аденомы предстательной железы, то существует вероятность развития стриктур уретры после трансуретральной резекции (5-7%), недержания мочи (1-2%), эректильной дисфункции (9-14%), ретроградной эякуляции (74-87%), шеечного склероза мочевого пузыря (2-4%).
Диагностика
Диагноз устанавливается урологом или андрологом. Ректальный осмотр информативен только при условии достижимого расположения опухоли. При пальцевом обследовании простата увеличена, однородна, безболезненна, консистенция ее эластична, срединная бороздка сглажена. Биопсия предстательной железы не является рутинным способом и показана только при подозрении на рак простаты. Пациенту с подозрением на нарушение функции почек необходима консультация нефролога.
Существует специальный опросник, разработанный для оценки степени выраженности симптомов обструкции нижних мочевыводящих путей. Анкета состоит из 7 вопросов, связанных с распространенными симптомами доброкачественной гиперплазии предстательной железы. Частота каждого симптома оценивается по шкале от 1 до 5. При суммировании получают общую оценку, которая влияет на дальнейшую тактику лечения (динамическое наблюдение, консервативная терапия или операция): от 0-7 — слабо выраженная симптоматика, 8-19 — средняя, 20-35 ‒ серьезная проблема с мочеиспусканием. Инструментальная и лабораторная диагностика при ДГПЖ включает:
Дифференциальную диагностику проводят с опухолевым процессом мочевого пузыря или простаты, цистолитиазом, травмой, интерстициальным и пострадиационным циститом, нейрогенным мочевым пузырем, стриктурой уретры, склерозом простаты, меатостенозом, клапанами уретры, фимозом, простатитом.
Лечение ДГПЖ
Терапия аденомы простаты коррелирует со степенью выраженности обструктивных симптомов и осложнений, на выбор тактики лечения влияет возраст пациента и сопутствующая патология. Все существующие способы лечения направлены на восстановление адекватной деривации мочи. Варианты терапии включают:
Прогноз и профилактика
Прогноз для жизни благоприятный, большинству пациентов достаточно длительного (пожизненного) приема современных лекарственных препаратов для нормализации функции мочеиспускания. Необходимость в операции возникает только у 15-20% мужчин. После аденомэктомии рецидив болезни не превышает 5%, малонивазивные методики не дают 100% гарантии исцеления и могут выполняться неоднократно. Улучшению прогноза в последнее десятилетие поспособствовало внедрение малоинвазивных методов лечения, что позволяет минимизировать осложнения, угрожающие жизни больных. Для нормализации эректильной функции необходима консультация андролога-сексолога.
Данные исследований по профилактике рака простаты показывают, что диета с низким содержанием животного жира и красного мяса и высоким содержанием белка и овощей может снизить риск симптоматической ДГПЖ. Физическая активность хотя бы 1 час в неделю на 34% уменьшает вероятность ноктурии.
Гиперплазия предстательной железы: заболевания и лекарства
Ч. 1 Гиперплазия (лат. hyperplasia; др.–греч. υπερ — сверх– + πλáσις — образование, формирование) — процесс, протекающий в различных частях организма человека в виде увеличения числа клеток тканей путем их избыточного новообразования (разрастания). В частности, этот процесс при определенных условиях может протекать и в предстательной железе.
Преферанская Нина Германовна
Доцент кафедры фармакологии института фармации им. А.П. Нелюбина Первого МГМУ им. И.М. Сеченова (Сеченовский университет), к.фарм.н.
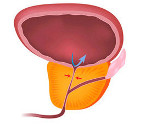
Предстательная железа (лат. prostata — простата) — непарная экзокринная трубчато-альвеолярная железа у мужчин, расположенная ниже мочевого пузыря, с дном которого срастается в его передней части. Через нее проходит начальная часть мочеиспускательного канала. Выводные протоки предстательной железы открываются в мочеиспускательный канал. Функционально простата вырабатывает секрет, который является частью спермы и играет роль клапана, перекрывающего мочеточник во время эрекции. Секрет простаты содержит иммуноглобулины, ферменты, витамины, лимонную кислоту, ионы цинка и другие биологически активные вещества (БАВ). Этот секрет выбрасывается во время эякуляции и участвует в разжижении эякулята.
Простатит (лат. prostatitis / prostata + itis — простата + воспаление) — термин, определяющий воспалительные поражения предстательной железы. Простатит часто сочетается с уретритом, везикулитом, а в пожилом возрасте с доброкачественной гиперплазией предстательной железы (ДГПЖ). Различают простатит неинфекционный и инфекционный. Неинфекционный — это хронический застойный простатит, который возникает при переохлаждении, малоподвижном сидячем образе жизни, снижении физической активности и иммунитета, а также при злоупотреблении алкоголем. Инфекционный простатит возникает в результате проникновения и размножения в ее тканях патогенных микроорганизмов — бактерий (стафилококков, стрептококков, кишечной палочки), хламидий, вирусов (герпеса, папилломы, реже гриппа (лат. Influenzavirus) или грибковых инфекций и т.п.
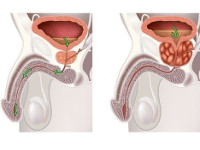
Гиперплазия простаты или аденома предстательной железы —это доброкачественная опухоль в виде уплотнения, когда образуются маленькие узелки, которые по мере роста все больше и больше сдавливают мочеиспускательный канал. Разросшиеся узловые образования при аденоме предстательной железы сложно уменьшить медикаментозными методами.
ДГПЖ характеризуется риском возникновения широкого спектра осложнений, которые имеют отношение к функциональной деятельности органов мочевыделительной системы. ДГПЖ находят примерно у 15–17% сильной половины человечества. Возникает у мужчин чаще всего в возрасте 50–55 лет, поскольку этот период сопровождается значительной гормональной перестройкой всего организма. Своевременная диагностика и лечение аденомы предстательной железы позволяют избежать тяжелых последствий для здоровья. Если не лечить аденому простаты, то в 30–40% случаев она может перерождаться в злокачественную. Постепенное нарастание симптома характерно для развития новообразования. Самая опасная причина, когда плохо проходит моча, — это рак простаты или рак мочевого пузыря. Опухоль давит на уретру или шейку, сужая проход.
Затрудненное мочеиспускание у мужчин — неприятный и опасный симптом, который является признаком сужения или частичной закупорки уретры. В норме мочевыделение должно происходить свободно и без ощущения дискомфорта. Если моча выделяется прерывисто, с болями, разбрызгивается, выходит порциями и отвесно, не образуя характерной струи, а для полного опорожнения мочевого пузыря требуется приложить усилия и напрягать мышцы брюшного пресса, то налицо патология. Этот симптом особенно выражен по утрам. Резкое нарушение оттока возникает обычно по причине воспаления. Причина в том, что воспаленная железа отекает и частично перекрывает просвет простатической части уретры.
Затрудненное мочеиспускание приводит к накоплению остаточной мочи, повышению внутрипузырного давления и расширению мочеточников. Стенки мочевого пузыря растягиваются и атрофируются. Мочеиспускание сопровождается дискомфортом, который нарастает в течение дня. Рецидив может перейти в острое состояние. Исход зависит от силы иммунного ответа организма. Попытки его самостоятельного устранения могут привести к обострению и острой задержке мочи. Необходимы обязательные консультации у врача-уролога с полной диагностикой заболевания и назначения специфической фармакотерапии.
Лекарственные средства, применяемые при нарушениях мочеиспускания, простатите и связанных с доброкачественной гиперплазией предстательной железы, классифицируют на:
II. Ферментные препараты:
III. Комбинированые преараты:
Тамсулозин + Финастерид (Сонирид Дуо),
Тамсулозин + Дутастерид (Дуодарт).
IV. Специфические препараты антител:
Действие препаратов данной группы связано с селективной блокадой постсинаптических α1-адренорецепторов, расположенных в строме и капсуле предстательной железы и шейке мочевого пузыря. 70% всех подтипов α1-адренорецепторов, представленных в предстательной железе, является подтип 1А. Препараты прямо воздействуют на гладкую мускулатуру ткани предстательной железы и во время мочеиспускания уменьшают сопротивление оттоку мочи.
Симптомы, вызываемые ДГПЖ, связаны с инфравезикальной обструкцией выходного тракта мочевого пузыря и обусловлены двумя составляющими: статической обструкцией, в результате сдавливания мочеиспускательного канала гиперплазированной тканью предстательной железы, и динамической обструкцией, вследствие гиперактивности α1А-адренорецепторов, от этого зависит тонус гладкой мускулатуры простатической части мочеиспускательного канала и шейки мочевого пузыря и предстательной железы, управляемой симпатической нервной системой.
Адреноблокаторы способствуют нормализации мочеиспускания, уменьшаются симптомы, связанные с ДГПЖ, улучшается отток мочи, снижается мышечный тонус и облегчается опорожнение мочевого пузыря.
Дозу препаратов следует подбирать на основании индивидуальной реакции пациента на проводимую терапию. Все препараты принимают внутрь, не разжевывая, запивая ½–1 стаканом воды. Запрещается измельчать, размалывать таблетку и растирать в порошок. Эти действия могут привести к ненадлежащему высвобождению действующих веществ из таблетки и его быстрой абсорбции, что повышает риск развития нежелательных реакций.
Важно! При применении препаратов этой группы может возникать выраженное снижение АД — ортостатическая гипотензия; очень редко — «приливы» крови к коже лица, головная боль, сонливость, парестезия (онемение, жжение или покалывание), ортостатическое головокружение, слабость, сухость слизистой оболочки полости рта.
Перед началом терапии пациента необходимо предупредить, каким образом следует избегать симптомов развития ортостатической гипотензии, в частности, необходимо воздержаться от резких перемен положения тела и желательно принимать препараты на ночь перед сном в положении «сидя» или «лежа», после чего пациент должен находиться в постели в течение 6–8 час.
В начале лечения пациенту следует дать рекомендации о необходимости соблюдать осторожность в случае появления слабости или головокружения, проинформировать об увеличении риска развития ортостатической гипотензии при употреблении алкоголя, выполнении физических упражнений, а также при жаркой погоде. В период лечения необходимо воздержаться от управления транспортными средствами и занятий потенциально опасными видами деятельности, требующими повышенной концентрации внимания и быстроты психомоторных реакций.
Доксазозин (Doxazosinum) — ТН «Кардура», «Камирен», «Урокард»,табл. 1 мг, 2 мг, 4 мг — применяется для улучшения показателя уродинамики и уменьшает проявления симптомов ДГПЖ. Действующее вещество — доксазозина мезилат. Действие препарата вызвано селективной блокадой α1-адренорецепторов. Поддерживающий эффект при лечении Доксазозином и его безопасность доказаны при длительном применении препарата (до 48 мес.), толерантность к препарату не развивается. У пациентов, получавших препарат, отмечалось улучшение эректильной функции. Рекомендуемая начальная доза препарата составляет 1 мг 1 раз в сутки для того, чтобы свести к минимуму возможность развития ортостатической гипотензии и/или обморока. В зависимости от индивидуальных особенностей показателей уродинамики и наличия симптомов ДГПЖ дозу можно увеличить до 2 мг, а затем до 4 мг и до максимальной суточной дозы 8 мг. Рекомендуемый интервал для повышения дозы составляет 1–2 недели. Обычно рекомендуемая поддерживающая доза равна 2–4 мг — 1 раз в сутки.
Доксазозин подвергается пресистемному метаболизму и активной биотрансформации в печени. Его метаболиты не обладают фармакологической активностью и не оказывают побочные метаболические эффекты, поэтому могут применяться у пациентов с бронхиальной астмой, сахарным диабетом, левожелудочковой недостаточностью и подагрой. Большая часть принятого внутрь ЛП выводится в виде неактивных метаболитов через кишечник, менее 5% дозы выводится в неизмененном виде.
Теразозин (Terazosin) — ТН «Корнам»,табл. 2 мг, 5 мг и «Сетегис»,табл. 1 мг, 2 мг, 5 мг, 10 мг. Активное вещество: теразозина гидрохлорида дигидрат. После приема внутрь препарат быстро и практически полностью абсорбируется из ЖКТ. Прием пищи не влияет на абсорбцию. Биодоступность составляет 80–100%. Для Теразозина не характерен эффект «первичного прохождения», поэтому почти вся доза неизмененного Теразозина поступает в системный кровоток. Максимальная концентрация в сыворотке крови достигается в течение 1–2 ч после приема внутрь. Около 90–94% препарата связывается с белками плазмы крови. Метаболизируется в печени путем гидролиза, деметилирования и деалкилирования с образованием 5 метаболитов, один из которых — пиперазиновое производное Теразозина — фармакологически активен. Примерно 60% от принятой дозы выводится через кишечник (из них 20% в неизмененном виде, остальное — в виде метаболитов), 40% выводится почками. Период полувыведения составляет 8–13 ч.
Алфузозин (Alfuzosin) — ТН «Дальфаз ретард», табл., покр. обол., 5 мг и 10 мг пролонгированного действия, являясь производным хиназолина, активен при пероральном применении. Препарат оказывает благоприятный эффект на уродинамику, приводит к уменьшению симптомов раздражения мочевыводящих путей и снижает симптомы, обусловленные нарушением оттока мочи. Уже начиная с первой дозы значительно увеличивает отток в среднем на 30%, снижает давление в детрузоре мочевого пузыря и увеличивает объем мочи, вызывающий позыв к мочеиспусканию, а также значительно снижает объем остаточной мочи. Препарат не оказывает неблагоприятного действия на сексуальную функцию. В связи с селективностью действия Алфузозина, его влияние на α1-адренорецепторы сосудов и на артериальное давление (АД) в случае его применения в терапевтических дозах практически отсутствует. После приема внутрь 5 мг Алфузозина максимальная концентрация в плазме крови достигается через 3 ч. Прием пищи не оказывает влияния на всасывание активного вещества. Период полувыведения из плазмы крови составляет 8 ч. Биодоступность — 45–53%.
Важно! Одновременное назначение препарата с сильными ингибиторами изофермента CYP3A4 может привести к увеличению концентрации. Большинство метаболитов выводится через кишечник (75–90%). В моче обнаруживается только 11% неизмененного Алфузозина.
Противопоказанием служит гиперчувствительность к препарату, детский возраст до 18 лет, пожилой возраст (старше 75 лет). Рекомендованная доза составляет 5 мг 2 раза в сутки (утром и вечером). Из побочных эффектов наиболее часто возникают тошнота, боль в животе, диарея, сухость слизистой оболочки полости рта, головокружение, головная боль. Перед началом лечения пациент должен быть предупрежден о возможности возникновения симптомов пастуральной гипотензии.
Тамсулозин ( Tamsulosin ) — ТН «Омник», табл. и капс. 0,4 мг (0,0004 г) — я вляется специфическим блокатором постсинаптических α1А-адренорецепторов, находящихся в гладкой мускулатуре предстательной железы, шейки мочевого пузыря, простатической части уретры и подтипа αI D в теле мочевого пузыря. Активное вещество: тамсулозина гидрохлорид.
Препарат хорошо всасывается в кишечнике, обладает почти 100% биодоступностью. После однократного приема препарата 0,4 мг внутрь его Сmах в плазме достигается через 6 ч. Терапевтический эффект проявляется приблизительно через 2 недели от начала лечения. При незначительной и умеренной степени печеночной и почечной недостаточности не требуется коррекции режима дозирования. Прием пищи замедляет всасывание Тамсулозина.
Важно! Препарат противопоказан при выраженной печеночной и тяжелой почечной недостаточности с клиренсом креатинина менее 10 мл/мин., потому что медленно метаболизируется в печени с образованием менее активных метаболитов
Препарат следует использовать с осторожностью в комбинации с сильными и умеренными ингибиторами CYP3A4.
Силодозин ( Silodosin ) — ТН « Урорек»,табл. 4 мг и 8 мг — высокоселективный конкурентный антагонист α1А-адренорецепторов, блокирует постсинаптические α1А-адренорецепторы. Активное вещество : силодозин.
При приеме внутрь Силодозин хорошо абсорбируется, абсолютная биодоступность составляет 32%. Пища снижает Сmах примерно на 30%, увеличивая время достижения максимальной концентрации примерно до 1 ч и оказывает минимальное влияние на площадь под кривой «концентрация–время». Экскретируется в основном в виде метаболитов и в очень малом количестве в неизмененном виде с мочой. Рекомендуемая доза — 8 мг однократно, одновременно с приемом пищи, предпочтительно в одно и то же время суток.
Важно! Из побочных эффектов наиболее часто: заложенность носа, диарея.
Диагностика и лечение доброкачественной гиперплазии предстательной железы
Доброкачественная гиперплазия предстательной железы (ДГПЖ) распространена настолько, что многие исследователи говорят о неизбежности этого состояния у мужчин. К 80 годам 80% мужчин страдают этим недугом. Этиология заболевания изучена недостаточно. Впервы
Доброкачественная гиперплазия предстательной железы (ДГПЖ) распространена настолько, что многие исследователи говорят о неизбежности этого состояния у мужчин. К 80 годам 80% мужчин страдают этим недугом. Этиология заболевания изучена недостаточно. Впервые ДГПЖ проявляется гистологически у мужчин старше 40 лет появлением стромальных узелков в периуретральной области переходной зоны простаты. За узлообразованием следует непосредственно железистая гиперплазия [5, 6].
Клинически данное заболевание проявляется различными симптомами, связанными с нарушением пассажа мочи по нижним мочевым путям. Причинами нарушения мочеиспускания являются инфравезикальная обструкция и ослабление функции детрузора. В основе обструкции лежит увеличение простаты в размерах с постепенным сужением просвета мочеиспускательного канала (механический компонент) и повышением тонуса гладкомышечных волокон простаты и задней уретры (динамический компонент) [6].
У части пожилых мужчин с ДГПЖ вторичные структурно-функциональные изменения детрузора обструктивного характера усугубляются стрессорными (прямое катехоламиновое воздействие) и ишемическими (спазм сосудов) повреждениями гладкомышечных элементов мочевого пузыря.
Эфферентным звеном стресс-реакции являются соответствующие волокна симпатических нервов и адренорецепторы. В этих случаях мочевой пузырь испытывает повышенное воздействие катехоламинов и, как следствие этого процесса, возникают расстройства биоэнергетики и функции детрузора [6, 7]. Качество мочеиспускания начинает все более ухудшаться, что заставляет пациентов обращаться за медицинской помощью.
«Золотым стандартом» лечения ДГПЖ во всем мире является трансуретральная резекция предстательной железы. Тем не менее терапия расстройств мочеиспускания, обусловленных ДГПЖ, в последние годы находит все более широкое применение. С одной стороны, это связано с появлением новых лекарственных препаратов, а с другой — с расширением показаний к медикаментозной терапии и одновременной возможностью наблюдения за больными.
Учитывая многообразие доступных на данный момент способов медикаментозной терапии, большую актуальность имеет вопрос формулировки показаний и выбор препарата для ее проведения.
Для принятия решения о целесообразности медикаментозной терапии ДГПЖ все пациенты должны пройти соответствующее предварительное обследование.
Современные методы диагностики заболевания характеризуются минимальной инвазивностью и высокой точностью. Исследования, проводимые у больных ДГПЖ, подразделяют на основные и уточняющие. К основным исследованиям относятся:
В соответствии с современной концепцией основные методы исследования должны не только точно диагностировать ДГПЖ и ее основные осложнения, но и выявлять факторы риска прогрессирования заболевания, к которым следует отнести:
Так, у мужчин с умеренными или выраженными симптомами гиперплазии простаты (IPSS > 7), сниженной максимальной скоростью мочеиспускания (Qmax 30 см 3 ) или повышенным (> 1,4 нг/мл) уровнем ПСА риск оперативного лечения приблизительно в 4 раза выше, чем у мужчин, не имеющих этих клинических признаков. Таким образом, любой из вышеупомянутых показателей определяет клиническую значимость заболевания и соответственно может быть показанием к назначению лечения (в ряде случаев — профилактического).
Применение уточняющих методов исследования представляется целесообразным в следующих случаях:
К уточняющим методам можно отнести как традиционные — ретроградную уретроцистографию, экскреторную урографию, комплексное уродинамическое исследование и уретроцистоскопию, так и относительно новые — трансректальную эхо-допплерографию, эхо-уродинамическое исследование, микционную мультиспиральную цистоуретрографию, магнитно-резонансную томографию (МРТ). Рассмотрим несколько подробнее возможности самых новых методов визуализации.
Трансректальная ультразвуковая допплерография простаты в первую очередь расширяет возможности диагностики рака предстательной железы. По полученным нами данным, специфичность (85%) и чувствительность (65%) этого метода при диагностике рака простаты выше, чем у обычного УЗИ [1–5, 9]. Кроме того, известные сегодня допплерографические факторы риска развития интраоперационных кровотечений позволяют планировать ход трансуретральных резекций простаты в зависимости от топического расположения избыточно васкуляризированных зон, определять показания к предоперационной подготовке (лечение ингибиторами 5α-редуктазы), направленной на снижение указанного риска ([4, 9].
Эхо-уродинамическое исследование позволяет без вмешательства в мочевые пути определить сократительную способность мышцы мочевого пузыря — детрузора, а также визуализировать шейку мочевого пузыря и простатический отдел уретры в момент мочеиспускания. Использование данной методики целесообразно для дифференциальной диагностики ДГПЖ и других причин нарушенного мочеиспускания, например гипотонии детрузора, стриктуры или камня уретры [1–3, 5].
В ходе микционной мультиспиральной цистоуретрографии с использованием мультиспирального компьютерного томографа визуализируются нижние мочевые пути во время мочеиспускания. Метод уникально информативен при выраженных изменениях анатомии нижних мочевых путей, в частности после оперативных вмешательств, что важно при планировании повторной операции. МРТ главным образом используется для распознавания и установления стадии рака простаты. В то же время информация, получаемая в результате МРТ, позволяет не только с высокой точностью диагностировать структурные изменения в простате, но и определять размеры и характер роста предстательной железы, что также важно при планировании оперативных вмешательств по поводу ДГПЖ, в особенности при повторных вмешательствах. При МРТ, однако, в отличие от мультиспиральной микционной цистоуретрографии нижние мочевые пути четко не визуализируются [4, 8].
Опыт применения современных диагностических методик у больных ДГПЖ показывает, что они позволяют установить диагноз гиперплазии простаты и распознать клинически значимые формы заболевания, выявить особенности гиперплазии, определяющие индивидуальный план лечения, рационально планировать оперативные вмешательства по поводу ДГПЖ, в том числе повторные, когда имеются выраженные изменения анатомии простаты и нижних мочевых путей.
В соответствии с клиническими рекомендациями Европейской ассоциации урологов актуальными целями лечения больных ДГПЖ являются:
Методы лечения больных ДГПЖ подразделяются на консервативные и оперативные. Консервативное ведение больного может быть медикаментозным или заключаться в динамическом наблюдении. При динамическом наблюдении пациент регулярно посещает врача без назначения какой-либо дополнительной терапии. По рекомендациям Европейской ассоциации урологов интервалы между посещениями и повторными обследованиями составляют приблизительно 1 год. Данный вид ведения больного допустим при незначительной (IPSS ё 7) и/или не доставляющей беспокойства симптоматике и при условии отсутствия абсолютных показаний к оперативному лечению.
Медикаментозная терапия — наиболее широко используемый метод лечения больных ДГПЖ. Именно появление современных лекарственных средств привело в 90-х годах прошлого века к существенному снижению числа операций по поводу данного заболевания.
Современные медикаментозные средства терапии ДГПЖ обладают высокой эффективностью и безопасностью, доказанными при многолетнем использовании. Сегодня наиболее изучены и широко используются в клинической практике препараты трех групп:
Помимо способности уменьшать степень выраженности симптомов и улучшать объективные параметры мочеиспускания, каждая группа препаратов обладает рядом свойств, определяющих дополнительные показания к их применению.
Так, установлено, что α1-адреноблокаторы являются наиболее быстро действующими препаратами — эффект от их применения развивается уже через 5–10 дней. В то же время в ходе клинических исследований установлено, что доксазозин (Кардура) и тамсулозин (Омник) эффективны как при острой задержке мочи, так и в профилактике послеоперационной ишурии. Теразозин, доксазозин и альфузозин способны снижать артериальное давление при сопутствующей артериальной гипертензии, а тамсулозин позволяет улучшить показатели сердечной деятельности у больных ДГПЖ с сопутствующей ИБС.
Ингибиторы 5α-редуктазы не только способствуют уменьшению размеров предстательной железы (в среднем на 30%), но и эффективны при макрогематурии, обусловленной гиперплазией простаты, а также снижают интраоперационную кровопотерю (при использовании препаратов в порядке подготовки к трансуретральной резекции простаты).
В ходе исследования PCPT (Prostate Cancer Prevention Trial) установлено, что прием ингибитора 5α-редуктазы финастерида снижает риск развития рака простаты на 25%. Не менее авторитетное исследование MTOPS (Medical Treatment Of Prostatic Symptoms) показало, что монотерапия ингибитором 5a-редуктазы финастеридом (Финаст) снижает риск прогрессирования ДГПЖ в 2 раза, а при его сочетании с α1-адреноблокатором — на 67%.
Таким образом, было доказано, что комбинированное лечение ингибитором 5α-редуктазы и α1-адреноблокатором может быть целесообразным с точки зрения не только более быстрого ослабления расстройств мочеиспускания, но и предотвращения развития осложнений ДГПЖ (например, острой задержки мочи).
Из растительных препаратов наиболее глубоко изучен экстракт Serenoa repens (Пермиксон, Простамол уно), который также обладает способностью уменьшать объем гиперплазированной простаты (в среднем на 20%). Данные клинических исследований свидетельствуют о том, что указанный экстракт обладает противовоспалительной и противоотечной активностью, что делает целесообразным его назначение больным ДГПЖ при сопутствующем простатите.
Нельзя не отметить, что современный подход к выработке лечебной тактики у больных гиперплазией простаты предусматривает активное участие пациента в этом процессе. В связи с этим задача врача — подробно информировать пациента о заболевании и сопряженных с ним рисках, преимуществах и недостатках различных вариантов лечения, особенностях лечения в данном конкретном случае. Целесообразность подобного подхода диктуется тем, что когда речь идет о качестве жизни, никто лучше пациента не способен определить, что для него наиболее значимо как в самом заболевании, так и в способах его лечения. В результате вид лечения определяется не только исходя из индивидуальных особенностей заболевания, но и с учетом личных предпочтений больного.
При соблюдении указанных принципов медикаментозная терапия высокоэффективна. Перспективы дальнейшего развития данного направления в лечении ДГПЖ огромны и базируются на успехах современной медицинской науки.
Литература
Ю. Г. Аляев, доктор медицинский наук, профессор, член-корреспондент РАМН
В. А. Григорян, доктор медицинский наук, профессор
Д. В. Чиненов, кандидат медицинский наук
ММА им. И. М. Сеченова, Москва