Диагноз дтз что это
Что такое зоб диффузный токсический (Базедова болезнь)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Родионова Е. А., терапевта со стажем в 13 лет.
Определение болезни. Причины заболевания
Диффузный токсический зоб — это аутоиммунное поражение щитовидной железы.
В англоязычных странах это заболевание называют болезнью Грейвса, а немецкоязычных — Базедовой болезнью. Диффузный токсический зоб развивается из-за нарушенной функции СД8+-лимфоцитов и выработки антитиреоидных антител, среди которых особое значение придаётся тем, которые имеют сродство к рецепторам тиреотропного гормона в щитовидной железе. Эти антитела выявляются в среднем у 50% пациентов с диффузным токсическим зобом. С этими рецепторами в норме связывается тиреотропный гормон (ТТГ), что стимулирует выработку и выделение тиреоидных гормонов (ТГ). Антитела при связывании с рецепторами ТТГ увеличивают секрецию тироксина (Т4) и трийодтиронина (Т3) «в обход» регуляции ТТГ. Повышенный уровень тиреотропного гормона обуславливает развитие тиреотоксикоза. До конца не ясна причина такого дефекта иммунной системы. Имеются данные, позволяющие говорить о роли генетической предрасположенности, в частности, более широкой распространённости аллелей HLA-B8 и BW-35 у пациентов с этой болезнью. [4] Однако не выявлено какой-то одной аллели, ответственной за болезнь Грейвса. Вероятно, здесь имеет место взаимодействие нескольких аллелей.
Симптомы диффузного токсического зоба
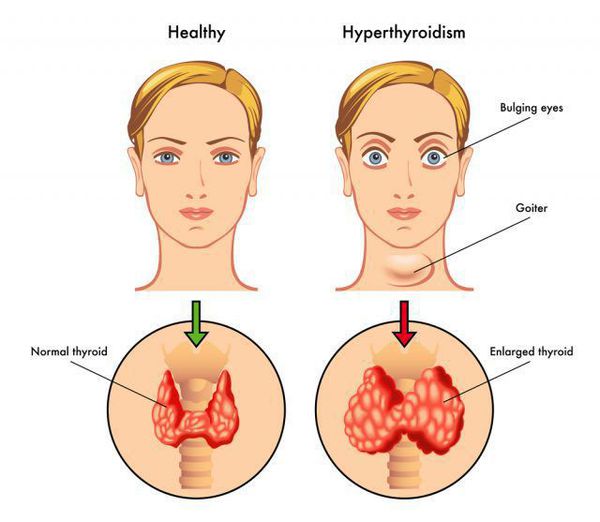
При Базедовой болезни могут появляться признаки эндокринной офтальмопатии, возникающей из-за поражения периорбитальной клетчатки: выраженный экзофтальм (не всегда симметричный), диплопия, отечность век, ощущение «инородного тела в глазах». Это сильно облегчает работу врача в плане диагностики, так как среди всех состояний с тиреотоксикозом эндокринная офтальмопатия характерна именно для диффузного токсического зоба. Не следует путать эндокринную офтальмопатию с глазными симптомами тиреотоксикоза, среди которых можно выделить синдром Грефе и синдром Кохера (верхнее веко отстаёт при взгляде вверх и вниз соответственно), синдром Мебиуса (взгляд не фиксируется вблизи), синдром Штельвага (уменьшение частоты морганий). Стоит отметить, что выраженность глазных симптомов не зависит от тяжести дисфункции щитовидной железы. [4]
Некоторые авторы в развитии диффузного токсического зоба выделяют четыре стадии:
Патогенез диффузного токсического зоба
Классификация и стадии развития диффузного токсического зоба
Согласно классификации тиреотоксикоза по Фадееву В.В. и Мельниченко Г.А., выделяется:
Также существует классификация зоба (патологического увеличения щитовидной железы), в которой выделяется три степени зоба, в зависимости от данных осмотра и пальпации щитовидной железы.
Классификация зоба, рекомендованная ВОЗ (2001)
Осложнения диффузного токсического зоба
Развившийся при диффузном токсическом зобе тиреотоксикоз поражает все системы организма. Если надлежащим образом не лечить это заболевание, то оно грозит тяжёлой инвалидизацией, а аритмии и сердечная недостаточность даже могут привести к летальному исходу.
Наиболее опасным осложнением болезни Грейвса является тиреотоксический криз, развитие которого связывают с неблагоприятными факторами (стресс, различные заболевания, выраженная физическая нагрузка, операция и др.). Появляется резкое возбуждение, температура повышается до 40 о С, частота сердечных сокращений достигает 200 ударов в минуту, может развиться фибрилляция предсердий, усиливаются явления диспепсии (тошнота, рвот, понос, жажда), повышается пульсовое артериальное давление. Затем могут появиться признаки недостаточности надпочечников (гиперпигментация, нитевидный пульс, нарушение микроциркуляции). Состояние ухудшается за несколько часов. Это ургентная ситуация, требующая неотложных мер, направленных на снижение концентрации ТГ, борьбу с надпочечниковой недостаточностью, дегидратацией, гипертермией, метаболическими нарушениями и недостаточностью кровообращения. В/в вводится гидрокортизон, проводится дезинтоксикационная и тиреостатическая терапия. К осложнениям диффузного токсического зоба также можно отнести осложнения хирургического его лечения: гипопаратиреоз, повреждение n. laryngeus recurrens (при повреждении одного нерва появляется осиплость голоса, при повреждении двух может возникнуть асфиксия), кровотечения, аллергические реакции на препараты. Об осложнениях тиреостатической терапии будет сказано ниже. [5]
Диагностика диффузного токсического зоба
При наличии у пациента признаков тиреотоксикоза ему определяют уровень тиреотропного гормона (ТТГ) высокочувствительным методом (чувс. 0,01 мЕд/л). Если уровень ТТГ меньше нормы, то исследуют концентрацию св. Т4 (тетрайодтиронин, тироксин) и Т3 (трийодтиронин). Существует понятие о так называемом субклиническом тиреотоксикозе, когда уровни Т4 и Т3 оказываются в норме. Среди антител наибольшее клиническое значение имеет уровень антител к рецепторам ТТГ (АТ-рТТГ). Высокие их титры с большой долей вероятности указывают на то, что мы имеем дело именно с болезнью Грейвса. Другие антитела, такие, как антитела к тиреоидной пероксидазе и тиреоглобулину (АТ-ТПО и АТ-ТГ), выявляются и при других состояниях, поэтому имеют значение только в комплексной оценке, и их определение может помочь в некоторых ситуациях.
Лечение диффузного токсического зоба
Лечение болезни Грейвса может проводиться эндокринологом или терапевтом. К сожалению, в настоящее время лечение диффузного токсического зоба направлено только на орган-мишень, то есть щитовидную железу, а не на выработку антител, являющуюся непосредственной причиной развития болезни. Даже после удаления щитовидной железы продолжают синтезироваться антитела к рецепторам тиреотропного гормона, хотя тиреотоксикоза уже не возникает (при адекватной заместительной терапии). [9]
Итак, существует три способа лечения диффузного токсического зоба:
Выбор метода зависит от возраста, сопутствующих заболеваний, степени увеличения щитовидной железы, желания пациента и возможностей лечебного учреждения. Консервативный метод лечения диффузного токсического зоба заключается в назначении тиреостатиков. В некоторых случаях (до 30%) курс такого лечения способен привести к стойкой ремиссии, в некоторых — является подготовкой к использованию другого, более радикального метода (хирургическое лечение или терапия йодом-131). Считается, что консервативная терапия неэффективна при выраженном увеличении щитовидной железы (более 40 см 3 ) и с признаками сдавления окружающих тканей, при наличии крупных узлов в ней, а также при наличии осложнений (фибрилляция предсердий, остеопороз и др.). При рецидиве после курса терапии тиреостатиком, повторный длительный курс не назначается. [5] В подобных случаях проводится курс медикаментозной подготовки к радиойодтерапии или операции.
Важным условием адекватного проведения консервативного лечения является приверженность пациента к лечению и доступность лабораторного контроля. Тиреостатики блокируют синтез тиреоидных гормонов и купируют тиреотоксикоз. По прошествии 4-6 недель тиреостатической терапии, при наступлении эутиреоидного состояния, обычно к лечению добавляют левотироксин. [4] В период тиреотоксикоза (до нормализации Т4) также целесообразно назначение препаратов из группы β-адреноблокаторов: они подавляют тканевое превращение Т4 в Т3, снижают частоту сердечных сокращений. Критерием адекватности лечения является нормальный уровень Т4 и ТТГ. Курс лечения продолжается 12-18 месяцев. Во время лечения необходимо контролировать показатели общего анализа крови. Это необходимо для контроля грозных осложнений тиреостатической терапии — агранулоцитоза и тромбоцитопении, требующих немедленной отмены препаратов. Симптомы агранулоцитоза: лихорадка, боль в горле, жидкий стул. [4] При их появлении пациенту необходимо экстренно сдать кровь на общий анализ и прекратить приём тиреостатиков до получения результатов анализа. Рецидив чаще всего наступает в первые 12 месяцев после завершения курса.
Под хирургическим лечением подразумевается удаление всей или большей части щитовидной железы. [8] Операция проводится только в состоянии эутиреоза. В настоящее время удаление этого органа не является фатальным для человека, так как имеются все возможности адекватной и недорогой заместительной терапии левотироксином. С другой стороны, при оставлении даже небольшого фрагмента железы, сохраняется вероятность рецидива заболевания, это орган-мишень для антитиреоидных антител, выделяемых иммунной системой. Таким образом, послеоперационный гипотиреоз теперь не рассматривается в качестве осложнения операции, а является её целью. Доза левотироксина после операции подбирается индивидуально и обычно составляет 1,7 мкг/кг в сутки.
Прогноз. Профилактика
Болезнь Грейвса, гипертиреоз
Диффузный токсический зоб (ДТЗ, болезнь Грейвса-Базедова) – аутоиммунное заболевание, характеризующееся стойкой патологической гиперсекрецией гормонов щитовидной железы и, как правило, диффузно увеличенной щитовидной железой (ЩЖ).
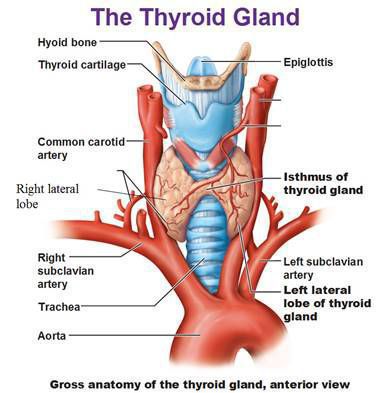
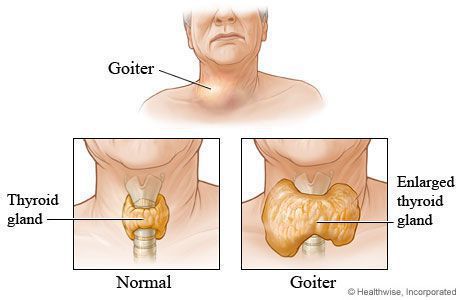
Зоб – патологическое увеличение ЩЖ, без уточнения ее функционального состояния. Нормальный объем ЩЖ, определяемый с помощью УЗИ, у мужчин не должен превышать 25 мл, у женщин 18 мл. Пальпация ЩЖ, являясь основным методом клинического исследования ЩЖ, не позволяет определить ее объем и самостоятельного значения для диагностики зоба не имеет.
Тиреотоксикоз – это не болезнь, а клинический синдром, вызванный стойкой патологической гиперсекрецией гормонов щитовидной железы. Термин гипертиреоз означает повышение функциональной активности щитовидной железы, которая может быть патологическим (тиреотоксикоз) и физиологическим (например при беременности). Тяжесть тиреотоксикоза оценивают по клинической картине и наличию осложнений, связанных с заболеванием (мерцательная аритмия, дистрофические изменения внутренних органов, тиреотоксический психоз и т.д.).
Причиной ДТЗ является дефект иммунной системы, приводящей к образованию антител, которые стимулируют продукцию избыточного количества гормонов щитовидной железы.
Антитела – это белки, которые вырабатывают клетки иммунной системы – лимфоциты. Эти антитела способны соединяться с рецепторами ТТГ (гормон, который в норме регулирует функцию ЩЖ) и, как волк в овечьей шкуре, бесконтрольно стимулировать выработку тиреоидных гормонов. Щитовидная железа просто «не понимает», кто ее стимулирует. Отсюда они получили название – антитела к рецепторам ТТГ (АТрТТГ).
У 50% родственников пациента ДТЗ выявляют циркулирующие антитела. Иногда встречается сочетание с другими аутоиммунными заболеваниями (хронической надпочечниковой недостаточностью, сахарным диабетом 1 типа и т.д.). Женщины болеют в 5-10 раз чаще мужчин. Как правило, ДТЗ манифестирует в молодом и среднем возрасте.
Клиническая картина
Глазные симптомы тиреотоксикоза принципиально отличать от самостоятельного заболевания эндокринной офтальмопатии.
Эндокринная офтальмопатия (ЭОП) — поражение периорбитальных тканей аутоиммунного генеза, в 95% случаев сочетающееся с аутоиммунными заболеваниями щитовидной железы (ЩЖ), клинически проявляющееся дистрофическими изменениями глазодвигательных мышц (ГДМ) и других структур глаза.
Антитела к рецепторам ТТГ (АТрТТГ) имеют несколько функционально и иммунологически различных субпопуляций. АТрТТГ могут вызывать иммунное воспаление и отек ретробульбарной клетчатки, что приводит к уменьшению объема полости глазницы с развитию экзофтальма (пучеглазия) и дистрофии глазодвигательных мышц.
ЭОП начинается постепенно, часто с одной стороны. Начальные симптомы: чувство давления за глазными яблоками, повышенная светочувствительность, ощущение инородного тела, «песка в глазах». Далее симптоматика нарастает.
Диагностика
Лечение
Медикаментозная терапия.
Тионамиды мерказолил (метимазол, тиамазол) и пропилтиоурацил (пропицил) тормозят ряд процессов в щитовидной железе, что приводит к блокаде синтеза и освобождения тиреоидных гормонов.
Мерказолил назначается под еженедельным, а в дальнейшем ежемесячным контролем уровня лейкоцитов крови. По мере постепенного уменьшения симптоматики доза мерказолила также постепенно снижается до поддерживающей, которая принимается 16-18 месяцев (у детей 2 года).
Длительная терапия одновременно мерказолилом и левотироксином известна как схема «блокируй и замещай». Мерказолил в данном случае блокирует секрецию тиреоидных гормонов, а левотироксин поддерживает эутиреоидное состояние (при монотерапии мерказолилом развивается медикаментозный гипотиреоз). Частота рецидивов после медикаментозного лечения составляет порядка 40%.
Тяжелыми, но редкими ( 131 I: послеоперационный рецидив ДТЗ, пожилой возраст, сопутствующая патология, делающая нежелательным или исключающая назначение тиреостатиков и/или проведение операции, отказ пациента от оперативного лечения. Первичный гипотиреоз, который может развиться после резекции ЩЖ и развивается практически у всех пациентов после терапии радиоактивным йодом в современных условиях при возможности назначения заместительной терапии L-тироксином следует считать не осложнением, а исходом лечения. В Европе и, особенно в США показания для терапии радиоактивным йодом значительно шире, чем в России. Она считается методом первого выбора у пациентов старше 35 лет (у женщин не планирующих беременность), поскольку эффективно (быстро купирует симптомы тиреотоксикоза, рецидивы крайне редки), недорого (по сравнению с длительными курсами терапии тиреостатиками и другими препаратами, оперативное лечение), безопасно (лучевая нагрузка минимальна; тяжелые осложнения, возможные при хирургическом лечении, исключаются).
Лечение эндокринной офтальмопатии
1. Лечение заболевания ЩЖ с поддержанием стойкого эутиреоза. Гипотиреоз и курение провоцируют прогрессирование ЭОП.
2. Местное лечение: светозащитные очки, глазные капли с дексаметазоном.
3. Глюкокортикоиды (ГК) начиная со 2 степени ЭОП. Глюкокортикоиды назначают по специальной схеме с постепенным снижением дозы на протяжении 3 месяцев. При тяжелой, быстропрогрессирующей ЭОП лечение начинают с курса пульс-терапии – преднизолон вводится внутривенно в большой дозе на протяжении 3 дней с последующим переходом на пероральные препараты. В случае резистентной к терапии ГК ЭОП, в единичных случаях, показано назначение цитостатических препаратов.
4. Рентгенотерапия на область орбиты при резистентности к терапии ГК, в сочетании с ней, при рецидивах ЭОП после отмены ГК.
5. Хирургическая декомпрессия глазницы с удалением ретробульбарной клетчатки, а при необходимости костных стенок глазницы.
6. Косметические операции на глазном яблоке с целью коррекции экзофтальма и косоглазия, развивающихся в результате фиброза ГДМ.
Диффузный токсический зоб (болезнь Базедова, болезнь Грейвса) – заболевание, обусловленное гипертрофией и гиперфункцией щитовидной железы, сопровождающееся развитием тиреотоксикоза. Клинически проявляется повышенной возбудимостью, раздражительностью, похуданием, сердцебиением, потливостью, одышкой, субфебрильной температурой. Характерный симптом – пучеглазие. Ведет к изменениям со стороны сердечно-сосудистой и нервной систем, развитию сердечной или надпочечниковой недостаточности. Угрозу для жизни пациента представляет тиреотоксический криз.
Общие сведения
Диффузный токсический зоб носит аутоиммунную природу и развивается вследствие дефекта в иммунной системе, при котором происходит выработка антител к рецепторам ТТГ, оказывающих постоянное стимулирующее воздействие на щитовидную железу. Это приводит к равномерному разрастанию тиреоидной ткани, гиперфункции и повышению уровня производимых железой тиреоидных гормонов: Т3 (трийодтиронина) и Т4 (тироксина). Увеличенную в размере щитовидную железу называют зобом.
Избыток тиреоидных гормонов усиливает реакции основного обмена, истощает запасы энергии в организме, необходимые для нормальной жизнедеятельности клеток и тканей различных органов. Наиболее восприимчивы к состоянию тиреотоксикоза сердечно – сосудистая и центральная нервная системы.
Диффузный токсический зоб развивается преимущественно у женщин от 20 до 50 лет. В пожилом и детском возрасте возникает довольно редко. Пока эндокринология не может точно ответить на вопрос о причинах и механизмах запуска аутоиммунных реакций, лежащих в основе диффузного токсического зоба. Заболевание нередко выявляется у пациентов, имеющих наследственную предрасположенность, которая реализуется под влиянием многих факторов внешней и внутренней среды. Появлению диффузного токсического зоба способствуют инфекционно-воспалительные заболевания, психические травмы, органические поражения головного мозга (черепно-мозговые травмы, энцефалит), аутоиммунные и эндокринные нарушения (функции поджелудочной железы, гипофиза, надпочечников, половых желез) и многие другие. Почти в 2 раза увеличивается риск развития зоба, если пациент курит.
Классификация
Диффузный токсический зоб проявляется следующими формами тиреотоксикоза, вне зависимости от размеров щитовидной железы:
Симптомы
Поскольку тиреоидные гормоны отвечают за выполнение множества физиологических функций, тиреотоксикоз имеет разнообразные клинические проявления. Обычно основные жалобы пациентов связаны с сердечно-сосудистыми изменениями, проявлениями катаболического синдрома и эндокринной офтальмопатии. Сердечно-сосудистые нарушения проявляются выраженным учащенным сердцебиением (тахикардией). Ощущения сердцебиения у пациентов возникают в груди, голове, животе, в руках. ЧСС в состоянии покоя при тиреотоксикозе может увеличиваться до 120-130 уд. в мин. При средней тяжести и тяжелой формах тиреотоксикоза происходит увеличение систолического и снижение диастолического артериального давления, повышение пульсового давления.
В случае длительного течения тиреотоксикоза, особенно у пациентов пожилого возраста, развивается выраженная миокардиодистрофия. Она проявляется нарушениями сердечного ритма (аритмией): экстрасистолией, фибрилляцией предсердий. Впоследствии это ведет к изменениям миокарда желудочков, застойным явлениям (периферическим отеками, асциту), кардиосклерозу. Отмечается аритмия дыхания (учащение), склонность к частым пневмониям.
Проявление катаболического синдрома характеризуется резким похуданием (на 10-15 кг) на фоне повышенного аппетита, общей слабостью, гипергидрозом. Нарушение терморегуляции проявляется в том, что больные тиреотоксикозом испытывают чувство жара, не замерзают при достаточно низкой окружающей температуре. У некоторых пожилых пациентов может наблюдаться вечерний субфебрилитет.
Для тиреотоксикоза характерно развитие изменений со стороны глаз (эндокринной офтальмопатии): расширение глазных щелей за счет подъема верхнего века и опущения нижнего, неполное смыкание век (редкое мигание), экзофтальм (пучеглазие), блеск глаз. У больного с тиреотоксикозом лицо приобретает выражение испуга, удивления, гнева. Из-за неполного смыкания век у пациентов появляются жалобы на «песок в глазах», сухость и хронический конъюнктивит. Развитие периорбитального отека и разрастание периорбитальных тканей сдавливают глазное яблоко и глазной нерв, вызывают дефект поля зрения, повышение внутриглазного давления, боль в глазах, а иногда полную потерю зрения.
При длительном тиреотоксикозе под действием избытка тироксина происходит вымывание кальция и фосфора из костной ткани, наблюдается костная резорбция (процесс разрушения костной ткани) и развивается синдром остеопении (уменьшение костной массы и плотности костей). Отмечаются боли в костях, пальцы рук могут приобретать вид «барабанных палочек».
Дисфункция яичников и нарушение менструального цикла при тиреотоксикозе встречаются нечасто. У женщин в пременопаузу может отмечаться уменьшение частоты и интенсивности менструаций, развитие фиброзно-кистозной мастопатии. Умеренно выраженный тиреотоксикоз может не снижать способность к зачатию и возможность наступления беременности. Антитела к рецепторам ТТГ, стимулирующие щитовидную железу, могут передаваться трансплацентарно от беременной женщины с диффузным токсическим зобом плоду. В результате у новорожденного возможно развитие транзиторного неонатального тиреотоксикоза. Тиреотоксикоз у мужчин часто сопровождается эректильной дисфункцией, гинекомастией.
При тиреотоксикозе кожа мягкая, влажная и теплая на ощупь, у некоторых больных появляется витилиго, потемнение складок кожи, особенно на локтях, шее, пояснице, повреждение ногтей (тиреоидная акропахия, онихолиз), выпадение волос. У 3 – 5% пациентов с тиреотоксикозом развивается претибиальная микседема (отек, уплотнение и эритема кожи в области голени и стоп, напоминающие апельсиновую корку и сопровождающиеся зудом).
При диффузном токсическом зобе отмечается равномерное увеличение щитовидной железы. Иногда железа бывает значительно увеличена, а иногда зоб может отсутствовать (в 25-30 % случаев заболевания). Тяжесть заболевания не определяется размерами зоба, так как при небольших размерах щитовидной железы возможна тяжелая форма тиреотоксикоза.
Осложнения
Тиреотоксикоз грозен своими осложнениями: серьезными поражениями ЦНС, сердечно-сосудистой системы (развитием тиреотоксического сердца), желудочно-кишечного тракта (развитием тиреотоксического гепатоза). Иногда может развиться тиреотоксический гипокалиемический преходящий паралич с внезапными, периодически возникающими приступами мышечной слабости.
Течение тиреотоксикоза зоб может осложниться развитием тиреотоксического криза. Основными причинами тиреотоксического криза служат неправильная терапия тиреостатиками, лечение радиоактивным йодом или проведение хирургического вмешательства, отмена лечения, а также инфекционные и другие заболевания. Тиреотоксический криз сочетает в себе симптомы тяжелого тиреотоксикоза и тиреогенной надпочечниковой недостаточности. У пациентов с кризом отмечаются ярко выраженная нервная возбудимость вплоть до психоза; сильное двигательное беспокойство, которое сменяется апатией и нарушением ориентации; лихорадка (до 400С); боли в области сердца, синусовая тахикардия с ЧСС более 120 уд. в мин.; нарушение дыхания; тошнота и рвота. Может развиваться мерцательная аритмия, повышение пульсового давления, нарастание симптомов сердечной недостаточности. Относительная надпочечниковая недостаточность проявляется гиперпигментацией кожи.
При развитии токсического гепатоза кожные покровы приобретают желтушность. Летальный исход при тиреотоксическом кризе составляет 30-50 %.
Диагностика
Объективный статус пациента (внешний вид, вес тела, состояние кожных покровов, волос, ногтей, манера разговора, измерение пульса и артериального давления) позволяет врачу предположить имеющуюся гиперфункцию щитовидной железы. При наличии явных симптомов эндокринной офтальмопатии диагноз тиреотоксикоза почти очевиден.
При подозрении на тиреотоксикоз обязательно определение уровня тиреоидных гормонов щитовидной железы (Т3, Т4), тиреотропного гормона гипофиза (ТТГ), свободных фракций гормонов в сыворотке крови. Диффузный токсический зоб следует отличать от других заболеваний, сопровождающихся тиреотоксикозом. С помощью иммуноферментного анализа (ИФА) крови определяют наличие циркулирующих антител к рецепторам ТТГ, тиреоглобулину (АТ-ТГ) и к тиреоидной пероксидазе (АТ-ТПО). Методом УЗИ щитовидной железы определяется ее диффузное увеличение и изменение эхогенности (гипоэхогенность, характерная для аутоиммунной патологии).
Обнаружить функционально активную ткань железы, определить форму и объем железы, наличие в ней узловых образований позволяет сцинтиграфия щитовидной железы. При наличии симптомов тиреотоксикоза и эндокринной офтальмопатии сцинтиграфия не обязательна, она проводится только в случаях, когда необходимо дифференцировать диффузный токсический зоб от других патологий щитовидной железы. При диффузном токсическом зобе получают изображение щитовидной железы с повышенным поглощением изотопа. Рефлексометрия является косвенным методом определения функции щитовидной железы, измеряющим время рефлекса ахиллова сухожилия (характеризует периферическое действие тиреоидных гормонов – при тиреотоксикозе оно укорочено).
Лечение
Хирургическое лечение подразумевает практически тотальное удаление щитовидной железы (тиреоидэктомия), что приводит к состоянию послеоперационного гипотиреоза, который компенсируется медикаментозно и исключает рецидивы тиреотоксикоза. Показаниями к проведению хирургической операции являются аллергические реакции на назначенные препараты, стойкое снижение уровня лейкоцитов крови при консервативном лечении, зоб большого размера (выше III степени), сердечно – сосудистые нарушения, наличие выраженного зобогенного эффекта от мерказолила. Проведение операции при тиреотоксикозе возможно только после медикаментозной компенсации состояния пациента для предупреждения развития тиреотоксического криза в раннем послеоперационном периоде.
При наличие диффузного токсического зоба у беременной женщины ведение беременности должно осуществляться не только гинекологом, но и эндокринологом. Лечения диффузного токсического зоба при беременности проводится пропилтиоурацилом (он плохо проникает через плаценту) в минимальной дозе, необходимой для поддержания количества свободного тироксина (Т4) на верхней границе нормы или немного выше нее. С увеличением срока беременности потребность в тиреостатике уменьшается, и большинство женщин после 25-30 нед. беременности препарат уже не принимает. После родов (через 3-6 месяцев) у них обычно развивается рецидив тиреотоксикоза.
Лечение тиреотоксического криза включает интенсивную терапию большими дозами тиреостатиков (предпочтительно – пропилтиоурацилом). При невозможности приема препарата пациентом самостоятельно, его вводят через назогастральный зонд. Дополнительно назначаются глюкокортикоиды, b-адреноблокаторы, дезинтоксикационная терапия (под контролем гемодинамики), плазмаферез.
Прогноз
После хирургического лечения тиреотоксикоза возможно развитие состояния гипотиреоза. Пациентам с тиреотоксикозом необходимо избегать инсоляции, употребления йодсодержащих лекарственных препаратов и пищевых продуктов.
Профилактика
Развитие тяжелых форм тиреотоксикоза необходимо предупреждать, проводя диспансерное наблюдение за пациентами с увеличенной щитовидной железой без изменения ее функции. Если анамнез указывает на семейный характер патологии, под наблюдением должны находиться и дети. В качестве профилактических мер важно проводить общеукрепляющую терапию и санацию хронических очагов инфекции.