Диагноз фрж у ребенка что это
Функциональные нарушения желудочно-кишечного тракта у детей грудного возраста: роль диетотерапии
Функциональные нарушения желудочно-кишечного тракта (ЖКТ) представляют одну из наиболее широко распространенных проблем среди детей первых месяцев жизни [1].
Функциональные нарушения желудочно-кишечного тракта (ЖКТ) представляют одну из наиболее широко распространенных проблем среди детей первых месяцев жизни [1]. Отличительной особенностью данных состояний является появление клинических симптомов при отсутствии каких-либо органических изменений со стороны ЖКТ (структурных аномалий, воспалительных изменений, инфекций или опухолей) и метаболических отклонений. При функциональных нарушениях ЖКТ могут изменяться моторная функция, переваривание и всасывание пищевых веществ, а также состав кишечной микробиоты и активность иммунной системы [2–4]. Причины функциональных расстройств часто лежат вне пораженного органа и обусловлены нарушением нервной и гуморальной регуляции деятельности пищеварительного тракта.
В соответствии с Римскими критериями III, предложенными Комитетом по изучению функциональных расстройств у детей и Международной рабочей группой по разработке критериев функциональных расстройств в 2006 г. [5], к функциональным нарушениям ЖКТ у младенцев и детей второго года жизни относят:
У детей грудного возраста, особенно первых 6 месяцев жизни, наиболее часто встречаются такие состояния, как срыгивания, кишечные колики и функциональные запоры. Более чем у половины детей они наблюдаются в различных комбинациях, реже — как один изолированный симптом. Поскольку причины, приводящие к функциональным нарушениям, оказывают влияние на различные процессы в ЖКТ, сочетание симптомов у одного ребенка представляется вполне закономерным. Так, после перенесенной гипоксии могут возникнуть вегетовисцеральные нарушения с изменением моторики по гипер- или гипотоническому типу и нарушения активности регуляторных пептидов, приводящие одновременно к срыгиваниям (в результате спазма или зияния сфинктеров), коликам (нарушения моторики ЖКТ при повышенном газообразовании) и запорам (гипотоническим или вследствие спазма кишки). Клиническую картину усугубляют симптомы, связанные с нарушением переваривания нутриентов, обусловленным снижением ферментативной активности пораженного энтероцита, и приводящие к изменению микробиоценоза кишечника [6].
Причины функциональных нарушений ЖКТ можно разделить на две группы: связанные с матерью и связанные с ребенком.
К первой группе причин относятся:
Причины, связанные с ребенком, заключаются в:
Частыми и наиболее серьезными причинами, приводящими к возникновению срыгиваний, колик и нарушений характера стула, являются перенесенная гипоксия (вегетовисцеральные проявления церебральной ишемии), частичная лактазная недостаточность и гастроинтестинальная форма пищевой аллергии. Нередко в той или иной степени выраженности они наблюдаются у одного ребенка, поскольку последствиями гипоксии являются снижение активности ферментов и повышение проницаемости тонкой кишки.
Под срыгиваниями (регургитацией) понимают самопроизвольный заброс желудочного содержимого в пищевод и ротовую полость.
Частота синдрома срыгиваний у детей первого года жизни, по данным ряда исследователей, составляет от 18% до 50% [7, 8]. Преимущественно срыгивания отмечаются в первые 4–5 месяцев жизни, значительно реже наблюдаются в возрасте 6–7 месяцев, после введения более густой пищи — продуктов прикорма, практически исчезая к концу первого года жизни, когда ребенок значительную часть времени проводит в вертикальном положении (сидя или стоя).
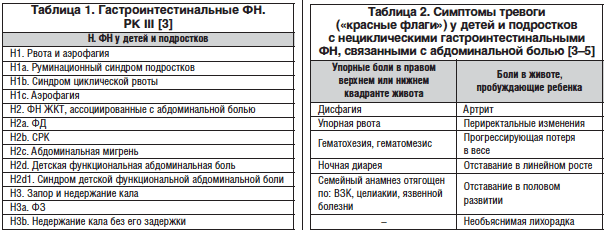
Степень выраженности синдрома срыгиваний, согласно рекомендациям группы экспертов ESPGHAN, предложено оценивать по пятибалльной шкале, отражающей совокупную характеристику частоты и объема регургитаций (табл. 1).
Нечастые и необильные срыгивания не расцениваются как заболевание, поскольку они не вызывают изменений в состоянии здоровья детей. У детей с упорными срыгиваниями (оценка от 3 до 5 баллов) нередко отмечаются осложнения, такие как эзофагит, отставание в физическом развитии, железодефицитная анемия, заболевания ЛОР-органов. Клиническими проявлениями эзофагита являются снижение аппетита, дисфагия и осиплость голоса.
Следующим, часто встречающимся функциональным расстройством ЖКТ у детей грудного возраста являются кишечные колики — это эпизоды болезненного плача и беспокойства ребенка, которые занимают не менее 3 часов в день, возникают не реже 3 раз в неделю. Обычно их дебют приходится на 2–3 недели жизни, достигают кульминации на втором месяце, постепенно исчезая после 3–4 месяцев. Наиболее типичное время для кишечных колик — вечерние часы. Приступы плача возникают и заканчиваются внезапно, без каких-либо внешних провоцирующих причин [9].
Частота кишечных колик, по разным данным, составляет от 20% до 70% [9, 10]. Несмотря на длительный период изучения, этиология кишечных колик остается не вполне ясной.
Для кишечных колик характерен резкий болезненный плач, сопровождающийся покраснением лица, ребенок принимает вынужденное положение, прижав ножки к животу, возникают трудности с отхождением газов и стула. Заметное облегчение наступает после дефекации.
Эпизоды кишечных колик вызывают серьезное беспокойство родителей, даже если аппетит ребенка не нарушен, он имеет нормальные показатели весовой кривой, хорошо растет и развивается.
Кишечные колики практически с одинаковой частотой встречаются как на естественном, так и на искусственном вскармливании. Отмечено, что чем меньше масса тела при рождении и гестационный возраст ребенка, тем выше риск развития данного состояния.
В последние годы большое внимание уделяется роли микрофлоры кишечника в возникновении колик. Так, у детей с данными функциональными расстройствами выявляются изменения состава кишечной микробиоты, характеризующиеся увеличением количества условно-патогенных микроорганизмов и снижением защитной флоры — бифидобактерий и особенно лактобацилл [11, 12]. Повышенный рост протеолитической анаэробной микрофлоры сопровождается продукцией газов, обладающих потенциальной цитотоксичностью. У детей с выраженными кишечными коликами нередко повышается уровень воспалительного белка — кальпротектина [13].
Функциональные запоры относятся к числу распространенных нарушений функции кишечника и выявляются у 20–35% детей первого года жизни [14, 15].
Под запорами понимают увеличение интервалов между актами дефекации по сравнению с индивидуальной физиологической нормой более 36 часов и/или систематически неполное опорожнение кишечника.
Частота стула у детей считается нормальной, если в возрасте от 0 до 4 месяцев происходит от 7 до 1 акта дефекации в сутки, от 4 месяцев до 2 лет от 3 до 1 опорожнения кишечника. К расстройствам дефекации у младенцев также относятся дисхезия — болезненная дефекация, обусловленная диссинергией мышц дна малого таза, и функциональная задержка стула, для которой характерно увеличение интервалов между актами дефекации, сочетающихся с калом мягкой консистенции, большого диаметра и объема.
В механизме развития запоров у грудных детей велика роль дискинезии толстой кишки. Наиболее частой причиной возникновения запоров у детей первого года жизни являются алиментарные нарушения.
Отсутствие четко очерченной границы между функциональными нарушениями и патологическими состояниями, а также наличие отдаленных последствий (хронические воспалительные гастроэнтерологические заболевания, хронические запоры, аллергические заболевания, расстройства сна, нарушения в психоэмоциональной сфере и др.) диктуют необходимость внимательного подхода к диагностике и терапии данных состояний.
Лечение детей грудного возраста с функциональными нарушениями ЖКТ является комплексным [3, 16] и включает ряд последовательных этапов, которыми являются:
Наличие срыгиваний диктует необходимость использования симптоматической позиционной (постуральной) терапии — изменение положения тела ребенка, направленного на уменьшение степени рефлюкса и способствующего очищению пищевода от желудочного содержимого, тем самым снижается риск возникновения эзофагита и аспирационной пневмонии. Кормить ребенка следует в положении сидя, при положении тела младенца под углом 45–60°. После кормления рекомендуется удерживание ребенка в вертикальном положении, причем достаточно продолжительно, до отхождения воздуха, не менее 20–30 минут. Постуральное лечение необходимо проводить не только на протяжении всего дня, но и ночью, когда нарушается очищение нижнего отдела пищевода от аспирата вследствие отсутствия перистальтических волн (вызванных актом глотания) и нейтрализующего эффекта слюны.
Ведущая роль в лечении функциональных нарушений ЖКТ у детей принадлежит лечебному питанию. Назначение диетотерапии, прежде всего, зависит от вида вскармливания ребенка.
При естественном вскармливании в первую очередь необходимо создать спокойную обстановку для кормящей матери, направленную на сохранение лактации, нормализовать режим кормления ребенка, исключающий перекорм и аэрофагию. Из питания матери исключают продукты, повышающие газообразование в кишечнике (сладкие: кондитерские изделия, чай с молоком, виноград, творожные пасты и сырки, безалкогольные сладкие напитки) и богатые экстрактивными веществами (мясные и рыбные бульоны, лук, чеснок, консервы, маринады, соленья, колбасные изделия).
По мнению ряда авторов, функциональные расстройства ЖКТ могут возникать в результате пищевой непереносимости, чаще всего аллергии к белкам коровьего молока. В таких случаях матери назначается гипоаллергенная диета, из ее рациона исключаются цельное коровье молоко и продукты, обладающие высоким аллергизирующим потенциалом.
В процессе организации диетотерапии необходимо исключить перекорм ребенка, особенно при свободном вскармливании.
При отсутствии эффекта от вышеописанных мероприятий, при упорных срыгиваниях используют «загустители» (например, Био-рисовый отвар), которые разводят грудным молоком и дают с ложечки перед кормлением грудью.
Необходимо помнить, что даже выраженные функциональные расстройства ЖКТ не являются показанием для перевода ребенка на смешанное или искусственное вскармливание. Сохранение симптоматики является показанием к дополнительному углубленному обследованию ребенка.
При искусственном вскармливании необходимо обратить внимание на режим кормления ребенка, на адекватность выбора молочной смеси, соответствующей функциональным особенностям его пищеварительной системы, а также ее объем. Целесообразно введение в рацион адаптированных молочных продуктов, обогащенных пре- и пробиотиками, а также кисломолочных смесей: Агуша кисломолочная 1 и 2, NAN Кисломолочный 1 и 2, Нутрилон кисломолочный, Нутрилак кисломолочный. При отсутствии эффекта используются продукты, специально созданные для детей с функциональными нарушениями ЖКТ: NAN Комфорт, Нутрилон Комфорт 1 и 2, Фрисовом 1 и 2, Хумана АР и др.
Если нарушения обусловлены лактазной недостаточностью, ребенку постепенно вводят безлактозные смеси. При пищевой аллергии могут быть рекомендованы специализированные продукты на основе высокогидролизованного молочного белка. Поскольку одной из причин срыгиваний, колик и нарушений характера стула являются неврологические нарушения вследствие перенесенного перинатального поражения центральной нервной системы, диетологическая коррекция должна сочетаться с медикаментозным лечением, которое назначается детским неврологом.
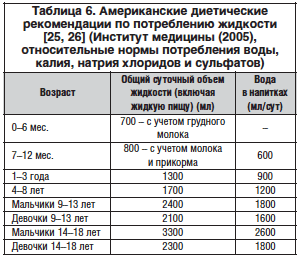
Как при искусственном, так и при естественном вскармливании между кормлениями целесообразно предлагать ребенку детскую питьевую воду, особенно при склонности к запорам.
Особого внимания заслуживают дети с синдромом срыгиваний. При отсутствии эффекта от использования стандартных молочных смесей целесообразно назначать антирефлюксные продукты (АР-смеси), вязкость которых повышается за счет введения в их состав специализированных загустителей [17, 18]. С этой целью используются два вида полисахаридов:
КРД, безусловно, является интересным компонентом в составе продуктов детского питания, и на ее свойствах хотелось бы остановиться подробнее. Основным физиологически активным компонентом КРД является полисахарид — галактоманнан. Он относится к группе пищевых волокон и выполняет две взаимосвязанные функции. В полости желудка КРД обеспечивает более вязкую консистенцию смеси и препятствует возникновению срыгиваний. Вместе с тем КРД относится к нерасщепляемым, но ферментируемым пищевым волокнам, что и придает этому соединению классические пребиотические свойства.
Под термином «нерасщепляемые пищевые волокна» понимается их устойчивость к воздействию панкреатической амилазы и дисахидаз тонкой кишки. Понятие «ферментируемые пищевые волокна» отражает их активную ферментацию полезной микрофлорой толстой кишки, прежде всего — бифидобактериями. В результате такой ферментации происходит ряд важных для организма физиологических эффектов, а именно:
Положительное влияние КРД на состав кишечной микрофлоры у детей первого года жизни описано в ряде исследований [19]. Это является одним из важных аспектов применения современных АР-смесей в педиатрической практике.
Смеси, включающие КРД (камедь), обладают доказанным клиническим эффектом и при функциональных запорах. Увеличение объема кишечного содержимого за счет развития полезной кишечной микрофлоры, изменение рН среды в кислую сторону и увлажнение химуса способствуют усилению перистальтики кишечника. Примером таких смесей являются Фрисовом 1 и Фрисовом 2. Первая предназначена для детей с рождения до 6 месяцев, вторая — с 6 до 12 месяцев [20]. Эти смеси могут быть рекомендованы как в полном объеме, так и частично, в количестве 1/3–1/2 от необходимого объема в каждое кормление, в сочетании с обычной адаптированной молочной смесью, до достижения стойкого терапевтического эффекта.
Другая группа АР-смесей — продукты, включающие в качестве загустителя крахмалы, которые действуют только в верхних отделах ЖКТ, причем положительный эффект наступает при использовании их в полном объеме. Эти смеси показаны детям с менее выраженными срыгиваниями (1–3 балла), как при нормальном стуле, так и при склонности к разжиженному. Среди продуктов этой группы выделяется смесь NAN Антирефлюкс, обладающая двойной защитой против срыгиваний: за счет загустителя (картофельного крахмала), увеличивающего вязкость желудочного содержимого и умеренно гидролизованного белка, повышающего скорость опорожнения желудка и дополнительно профилактирующего запоры.
В настоящее время на Российском потребительском рынке появилась обновленная антирефлюксная смесь Хумана АР, в состав которой одновременно введены камедь рожкового дерева (0,5 г) и крахмал (0,3 г), что позволяет усилить функциональное действие продукта.
Несмотря на то, что АР-смеси являются полноценными по составу и призваны обеспечить физиологические потребности ребенка в пищевых веществах и энергии, согласно международным рекомендациям они относятся к группе продуктов детского питания «для специального медицинского назначения» (Food for special medical purpose). Поэтому продукты данной группы следует использовать строго при наличии клинических показаний, по рекомендации врача и под медицинским контролем. Продолжительность применения АР-смесей должна определяться индивидуально и может быть достаточно длительной, около 2–3 месяцев. Перевод на адаптированную молочную смесь осуществляется после достижения стойкого терапевтического эффекта.
Литература
*НЦЗД РАМН, **РМАПО, Москва
Функциональные расстройства желудочно-кишечного тракта у детей: диагностика и возможности спазмолитической терапии
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
Статья посвящена проблеме функциональных расстройств желудочно-кишечного тракта у детей и вопросам их диагностики и лечения
Введение
Функциональные нарушения (ФН) желудочно-кишечного тракта (ЖКТ) – одна из самых распространенных проблем в детской гастроэнтерологии. По данным различных авторов, ФН ЖКТ встречаются у 55–75% детей первых месяцев жизни [1]. По мере взросления ребенка частота функциональных расстройств нарастает, формы их становятся более разнообразными. У многих детей c возрастом наблюдается эволюция симптомов ФН, к примеру: срыгивания у детей до 1 года, циклическая рвота у детей 3–8 лет и абдоминальные боли, диспепсия у детей старше 8 лет [2]. Этому способствуют анатомо-физиологические возрастные особенности развития ЖКТ у детей, нарушения режима и техники вскармливания у младенцев, режима и характера питания – у старших детей, а также нарастающие физические и психоэмоциональные нагрузки, частая сочетанная патология ЦНС. Особенностями детского возраста являются неспецифичность жалоб, которые может предъявить маленький пациент, невозможность локализации боли у детей младшего возраста. Многочисленные жалобы ребенка вызывают значительную тревогу у родителей. На их простые вопросы «Что не так с моим ребенком? Почему такое происходит? Как долго это будет продолжаться? Можно ли это вылечить?» должен ответить педиатр.
Терминология и классификация
Согласно Римским критериям III пересмотра (РК III, 2006) [3] (табл. 1), гастроинтестинальные ФН у детей и подростков включают разнообразную комбинацию хронических или рецидивирующих симптомов без структурных или биохимических нарушений.
Задача педиатра на первичном приеме при сборе анамнеза болезни и осмотре ребенка обратить внимание на возможные «симптомы тревоги» («красные флаги») (табл. 2) для исключения органической патологии ЖКТ [4–5]. Такие изменения требуют углубленного, нередко инвазивного обследования.
Преимущественный симптом ФН позволяет установить диагноз и определить подходы к терапии. РК III являются важным диагностическим инструментом в ежедневной работе педиатра.
Наиболее часто среди детей и подростков выявляются следующие ФН ЖКТ: абдоминальная боль (25–40% случаев), функциональная диспепсия (ФД) (до 27% случаев), синдром раздраженного кишечника (СРК) (до 45% детей) и функциональный запор (ФЗ) (до 25% случаев). Остальные расстройства (рвота и аэрофагия, абдоминальная мигрень, детская функциональная абдоминальная боль, недержание стула) наблюдаются значительно реже [2, 3, 5, 14, 21].
H2. Функциональные расстройства ЖКТ, связанные с абдоминальной болью
Абдоминальная боль – самая частая, пугающая, но неспецифичная из жалоб у детей при ФН ЖКТ. Она заставляет пациентов и их родителей обращаться за врачебной помощью. 10–15% детей и подростков, не имеющих каких-либо органических заболеваний, предъявляют жалобы на боли в животе [6], т. е. имеют ФН. С другой стороны, боли в животе у ребенка в 90% случаев являются функциональными.
Диагностические РК III [3] позволяют установить преимущественную форму ФН.
H2a. Функциональная диспепсия (табл. 3)
Диспепсия беспокоит от 3,5 до 27% детей и подростков в различных странах [2, 5]. Разграничение диспепсии на варианты – язвенноподобный и дискинетический – у младших детей не оправданно вследствие неспецифичности жалоб, невозможности разграничить чувства боли и дискомфорта в животе [3].
Обязательная необходимость эндоскопического обследования при постановке такого диагноза ставится под сомнение. Частота изменений слизистой оболочки верхних отделов ЖКТ, объясняющих диспепсические жалобы, у детей значительно меньше, чем у взрослых [7]. При «симптомах тревоги» (табл. 2) проведение эзофагогастродуоденоскопии, подтверждение ассоциации с Helicobacter pylori (H. pylori) обязательно, особенно при наличии дисфагии и сохранении или рецидиве упорной симптоматики на фоне антисекреторной терапии [8]. Диспепсия может длительно сохраняться после перенесенных кишечных и респираторных вирусных инфекций [9]. Поэтому наличие умеренных воспалительных изменений в биоптатах слизистой оболочки пищевода, желудка, двенадцатиперстной кишки при морфологическом исследовании не противоречит диагнозу ФН [9]. У детей с ФД наблюдаются: расстройства миоэлектрической активности желудка, замедленная эвакуация пищи из желудка, изменение антродуоденальной моторики, снижение ответа стенки желудка на нагрузку объемом пищи [10–12].
Принципы и подходы к терапии ФД у детей: отказ от применения нестероидных противовоспалительных препаратов, диета с исключением/ограничением провоцирующих продуктов (таких как кофеин, специи, жирная пища). При преимущественно болевом синдроме применяются антисекреторные препараты (ингибиторы протонной помпы), прокинетики – при дискомфорте в верхней половине живота [3]. При подтверждении H. pylori-этиологии функциональных расстройств показана эрадикационная терапия [13].
H2b. Синдром раздраженного кишечника (табл. 4)
Согласно данным западных исследователей, СРК встречается у 22–45% детей 4–18 лет [14].
Подтверждают диагноз СРК сочетание дискомфорта или боли в животе с изменениями стула: частоты (4 и более раз в день или 2 и менее раз в неделю), формы (от «овечьего»/твердого стула до неоформленного/водянистого), нарушение пассажа стула (натуживание, внезапные позывы к дефекации или ощущение неполного опорожнения прямой кишки), пассаж слизи, метеоризм [3].
Основным патогенетическим компонентом СРК является висцеральная гиперчувствительность [15], возникающая из-за ряда патологических процессов: инфекций, воспаления, травмы кишечника, аллергии, нарушающих моторику кишечника [16]. Также имеют значение генетическая предрасположенность, стрессовые ситуации, наличие схожих нарушений у родителей. Часто симптомам СРК сопутствуют тревожность, депрессия и спектр различных соматических жалоб.
В зависимости от ведущего клинического синдрома выделяют 3 варианта течения СРК: с преобладанием болей и метеоризма, с запорами, с диареей. Хотя нередки комбинации и чередование основных симптомов СРК.
Внимательное изучение анамнеза заболевания, возможных триггерных факторов возникновения СРК у пациента, отсутствие «симптомов тревоги», нормальные данные физикального обследования, неизмененные ростовые кривые ребенка позволяют избежать инвазивных процедур в большинстве случаев [17].
Принципы и подходы к терапии разнообразны: беседа с родителями и самим пациентом (снижение тревожности, объяснение причин и механизмов развития данных нарушений), психологическая коррекция, диетотерапия, фармакотерапия (в зависимости от варианта течения СРК – спазмолитики, слабительные или антидиарейные, седативные препараты, пре- и пробиотики), лечебная физкультура и физиотерапия, в т. ч. иглорефлексотерапия.
Лечение
Лечение СРК начинается с изменения стиля жизни, выработки определенного стереотипного поведения в отношении туалета: регулярное посещение туалета и ведение дневника стула, поощрение продуктивного посещения туалета.
Диетотерапия при преобладающих запорах обогащена пищевыми волокнами, включает достаточный объем жидкости, продукты, стимулирующие моторику толстой кишки (фрукты и овощи, молочнокислые продукты). При преобладании диареи включаются продукты с закрепляющим действием. При преобладании метеоризма исключают газообразующие продукты.
Фармакотерапия СРК зависит от варианта его течения [18–20, 30], общим является обязательное подключение седативных средств, адаптогенов, которые может назначить педиатр или невролог. Предпочтительны в педиатрии растительные седативные средства с доказанной эффективностью на основе мяты перечной, мяты лимонной, валерианы. Полезен их дополнительный спазмолитический эффект. Также дополнительный терапевтический эффект при любом варианте СРК дает присоединение к терапии ферментов (при запорах – желчесодержащих), пре- и пробиотиков.

При преимущественно болевом синдроме применяются спазмолитики различных групп и средства, уменьшающие метеоризм (симетикон).
При запорах показаны слабительные, увеличивающие объем каловых масс (лактулоза, макрогол и др.), короткие курсы стимулирующих слабительных, спазмолитики. При диарее применяются антидиарейные средства (лоперамид), сорбенты, спазмолитики. Интересно применение комплексного препарата, содержащего релиз-активные антитела к гистамину, фактору некроза опухоли-a, белку S-100, применяемого при различных вариантах СРК [20]. Терапия направлена не только на купирование основных симптомов СРК, но и на нормализацию моторных нарушений кишки, снижение висцеральной гиперчувствительности, коррекцию механизмов восприятия болей.
H3. Функциональный запор (табл. 5)
Каждый четвертый ребенок страдает запорами [21], более чем у 1/3 детей с этой проблемой заболевание принимает хроническое течение. Истинная частота запоров неизвестна, т. к. не все родители понимают серьезность проблемы и не обращаются за медицинской помощью, занимаясь самолечением. Кроме того, имеется множество возрастных и индивидуальных детских особенностей строения и развития толстой кишки, что обусловливает значительную вариабельность частоты стула у ребенка.
Запор (от лат. constipatio) (по W.G. Thommpson, 1999 [22]) – нарушение функции кишечника, выражающееся увеличением интервалов между актами дефекации по сравнению с индивидуальной физиологической нормой, затруднением акта дефекации, чувством неполного опорожнения кишечника, отхождением малого количества кала повышенной плотности (табл. 6).
Запоры принято подразделять на первичные (функциональные, идиопатические) либо вторичные, связанные с множеством патогенетических механизмов. Вторичные запоры чаще связаны с органическими и неврологическими причинами и очень редко – с эндокринными [23]. Хронические запоры вследствие органических причин, как правило, развиваются постепенно, утяжеляются с ростом ребенка и отражают декомпенсацию функции кишки. Большая часть детей (до 95%) страдают ФЗ [24].
При сборе анамнеза болезни и осмотре следует обратить внимание на возможные «симптомы тревоги» [25, 26], подозрительные в отношении врожденной органической патологии толстой кишки, аномалии развития спинного мозга и метаболических расстройств: возникновение запора с рождения, позднее (более 48 ч) отхождение мекония; отставание в развитии ребенка; выраженный метеоризм и рвота; нарушения раннего моторного развития.
Оценка комплекса данных анамнеза и специализированного физикального обследования ребенка с запором, включающего осмотр перианальной области, ягодиц, спины, оценку мышечного тонуса, силы и рефлексов в нижних конечностях, в некоторых случаях – пальцевое ректальное исследование, позволяет решить вопрос о необходимости дальнейших диагностических мероприятий. Если запор носит функциональный характер, назначается стартовая терапия. В большинстве случаев не требуется дальнейших инструментальных исследований. Обнаружение «симптомов тревоги» является показанием к дообследованию ребенка [26].
Для успешного лечения запора необходим индивидуальный подход к каждому ребенку. Нужно учитывать все возможные факторы: возраст ребенка, этиологию и длительность запора, наличие сочетанной патологии, эффективность ранее проведенного лечения. Комплексное лечение запоров включает изменение образа жизни, коррекцию питания, медикаментозные и немедикаментозные методы лечения (лечебная физкультура, физиотерапевтические процедуры, санаторно-курортное лечение, методика биологической обратной связи).
Для ребенка старшего возраста крайне важна «информационная поддержка»: в беседе с ребенком и родителями обсуждаются вопросы о частоте и качестве стула, запорах, на руки даются материал о содержании диеты, лечебной физкультуре, памятка о приеме лекарств, информация о наблюдении для участкового педиатра. В рационе ребенка старше 1 года, страдающего запором, должна быть пища с высоким содержанием пищевых волокон (отруби, овощи, фрукты), лакто- и ацидофильными бактериями.
Для профилактики запоров у детей старшего возраста необходимым условием является постоянная физическая нагрузка. Лечебная физкультура должна быть направлена на повышение давления в брюшной полости, стимуляцию кишечной моторики, укрепление мышц тазового дна. Необходимы соблюдение режима дня, профилактика острых инфекционных заболеваний.
Согласно данным большинства исследователей, даже стартовая терапия запоров не должна ограничиваться рекомендациями относительно режима и диеты (достаточный прием жидкости и пищевых волокон) [26]. Имеющиеся в арсенале педиатра слабительные средства разделяются на группы по механизму действия (табл. 7) [23].
Лекарственная терапия запоров для детей до 1 года: в качестве смягчителей показаны лактулоза, сорбит, кукурузный сироп, изредка стимулирующие слабительные, не показаны минеральные масла. Дети старше 1 года: возможна диетическая коррекция (фрукты, овощи, зерна), из лекарственных средств применяются минеральные масла, магния сульфат, лактулоза, сорбитол, короткие курсы стимулирующих слабительных(возможно использование пикосульфата натрия (Гуттулакс®) у детей младше 4-х лет в дозировке 1 капля на 2 кг массы тела), длительный прием полиэтиленгликоля (макрогол) в низких дозах у детей с упорным запором [3, 23–28].
Дополнительное назначение препаратов определяется преимущественным механизмом развития запора и спектром сочетанной патологии, применяются спазмолитики, прокинетики, желчегонные препараты, ферменты с желчными кислотами, пре- и пробиотики.
Правильное формирование туалетных навыков, метод биологической обратной связи высокоэффективны при аноректальной дисфункции [27, 28].
Гладкомышечный спазм часто является патогенетически последним звеном и основной причиной многих ФН ЖКТ у детей, прежде всего синдрома абдоминальной боли, СРК, большинства случаев ФЗ.
В арсенале педиатра имеется большой спектр спазмолитических препаратов, список их постоянно пополняется [29].
Регуляция активности гладкомышечных клеток осуществляется центральной и вегетативной нервными системами, а также воздействием на опиоидные и серотониновые рецепторы с помощью нейропептидов. Спазмолитические препараты можно разделить на 2 группы: нейротропные и миотропные.
Нейротропные препараты влияют на проведение импульса в вегетативной нервной системе путем действия на холино- и адренорецепторы. Наиболее известен и активно применяется в педиатрии препарат тримебутин, действующий на энкефалиновые рецепторы нервных сплетений Мейсснера и Ауэрбаха, обладающий прокинетическим и спазмолитическим действием. Показания к применению анксиолитиков и антидепрессантов, также обладающих нейротропным спазмолитическим действием, в педиатрии ограничены.
В практической педиатрии наиболее широко применяются миоспазмолитики. Возбуждение М-холинорецепторов вызывает открытие натриевых каналов, поступление ионов натрия в клетку приводит к деполяризации мембраны, открытию потенциал-зависимых кальциевых каналов и поступлению ионов кальция в клетку. Далее следует каскад биохимических реакций, приводящий к образованию актин-миозинового комплекса, сокращению миоцита. Расслабление миоцита происходит за счет накопления в клетке циклического аденозинмонофосфата (цАМФ) и циклического гуанозинмонофосфата.
В настоящее время известно несколько групп миотропных спазмолитиков, отличающихся по механизму действия.
Дротаверин и папаверин давно используются в педиатрии и доказали свою эффективность. Препараты ингибируют фосфодиэстеразу 4-го типа, что ведет к накоплению цАМФ и расслаблению миоцита. Однако системность их действия на гладкомышечные органы, наличие постспазмовой гипотонии ограничивают курсовое применение, препараты чаще применяются по требованию.
Необходимость селективного действия спазмолитиков привела к созданию новых препаратов.
Мебеверин – миотропный спазмолитик, блокирующий натриевые каналы. Эффективность препарата выше, чем у традиционных спазмолитиков, он хорошо переносится, действует длительно (до 12 ч), включен в схемы лечения заболеваний кишечника, билиарных путей, поджелудочной железы, но имеет возрастные ограничения – применяется только с 18 лет.
Сочетанное действие пинаверия бромида связано с блокадой кальциевых каналов, подавлением спазма, вызванного холецистокинином и субстанцией Р, умеренным М-холиноблокирующим эффектом. Препарат широко используется в гастроэнтерологии при многих ФН ЖКТ у взрослых больных. Опыт применения его в педиатрии ограничен, препарат не рекомендован до 18 лет.
К спазмолитикам первой ступени применяется ряд требований: высокий уровень безопасности, высокая спазмолитическая активность, длительный спазмолитический эффект, большой международный опыт применения, доступность (невысокая стоимость), возможность самолечения (безрецептурный отпуск), наличие пероральных форм.
Гиосцина бутилбромид (Бускопан®, «Берингер Ингельхайм Фарма», Германия) как медицинский препарат известен с 1950-х гг., впервые получен и применен в Германии и неоднократно доказал свою эффективность и безопасность во многих странах при различных заболеваниях, сопровождающихся болевым синдромом [30]. Гиосцина бутибромид – М-холиноблокатор на натуральной основе (получен из листа растения Datura stramonium) и является уникальным спазмолитиком направленного действия, тропным к гладкомышечным клеткам стенок внутренних органов: ЖКТ, желчевыводящих и мочевыводящих путей [31]. Бускопан® обладает также антисекреторным эффектом, снижая секрецию пищеварительных желез. Быстрый клинический эффект (через 15 мин) объясняется прямым М-холиноблокирующим действием. Действие холинолитических препаратов тем сильнее, чем выше начальный тонус блуждающего нерва, что важно при вегетативной дисфункции, являющейся фоном ФН ЖКТ.
Гиосцина бутилбромид является четвертичным аммониевым производным и не проникает через гематоэнцефалический барьер [31], поэтому не оказывает антихолинэргического влияния на ЦНС, что важно для более свободного и безопасного применения препарата Бускопан® в педиатрии. Большим преимуществом данного лекарственного средства является избирательность его спазмолитического действия – только в месте возникновения спазмов. Сохранение перистальтической активности ЖКТ при ФН способствует нормализации моторной функции толстой кишки.
Бускопан® имеет широкий спектр показаний к применению: различные спастические состояния – желчные, кишечные и почечные колики, спастическая дискинезия желчевыводящих путей, пилороспазм, комплексная терапия обострений язвенной болезни желудка и двенадцатиперстной кишки, холецистита. Однозначным преимуществом для применения в педиатрии является наличие различных форм препарата: Бускопан® выпускается в виде таблеток, покрытых сахарной оболочкой, и ректальных суппозиториев по 10 мг; назначается детям старше 6 лет по 1–2 таблетке (10 мг) 3 р./сут или по 1 суппозиторию (10 мг) 3 р./сут per rectum [31].
Множество исследований [33–36] показало безопасность и эффективность применения препарата Бускопан® в педиатрии для купирования абдоминального болевого сидрома, различных диспепсических расстройств, симптомов СРК, улучшения качества жизни таких пациентов. Интересно применение различных форм препарата в комплексной терапии хронических ФЗ у детей в зависимости от преимущественного механизма их возникновения [36]. Подчеркивается дополнительное преимущество ректальной формы препарата (прямое спазмолитическое на сфинктеры прямой кишки и местнораздражающее действие) при дисфункции анального сфинктера.
Таким образом, ФН ЖКТ – распространенная проблема среди детей различного возраста. Проявления ФН ЖКТ разнообразны, имеются определенная динамика и эволюция симптомов с возрастом. ФН любой локализации свойственны рецидивирующее течение, повышенная тревожность пациента, сочетанные нарушения со стороны других систем органов, что значительно снижает качество жизни ребенка.
Учитывая необходимость уменьшения инвазивности процедур в детском возрасте диагностика функциональных состояний ЖКТ педиатром возможна на основе РК III, но следует осуществлять обязательный динамический контроль «симптомов тревоги».
Патогенетическая терапия ФН ЖКТ может быть только комплексной с обязательной коррекцией сопутствующих нейрогенных расстройств, сочетанным применением медикаментозной и различных методов немедикаментозной терапии.
Гиосцина бутилбромид (Бускопан®) является высокоэффективным безопасным спазмолитиком для купирования спастических состояний при различных ФН ЖКТ у детей, особенно при ФН с диспепсией, абдоминальной болью, СРК, ФЗ. Наличие оральных и ректальных форм препарата удобно в педиатрии, в т. ч. при запорах с аноректальной дисфункцией.
.gif)
.gif)