Диагноз мдс что это такое
Миелодиспластические синдромы
Миелодиспластические синдромы (МДС) объединяют группу злокачественных опухолевых заболеваний системы кроветворения.
При этих заболеваниях происходит нарушение созревания клеток костного мозга с изменением их строения и функциональных свойств.
Характерной, но не обязательной чертой заболевания является исход в острый лейкоз.
Эпидемиология
Заболеваемость МДС в среднем составляет 3-4 случая на 100 000 населения в год и увеличивается с возрастом.
Заболеваемость мужчин незначительно преобладает над заболеваемостью женщин. МДС в детском возрасте встречается крайне редко.
В 10-15% случаев МДС является осложнением проведенной химиотерапии и облучения по поводу другого онкологического заболевания.
Истинная заболеваемость МДС остается неизвестной. Связано это с бессимптомным течением заболевания у многих больных, трудностями диагностики и др. причинами.
Факторы риска
Известно, что факторы риска развития МДС и острых миелоидных лейкозов схожи.
В детском возрасте основными предрасполагающими факторами развития МДС являются генетические заболевания (синдромы Дауна, Фанкони, нейрофиброматоз, врожденный дискератоз и др.).
Генетическая предрасположенность отмечена и у лиц зрелого возраста, родители которых страдали МДС.
К химическим факторам риска относятся органические соединения (бензин и его производные, пестициды, растворители), а также неорганические (асбест, кварц, мышьяк) вещества.
МДС развивается чаще у курящих по сравнению с некурящими.
Более высокий риск возникновения МДС отмечен у работников сельского хозяйства, текстильной промышленности, лечебных учреждений, операторов машин, у лиц, проживающих вблизи заводов.
Наиболее изученным фактором риска является влияние химиопрепаратов и лучевого лечения. Чаще всего МДС диагностируется у больных, лечившихся по поводу рака молочной железы, множественной миеломы, лимфомы Ходжкина (лимфогранулематоза), неходжкинской лимфомы (лимфосаркомы), мелкоклеточного рака легкого.
Лучше всего МДС изучены у больных лимфомой Ходжкина. Частота развития МДС у этой категории больных колеблется от 1,5 до 10% и зависит от возраста, предшествующего лечения и длительности наблюдения.
Средний период от начала лечения болезни Ходжкина до установления диагноза МДС составляет около 4-6 лет. Убедительных данных об увеличении риска МДС при комбинации химиотерапии и облучения по сравнению с использованием только химиотерапии нет.
Клинические проявления
Признаки и симптомы у больных с МДС неспецифичны. У многих больных на протяжении ряда лет МДС протекает бессимптомно и выявляется лишь при обследовании по поводу других заболеваний.
Анемия (малокровие) является самым частым симптомом МДС и обнаруживается в 85-90% случаев. Большинство жалоб обусловлено выраженностью малокровия. Лейкопения (снижение числа лейкоцитов), отмечаемая у 50% больных, может быть причиной склонности к инфекционным осложнениям. В отдельных случаях повышение температуры может быть симптомом МДС. Иногда больные обращаются к врачу в связи со склонностью к кровотечениям из-за снижения числа тромбоцитов.
Несколько реже имеется увеличение лимфатических узлов. Увеличение, печени и лимфатических узлов при других вариантах МДС встречается редко.
Диагностика
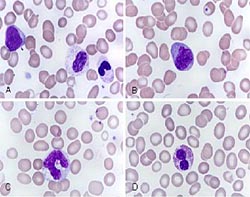
Выявление МДС основывается на обнаружении признаков дисплазии (нарушений формирования ткани) в одном или нескольких ростках кроветворения.
При этом выявленные изменения могут быть чрезвычайно разнообразными. Соотношение нормальных и измененных клеток у разных больных существенно варьируют.
Принято считать клеточные линии (ростки кроветворения) измененными, если число клеток с признаками дисплазии составляет более 10%.
В том случае, если число измененных клеток в костном мозге невелико (менее 10%), для достоверной диагностики МДС необходимо проводить цитогенетическое исследование.
Прогностические факторы
Прогноз (исход) МДС зависит от многих факторов.
Продолжительность жизни и вероятность трансформации (перехода) в острый лейкоз при МДС существенно варьируются.
Самая короткая продолжительность жизни (5-7 месяцев) отмечается у больных МДС, вызванным химиотерапией и облучением. Кроме того, прогноз менее благоприятный у пациентов старше 60 лет, мужского пола и при наличии симптомов интоксикации.
Среди показателей крови к неблагоприятным прогностическим признакам относятся:
Наибольшее прогностическое значение имеет степень опухолевой инфильтрации (поражения) костного мозга. Прогноз менее благоприятный, если число опухолевых клеток в костном мозге превышает 10%. Некоторые выявленные хромосомные изменения также отрицательно сказываются на исходе заболевания.
Лечение
Существует два подхода к лечению МДС:
— радикальный, направленный на достижение и сохранение полной ремиссии,
— нерадикальный, направленный на улучшение качества жизни больных.
При нерадикальном подходе допускается существование (персистирирование) болезни, что принципиально отличает лечение МДС от терапии острых лейкозов.
Методы лечения МДС:
Выбор различных направлений терапии определяется: возрастом больного, наличием донора стволовых клеток, возможностью проведения адекватной сопроводительной терапии, а также эффективностью отдельных препаратов, подобранных с учетом исходных клинико-лабораторных показателей.
Практически с помощью каждого из перечисленных методов терапии возможно достижение полной ремиссии. Препараты, улучшающие качество жизни, успешно используются у больных с благоприятным прогнозом (с длительным сроком жизни и низкой вероятностью развития острого лейкоза).
При благоприятном прогнозе с минимальными проявлениями заболевания можно ограничиться наблюдением за больным, пока показатели крови и костного мозга остаются стабильными.
При выраженном малокровии показано переливание эритроцитарной массы. В ряде случаев необходимо применение ростовых факторов, антитимоцитарного глобулина, индукторов дифференцировки клеток и пр.
При прогрессировании МДС проводится химиотерапия.
У больных с неблагоприятным прогнозом проводится химиотерапия по программам лечения острого миелоидного лейкоза. При невозможности химиотерапии или высоком риске осложнений допустимо использование противоопухолевых препаратов в малых дозах.
Такой подход может позволить улучшить качество жизни больных и провести адекватное лечение в более поздние сроки.
После достижения полной ремиссии и при невозможности проведения аллогенной трансплантации костного мозга может осуществляться аутологичная трансплантация костного мозга или периферических стволовых клеток.
Необходимо подчеркнуть, что единственным методом лечения, позволяющим существенно увеличить продолжительность жизни больных МДС, является аллогенная трансплантация костного мозга или периферических стволовых клеток.
Однако применение аллогенной трансплантации не всегда возможно в связи с пожилым возрастом большинства больных и отсутствием идентичного родственного донора.
До настоящего времени результаты лечения больных МДС остаются неудовлетворительными.
В связи с этим практически не существует общепринятых стандартов лечения, а определены лишь общие подходы к терапии для разных групп больных при разных вариантах заболевания.
Миелодиспластический синдром: причины, симптомы, лечение
Термин « миелодиспластический синдром » (сокращённо МДС) объединяет различные патологии, при которых обнаруживаются цитопения (понижение концентрации форменных элементов крови), дисплазия (неправильное развитие) гемоцитобластов (предшественников кровяных клеток), гипоклеточность или гиперклеточность костного мозга.
МДС встречается достаточно редко – 3-5 случаев на 100 тысяч населения. Но после 60 лет частота болезни повышается до 20-40 случаев ( https://www.eduherald.ru/pdf/2021/2/20538.pdf ).
Причины болезни
Точные причины МДС пока не удалось установить. Известно, что в 10-20% случаев патология развивается у людей, проходивших лучевую или химиотерапевтическую терапию ( https://cyberleninka.ru/article/n/mielodisplasticheskiy-sindrom/viewer ).
Ученые предполагают, что спровоцировать миелоидный синдром способен также парвовирус В19.
Повышают риск возникновения патологии постоянная работа с некоторыми химическими веществами (пестицидами, бензином, органическими растворителями), неблагоприятная экологическая ситуация, курение, некоторые врожденные и наследственные болезни.
Под влиянием повреждающих факторов в стволовых клетках возникают мутации, которые способствуют развитию МДС. Постепенно они накапливаются, способствуя переходу болезни в лейкоз.
Симптомы патологии
Признаки МДС зависят от того, дефицит каких кровяных клеток испытывает организм.
Выделяют 3 группы клинических проявлений:
У некоторых пациентов в число симптомов миелодиспластического синдрома входят увеличение размеров селезенки (спленомегалия) и печени (гепатомегалия).
Диагностика МДС
Основной метод диагностики миелодиспластического синдрома – исследование крови. При МДС возможно понижение как одного показателя, так и их комбинация. Диагноз ставят только при устойчивой (не менее полугода) цитопении, если не найдены другие причины.
Если возникает подозрение на миелодиспластический синдром, делают трепанобиопсию и пункцию костного мозга. Полученный биоматериал подвергают гистологическому и цитологическому исследованию.
Чтобы исключить другие причины цитопении, пациента направляют на дополнительные лабораторные и инструментальные исследования, которые могут включать:
Цитопения сопровождает различные заболевания. Поэтому важно исключить другие причины: рак, аутоиммунные заболевания, хронические инфекции, нарушение гемопоэза, отравление бензином или тяжелыми металлами, нехватку меди, избыток цинка, побочное действие лекарств.
Чтобы дифференцировать миелодиспластический синдром от миелоидного лейкоза, определяют число бластных клеток. Согласно ВОЗ, если показатель превышает 20%, то диагностируют острый лейкоз ( https://cyberleninka.ru/article/n/mielodisplasticheskiy-sindrom/viewer ).
Лечение МДС
Выбор способа лечения зависит от степени и прогрессирования цитопении, группы риска, имеющихся сопутствующих заболеваний.
Единственный действенный метод лечения, обеспечивающий лечение , – пересадка костного мозга.
Выделяют 3 основные способа лечения:
o Чтобы купировать либо предотвратить кровоточивость, прибегают к трансфузии тромбоцитов.
o При гипопластическом типе кроветворения эффективное действие оказывают иммунодепрессанты, которые защищают костный мозг от иммунной атаки.
В клинике Спиженко лечение подбирают индивидуально для каждого пациента в соответствии с международными рекомендациями и утвержденными протоколами.
Миелодиспластические синдромы (МДС)
Миелодиспластические синдромы (МДС) – разнородная группа хронических заболеваний крови, при которых происходит нарушение созревания клеток крови, с возможным переходом в лейкоз.
Ранее МДС имел различные названия (малопроцентный острый лейкоз, предлейкоз, тлеющая лейкемия и др.).
Заболеваемость МДС составляет 3-5 случаев на 100 тысяч населения в год. Более 85% пациентов старше 60 лет, причем риск развития заболевания с возрастом увеличивается. В 2/3 случаев МДС носит вторичный характер и развивается на фоне других заболеваний крови (множественная миелома, лимфогранулематоз, неходжкинские лимфомы, хронический лимфолейкоз) и после цитостатической терапии при ревматоидном артрите, системной красной волчанке, хроническом гломерулонефрите.
Причина заболевания окончательно не выяснена, определенную роль играют ионизирующее излучение, прием цитостатические препараты, производные бензола.
ДИАГНОСТИКА
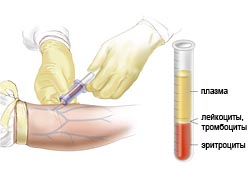
Клинический анализ крови позволяет выявить анемию (малокровие), которая является самым частым симптомом МДС и обнаруживается в 85-90% случаев, лейкопению (снижение числа лейкоцитов), выявляемую у 50% больных и тромбоцитопению (снижение количества тромбоцитов), проводящую к кровотечениям.
Цитогенетический анализ позволяет определить изменения в хромосомном аппарате клеток крови и является ключевым методом диагностики и определения прогноза заболевания.
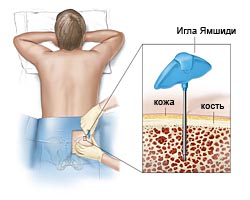
Аспирация (пункция костного мозга) и биопсия (трепанобиопсия) костного мозга – получение небольшого количества (0,2-0,5 мл) аспирата костного мозга и небольшого фрагмент кости. Процедура абсолютно безопасна и выполняется под местной анестезии в течение 2-5 мин. Может также проводиться амбулаторно. Исследования материала биопсий позволяют выявить изменения в костном мозге характерные для МДС.
У 20% пациентов можно выявить увеличение размеров селезенки, печени.
Выбор лечения определяется вариантом заболевания, прогнозом а также наличием сопутствующих заболеваний, которые могут существенно повлиять на терапию.
При благоприятном прогнозе и минимальных проявлениях заболевания можно ограничиться наблюдением за больным, пока показатели крови и костного мозга остаются стабильными.
При выраженном малокровии (анемии) показано переливание эритроцитарной массы, а при повышенной кровоточивости переливание тромбомассы. В ряде случаев возможно применение ростовых факторов (колониестимулирующие факторы).
Единственным методом лечения, позволяющим существенно увеличить продолжительность жизни больных МДС, является аллогенная трансплантация костного мозга/периферических стволовых клеток, Однако применение аллогенной трансплантации не всегда возможно в связи с пожилым возрастом большинства больных и отсутствием идентичного родственного донора.
До настоящего времени результаты лечения больных МДС остаются неудовлетворительными, в связи с этим не существует общепринятых стандартов лечения, а определены лишь общие подходы к терапии для разных групп больных при разных вариантах заболевания. Поэтому сохранение качества жизни пациентов с МДС в большинстве случаев, выходит на первый план при проведении лечения.
Миелодиспластический синдром у взрослых
Общая информация
Краткое описание
Приложение 5
к приказу
Министерства здравоохранения
Республики Беларусь
КЛИНИЧЕСКИМ ПРОТОКОЛ
диагностики и лечения пациентов в возрасте старше 18 лет
с миелодиспластическим синдромом
1. Клинический протокол диагностики и лечения пациентов с заболеванием «миелодиспластический синдром» (далее-МДС) предназначен для оказания медицинской помощи в амбулаторных и стационарных условиях районных, областных и республиканских организаций здравоохранения, имеющих в своем составе гематологические отделения.
2. Возрастная категория: взрослое население.
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
Классификация
КЛАССИФИКАЦИЯ ЗАБОЛЕВАНИЯ
5. Классификация МДС, принятая Всемирной организацией здравоохранения (далее-ВОЗ) в 2008 году базируется на цитоморфологических, кариотипических и клинических признаках заболевания.
Классификация миелодиспластических синдромов
сбалансированные аномалии: t(l 1; 16)(q23;p 13.3); t(3;21) (q26.2;q22.1); t(l;3) (рЗб.З; q21.1); t(2;l 1) (p21;q23); inv(3) (q21q26.2); t(6;9)(p23;q34);
сложный кариотип (3 или более хрмосомных аномалий) с вовлечением вышеупомянутых нарушений.
Диагностика
КРИТЕРИИ ДИАГНОЗА МДС
8. Вспомогательные критерии (С) (для пациентов, имеющих критерии А, но не имеющих критерии В).
8.1. Аномальный иммунный фенотип эритроидных или миелоидных клеток костного мозга, указывающий на их клональное происхождение (по результатам проточной цитометрии).
8.2. Молекулярно-генетические признаки наличия клональной клеточной популяции в костном мозге (по результатам HUMARA исследования или биологического микрочипирования).
8.3. Значительное и стабильное снижение колониеобразующей активности костного мозга и/или периферической крови.
Диагноз устанавливается при наличии 2 предварительных критериев (А) и не менее чем одного МДС-ассоциированных критериев (В). Вспомогательные
критерии (С) используются при отсутствии критериев В и наличии у пациента признаков клональной миелоидной пролиферации. Критерии группы С не входят в обязательный стандарт диагностики МДС.
Диагноз «идиопатическая цитопения неопределенного значения» применяется для обозначения случаев цитопении по одной и более клеточным линиям в течение > 6 месяцев при отсутствии критериев МДС и других причин цитопении. Такие пациенты должны наблюдаться и обследоваться гематологом с интервалом 1-6 месяцев.
Диагностические критерии разработаны ICWG (International Consensus Working Group), 2007 г.
Алгоритм диагностики МДС включает в себя клинические и лабораторные исследования, мультидисциплинарный подход с привлечением смежных специалистов и последовательно проводится на базе учреждений здравоохранения различного уровня с соблюдением преемственности на всех этапах. Это обусловлено полиэтиологичностью и гетерогенностью проявлений при данной патологии, стремлением к рационализации использования специального диагностического оборудования, минимизации диагностических ошибок.
Этапы диагностики МДС:
Лечение
КЛИНИЧЕСКИЕ ВАРИАНТЫ МДС
10. Определение клинического варианта МДС имеет значение для выбора тактики лечения.
10.1. 5ц-синдром: болеют преимущественно женщины, характерны вялотекущий характер заболевания, низкая вероятность трансформации в ОМЛ (10%), тяжелая макроцитарная анемия, нормальный или умерено сниженный уровень лейкоцитов и тромбоцитов, дисплазия мегакариоци- тарного ростка, отсутствие значительно повышения уровня бластных клеток в костном мозге; хороший ответ на леналидомид*.
10.2. Вторичный МДС: частота вторичного МДС нарастает в связи с успехами химиотерапии опухолей и воздействием загрязнения окружающей среды; для большинства пациентов характерны множественные хромосомные аберрации; прогноз хуже, чем при первичном МДС.
10.3. Гипопластический МДС:
до 15% случаев МДС характеризуются низкой клеточностью костного мозга при гистологическом исследовании (доля кроветворной ткани в препарате менее 30% у пациентов моложе 60 лет или менее 20% у пациентов 60 лет и старше);
дисплазия мегакариоцитов и клеток миелоидного ряда может отсутствовать;
возможны трудности в дифференциации от апластической анемии, для которой характерна более выраженная панцитопения, отсутствие типичных для МДС хромосомных аббераций и снижение содержания CD34+ клеток в костном мозге.
10.4. МДС с миелофиброзом: до 50% случаев всех вариантов МДС характеризуется фиброзом костного мозга (до 15% имеют выраженный фиброз); фиброз более характерен для вторичного МДС; характерны ги- перклеточность костного мозга, диффузный ретикулиновый фиброз его стромы и дисплазия не менее чем в 2 клеточных линиях; в периферической крови панцитопения, признаки клеточной дисплазии и лейкоэрит- робластоза; органомегалия нехарактерна; заболевание быстро прогрессирует; необходимо дифференцировать от острого мегакариобластного лейкоза, острого миелофиброза (острого панмиелоза с фиброзом), хронических миелопролиферативных заболеваний, метастатического рака, лимфом и волосатоклеточного лейкоза.
ЛЕЧЕНИЕ
11. Выбор терапии основан на диагнозе и группе риска по международной прогностической бальной системе (IPSS). В соответствии с международными рекомендациями для выбора терапевтической тактики пациентов с МДС подразделяют на 2 большие группы риска:
группу относительно низкого риска, включая в нее пациентов с низким и промежуточным 1 риском по системе IPSS;
группу высокого риска, включая в нее пациентов с промежуточным 2 и высоким риском по системе IPSS.
У пациентов из группы относительно низкого риска возможно применение только поддерживающей терапии либо терапии малой интенсивности. Интенсивная терапия показана пациентам группы высокого риска с учетом возраста, анамнеза заболевания, клинических проявлений, общего состояния и наличия признаков прогрессирования заболевания.
11.1. Поддерживающее лечение.
Поддерживающее лечение назначают с целью уменьшения проявлений заболевания и поддержания качества жизни. У пациентов из группы относительно низкого риска это может быть основным видом терапии.
11.1.1. Трансфузии донорских эритроцитов. Основным клиническим показанием для трансфузии донорских эритроцитов является не столько уровень гемоглобина, сколько степень адаптированности пациента к анемии.
11.1.2. Применение хелаторов железа.
Показаниями к применению хелаторов железа является переливание более 20-25 доз эритроцитной массы, уровень сывороточного ферритина более 2500 мкг/л, наличие дисфункции сердца (аритмия, сердечная недостаточность) и поражения печени.
Дефероксамин применяют в дозе 30-40 мг/кг в виде 12 часовых подкожных инфузий 5-7 раз в неделю (ночью). Дозу лекарственного средства снижают до 25 мг/кг при уровне ферритина ПО г/л, тромбоциты > 100 • 10 9 /л, нейтрофилы >1,0-10 9 /л, нет бластных клеток
время ремиссии, уменьшение абсолютного числа гранулоцитов, тромбоцитов, снижение концентрации НЬ на > 15 г/л или появление трансфузионной зависимости
Частичный: сокращение количества клеток, имеющих хромосомные аномалии на > 50 %
Гранулоциты (начальное количество 9 /л): прирост на 100 % и абсолютное количество > 0,5 • 10 9 /л
Прогноз
Для оценки прогноза и определения тактики лечения пациентов с МДС используют международную прогностическую бальную систему (далее IPSS).