Диагноз пмо что это такое
Стадии рака: классификация онкологических заболеваний
Стадия онкологического заболевания дает информацию о том, насколько велика опухоль и распространилась ли она по организму. Это помогает врачам определять прогноз пациента и план лечения.
С помощью врача-онколога, резидента Высшей школы онкологии Сергея Югая разбираемся, как врачи устанавливают стадии рака и что каждая из них означает.
На что влияет стадия онкологического заболевания?
Стадирование нужно, чтобы спрогнозировать, какие у пациента шансы на выздоровление, а также чтобы определить, какой метод лечения будет наиболее эффективен в конкретном случае, — поясняет Сергей Югай.
Все начинается с медицинского осмотра и обследований — УЗИ, КТ, МРТ, ПЭТ-КТ и других методов в зависимости от вида рака. Затем врач берет кусочек опухоли — биопсию или удаляет опухоль целиком во время операции, а после отправляет материал на гистологический анализ, чтобы поставить диагноз.
Стадии рака по TNM-классификации
Стадии онкологического процесса описывают разными способами — это зависит от вида опухоли. Один из самых распространенных способов — стадирование с помощью TNM-классификации.
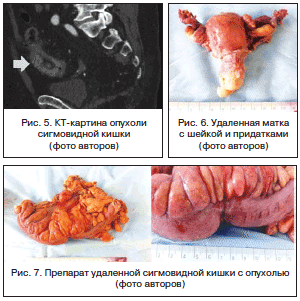
Т характеризует первичную опухоль, ее размеры и вовлечение окружающих структур в опухолевый рост, например, прорастание в стенку кишки или желудка. N говорит о наличии в лимфоузлах метастазов и количестве пораженных лимфоузлов, а М — о наличии отдаленных метастазов (во внутренних органах, костях, ЦНС или лимфоузлах, которые расположены далеко от первичной опухоли), — объясняет Сергей Югай.
Индекс Т принимает значения от 0 до 4. 0 означает, что первичная опухоль не обнаружена, 1 — опухоль маленькая, а 4 — опухоль проросла в прилегающие ткани. Таким образом, чем больше цифра рядом с Т, тем ситуация сложнее. При некоторых видах рака N принимает значение 0 или 1, при других — 0, 1 или 2, а иногда — 0, 1, 2 и 3. 0 означает, что опухоль не проникла в ближайшие лимфоузлы, а 3 — что поражено множество лимфоузлов. M0 показывает, что метастазов нет, а 1 — что метастазы есть.
Онкологи выставляют стадию по TNM клинически — до операции или когда операция не планируется и патоморфологически — при изучении удаленной во время операции опухоли, — объясняет Сергей.
Клиническая стадия обозначается буквой «c», например, cT2. Патоморфологическая — буквой «p», например, pN1.
От правильной стадии зависит тактика лечения. Например, пациент — мужчина с раком желудка и стадией cT1N0M0. Это значит, что опухоль прорастает в слизистую и подслизистый слой стенки желудка. В этом случае пациенту показана операция. Если же стадия выше (cT2N1M0, например), то есть опухоль пациента прорастает в мышечный слой, и есть метастазы в лимфоузлах, то может понадобиться химиотерапия перед операцией, которая позволит улучшить результаты лечения, — добавляет Сергей.
Стадию рака могут обозначать с помощью цифр — 0, I, II, III, IV. Что это значит?
Клинические стадии (0, I, II, III, IV) тесно связаны с системой TNM. Как правило, одна клиническая стадия включает в себя несколько вариантов стадирования по TNM. Эти варианты характеризуются схожими прогнозом и подходом к лечению. Например, стадии T1N3M0, T2N3M0, T3N2M0 рака легкого объединяются в IIIВ стадию, так как при любой из этих ситуаций пациент будет иметь примерно одинаковый прогноз и тактику лечения. В этом конкретном примере необходима химиолучевая терапия, а не операция, — комментирует Сергей Югай.
Меняется ли стадия после лечения, при прогрессировании заболевания?
Нет, стадия выставляется один раз. Но есть нюансы:
Например, мы хотим посмотреть, как опухоль ответила на лечение, чтобы понять, можно ли делать операцию. После лечения опухоль уменьшилась, и мы добавляем к стадии новые данные. При прогрессировании опухолевого процесса первоначальная стадия также остается прежней, но, к сожалению, прогноз будет менее благоприятный. Например, у человека II стадия рака желудка. Он прооперирован, и прогноз у него хороший. Через 2 года врачи обнаруживают у пациента метастазы в легких. Стадия остается II, но рак у пациента уже метастатический, что очень усложняет положение, — говорит Сергей.
Бывает, что люди сравнивают свою ситуацию с историями других пациентов. Если речь идет о разных онкологических заболеваниях, то такие сравнения некорректны — это заболевания с разными прогнозами и схемами лечения:
Например, с нейроэндокринным раком поджелудочной железы люди могут жить десятилетиями, а при метастатической стадии рака поджелудочной железы — полгода или год, — объясняет врач-онколог.
Что может повлиять на прогноз людей с одинаковой стадией и одним видом рака?
Сергей Югай выделяет три фактора:
Тактика лечения больных с первично-множественными злокачественными новообразованиями (обзор клинического наблюдения)
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
Первично-множественные злокачественные новообразования (ПМЗНО) – это состояние, при котором у одного и того же человека выявляется два и более злокачественных новообразования одновременно или через определенный (любой по продолжительности) промежуток времени. ПМЗНО являются группой заболеваний, входящих в более обширную группу первично-множественных опухолей (ПМО), включающих и доброкачественные опухоли [1, 2, 7, 8].
Впервые случай ПМО в литературе был описан Авиценной у женщины с двусторонним поражением опухолями молочных желез. В последующем появлялись единичные описания одномоментного или последовательного возникновения опухолей у пациентов [1, 2].
Понятие первичной множественности опухолей впервые было введено в практику в 1869 г. Бильротом, который и считается основоположником изучения данной проблемы. Он определил 3 основных критерия первичной множественности опухолей:
1) опухоли располагаются в различных органах;
2) имеют различную морфологическую структуру;
3) каждая из опухолей дает собственные метастазы.
В дальнейшем данные положения были пересмотрены, и в 1932 г. S. Warren совместно с O. Gates установили, что единственным и обязательным условием постановки диагноза ПМО является доказанная первичность каждой из опухолей, т. е. они не должны являться метастатическими (лимфогенными, гематогенными или имплантационными метастазами).
В России вопросами ПМО занимались А.А. Серебряков (пионер в области изучения данной проблематики), Г.Г. Непряхин, Н.Н. Петров [2, 7].
В 1968 г. появилась одна из первых классификаций ПМО, предложенная С.М. Слипчаком (табл. 1).
Позднее был выявлен недостаток классификации С.М. Слипчака – отсутствие групп синхронно-метахронных и метахронно-синхронных опухолей. В 1974 г. вышла новая, дополненная классификация, предложенная В.Г. Бебякиным (табл. 2). Особенностью этой классификации является то, что в ней отражаются сочетания злокачественных, злокачественных и доброкачественных, множественных злокачественных и доброкачественных опухолей.
На сегодняшний день накоплен большой опыт в изучении ПМО, в их структуре выделена группа ПМЗНО, предложена их классификация Г.Г. Непряхиным (табл. 3).
Отмечено, что в последнее время частота встречаемости ПМЗНО возросла примерно в 9 раз [10, 11]. Причиной многих случаев ПМЗНО являются аберрации в определенных генах или группах генов (синдром Ли – Фраумени, для которого характерен целый спектр новообразований: остеосаркома, саркомы мягких тканей, опухоли мозга, лейкозы, рак молочной железы и др.; наследственный рак молочной железы и яичников; наследственный неполипозный рак толстой кишки (HNPCC, Hereditary nonpolyposis colorectal cancer) – синдром Линча; семейный аденоматоз толстой кишки (FAP, Familial adenomatosis coli)) [3–6, 8, 9]. В других случаях выяснить причину множественности опухолей не всегда представляется возможным.
Ниже представлено клиническое наблюдение первично-множественных метахронно-синхронных опухолей.
Больная Г., 68 лет. Поступила в гастроэнтерологическое отделение № 4 (ГЭО-4) ГБУЗ «Московский клинический научный центр» Департамента здравоохранения г. Москвы (МКНЦ) с жалобами на периодически возникающие боли в нижних отделах живота, правом подреберье умеренной интенсивности. Данные симптомы сопровождаются появлением небольшого количества примеси крови в кале. Пациентка также отмечала похудение на 15 кг за 5 мес. при сохраненном аппетите и периодически возникающие кровянистые выделения из влагалища в течение 3 мес.
Из анамнеза было установлено, что больная более 15 лет страдает запорами. Стул регулировала самостоятельно приемом слабительных средств. В 2011 г. проходила курс лечения антибактериальными препаратами по поводу хронического пиелонефрита, после чего запоры усилились, появились боли в животе. За помощью не обращалась, не обследовалась. В августе 2013 г. отметила появление примеси крови в кале. Однако за помощью в лечебные учреждения вновь не обратилась. В декабре 2013 г. появились выраженные боли в эпигастрии. Обратилась к врачу в поликлинику по месту жительства. 30.12.2013 г. выполнена гастроскопия, при которой выявлены недостаточность кардии, эрозивный гастрит, бульбит, формирующийся полип антрального отдела желудка. Проведен курс лечения, включающий антисекреторные препараты, препараты солей висмута. Контрольного эндоскопического исследования не проводилось. В феврале 2014 г. пациентка обратилась в поликлинику по месту жительства с жалобами на вздутие живота, запоры, боли в животе, наличие небольшой примеси крови в кале. Рекомендованы колоноскопия, ирригоскопия. 05.02.2014 г. сделана попытка проведения колоноскопии. При этом аппарат введен до средней трети сигмовидной кишки, далее ввиду выраженного болевого синдрома аппарат провести не удалось. На осмотренных участках толстой кишки органических изменений выявлено не было. 14.02.2014 г. сделана попытка проведения ирригоскопии. Однако ввиду того, что пациентка не удерживает бариевую клизму, осмотреть удалось только прямую кишку и начальные отделы сигмовидной кишки – изменений также не выявлено. В дальнейшем пациентка принимала ферментативные препараты (панкреатин). В апреле – мае 2014 г. вновь появились боли в животе, вздутие живота, кровь в кале. Обратилась в клинико-диагностическое отделение (КДО) МКНЦ. 06.05.2014 г. госпитализирована в ГЭО № 4 МКНЦ для обследования и определения тактики лечения.
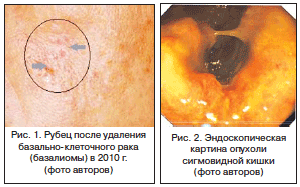
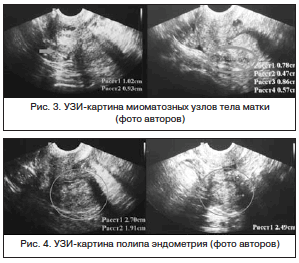
Объективный статус. Больная в сознании, адекватна, в пространстве и времени ориентирована, критика не нарушена. Рост – 159 см, вес – 81 кг. Кожные покровы чистые. Имеется белесый рубец на коже щеки слева после удаления базалиомы в 2010 г. (рис. 1). Грудная клетка цилиндрической формы; перкуторно – умеренный коробочный звук. Аускультативно – везикулярное дыхание, несколько жесткое. Границы легких – в пределах нормы. Область сердца не изменена, границы сердца расширены влево на 1 см, АД – 130/80 мм рт. ст., пульс – до 80 уд./мин. Область почек не изменена, почки не пальпируются. Мочеиспускание не нарушено. Живот не вздут, мягкий. При пальпации болезненный незначительно в левой половине. Перитонеальных симптомов нет. Печень не пальпируется, объемные образования через переднюю брюшную стенку не определяются. Периферические лимфатические узлы не увеличены.
Данные клинического обследования пациентки. При колоноскопии в верхней трети сигмовидной кишки выявлена циркулярная бугристая опухоль, суживающая просвет кишки, кровоточащая при контакте (рис. 2), взята биопсия; в остальных отделах толстой кишки – без патологии.
При эзофагогастродуоденоскопии выявлены хронический гастрит с наличием эрозий в теле желудка, эрозивный бульбит, недостаточность кардии; в антральном отделе желудка определяются 2 полипа 0,2 и 0,5 см в диаметре соответственно (взята биопсия). Гистологическое исследование № 14610-11/14: слизистая оболочка желудка с картиной хронического выраженного неактивного гастрита. HP+.
Выполнено УЗИ органов брюшной полости, при котором диагностированы умеренная гепатомегалия, диффузные изменения печени, поджелудочной железы (хронический панкреатит).
По данным УЗИ органов малого таза установлено, что тело матки с ровным контуром, миометрий симметричной толщины, средней эхогенности с наличием очаговой неоднородности; по задней стенке интерстициально и субсерозно лоцируется узел 10х9 мм, по задней стенке интерстициально – аналогичные узлы 8х5 и 8,6х6 мм. По передней стенке ближе к перешейку гипоэхогенный узел 7,4х5 мм (рис. 3); шейка матки неоднородной плотности, в ее стенке определяются кисты до 3 мм в диаметре; эндометрий неоднородный, толщиной до 18 мм; полость матки расширена за счет жидкостного скопления и объемного образования размерами 27х19х25 мм, исходящего из эндометрия (рис. 4).
Выполнена мультиспиральная компьютерная томография (КТ) органов грудной клетки, брюшной полости и малого таза. Данных о метастатическом поражении легких не получено, выявлен диффузный пневмосклероз, признаки хронической обструктивной болезни легких (ХОБЛ), данных о наличии метастазов в печени не получено, имеются признаки жирового гепатоза печени, в проекции входа в малый таз в сигмовидной кишке определяется утолщение ее стенки до 19 мм на протяжении до 40 мм (рис. 5). В теле матки определяются обызвествленные округлые миоматозные узлы; забрюшинные лимфатические узлы и узлы малого таза не увеличены.
Исследование функции внешнего дыхания не выявило изменений в спирограмме.
По данным эхокардиографии выявлена умеренная гипертрофия миокарда левого желудочка (ЛЖ); полость правого желудочка на верхней границе нормы, отмечены признаки изменений стенок аорты, митрального и аортального клапанных колец возрастного характера; митральная регургитация I степени, признаки диастолической дисфункции ЛЖ по первому типу; нарушения локальной сократимости миокарда не выявлено; фракция выброса ЛЖ – достаточная (58,9%); перикард – без особенностей.
Больной выполнена ирригоскопия, при которой в проекции верхней трети сигмовидной кишки выявлено стойкое циркулярное сужение просвета до 1 см протяженностью около 3,5 см, в остальных отделах толстой кишки патологических изменений не выявлено.
Рентгенологическое исследование органов грудной клетки выявило картину пневмосклероза, отмечено расширение тени ЛЖ сердца, атеросклероз аорты.
Постановка диагноза и лечение. 15.05.2014 г. проведен консилиум в составе онколога, гинеколога, колопроктолога, анестезиолога-реаниматолога, гастроэнтеролога. Заключение: с учетом наличия у пациентки кровоточащего крупного полипа эндометрия, циркулярной опухоли сигмовидной кишки рекомендовано на первом этапе выполнить диагностическое выскабливание матки и резекцию полипа эндометрия. После получения заключения гистологических исследований (биоптатов из опухоли сигмовидной кишки и удаленного полипа эндометрия) решить вопрос о дальнейшей тактике лечения.
19.05.2014 г. больной выполнены диагностическое выскабливание матки и резекция полипа эндометрия.
Гистологическое исследование № 14612-17/14 (биопсия из опухоли сигмовидной кишки): аденокарцинома толстой кишки.
Гистологическое исследование № 17069-84/14 (полип миометрия): в соскобе фрагменты солидной злокачественной опухоли: недифференцированный рак.
На основании данных обследования, анамнеза, данных патоморфологического исследования установлен клинический диагноз.
Основное заболевание: ПМЗНО: рак сигмовидной кишки сT3N0M0 II стадия; синхронный рак тела матки с TхN0M0; метахронный базально-клеточный рак кожи лица. Состояние после хирургического лечения по поводу базально-клеточного рака кожи лица в 2010 г.
Сопутствующие заболевания: множественная миома матки. ИБС: стенокардия напряжения II функционального класса (ФК). Атеросклеротический кардиосклероз. ГБ III степени, II стадии, риск сердечно-сосудистых осложнений (ССО) – 4. СД 2-го типа, инсулинопотребный, средней степени тяжести, субкомпенсированный. БА смешанного генеза (аллергическая и инфекционно-зависимая), хроническое рецидивирующее течение, ремиссия. Диффузный пневмосклероз. ХОБЛ. Хронический пиелонефрит, ремиссия. Хронический, рецидивирующий цистит, ремиссия. Глаукома левого глаза II–III, начальная катаракта левого глаза, ангиосклероз сетчатки левого глаза. Остеохондроз поясничного отдела позвоночника. Двухсторонний гонартроз I степени.
С учетом данных полученного гистологического исследования было решено выполнить одномоментно резекцию сигмовидной кишки и экстирпацию матки с придатками.
30.05.2014 г. под комбинированным обезболиванием больной выполнена нижне- и среднесрединная лапаротомия. При ревизии в брюшной полости и малом тазу выявлен выраженный спаечный процесс. Спайки разделены острым путем. При дальнейшей ревизии в печени метастазов не выявлено, забрюшинные лимфатические узлы не увеличены, асцита нет. Сигмовидная кишка удлинена – долихосигма. В сигмовидной кишке в проекции ее средней трети определяется опухоль до 4 см протяженностью, циркулярно стенозирующая просвет кишки. Отделы толстой кишки выше опухоли до левого изгиба ободочной кишки раздуты до 6 см в диаметре, заполнены газом и плотным калом, стенка гипертрофирована, отечна. Ниже опухоли – сигмовидная кишка спавшаяся. Матка обычных размеров и формы с субсерозными узлами до 1,5 см в диаметре. Правый яичник – 2,5х2,0х1,5 см, не изменен, правая маточная труба длиной около 5 см, деформирована. Левый яичник – 2,5х2,0х1,5 см, не изменен, левая маточная труба длиной около 5 см. Передне- и позадиматочное пространство без патологии. Первым этапом операции выполнена экстирпация матки с придатками. Вторым этапом выполнена резекция сигмовидной кишки с опухолью. С учетом картины субкомпенсированной кишечной непроходимости решено сформировать концевую сигмостому в левой подвздошной области (рис. 6, 7).
Общая длительность оперативного вмешательства составила 210 мин. Общая кровопотеря – 150 мл.
В раннем послеоперационном периоде больной проводилось лечение в отделении реанимации и интенсивной терапии. На 2 сут после операции переведена в общую палату колопроктологического отделения. В день перевода больная была активирована. Еще в реанимационном отделении на 1 сут после операции больной было разрешено пить негазированную воду до 500 мл/сут. Пищу больная начала принимать на 2 сут после оперативного лечения. Отделяемое по сигмостоме появилось на 4 сут после операции.
В целом послеоперационный период протекал гладко. Рана зажила первичным натяжением. Швы сняты на 10 сут после операции.
Гистологическое исследование послеоперационного материала: в матке выявлена низкодифференцированная эндометриальная аденокарцинома, прорастающая более чем на половину толщины миометрия и устье левой маточной трубы; в клетчатке брыжеечной артерии лимфоидной ткани не обнаружено; в сигмовидной кишке выявлено разрастание умеренно дифференцированной аденокарциномы кишечного типа, прорастающей все слои стенки кишки и врастающей в брыжейку; в 12 исследованных лимфатических узлах опухолевого роста выявлено не было; края резекции – без опухолевого роста.
Таким образом, на основании данных патоморфологического заключения операционного материала выставлен окончательный клинический диагноз.
Основное заболевание: ПМЗНО: рак сигмовидной кишки рT3N0M0 II стадия; синхронный рак тела матки рT1сN0M0 IC стадия; метахронный базально-клеточный рак кожи лица. Состояние после хирургического лечения по поводу базально-клеточного рака кожи лица в 2010 г.
Осложнения основного заболевания: субкомпенсированная кишечная непроходимость.
Сопутствующие заболевания: миомы матки. ИБС: стенокардия напряжения ФК II. Атеросклеротический кардиосклероз. ГБ III степени, II стадии, риск ССО 4. СД 2-го типа, инсулинопотребный, средней степени тяжести, субкомпенсированный. БА смешанного генеза (аллергическая и инфекционно-зависимая), хроническое рецидивирующее течение, ремиссия. Диффузный пневмосклероз. ХОБЛ. Хронический пиелонефрит, ремиссия. Хронический, рецидивирующий цистит, ремиссия. Глаукома левого глаза II–III, начальная катаракта левого глаза, ангиосклероз сетчатки левого глаза. Остеохондроз поясничного отдела позвоночника. Двухсторонний гонартроз I степени.
Больная выписана из стационара на 11 сут после оперативного лечения в удовлетворительном состоянии.
В настоящий момент больная получает курс химиотерапии по схеме XELOX и гормонотерапию прогестинами.
Выводы
1. При наблюдении за пациентами с различными заболеваниями (тем более с ранее выявленными злокачественными опухолями) следует помнить о возможном возникновении 2-х и более злокачественных опухолей у одного и того же больного, причем как синхронно (одновременно), так и метахронно (с интервалом 6 мес. и более), и при возникновении жалоб, которые могут указывать на развитие опухолевого процесса, проводить им комплексное обследование.
2. Успешность лечения больных с ПМЗНО достигается выбором адекватной состоянию больного комплексной терапии, включающей в т. ч. специальные методы лечения.
3. Очень важным остается вопрос этапного наблюдения в группе лиц с уже установленными опухолями и получившими лечение по поводу них.


Только для зарегистрированных пользователей
Первично-множественные опухоли
Первично множественные опухоли – неоплазии, возникающие одновременно или через определенный промежуток времени и не являющиеся метастазами друг друга. Могут быть доброкачественными или злокачественными, мультицентрически располагаться в одном органе, возникать в парных органах, локализоваться в пределах одной системы или нескольких систем. Возникают в результате соматических мутаций или наследственных генетических аномалий. Диагностируются на основании клинических симптомов, лабораторных и инструментальных исследований. Тактика лечения определяется типом, распространенностью, локализацией и степенью злокачественности новообразований.
Общие сведения
Первично множественные опухоли – две или более неоплазии различного генеза, одновременно либо последовательно развившиеся в одном или нескольких органах. В большинстве случаев диагностируются два новообразования. Три узла обнаруживаются у 5-8% пациентов. Случаи четырех и более неоплазий являются крайне редкими и рассматриваются как казуистические. В последние десятилетия отмечается резкое увеличение количества первично множественных опухолей, однако истинная частота их развития пока является предметом исследований.
Согласно статистическим данным, первично множественные опухоли выявляются у 13% пациентов с онкологическими заболеваниями, однако некоторые специалисты указывают, что эта цифра может быть заниженной из-за возможных диагностических ошибок (при определении независимого процесса, как метастаза первичного новообразования) и гибели некоторых больных до появления симптомов второй неоплазии. Лечение первично множественных опухолей осуществляют онкологи, гастроэнтерологи, эндокринологи, маммологи, гинекологи и специалисты в других сферах медицины (в зависимости от локализации новообразований).
Первое упоминание о множественных неоплазиях встречается в трудах Авиценны, который более тысячи лет назад описал двухсторонний рак молочных желез. В XIX веке описания первично множественных опухолей стали все чаще встречаться в специализированной литературе. Наиболее существенный вклад в определение понятия и изучение данной патологии внес немецкий хирург Бильрот. В частности, он первым дал определение подобным патологическим состояниям, отнеся к первично множественным опухолям новообразования различной структуры, локализующиеся в разных органах и дающие собственные метастазы.
В первой половине XX века формулировка Бильтота была пересмотрена. В настоящее время первично множественными опухолями считаются неоплазии, которые могут располагаться в одном или в разных органах. Основным условием отнесения заболеваний к этой категории является одновременное или последовательное появление в организме нескольких независимых друг от друга очагов трансформации клеток. Второе и последующие новообразования не должны возникать в результате контактного распространения, лимфогенного или гематогенного метастазирования.
Причины
Непосредственной причиной развития солитарных и первично множественных опухолей являются генетические мутации, обусловленные несколькими факторами. С учетом особенностей этиопатогенеза различают три основных типа неоплазий: возникшие в результате спонтанных соматических мутаций, образовавшиеся вследствие индуцированных соматических мутаций, являющиеся результатом передающихся по наследству генетических мутаций. Следует учитывать, что подобное разделение является достаточно условным. На практике, скорее, можно выделить преобладающую причину развития, которая сочетается с другими, менее значимыми факторами.
При первично множественных опухолях перечисленные мутации могут сочетаться. Возможны любые комбинации, например, первое новообразование развивается спонтанно, второе – в результате индукции; первое является наследственным, второе – индуцированным; оба рака имеют одну и ту же природу (наследственность, воздействие экзогенных факторов) и т. д. При этом у больных первично множественными опухолями отмечается преобладание индуцированных и наследственных мутаций.
В числе наиболее значимых факторов, индуцирующих развитие первично множественных опухолей, рассматривают курение, проживание в неблагоприятных экологических зонах, профессиональные вредности (контакт с химическими мутагенами на некоторых производствах, превышение установленных нагрузок у радиологов), многократные рентгенологические обследования, лучевую терапию и химиотерапию предшествующих онкологических заболеваний. Вероятность возникновения первично множественных опухолей также повышается при нарушениях питания, иммунодефицитных состояниях, гормональных расстройствах и некоторых эндемических заболеваниях.
В список наследственных синдромов, сопровождающихся облигатным развитием или повышенной вероятностью возникновения онкологических поражений, включают более 100 заболеваний. Первично множественные опухоли развиваются или могут развиться при трети таких заболеваний. Наиболее известными синдромами являются МЭН-1, МЭН-2 и МЭН-3, при которых выявляются множественные эндокринные неоплазии. Кроме того, первично множественные опухоли могут диагностироваться при синдроме Линча, синдроме Гарднера, болезни Гиппеля-Линдау, синдроме Пейтца-Егерса и других.
Классификация
Существует несколько классификаций, созданных на разных этапах изучения данной патологии. Современные специалисты обычно используют классификацию Бебякина, разработанную в 1974 году. Согласно этой классификации выделяют следующие типы первично множественных опухолей:
Диагностика
Основой успешной диагностики первично множественных неоплазий является комплексный подход, разработанный с учетом особенностей возникновения и течения этой группы заболеваний. Одной из наиболее распространенных проблем при обнаружении первично множественных опухолей является отсутствие четкой клинической картины, характерной для каждого новообразования. Проявления неоплазий могут накладываться друг на друга, симптомы одного из поражений могут быть слабо выраженными, маскироваться под неопухолевое заболевание или имитировать признаки отдаленных метастазов.
Хотя бы частично решить эту проблему позволяют продуманные планы первичного и последующих обследований, составленные с учетом возможности развития первично множественных опухолей. Так, при локализации солитарного новообразования в зоне молочной железы специалисты уделяют пристальное внимание состоянию второй молочной железы и внутренних женских половых органов, при расположении неоплазии в области желудка – состоянию толстого кишечника, кожи, яичников, матки и молочных желез и т. д. План обследования в каждом конкретном случае составляется индивидуально. Решающую роль при постановке диагноза обычно играют радиологические методики (рентгенография, КТ), УЗИ, МРТ и гистологические исследования.
Вероятность развития первично множественных опухолей у онкологических больных в 6 раз выше, чем в среднем по популяции. С учетом этого обстоятельства, все пациенты с такими заболеваниями после лечения должны находиться под диспансерным наблюдением и проходить регулярные обследования. Такая мера позволяет выявлять рецидивы первичной неоплазии и диагностировать метахронные первично множественные опухоли. Риск развития второго онкологического поражения увеличивается в возрасте 55-70 лет, что должно учитываться при планировании обследования пациентов.
Лечение первично множественных опухолей
Лечение синхронных неоплазий осуществляется одновременно. В зависимости от локализации новообразований и состояния больного хирургическое вмешательство может проводиться единовременно либо быть поэтапным. При планировании очередности операций при первично множественных опухолях учитывают степень распространенности каждого онкологического процесса. В ряде случаев по поводу одного новообразования может быть проведено радикальное лечение, по поводу другого – симптоматическое или паллиативное.
При выборе консервативных методик ориентируются на чувствительность каждой опухоли к радиотерапии и различным химиопрепаратам. Тактика лечения метахронных первично множественных опухолей соответствует тактике лечения солитарных новообразований аналогичных стадий и локализаций. Прогноз определяется видом, расположением, стадией и степенью злокачественности первично множественных опухолей. Отдаленные результаты лечения метахронных неоплазий примерно совпадают с результатами терапии одиночных образований. При синхронных процессах прогноз ухудшается.