Дискератоз в мазке что это
Что такое лейкоплакия шейки матки? Причины возникновения, диагностику и методы лечения разберем в статье доктора Игнатенко Т. А., гинеколога со стажем в 13 лет.
Определение болезни. Причины заболевания
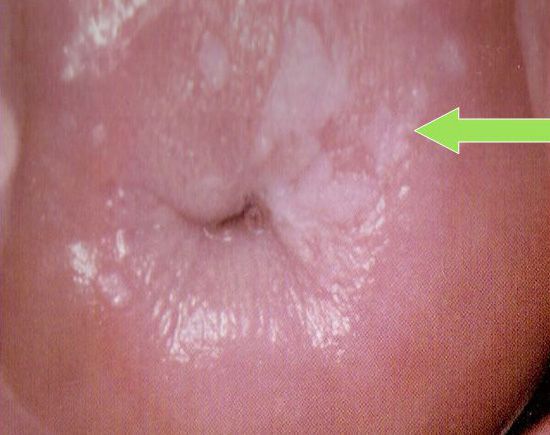
Лейкоплакия шейки матки — это утолщение и ороговение плоского эпителия слизистой оболочки шейки матки.
Термин «лейкоплакия» (в переводе с греческого — «белая бляшка») был предложен Швиммером в 1887 году для описания белесоватых участков слизистых оболочек щёк, которые расценивались как предраковые изменения. В отечественной литературе и клинической практике термин остаётся общепринятым до настоящего времени. За рубежом же предпочителен термин «дискератоз». [2]
Очаг лейкоплакии может располагаться на слизистой оболочке нижней губы, угла рта, дна полости рта, щёк, в аногенитальной области, на вульве, клиторе, во влагалище, на шейке матки, реже — в области головки полового члена, в окружности заднепроходного отверстия. [11]
Согласно статистике, частота лейкоплакии шейки матки составляет всего 0.7 на 100 000 случаев гинекологической заболеваемости, среди заболеваний шейки матки — 5.2%. [11]
Лейкоплакия шейки матки наиболее часто встречается в возрастной группе 17-39 лет. [9]
В большинстве стран Европы и США, где проводится организованный скрининг рака шейки матки, лейкоплакия шейки матки не попадает в активный поиск, пока цитологические мазки не выявят начальные степени дисплазии (предрака) шейки матки. В нашей стране тактика наблюдения и ведения лейкоплакии шейки матки более активная.
Причины развития лейкоплакии шейки матки делят на:
Под нарушением гормонального фона чаще подразумевают хроническое отсутствие овуляции, что приводит к дисбалансу эстрогена и прогестерона в организме с преобладанием первого. Относительно повышенные концентрации эстрогена, в свою очередь, действуют на органы-мишени (молочные железы, тело и шейка матки), приводя к гиперпластическим процессам (бесконтрольному увеличению числа клеток). [4] Часто у пациенток с лейкоплакией шейки матки диагностируют повышение уровня пролактина. Иммунные нарушения зачастую проявляются воспалительными процессами матки и ее придатков (вагиниты, сальпингоофориты, цервициты). [9] Отечественным исследованием выявлено повышение концентрации секреторного иммуноглобулина А (SIgA) у пациенток с такими фоновыми заболеваниями шейки матки, как эктопия цилиндрического эпителия и лейкоплакия шейки матки. [8]
Под химическими и травматическими воздействиями зачастую подразумевают интенсивное и неадекватное лечение по поводу «псевдоэрозии» шейки матки: приблизительно трети пациенток с лейкоплакией ранее проводилась диатермокоагуляция и другие деструктивные вмешательства на шейке матки. Немаловажным фактором развития лейкоплакии шейки матки является опущение и выпадение матки/шейки матки, которое сопровождается неизбежным нарушением влагалищной флоры и, при выраженных степенях, постоянным контрактом шейки матки с внешней средой. [5]
Симптомы лейкоплакии шейки матки
Зачастую заболевание протекает бессимптомно. Лишь около трети пациенток предъявляют жалобы на обильные бели и контактные кровяные выделения (после полового акта, использования тампонов, гинекологических осмотров).
Симптомы перерождения лейкоплакии в рак
Патогенез лейкоплакии шейки матки
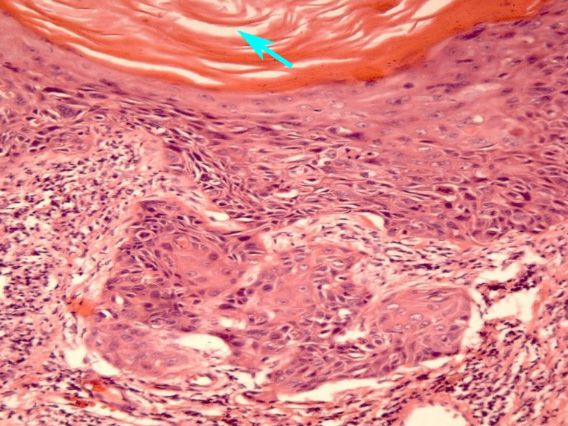
Механизм развития лейкоплакии в точности не выяснен. Считается, что под влиянием причинных факторов включаются механизмы ороговения в норме неороговевающего многослойного плоского эпителия шейки матки. На поверхности шейки матки формируются роговые чешуйки, клетки с деформированным ядром и внутриклеточными компонентами. [2]
Классификация и стадии развития лейкоплакии шейки матки
Согласно классификации Я.Б. Бохмана (1976), лейкоплакия, наряду с псевдоэрозией, эктропионом, полипом, эндометриозом шейки матки, цервицитами, истинной эрозией шейки матки, входит в группу фоновых заболеваний шейки матки, при которых не обнаруживается клеток с атипичными признаками, но длительное существование которых может послужить фактором риска развития предрака.
За рубежом лейкоплакию шейки матки с клеточным атипизмом относят к группе предраковой патологии шейки матки — ЦИН (цервикальной интраэпителиальной неоплазии, или дисплазии, шейки матки). [2]
Осложнения лейкоплакии шейки матки
Чем опасна лейкоплакия шейки матки
Лейкоплакия может распространяться с шейки матки на своды влагалища. Злокачественное перерождение клеток лейкоплакии наблюдается у 31,6% больных по данным отечественных авторов, 4,9-9% — по зарубежным данным. [11]
Диагностика лейкоплакии шейки матки
Комплексное обследование при лейкоплакии включает:
Кольпоскопия
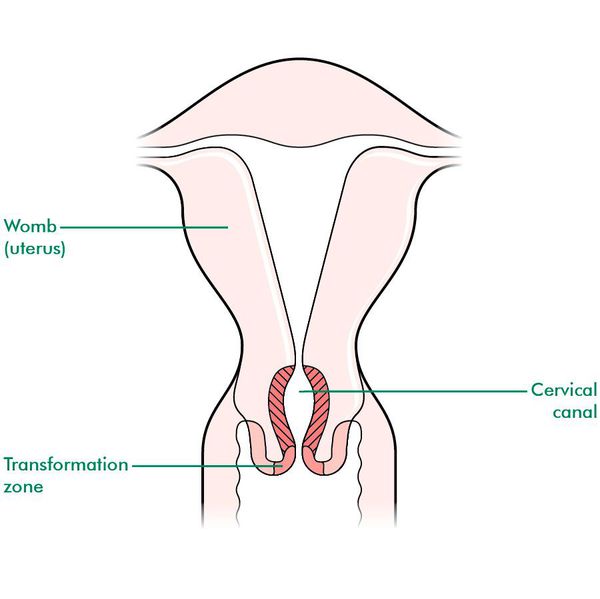
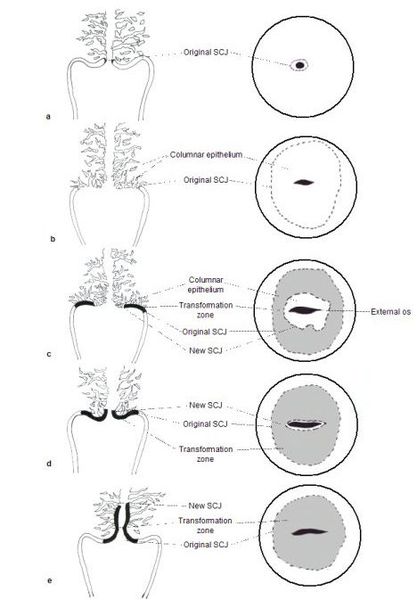
При кольпоскопии устанавливается тип зоны трансформации (переходной зоны стыка двух видов покровного эпителия шейки матки — многослойного плоского и цилиндрического), место расположения лейкоплакии.
Влагалищная часть шейки матки (экзоцервикс) покрыта многослойным плоским эпителием. В канале шейки матки (цервикальном канале, эндоцервиксе) — цилиндрический эпителий. Место перехода цилиндрического эпителия цервикального канала в многослойный плоский эпителий поверхности шейки матки носит название зоны трансформации. Эта область имеет большое клиническое значение, поскольку именно в ней возникает более 80% случаев дисплазии и рака шейки матки.
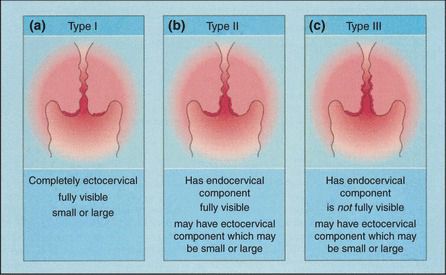
Зона трансформации 1 типа — переходная зона видна полностью. Это самый оптимальный и прогностически «благоприятный» вариант кольпоскопического заключения.
Зона трансформации 2 типа — переходная зона частично скрыта в канале шейки матки. Адекватно оценить такую картину сложно, так как наиболее измененные участки могут быть не видны и пропущены.
Зона трансформации 3 типа — переходная зона находится глубоко в канале шейки матки и оценить её кольпоскопически невозможно. Кольпоскопия в этом случае считается неинформативной, поскольку глубина залегания патологического очага остается неизвестной.
Цитологическое и гистологическое исследование
Сложность диагностики лейкоплакии при помощи простого цитологического соскоба с шейки матки заключается в невозможности оценки полноценного клеточного состава, так как из-за плотных роговых чешуек на поверхности многослойного плоского эпителия шейки матки в соскоб могут не попасть клетки из глубоких слоев. Таким образом может быть пропущена предраковая трансформация или даже рак шейки матки. [3] Именно поэтому основным методом диагностики лейкоплакии шейки матки является исследование ткани шейки матки, полученной при обязательно прицельной биопсии на фоне кольпоскопии. Зона трансформации 2 и 3 типа, определенные при кольпоскопии, могут послужить поводом для проведения не только биопсии, но и выскабливания слизистой канала шейки матки. Более щадящий метод оценки состояния слизистой канала шейки матки возможен при помощи микрокольпогистероскопии (офисная гистероскопия). Преимущество метода заключается в возможности нетравматичного прохождения канала шейки матки (цервикального канала) под визуальным контролем без анестезии. В процессе процедуры можно провести прицельную биопсию. При гистологическом исследовании лейкоплакия характеризуется терминами: кератоз, паракератоз, акантоз.
Бактериологическое исследование
Включает анализ влагалищного мазка и бактериальных посевов на флору и половые инфекции. Исследования важны тем, что при наличии воспаления шейки матки результаты цитологического и гистологического анализов могут быть искажены.
Анализ на ВПЧ
Исследование ДНК ВПЧ высокого онкогенного риска в соскобе с шейки матки и цервикального канала
В настоящее время изучают влияние вирусной инфекции на развитие лейкоплакии. Некоторые авторы считают, что процессы ороговения можно рассматривать как косвенный маркер папилломавирусной инфекции. Лейкоплакия, существующая вне инфицирования ВПЧ, зачастую не озлокачествляется. При сочетании с вирусом вероятность озлокачествления есть, но серьезных подтверждений этому факту пока нет. [12] [13]
Иммунограмма
Контроль уровня гормонов
Лечение лейкоплакии шейки матки
Консервативное лечение
Медикаментозное лечение при лейкоплакии включает:
В нашей стране лейкоплакию обычно подвергают деструкции — разрушению патологической ткани. Это обосновано, так как со временем лейкоплакия может трансформироваться, пациентка может заразиться ВПЧ и произойдёт перерождение ткани, что потребует новых биопсий и лишних визитов к врачу.
Хирургическое лечение
Наиболее часто применяемыми методами лечения лейкоплакии шейки матки являются:
Подготовка к операции включает:
Как проходят гинекологические операции
Манипуляции производят в первой половине менструального цикла (4-7 день от начала менструации). Для более точного определения патологической ткани процедура контролируется проведением кольпоскопии, а шейку матки обрабатывают раствором Люголя. Полное заживление и возвращение пациентки к привычной жизни (возможность половой жизни, использования вагинальных тампонов, посещение бассейна и прочее) зачастую ожидается через 28-40 дней после проведения процедуры. Коррекция гормональных нарушений и адекватная гормонотерапия, по некоторым данным, позволяет ускорить сроки заживления послеоперационной раны и снизить частоту повторного возникновения доброкачественных заболеваний шейки матки. [10]
При сочетании лейкоплакии с деформацией и гипертрофией шейки матки целесообразно проведение реконструктивно-пластических операций (пластика шейки матки) с целью восстановления анатомии цервикального канала. [14] [15]
Современные зарубежные исследователи расценивают лейкоплакию как доброкачественный физиологический процесс и в большинстве ситуаций рекомендуют профилактическое наблюдение.
Криодеструкция
Химическая коагуляция
Химическими коагулянтами, например Солковагином, лейкоплакию лечили в 90-х годах ХХ века. Эффективность лечения простой лейкоплакии шейки матки у молодых нерожавших женщин составляла около 70 %. Сейчас этот метод не применяют.
Антибиотикотерапия
Физиотерапия
Физиопроцедуры после операций на шейке матки, в том числе и при лейкоплакии, не проводятся.
Народные способы лечения
Беременность и лейкоплакия
При обнаружении лейкоплакии шейки матки у беременных обязательно лечат урогенитальную инфекцию, бактериальный вагиноз и восстанавливают микробиоценоз влагалища.
Реабилитация
Сразу после процедуры пациентку могут беспокоить тянущие боли внизу живота, однако они быстро проходят. Выделения чаще всего светлые слизистые или водянистые, редко с прожилками крови.
Кровянистые выделения после операции возникают редко. Но если они появились, беспокоят дольше 5–10 дней и/или менструации становятся обильнее и выделяются кровяные сгустки, то следует немедленно обратиться к врачу.
Также должна насторожить температуры тела свыше 37,5 °C, сильные боли внизу живота и гноевидные выделения из половых путей с резким неприятным запахом.
После операции в течение месяца рекомендуется:
Через две недели после операции врач проводит гинекологический осмотр, чтобы удостовериться, что пациентка восстанавливается. Слизистая полностью приходит в норму за 4–6 недель.
Наблюдение после лечения
Частота посещения доктора зависит от формы заболевания, эффективности лечения и наличия факторов риска, которые могут осложнить выздоровление: курение, ВИЧ-инфекция, заболевания, передаваемые половым путём, носительство онкогенных типов ВПЧ и т. п.
Диета
После лечения лейкоплакии следует придерживаться принципов правильного питания, специфическая диета не требуется.
Прогноз. Профилактика
При лейкоплакии шейки матки прогноз, как правило, благоприятный.
Принципы профилактики развития лейкоплакии шейки матки включают:
Классификация патологии шейки матки
Существует несколько классификаций патологий шейки матки:
Различают три основные группы заболеваний шейки матки: фоновые, предраковые и рак.
Фоновые или доброкачественные процессы – состояния, при которых изменений в клетках нет, т.е., сохраняется так называемая нормоплазия эпителия. Клетки правильно размножаются, растут, дифференцируются. К этим заболеваниям относятся: эктопия шейки матки, эктропион, полип, эндометриоз, лейкоплакия, папиллома, цервициты, истинная эрозия.
Эктопия шейки матки или эктопия цилиндрического эпителия. Это особенный диагноз и требует специального акцента. Состояние эктопии выявляется примерно у половины гинекологических пациенток. Представляет собой смещение границ эпителия, то есть внутренняя часть клеток как бы сползает вниз. Это не болезнь, а скорее нарушение клеточных границ. Обычно стык внутренних и внешних клеток шейки (зона трансформации) располагается во внутренней части канала и не видна. Но если граница смещается на влагалищную часть шейки, то это визуализируется при осмотре.
Врожденная неосложненная форма эктопии в номенклатуру патологий не внесена, болезнью не является и представляет собой физиологическое состояние. Буквально еще несколько лет назад любое красное пятно на шейке называлось «эрозией» и нещадно залечивалось. Именно поэтому эрозией болели огромное количество советских и российских женщин, и это был лидирующий диагноз! На сегодняшний день правильным определением смещения цилиндрического эпителия является «эктопия цилиндрического эпителия». Физиологическая эктопия шейки матки является вариантом нормы у молодых женщин до 25 лет, в более зрелом возрасте требует регулярного осмотра, цитологического и кольпоскопического контроля. Риск развития рака на фоне эктопии возникает при сочетании с другой патологией – воспаления, лейкоплакии, плоских кондилом. Осложненная форма эктопии сочетается с воспалительными и предраковыми процессами и требует тщательного подхода к обследованию и лечению.
Эктропион – выворот слизистой оболочки канала. Он возникает после разрывов и/или неправильного ушивания шейки матки. Это последствие послеродовых травм или абортов. То есть приобретенный эктропион всегда имеет травматический генез; врожденный встречается крайне редко и обычно сочетается с нарушением менструального цикла.
Полип шейки матки – разрастание слизистой оболочки округлой формы, с гладкой поверхностью. При расположении полипа внутри цервикального канала никаких симптомов не бывает, но если он разрастается и выглядывает из шеечного канала, то может себя проявить кровянистыми выделениями вне менструации и/или во время полового контакта.
Эндометриоз шейки матки характеризуется появлением очагов эндометриоза на шейке. Обычно протекает бессимптомно и выявляется только при осмотре в виде красных точек, так называемых «глазков». Редко проявляет себя кровянистыми выделениями или ощущением дискомфорта. Эндометриоз шейки возникает после хирургических вмешательств с использованием острых инструментов – в место прокола или надреза проникают клетки эндометрия и приживаются там, как при любом экстрагенитальном эндометриозе. Эндометриоз шейки, как правило, не представляет никакой опасности и требует обычного наблюдения и цитологической диспансеризации.
Кондиломы и папилломы – ВПЧ (HPV) – называют ассоциированными патологиями. Проявляются разрастаниями эпителия, являясь следствием инфицирования вирусом папилломы человека. Остроконечные кондиломы (папилломы) представляют собой отдельные прозрачные сосочки, имеют складчатость, выросты и ворсинки. Плоская кондилома выглядит как контур неправильной формы, слегка возвышающийся над слизистой. Эти образования могут располагаться как на шейке, так и в складках влагалища, на промежности и в перианальной зоне.
Предраковыми называют процессы, при которых возникают изменения в строении и росте клеток с нарушением дифференцирования. К этим процессам относятся: CIN, лейкоплакия с атипией, эритроплакия, аденоматоз. Это группа патологических изменений, занимающая промежуточное положение между нормальным эпителием шейки и раком.
По Международной классификации болезней выделяют следующие виды дисплазий:
CIN I – слабая дисплазия
CIN III – резко выраженная, а также карцинома in situ
Распространенность дисплазии в мире чрезвычайно высока. Этот диагноз поставлен миллионам женщин в мире. Наиболее часто регистрируется CIN II, ежегодно около 10 миллионов случаев. Но не каждая дисплазия переходит в рак и об этом важно знать! Скрининг, своевременная диагностика и лечение значительно (!) снижают вероятность перехода дисплазии в рак.
Дисплазии слабой и умеренной степени часто сочетаются с воспалительным процессом. Качественное лечение воспаления позволяет не только предотвратить переход дисплазии в следующую фазу, но и восстановить нормальную структуру тканей и избавиться от самой дисплазии. Важно обращать внимание на самочувствие, регулярно сдавать гинекологический мазок на микрофлору и половые инфекции, и своевременное обнаружение проблем и лечение позволят содержать флору влагалища в устойчивом состоянии, и снизит вероятность возникновения дисплазии.
Рак шейки матки никогда не возникает «вдруг», это заболевание обязательно должно пройти все стадии своего развития. И на каждом этапе правильные диагностика и лечение в состоянии прервать процесс развития рака. Именно поэтому столь важно относиться к диагностике внимательно – цитология, кольпоскопия, своевременная (!) биопсия могут дать быстрое обнаружение предраковых процессов.
Клетки эпителия
Плоскоклеточная метаплазия
Процесс, который характеризуется нераковыми изменениями в эпителиальных клетках шейки матки. Плоскоклеточная метаплазия возникает в результате совокупности общих и местных факторов, которые негативно влияют на организм, вызывая обратимый процесс, в ходе которого дифференцированные эпителиальные клетки преобразуются в более выносливые клетки многослойного плоского эпителия, с ороговением или без. Плоскоклеточная метаплазия цервикального канала также возникает как результат слияния с находящимся рядом эндоцервиксом. Изменение типа клеток может приводить к снижению функции эпителия. Когда патологические раздражители устраняются, метапластические клетки приобретают свою первоначальную форму и функцию. Сохранение физиологических стрессоров в областях, подверженных метаплазии, может приводить к дисплазии или предраковым клеточным изменениям. Развитие метаплазированных клеток происходит под влиянием герпеса или бактериальных инфекций (хламидиоз, токсоплазмоз, уреаплазмоз), протекающих на фоне ослабленного иммунитета и имеющих хроническую форму.
Кератоз
Представляет собой патологический процесс, который характеризуется пролиферацией и ороговением клеток плоского эпителия, выстилающего влагалищную часть шейки матки. При этом образуются утолщения или бляшки белого цвета с четкими границами, выступающие над поверхностью слизистых оболочек и могут быть видимы невооруженным глазом до любой обработки растворами.
Гиперкератоз
Это усиленное ороговение верхнего слоя многослойного плоского эпителия шейки матки. Считается, что причиной может быть недостаток эстрогена в организме женщины. В процессе ороговения слизистая покрывается плотными белесоватыми структурами, слегка выступающими над поверхностью здоровой ткани.
Паракератоз
Нарушения Ороговения эпителиального слоя эпидермиса (неполное ороговение). Характеризуется ороговением слизистых оболочек, потерей эпидермисом способности синтезировать кератогиалин (предшественник кератина) и нарушением морфологии слизистой оболочки. При данном процессе пораженный участок цервикального канала выглядит сморщенным из-за нарушения эластичности ткани. Такие островки более грубые.
Опасность представляет лейкоплакия, возникшая в результате активизации вируса папилломы человека высокого канцерогенного риска.
Трубная метаплазия
Характеризуется наличием в строме шейки матки нормальных по строению желез, выстланных клетками, напоминающими эпителий маточной трубы. Данная патология обычно представлена одиночной железой или группой желез и может быть реснитчатая либо секреторная. Трубная метаплазия часто встречается в неупорядоченном пролиферативном эндометрии
Атрофические изменения
Атрофия матки и шейки в большинстве случаев диагностируется у женщин в климактерическом периоде. Результатом данной патологии становится регресс эпителиальной ткани. Однако женщины детородного возраста также не застрахованы от атрофии шейки матки. Заболевание может развиться при дефиците эстрогенов, после оперативных вмешательств на шейке матки, при системных патологиях соединительной ткани. Атрофия шейки матки – один из факторов, вызывающих женское бесплодие.
В основном атрофические изменения происходят в период менопаузы. Снижение выработки гормонов приводит к исчезновению слизистой секреции, изменению бактериальной флоры. В результате происходит поэтапное сокращение толщины эпителия, что приводит ткани к раздражениям, травмам.
Изменения при беременности
В течение беременности устанавливается типичная для данного процесса картина мазка. Эти изменения связаны с продукцией гормонов плацентой и могут быть неверно трактованы как предопухолевые или опухолевые. Реактивные изменения шейки матки связаны с нарушением клеток ее эпителия. Возникают при: воспалениях, гиперкератозе, паракератозе, дискератозе, плоскоклеточной метаплазии, железистой гиперплазии, полипах, лимфоцитарном (фолликулярном) цервиците.
Внутриэпителияальные изменения клеток и рекомендуемые алгоритмы ведения пациенток
Атипичные железистые клетки (AGC)
Лечение и профилактика прогрессирования заболеваний шейки матки, ассоциированных с вирусом папилломы человека
Приведены основные профилактические мероприятия, направленные на раннее выявление и преодоление прогрессирования ВПЧ-ассоциированной патологии шейки матки. Применение препарата инозин пранобекс повышает эффективность терапии заболеваний шейки матки, ассоц
Main preventive measures directed to early diagnostics and liquidation of development of HPV-associated cervical pathology. Use of inozin pranobex medication increases efficiency of therapy of cervical diseases associated with HPV infection.
Основными проблемами в тактике ведения женщин с заболеваниями шейки матки, ассоциированными с вирусом папилломы человека (ВПЧ), являются несвоевременная и некачественная диагностика, отсутствие четких алгоритмов при принятии решения, а также недостаточная приверженность пациенток к лечению, в основном связанная с полным или частичным невыполнением рекомендаций врача.
По оценкам Центров по контролю заболеваемости (англ. Centers for Disease Control and Prevention, CDC) в США ВПЧ инфицируются до 5,5 млн человек в год [1]. В Европе в год регистрируется 554 000 случаев заболеваний, вызванных этими вирусами, в том числе: цервикальных внутриэпителиальных (интраэпителиалъных) неоплазий (cervical intraepithelial neoplasia — CIN) легкой степени (CIN I), генитальных бородавок, CIN средней и тяжелой степени (CIN II и III), рака шейки матки (РШМ). Несмотря на современные методы диагностики и лечения предраковых заболеваний шейки матки, ежегодно в мире фиксируют 470 тыс. новых случаев РШМ, из которых 233 тыс. заканчиваются смертельным исходом [2]. По данным российских ученых папилломавирусная инфекция (ПВИ) гениталий встречается у 44,3% женщин, обращающихся в гинекологические клиники [3], а заболевания шейки матки, ассоциированные с ВПЧ, встречаются у 50–80% населения и 99,7% случаев подтвержденного РШМ.
Течение ВПЧ-инфекции зависит от состояния иммунной системы и может быть транзиторным, латентным и персистирующим [4–8]. Возможно самоизлечение латентных и начальных субклинических форм ПВИ, для чего важен врожденный компонент иммунной системы. Главное значение имеют клеточные, рецепторные и молекулярные механизмы защиты. Наиболее неблагоприятное течение — персистирующее. При этом ВПЧ «обманывает» иммунную систему макроорганизма, что позволяет ему длительно персистировать ввиду своих эволюционно приобретенных особенностей — репликационный цикл ограничен эпителием, нет виремии и цитолиза, имеется локальная иммуносупрессия за счет вирусных белков [9–11]. Длительная персистенция высокоонкогенных типов ВПЧ более двух лет является наиболее опасным фактором прогрессии предрака шейки матки [12]. При персистенции ВПЧ 16-го типа риск развития CIN составляет 40–50%, 26-го типа — 30–40%, 31-го, 58-го, 82-го типов — по 20–30%, 18-го, 33-го, 35-го, 51-го, 52-го типов — по 10–20% [12]. При обследовании молодых женщин с ПВИ персистенция ВПЧ через 1 год выявлялась у 30%, через 2 года — у 9%, в то время как у женщин старшего возраста — у 50% [13].
В мировой практике используются различные классификации ПВИ и ассоциированных с ней заболеваний. Ориентировочная классификация ПВИ представлена J. Handley и соавт. [14]:
Аногенитальная ВПЧ-инфекция и ассоциированные с ВПЧ заболевания
ВПЧ-инфекция
1. Клинические формы (видимые невооруженным глазом или невидимые, но при наличии соответствующей симптоматики):
2. Субклинические формы (невидимые невооруженным глазом и бессимптомные, выявляемые только при кольпоскопии и/или цитологическом или гистологическом исследовании):
3. Латентные формы (отсутствие морфологических или гистологических изменений при обнаружении ДНК ВПЧ).
Заболевания, ассоциированные с ВПЧ
Клинические и субклинические формы:
Кроме этого, в литературе при описании поражений шейки матки, ассоциированных с ВПЧ, применяют классификацию по Папаниколау — в зависимости от степени изменений в мазках выделяют 5 классов. ВОЗ рекомендует использовать терминологическую систему Бетесда (The Bethesda System — TBS) — норма, ASCUS (Atypical squamous cells of undertermined significance (атипичные клетки плоского эпителия неясного значения)), LSIL (Low grade squamous intraepithelial lesion (интраэпителиальное плоскоклеточное поражение низкой степени тяжести)), HSIL (High grade squamous intraepithelial lesion (интраэпителиальное плоскоклеточное поражение высокой степени тяжести)), карцинома. Однако TBS не исключает использование терминов CIN и «дисплазия».
Согласно существующим принципам по ведению больных с клиническими проявлениями, связанными с ВПЧ, лечение аногенитальных ВПЧ-поражений направлено на разрушение тем или иным методом папилломатозных очагов, возникающих на месте внедрения вируса. Именно такой подход приведен во всех основных рекомендациях по ведению больных с ВПЧ-инфекцией (CDC, Европейских рекомендациях, рекомендациях ВОЗ). Такой подход представлен и в рекомендациях Российского общества дерматовенерологов и косметологов.
Как для лечения клинических проявлений ВПЧ-инфекции, так и ассоциированных с ней заболеваний (в первую очередь это касается CIN II и CIN III), применяют деструктивные методы — хирургические, физические (крио-, электро- или лазеротерапия, радиоволновая хирургия) и химические.
При CIN I тактика может различаться в зависимости от величины поражения шейки матки, наличия другой патологии и возможностей самой пациентки [15]. Также в этом вопросе нет единогласия и ввиду возможности регресса данного заболевания. Общеизвестно, что хирургическое лечение может повлечь за собой до 40% осложнений (шеечное кровотечение, стриктуры цервикального канала, экстравазаты и субэпителиальные гематомы, истмико-цервикальную недостаточность, эндометриоз и др.), поэтому однозначность такого подхода при CIN I у женщин, зачастую еще не реализовавших репродуктивный потенциал, подлежит сомнению [16]. Установили, что прогностическими критериями течения CIN I могут служить анамнестические данные (возраст пациенток, возраст начала половой жизни, интервал между возрастом менархе и возрастом начала половой жизни) и данные клинико-лабораторных методов исследования — уровни вирусной нагрузки ВПЧ 16/18, клинико-кольпоскопического и иммуногистохимического индекса p16ink4a [16].
Одним из главных методов, позволяющих снизить заболеваемость РШМ, являются профилактические осмотры с проведением активного скрининга, направленного на выявление патологии шейки матки.
В ходе профилактического осмотра основными диагностическими методиками являются цитологическое исследование, кольпоскопия и определение ВПЧ.
С введения государственных программ ранней диагностики РШМ накоплен большой опыт по цитологическому скринингу, изложенный во множестве публикаций [17]. Одним из критериев оценки эффективности скрининга является изменение структуры патологии шейки матки за счет увеличения количества ранних предраковых состояний эпителия. Анализ литературы показывает, что при хорошо организованном цитологическом скрининге с широким охватом населения эффективность его очень высока и популяция женщин, прошедших обследование, имеет низкий риск развития РШМ. У них в 5 раз снижена вероятность обнаружения рака и в 10 раз — смертность по сравнению с группой необследованных женщин [18]. При этом вероятность пропуска заболевания на его начальном этапе составляет 1–2%, что связывают с недостаточной чувствительностью цитологических исследований [18]. Неправильный забор материала или недостаточная квалификация врача-цитолога могут приводить к большому количеству ложноотрицательных ответов, требующих дополнительных уточняющих методик. Накопленный опыт в нашей стране показал наилучшие результаты обследований в системах ведомственных лечебных учреждений, где охват прикрепленного контингента женщин достигает 100%, что в результате приводит к отсутствию случаев инвазивного РШМ в течение 2–5 лет [17].
Следующим после цитологического исследования важным диагностическим методом профилактического осмотра женщин является кольпоскопия. Среди задач, поставленных Министерством здравоохранения РФ на ближайшие годы, по внедрению стандартов диагностики и лечения в повседневную клиническую практику кольпоскопическое исследование является обязательным для первичных пациенток женских консультаций с ненормальными цитологическими мазками, женщин с патологией шейки матки и любыми заболеваниями влагалища, вульвы, шейки (код кольпоскопии А03.20.001) [17]. Таким образом, кольпоскопия является одним из ведущих методов обследования женщин, дополняющих цитологическое исследование.
Поскольку основная роль в генезе заболеваний шейки матки принадлежит ВПЧ, то тестирование на этот вирус является также важнейшим инструментом профилактических мероприятий. Особую озабоченность представляют пациентки с длительной персистенцией высокоонкогенных типов ВПЧ в сочетании с ASCUS. Женщинам, инфицированным ВПЧ, особенно типами высокого онкологического риска, требуется более активная диагностическая и терапевтическая тактика, соблюдение курсов терапии, строгий комплаенс.
При активном выявлении заболеваний шейки матки в ходе профилактических осмотров, а также при их ранней диагностике у женщин, самостоятельно обратившихся к гинекологу, чрезвычайно важным является выделение группы пациенток с минимальными субклиническими формами болезни для своевременного лечения и диспансерного наблюдения в женских консультациях [17]. В этой связи важное значение приобретает необходимость длительного контроля и фармакотерапии, направленной на подавление вируса, а также готовность пациентки следовать рекомендованному лечению.
Ранняя диагностика и принципы лечения начальных проявлений CIN остаются одной из дискутабельных проблем в акушерско-гинекологической практике. При небольшом поражении чаще рекомендуют оставить женщину под наблюдением и периодически выполнять обследования — тесты на ВПЧ, кольпоскопию, цитологию. Очень важно при этом диагностировать и лечить воспалительные, дисгормональные и другие заболевания урогенитального тракта. Большую роль в определении тактики ведения больных в этих случаях имеет желание пациентки и ее возможность регулярного посещения врача для проведения обследования и желание следовать рекомендациям врача в выборе медикаментозной терапии. Выжидательная тактика при ПВИ часто связана с тем, что носительство и персистенция свидетельствуют не о предраковом процессе как таковом, а о многократно повышенном риске возникновения последнего, усугубляющегося при дополнительных факторах риска у ряда пациенток [25]. Так, G. Но и соавт. [10] показали, что персистенция ВПЧ более 6 мес встречалась с увеличением возраста женщины и обусловлена типом ВПЧ.
Появление патологических изменений в цитологических мазках возрастает по мере персистенции ВПЧ высокого канцерогенного риска у большинства женщин. Согласно данным литературы после инфицирования ВПЧ CIN II–III развивается уже через 3 года у 27% женщин. При анализе исходов CIN, ассоциированных с ВПЧ, было показано, что при CIN I регрессия наблюдается в 57%, персистенция — в 32%, прогрессия — 11%, а развитие инвазивного рака — только в 1% случаев. При CIN II регрессия наблюдается в 43%, персистенция — в 35%, прогрессия — в 22%, а развитие инвазивного рака — в 5% случаев. В то же время при CIN III малигнизация происходит более чем в 12% случаев, а регрессия — лишь в 32% [26, 27].
В связи с вышесказанным, другим подходом в тактике ведения пациенток с начальными проявлениями CIN может быть назначение противовирусной терапии и контроль со стороны врача за четким выполнением рекомендаций и схем медикаментозной терапии.
Этиопатогенез минимальных изменений эпителия (легкая дисплазия или атипические изменения неясной причины) связан с ВПЧ, который на этой стадии заболевания еще находится в клетке в эписомальном состоянии и не повреждает ее геном. Следовательно, именно на этом этапе развития системный и местный иммунитет будет играть ведущую роль в прогнозе развития болезни. По данным биопсий шейки матки латентные формы инфекции выявляются у 8,1% женщин, а субклинические у 40–60% [25, 28]. Именно поэтому медикаментозная терапия при начальных формах поражения эпителия должна быть направлена на подавление вируса при соблюдении комплаенса, понимании пациенткой необходимости завершения курса для повышения эффективности лечения.
В своем исследовании R. Richard и B. Barron [29] показали, что среднее время для развития карциномы in situ составляет примерно 5 лет для больных со слабой дисплазией, 3 года — с умеренной и 1 год — с выраженной дисплазией. Это позволило предположить, что 66% всех дисплазий будет прогрессировать до карциномы, но достаточно длительное время, которое необходимо использовать для раннего выявления и лечения. В клинической ситуации, несмотря на то, что имеется достаточный период безопасного времени для динамического наблюдения, многие врачи и пациентки после информирования о диагнозе не хотят длительно наблюдаться даже с начальной патологией эпителия. Женщины хотят быть излеченными сразу, что часто предопределяет активную тактику ведения больных, включая деструкцию активной зоны трансформации и иммуно/противовирусную терапию [29–33].
Таким образом, у пациенток с «минимальным» повреждением эпителия шейки матки, например ASCUS, с наличием цитоплазматического эффекта ВПЧ (койлоцитоз при цитологическом исследовании) и положительном ВПЧ-тесте и его высоком титре, может оказаться актуальным применение препарата с двойным противовирусным действием — инозин пранобекс (Изопринозин).
Это один из немногих иммунотропных и противовирусных препаратов, в инструкции по применению которого указана терапия заболеваний, вызванных ВПЧ. Он также входит в Европейскую классификацию методов лечения аногенитальных бородавок [34]. В настоящее время накоплен огромный опыт применения Изопринозина, так как используется он с 1970-х гг. и зарегистрирован в большинстве стран Европы.
Изопринозин — иммуномодулятор, стимулирующий противовирусную защиту организма. Помимо иммунотропного, Изопринозин обладает прямым противовирусным действием, угнетая синтез вирусов путем встраивания инозин-оротовой кислоты в полирибосомы пораженной вирусом клетки и нарушая присоединение адениловой кислоты к вирусной РНК.
Таким образом, обладая противовирусным действием и оказывая влияние на противовирусный иммунитет, Изопринозин прямо и косвенно способен подавлять репликацию ВПЧ и образование вирусных белков. Эти эффекты могут изменять механизм взаимодействия ВПЧ и макроорганизма, препятствуя переходу вируса из транзиторной в персистирующую форму, а также влияя на клиническую манифестацию инфекции.
Одним из показаний применения препарата являются инфекции, вызванные вирусом папилломы человека: остроконечные кондиломы, ПВИ вульвы, вагины и шейки матки (в составе комплексной терапии).
При инфекциях, вызванных ВПЧ, Изопринозин назначают по 3 г/сут (2 таблетки 3 раза в сутки) как дополнение к местной терапии или хирургическому вмешательству в течение 14–28 дней или 5 дней в неделю последовательно в течение 1–2 недель в месяц в течение 3 месяцев. При дисплазии шейки матки, ассоциированной с ВПЧ: по 2 таблетки (1000 мг) 3 раза в сутки в течение 10 дней, далее 2–3 курса с интервалом 10–14 дней.
Улучшение морфологической картины эпителия вульвы показано в исследовании Sun Kuie Tay [32]. Инозин пранобекс назначали по 1 г 3 раза в сутки в течение 6 недель. Положительный эффект был достигнут у 63,5% больных, а в группе, принимавшей плацебо, — у 16,7%.
В другом исследовании при монотерапии Изопринозином по 3 г в сутки у 44 женщин с CIN I (длительность лечения 10 дней) и CIN II (длительность лечения 21 день) установлено, что выраженный клинический эффект наблюдался у 88,6% пациенток — полностью исчезало поражение эпителия экзоцервикса, что подтверждалось кольпоскопически и гистологически [35].
В работе Т. В. Клинышковой и соавт. [36] показана высокая частота регресса CIN I (70%) и прекращения выделения ВПЧ (83,3%) при использовании Изопринозина в режиме монотерапии и комбинированного лечения в сочетании с деструкцией у пациенток с ВПЧ-ассоциированными поражениями шейки матки. Изопринозин назначали по 3 г в сутки двумя 10-дневными курсами — за 1 месяц до деструкции и с 1-го дня деструкции при четком контроле за выполнением курса лечения.
В. Н. Прилепская сообщает о прекращении выделения ВПЧ у 65,6% больных после комбинированной терапии (Изопринозин + деструкция очагов) CIN низкой степени [3]. При использовании только деструкции очагов этот результат был достигнут у 46,9% больных. Изопринозин назначали по 1 г 3 раза в сутки в течение 5 дней за 7–10 дней до проведения деструкции.
Похожие результаты — прекращение выделения ВПЧ у 77% больных — показаны в исследовании И. В. Шевниной (2009 г.) при комбинированной терапии женщин с CIN и аногенитальными бородавками. Изопринозин назначали по 1 г 3 раза в сутки в течение 10 дней, затем по 0,5 грамма 3 раза в сутки в течение 20 дней.
В другом исследовании Изопринозин назначали женщинам с патологией шейки матки, ассоциированной с ВПЧ [37]. Препарат назначали после проведения обследования и противовоспалительной терапии по 3 г в сутки в течение 10 дней. Элиминация ВПЧ достигнута у 95,3% пациенток.
Есть и другие исследования, в которых показано прекращение выделения ВПЧ из очагов поражения у 69,6–97,8% женщин, принимавших Изопринозин [30, 38, 39].
Представленные данные свидетельствуют о возможной эффективности монотерапии Изопринозином при бессимптомном вирусовыделении, когда применение деструктивных методик не показано.
Сравнительная оценка лечения с применением Изопринозина и без него показала преимущество дополнительной лекарственной терапии вне зависимости от степени онкологического риска. Так, в группе женщин с начальными изменениями эпителия самостоятельное улучшение после санации влагалища достигнуто в 64,9% наблюдений, а при применении Изопринозина в 80,4% случаев [17]. У пациенток с изменениями легкой степени тяжести, выявленными при кольпоскопическом или цитологическом исследованиях, даже в случаях отсутствия самостоятельных улучшений более 3 мес Изопринозин был эффективен почти в 85% наблюдений [17].
Результаты исследования, проведенного в ФГБУ НЦАГиП им. акад. В. И. Кулакова [40, 41], показали, что инозин пранобекс подавляет репликацию высокоонкогенных типов ВПЧ и способствует исчезновению койлоцитарной атипии у 94% пациенток с поражением эпителия шейки матки.
При использовании Изопринозина в режиме монотерапии и в комбинации с деструкцией у пациенток с ВПЧ-ассоцированными поражениями низкой степени получена высокая частота регресса CIN I, прекращение выделения ВПЧ, снижение вирусной нагрузки, активация интерферонового ответа в сравнении с традиционными подходами [16]. Через 4 мес у пациенток, принимавших Изопринозин, в 2 раза снизилась частота экспрессии онкобелка Е7 по сравнению с контрольной группой. Кроме этого были отмечены и другие значимые позитивные изменения в отличие от контрольной группы, где имелась лишь тенденция к этому. Выявленные различия позволяют расценивать их как патогенетические предпосылки неполного клинического эффекта и отдаленного рецидивирования заболевания у пациенток контрольной группы. Эффективность лечения в группе пациенток, принимавших Изопринозин, по окончании лечения была в 1,4 раза выше, чем при традиционном лечении.
Заключение
Таким образом, основными профилактическими мероприятиями, направленными на раннее выявление и преодоление прогрессирования ВПЧ-ассоциированной патологии шейки матки, могут быть:
Многочисленные исследования, проведенные во многих странах мира, в том числе и в России, показали, что при применении Изопринозина (в комбинации с деструкцией или в виде монотерапии), благодаря его двойному противовирусному и иммуномодулирующему действию, подавляющему репликацию ВПЧ, повышается эффективность терапии заболеваний шейки матки, ассоциированных с ПВИ.
Для достижения этих результатов важным является соблюдение дозировок и продолжительности лечения. Как было указано выше, наиболее опасной с точки зрения прогрессирования дисплазии является персистенция ВПЧ, при которой вирус встраивается в геном эпителиальной клетки. Противовирусное действие при этом должно продолжаться несколько месяцев, чтобы захватить несколько циклов полного обновления эпителия. Именно поэтому для консервативной терапии дисплазий предлагается длительное многокурсовое лечение — два-три 10-дневных курса с интервалом 10–14 дней. Такие курсы, как показали результаты многочисленных исследований, приведенные в данной работе, позволяют достичь высокой эффективности лечения. Чем ниже уровень выполнения пациентками предписаний врача, тем ниже уровень эффективности лечения и выше риск рецидивирования и прогрессирования патологии.
Литература
А. М. Соловьев*, кандидат медицинских наук
Д. В. Логвинова**
*ГБОУ ВПО МГМСУ им. А. И. Евдокимова МЗ РФ, Москва
**НПЦДК ДЗМ, Москва