Для чего используется инсулин
Инсулинотерапия сахарного диабета на современном этапе
Несмотря на значительные достижения за последние 10–15 лет в области диабетологии, сахарный диабет (СД) вообще и особенно СД 1 типа все еще остается неизлечимым заболеванием, и для сохранения жизни
Несмотря на значительные достижения за последние 10–15 лет в области диабетологии, сахарный диабет (СД) вообще и особенно СД 1 типа все еще остается неизлечимым заболеванием, и для сохранения жизни и трудоспособности больной должен постоянно получать инсулинотерапию, которая является не патогенетической, а заместительной терапией. Поэтому инсулинотерапия остается пожизненной, что естественно создает определенные трудности как для больного, так и для врача, в связи с необходимостью поддержания состояния углеводного обмена близкого к тому, которое имеется у здорового человека.
Несмотря на сложные механизмы патогенеза сосудистых осложнений диабета, которые являются причиной ранней инвалидизации и высокой летальности при сахарном диабете, установлено, что основной их причиной является гипергликемия. Справедливости ради следует отметить, что на развитие сосудистых осложнений диабета непосредственно влияет не собственно высокое содержание глюкозы в крови, а гипергликемия, опосредованно участвующая в сложном многоступенчатом процессе патогенеза сосудистых осложнений диабета. В связи с этим поиск новых препаратов и схем лечения СД направлен на восстановление нарушенного углеводного обмена и возможность его сохранения в течение длительного времени.
Проспективное исследование DCCT (Контроль сахарного диабета и его взаимосвязь с поздними осложнениями, 1993) показало, что как частота сосудистых осложнений диабета, так и время их манифестации четко коррелирует со степенью компенсации СД. Благодаря устойчивой компенсации диабета, т. е. поддержанию нормальной (или близкой к нормальной) концентрации глюкозы в крови в течение длительного времени, удается отсрочить появление поздних осложнений СД.
Понимание значимости гипергликемии в механизмах развития сосудистых осложнений находит отражение и в изменении критериев компенсации углеводного обмена при СД. Эти критерии через определенные промежутки времени изменяются в сторону приближения показателей углеводного обмена у больных СД к значениям гликемии, наблюдаемым у практически здоровых лиц.
Исходя из этого основной задачей лечения сахарного диабета является достижение компенсации. Современные критерии компенсации СД 1 типа, предложенные Европейской группой по политике СД 1 типа в 1998 г., представлены в таблице 1.
Лечение СД носит комплексный характер и включает в себя несколько компонентов: диету; дозированную физическую нагрузку; обучение больного, контроль и самоконтроль состояния углеводного обмена; применение сахароснижающих лекарственных средств; профилактику и лечение поздних осложнений СД.
Несмотря на то, что цель настоящей публикации заключается в ознакомлении практикующего врача с современными тенденциями в проведении инсулиновой терапии, тем не менее необходимо остановиться на основных моментах лечения сахарного диабета, без выполнения которых трудно добиться основной задачи лечения — снижения частоты сосудистых осложнений и стабилизации состояния больного, а также провести профилактику их развития.
Общие требования к диете:
Соотношение основных ингредиентов в суточном рационе больного не отличается от такового для здорового человека, т. е. около 60% от суточной калорийности пищи покрывается за счет углеводов, 24% — за счет жиров и 16% — за счет белков.
Многократный (4–5-кратный) прием пищи в течение суток позволяет более адекватно моделировать взаимоотношения между уровнем инсулина и содержанием глюкозы в крови, приближаясь к тем показателям, которые имеют место у здорового человека.
Физические нагрузки и лечебная физкультура являются обязательным компонентом терапии больных СД. Объем физической нагрузки должен быть определен с учетом возраста больного, состояния сердечно-сосудистой системы и компенсации углеводного обмена. Любая физическая нагрузка сопровождается снижением уровня глюкозы в крови, а интенсивность его снижения определяется двумя факторами: повышением скорости поглощения глюкозы из крови работающей мышцей и ускорением всасывания инсулина из места его введения благодаря усилению кровообращения при повышенной физической активности. Эти два фактора могут способствовать развитию гипогликемической комы, поэтому в день занятия физкультурой инъекцию инсулина необходимо сделать в область живота, а непосредственно перед физической нагрузкой принять дополнительно небольшое количество углеводов. Обычно рекомендуется 20 г углеводов до занятий физкультурой и через каждые 60 мин, если занятия продолжаются.
В случае, если занятия физкультурой требуют больших физических затрат или продолжительны по времени, то углеводы принимают по 40 г каждый час, а доза инсулина в этот период должна быть снижена.
Ежедневные физические нагрузки должны быть неотъемлемой и составной частью комплексной терапии СД. Они положительно влияют на течение диабета и способствуют поддержанию его стойкой компенсации при заметном снижении потребности в инсулине. Регулярные тренировки способствуют нормализации липидного обмена, улучшают микроциркуляцию, активируют фибринолиз, нормализуют повышенную секрецию катехоламинов в ответ на стрессовую ситуацию, что в итоге предотвращает развитие сосудистых осложнений (ангиопатии). У больных СД, регулярно занимающихся физкультурой, отмечены стабилизация, а у ряда пациентов регресс сосудистых осложнений сахарного диабета.
Многолетние исследования показывают, что обучение больного и выполнение им всех рекомендаций, которые он получил в период обучения в школе больного СД, способствуют снижению уровня гликированного гемоглобина в крови на 0,9–1,5%.
В процессе обучения больной должен получить четкое представление об ежедневном режиме и проведении различных манипуляций, необходимых для поддержания стабильного течения СД (выполнение рекомендаций по диете, умение проводить определение содержания глюкозы в крови и моче, рассчитать количество хлебных единиц в продуктах питания, принимаемых в конкретное время дня, и рассчитать при этом необходимую дозу инсулина и т. п.). Кроме этого, ему необходимо научиться поддерживать нормальный образ жизни (отказ от курения, сокращение до минимума приема алкоголя, соблюдение времени сна, отдыха и рабочей активности и т. д.).
Инсулинотерапия назначается всем больным СД 1 типа, которые составляют до 7–10% популяции больных диабетом, а также части больных СД 2 типа (так называемый инсулинопотребный подтип). На долю этой категории приходится 25–35% пациентов с СД 2 типа.
В соответствии с рекомендациями ВОЗ и Международной диабетической федерации и требованиями Фармакологического комитета Минздрава РФ рекомендуется использование для лечения детей, подростков и беременных женщин, страдающих СД, генно-инженерного (рекомбинантного или биосинтетического) инсулина человека, для терапии взрослых больных СД 1 типа — инсулина человека, а также для инсулинопотребных больных диабетом 2 типа — инсулина человека (у этой категории больных допускается использование монокомпонентного свиного инсулина). Следует отметить, что, несомненно, препаратом выбора при лечении больных с инсулинозависимым СД является генно-инженерный (биосинтетический или рекомбинантный) инсулин человека и все лекарственные формы, полученные на его основе. По данным Международной федерации диабета на конец 2004 г., более чем в 65% странах мира для лечения больных сахарным диабетом применяются только генно-инженерные инсулины человека. Ниже приведен рейтинг препаратов инсулина.
М. И. Балаболкин, доктор медицинских наук, профессор
Е. М. Клебанова, кандидат медицинских наук
ММА им. И. М. Сеченова, Москва
ИНСУЛИН ДЛЯ ИНЪЕКЦИЙ РАСТВОРИМЫЙ (INSULIN INJECTION, SOLUBLE) ОПИСАНИЕ
Фармакологическое действие
Инсулин короткого действия. Представляет собой монокомпонентный свиной инсулин. Понижает уровень глюкозы в крови, улучшает ее усвоение тканями, усиливает липогенез и гликогеногенез, синтез белка, снижает скорость продукции глюкозы печенью.
Показания активного вещества ИНСУЛИН ДЛЯ ИНЪЕКЦИЙ РАСТВОРИМЫЙ
Режим дозирования
Побочное действие
Возможно: гипогликемические состояния; гиперемия и зуд в месте инъекции; преходящие нарушения рефракции (обычно в начале терапии).
При длительном применении: липодистрофия в месте инъекции.
Противопоказания к применению
Применение при беременности и кормлении грудью
Применение при нарушениях функции почек
Дозу инсулина необходимо корректировать при выраженных нарушениях функции почек у лиц старше 65 лет.
Применение у детей
Инсулин монокомпонентный свиной не следует применять у детей раннего возраста.
Применение у пожилых пациентов
Дозу инсулина необходимо корректировать при выраженных нарушениях функции почек у лиц старше 65 лет.
Особые указания
Дозу инсулина необходимо корректировать в следующих случаях: при изменениях характера и режима питания, высокой физической нагрузке, инфекционных заболеваниях, хирургических вмешательствах, при нарушении функции щитовидной железы, болезни Аддисона, гипопитуитаризме, при выраженных нарушениях функции почек и сахарном диабете у лиц старше 65 лет.
При передозировке инсулина необходимо назначить глюкозу внутрь, если больной в сознании; при потере сознания необходимо п/к, в/м или в/в ввести глюкагон или в/в глюкозу.
При первичном применении инсулина, смене его вида или при значительных физических или психических стрессах возможно снижение скорости психомоторных реакций и способности к концентрации внимания.
Инсулин монокомпонентный свиной не следует применять у детей раннего возраста.
Лекарственное взаимодействие
Под влиянием резерпина и салицилатов возможно как ослабление, так и усиление действия инсулина.
При применении препаратов инсулина в комбинации с препаратами группы тиазолидиндиона у пациентов с сахарным диабетом 2 типа может возникать задержка жидкости в организме, в результате чего повышается риск развития и прогрессирования хронической сердечной недостаточности, особенно у пациентов с заболеваниями сердечно-сосудистой системы и наличием факторов риска хронической сердечной недостаточности. Пациентов, получающих такую терапию, следует регулярно обследовать с целью выявления признаков сердечной недостаточности. При возникновении сердечной недостаточности терапию следует осуществлять в соответствии с текущими стандартами лечения.
Техника инъекций и средства введения инсулина
Начало практического применения инсулина почти 85 лет тому назад остается одним из немногих событий, значение которых не оспаривается и современной медициной. С тех пор многие миллионы нуждающихся в инсулине больных
Начало практического применения инсулина почти 85 лет тому назад остается одним из немногих событий, значение которых не оспаривается и современной медициной. С тех пор многие миллионы нуждающихся в инсулине больных во всем мире были спасены от смерти в результате диабетической комы. Пожизненное заместительное лечение инсулином стало основным условием выживания больных диабетом 1 типа, оно также играет большую роль в терапии определенной части больных диабетом 2 типа. В первые годы существовало достаточно много проблем, связанных с получением препарата, техникой его введения, изменением доз, но постепенно все эти вопросы были решены. Сейчас каждому больному диабетом с потребностью в инсулине вместо фразы «Мы вынуждены колоть инсулин», следовало бы говорить: «Мы имеем возможность колоть инсулин». В последние годы интерес к возможностям совершенствования инсулинотерапии, т. е. приближения к физиологическим условиям, постоянно растет. Определенную роль здесь играют не только установка на уменьшение ограничений в образе жизни и улучшение качества жизни, но и признание необходимости коренных преобразований, направленных на улучшение метаболического контроля. Дж. Дж. Р. Маклеод (ассистенты которого — Фредерик Бантинг и Чарльз Бест — в 1921 г. открыли инсулин) писал в своей книге «Инсулин и его применение в лечении диабета»: «Чтобы больной мог доверить самому себе свою собственную жизнь, ему нужно отлично овладеть определением дозы и введением инсулина. » Эта фраза актуальна и по сей день, поскольку замены подкожному введению инсулина в обозримом будущем не предвидится.
В связи с этим очень важно правильно использовать инсулин и современные средства его введения, к которым относятся шприцы, шприц-ручки, носимые инсулиновые помпы.
Хранение инсулина
Как у любого лекарственного препарата, длительность хранения инсулина ограничена. На каждом флаконе обязательно указывается срок годности препарата. Запас инсулина необходимо хранить в холодильнике при температуре + 2. +8 °С (ни в коем случае не замораживать). Флаконы с инсулином или шприц-ручки, которые используются для ежедневных инъекций, могут храниться при комнатной температуре в течение 1 мес. Также нельзя допускать перегревания инсулина (например, запрещено оставлять его на солнце или летом в закрытой машине). После инъекции обязательно следует убирать флакон инсулина в бумажную упаковку, поскольку активность инсулина снижается под воздействием света (шприц-ручка закрывается колпачком). Не рекомендуется при перевозке запаса инсулина (во время отпуска, командировки и т. д.) сдавать его в багаж, так как он может потеряться, разбиться, замерзнуть или перегреться.
Инсулиновые шприцы
Стеклянные шприцы неудобны (требуют стерилизации) и не могут обеспечить достаточно точную дозировку инсулина, поэтому сегодня они практически не применяются. При использовании пластиковых шприцев рекомендуются шприцы со встроенной иглой, позволяющей устранить так называемое «мертвое пространство», в котором в обычном шприце со съемной иглой после инъекции остается некоторое количество раствора. Таким образом, при каждом введении теряется определенное количество препарата, что, учитывая масштабы заболеваемости диабетом, оборачивается огромными экономическими потерями. Пластиковые шприцы вполне можно использовать неоднократно, при условии, что с ними обращаются правильно, соблюдая правила гигиены. Желательно, чтобы цена деления инсулинового шприца была не более 1 ЕД, а для детей — 0,5 ЕД.
Концентрация инсулина
Пластиковые шприцы выпускаются для инсулина с концентрацией 40 ЕД/мл и 100 ЕД/мл, поэтому при получении или покупке новой партии шприцев следует обращать внимание на их шкалу. Больных, отправляющихся в поездку за рубеж, также стоит предупредить о том, что в большинстве стран используется только инсулин с концентрацией 100 ЕД/мл и соответствующие шприцы. В России в настоящее время встречается инсулин в обеих концентрациях, хотя ведущие мировые производители инсулина поставляют его в концентрации 100 ЕД в 1 мл.
Набор инсулина в шприц
Последовательность действий при наборе инсулина с помощью шприца следующая:
Смешивание инсулинов в одном шприце
Возможность смешивания инсулинов короткого и продленного действия в одном шприце зависит от вида пролонгированного инсулина. Смешивать можно только те инсулины, в которых использован белок (НПХ-инсулины). Нельзя смешивать появившиеся в последние годы аналоги человеческого инсулина. Целесообразность смешивания инсулинов объясняется возможностью уменьшения числа инъекций. Последовательность действий при наборе в один шприц двух инсулинов следующая:
Техника инъекций инсулина
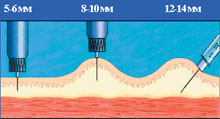 |
| Рисунок 1. Введение инсулина иглами различной длины |
Скорость всасывания инсулина зависит от того, куда вводится игла. Инъекции инсулина должны всегда осуществляться в подкожный жир, но не внутрикожно и не внутримышечно (рис. 1). Оказалось, что толщина подкожной клетчатки у лиц с нормальным весом, особенно у детей, часто меньше длины стандартной инсулиновой иглы (12–13 мм). Как показывает опыт, очень часто больные не формируют складку и делают инъекцию под прямым углом, что приводит к попаданию инсулина в мышцу. Это подтвердили специальные исследования с использованием ультразвуковой аппаратуры и компьютерной томографии. Периодическое попадание инсулина в мышечный слой может приводить к непредсказуемым колебаниям уровня гликемии. Для того чтобы избежать вероятности проведения внутримышечной инъекции, следует использовать короткие инсулиновые иглы — длиной 8 мм (Бектон Дикинсон Микрофайн, Новофайн, Дизетроник). Кроме того, эти иглы являются и самыми тонкими. Если диаметр стандартных игл составляет 0,4; 0,36 или 0,33 мм, то диаметр укороченной иглы — всего лишь 0,3 или 0,25 мм. Это особенно актуально для детей, поскольку такая игла практически не вызывает болезненных ощущений. В последнее время предлагаются и более короткие (5–6 мм) иглы, которые чаще применяют у детей, но дальнейшее уменьшение длины увеличивает вероятность внутрикожного попадания.
Для того чтобы сделать инъекцию инсулина, необходимо следующее:
Области инъекций инсулина
Для инъекций инсулина используются несколько областей: передняя поверхность живота, передняя поверхность бедер, наружная поверхность плеч, ягодицы (рис. 3). Делать инъекцию самому себе в плечо не рекомендуется, так как при этом невозможно сформировать складку, а значит, увеличивается риск внутримышечного введения инсулина. Следует знать, что инсулин из различных областей тела всасывается с разной скоростью (например, быстрее всего из области живота). Поэтому перед приемом пищи рекомендуется вводить инсулин короткого действия в эту область. Инъекции пролонгированных препаратов инсулина можно делать в бедра или ягодицы. Место инъекции должно быть каждый день новым, в противном случае возможны колебания уровня сахара крови.
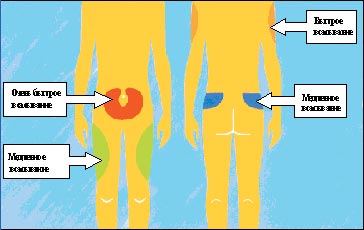 |
| Рисунок 3. Области инъекций инсулина |
Следует следить также за тем, чтобы в местах инъекций не появлялись изменения — липодистрофии, которые ухудшают всасывание инсулина (см. ниже). Для этого необходимо чередовать места инъекций, а также отступать от места предыдущей инъекции не менее чем на 2 см.
Шприц-ручки
В последние годы, наряду с пластиковыми инсулиновыми шприцами, все большее распространение получают полуавтоматические дозаторы инсулина, так называемые шприц-ручки. Их устройство напоминает чернильную авторучку, в которой вместо резервуара с чернилами находится картридж с инсулином, а вместо пера — одноразовая инсулиновая игла. Подобные «ручки» выпускаются сейчас практически всеми зарубежными производителями инсулинов (Ново Нордиск, Эли Лилли, Авентис), а также производителями медицинского оборудования (Бектон Дикинсон). Исходно они были разработаны для больных с нарушением зрения, которые не могли самостоятельно набрать инсулин в шприц. В дальнейшем их стали использовать все больные сахарным диабетом, так как они позволяют повысить качество жизни больного: отпадает необходимость носить с собой флакон с инсулином и набирать его шприцем. Особенно это значимо при современных режимах интенсифицированной инсулинотерапии, когда в течение дня больному приходится делать инъекции многократно (рис. 4).
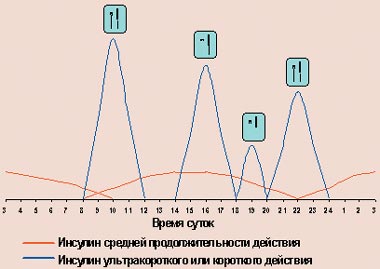 |
| Рисунок 4. Режим интенсифицированной инсулинотерапии с помощью многократных инъекций |
Однако освоить технику инъекций с помощью шприц-ручки несколько сложнее, поэтому больные должны тщательно изучить инструкцию по использованию и строго придерживаться всех указаний. Один из недостатков шприц-ручек также состоит в том, что, когда в картридже остается небольшое количество инсулина (меньше нужной больному дозы), многие пациенты просто выбрасывают такой картридж и вместе с ним инсулин. Кроме того, если больной вводит инсулины короткого и продленного действия в индивидуально подобранном соотношении (например, при интенсифицированной инсулинотерапии), то он лишен возможности смешать и ввести их вместе (как в шприце): приходится вводить их раздельно двумя «ручками», таким образом увеличивается число инъекций. Как и в случае с инсулиновыми шприцами, важное требование к инъекторам — возможность дозировать кратно 1 ЕД, а для маленьких детей — кратно 0,5 ЕД. Перед инъекцией пролонгированного инсулина нужно произвести 10–12 поворотов ручки на 180° для того, чтобы шарик, находящийся в картридже, равномерно перемешал инсулин. Наборным кольцом ставится необходимая доза в окошке корпуса. Введя иглу под кожу так, как было описано выше, следует нажать на кнопку до упора. Через 7–10 с (!) вынуть иглу.
Самой первой шприц-ручкой была Новопен, созданная в 1985 г. Необходимая доза с ее помощью вводилась дискретно, так как с каждым нажатием кнопки можно было ввести только 1 или 2 ЕД.
Следующие поколения шприц-ручек позволяли вводить всю дозу сразу, предварительно определив ее. В настоящее время в России используются шприц-ручки, в которые вставляется картридж объемом 3 мл (300 ЕД инсулина). К ним относятся Новопен 3, Хумапен, Оптипен, Инново.
Новопен 3 предназначена для введения инсулинов компании Ново Нордиск. Шприц-ручка имеет корпус, изготовленный из пластика и металла. Она позволяет одномоментно ввести до 70 Ед инсулина, при этом шаг введения — 1 ЕД. Кроме классического варианта серебристой окраски выпускаются разноцветные шприц-ручки (чтобы не путать разные инсулины). Для детей имеется модификация Новопен 3 Деми, которая позволяет вводить инсулин с кратностью дозы 0,5 ЕД.
Шприц-ручка Хумапен предназначена для введения инсулинов компании Эли Лилли. Ручка очень проста в использовании, можно легко перезарядить картридж (за счет специального механизма), а также скорректировать неправильно набранную дозу. Корпус устройства полностью пластиковый, что облегчает его вес, а специально разработанный эргономичный дизайн корпуса делает его удобным для руки во время инъекции. Цветовые вставки на корпусе предназначены для использования различных инсулинов. Хумапен позволяет одномоментно ввести до 60 ЕД инсулина, шаг вводимой дозы — 1 ЕД.
Шприц-ручка Оптипен предназначена для введения инсулинов компании Авентис. Основное ее отличие от других моделей — наличие жидкокристаллического дисплея, на котором отображается доза для введения. Чаще всего на российском рынке встречается вариант Оптипен Про 1. Он позволяет одномоментно ввести до 60 ЕД инсулина, цифра «1» означает, что шаг вводимой дозы — 1 ЕД. Еще одним преимуществом данной модели является тот факт, что невозможно установить дозу больше, чем остается инсулина в картридже.
В 1999 г. компания Ново Нордиск выпустила новую шприц-ручку Инново. За счет специального механизма была уменьшена длина устройства. Как и у Оптипена, доза отображается на жидкокристаллическом дисплее. Но главное отличие от всех предыдущих модификаций в том, что Инново показывает время, прошедшее с момента последней инъекции, и запоминает последнюю дозу инсулина. Также электронная система контроля гарантирует точное введение набранной дозы. Диапазон вводимых доз — от 1 до 70 ЕД, шаг дозирования — 1 ЕД. Установленная доза может быть увеличена или уменьшена простым поворотом дозатора вперед или назад без потери инсулина. Невозможно установить больше дозу, чем остается инсулина в картридже.
Смена игл
Поскольку больному, находящемуся на инсулинотерапии, за свою жизнь приходится делать огромное количество инъекций, большое значение приобретает качество инсулиновых игл. Для того чтобы обеспечить как можно более комфортное введение инсулина, производители постоянно делают иглы тоньше, короче, острее. Чтобы сделать введение инсулина практически безболезненным, острие иглы подвергается специальной заточке и смазке с использованием новейших технологий. Тем не менее повторное и многократное использование инсулиновой иглы ведет к повреждению ее острия и стиранию смазочного покрытия, что увеличивает болезненные ощущения и дискомфорт. Затупление иглы не только делает введение инсулина болезненным, но может стать причиной местного кровоизлияния. К тому же стирание смазки на игле способствует увеличению силы проталкивания иглы через кожу, в связи с чем возрастает опасность искривления иглы и даже ее поломки. Однако основной аргумент против многократного использования иглы — это микротравматизация ткани. Дело в том, что при повторном использовании иглы ее острие изгибается, приобретая форму крючка, что хорошо видно под микроскопом (рис. 5). При удалении иглы после введения инсулина этот крючок разрывает ткань, вызывая микротравму. Это способствует образованию у ряда больных выступающих уплотнений (плюс-ткань) в местах инъекций инсулина, т. е. липодистрофий. Помимо того, что липодистрофические уплотнения вызывают косметический дефект, они могут иметь серьезные медицинские последствия. Часто больные продолжают вводить инсулин в эти уплотнения в силу того, что уколы в этих местах менее болезненны. Однако всасывание инсулина в этих местах происходит неравномерно, в результате чего может ослабевать контроль гликемии. Довольно часто в таких ситуациях ставится ошибочный диагноз «лабильное течение диабета».
 |
| Рисунок 5. Деформация инсулиновых игл после многократного использования |
Повторное использование иглы может приводить к тому, что кристаллы инсулина забивают канал, что, в свою очередь, затрудняет подачу инсулина и делает ее неадекватной.
Многократное использование игл для инсулиновых шприц-ручек может повлечь за собой еще одну серьезную ошибку. В инструкции к шприц-ручкам написано, что после каждой инъекции необходимо снимать иглу. Но большинство больных не соблюдают этого правила (в связи с тем, что бесплатно выдается недостаточное количество игл). Таким образом, остается открытым канал между инсулиновым картриджем и окружающей средой. В результате температурных колебаний происходит утечка инсулина и попадание воздуха во флакон. Наличие пузырьков воздуха в инсулиновом картридже приводит к более медленному введению инсулина по мере проталкивания поршня. В результате введенная доза инсулина может оказаться неточной. При наличии больших пузырьков воздуха количество введенного инсулина в некоторых случаях может составлять только 50–70% от набранной дозы. Для того чтобы снизить влияние этого фактора, необходимо вынимать иглу не сразу, а через 7–10 с после того, как поршень достиг своего нижнего положения, о чем и следует проинструктировать больных.
Какие же выводы можно сделать, исходя из всех вышеперечисленных наблюдений? В идеале следует рекомендовать одноразовое использование инсулиновых игл; кроме того, после каждого введения инсулина нужно немедленно снимать иглу.
Учитывая важность вышеперечисленных моментов, врачам следует периодически проверять средства введения инсулина, технику инъекций и состояние мест инъекций у каждого больного.
Инсулиновые помпы
Носимые дозаторы инсулина (инсулиновые помпы) появились в конце 1970-х гг. Следующее десятилетие характеризовалось бурным интересом к этим новым техническим средствам введения инсулина, на них возлагались определенные надежды. После накопления опыта и проведения достаточного числа научно-клинических исследований помповый «бум» спал, и эти приборы заняли свое вполне определенное место в современной инсулинотерапии. В России в настоящее время используются помпы компании Медтроник Минимед.
При использовании дозаторов происходит следующее (рис. 6): для имитации физиологической секреции через установленную в теле канюлю (место инъекции меняется каждые 2–3 дня) инсулин короткого действия подается помпой непрерывно в виде подкожной инфузии (базальная скорость), а перед едой больной вводит различные дополнительные количества инсулина (болюсное введение).
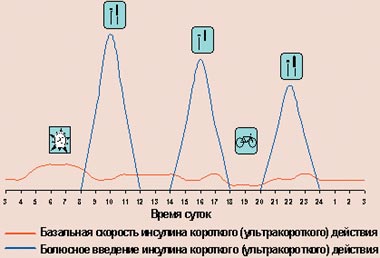 |
| Рисунок 6. Режим интенсифицированной инсулинотерапии с помощью помпы |
Таким образом, прибор представляет собой систему «открытого» типа. Это значит, что дозировку инсулина больной регулирует сам, изменяя ее в зависимости от результатов самоконтроля гликемии. Последнее и является тем звеном, которое как бы «замыкает цепочку», формируя обратную связь. Одно из главных преимуществ имеющихся носимых помп — возможность варьирования базальной скорости инфузии инсулина. Современные помпы позволяют устанавливать разную скорость для каждого часа суток, что помогает справиться с таким явлением, как «феномен утренней зари» (повышение уровня гликемии в ранние утренние часы, заставляющее больных в этом случае производить первую инъекцию инсулина в 5–6 ч утра). Также использование помп позволяет уменьшить количество инъекций, проявить большую гибкость в отношении времени приема пищи и количества потребляемых углеводов. Существуют и имплантируемые помпы, в которых инсулин попадает внутрибрюшинно, а значит, поступает в воротную вену, как это происходит при нормальной секреции инсулина.
Тем не менее многочисленные исследования показали, что значительной разницы в уровне метаболического контроля у больных, использующих дозаторы инсулина, и у тех, кто находится на режиме многократных инъекций, нет. Самым большим недостатком является высокая стоимость помп. Применение помп однозначно оправдано в определенных ситуациях, например во время беременности, у детей с лабильным течением диабета и т. д. Миниатюрного, портативного прибора, который бы не только вводил инсулин, но и имел датчик для определения гликемии, а также функцию автоматизированной подачи инсулина на основе полученных результатов, т. е. представлял бы собой искусственную b-клетку, для длительного клинического применения пока не разработано. Тем не менее экспериментальные модели уже существуют, и серийное производство таких приборов может начаться в ближайшем будущем. В связи с этим возрос интерес к применению обычных помп, так как и медицинским работникам, и больным необходимо привыкать к обращению со сложными техническими устройствами.
Таким образом, на сегодняшний день в нашем арсенале имеются средства самоконтроля и введения инсулина, которые во многом позволяют оптимизировать лечение больных сахарным диабетом. Остается лишь научить больных правильно их использовать, что представляет собой не менее трудную задачу, чем само создание этих средств.
Литература
А. Ю. Майоров, кандидат медицинских наук
ЭНЦ РАМН, Москва