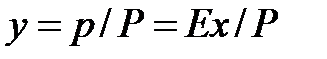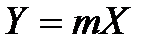Для чего используют процессы абсорбции
Определение явления абсорбции и его применение
Обзор особенностей физической и химической абсорбции. Анализ материальных потоков в абсорбере и хода рабочей и равновесной линий. Изучение областей применения абсорбционных процессов в химической и смежных отраслях промышленности. Регенерация абсорбентов.
| Рубрика | Химия |
| Вид | реферат |
| Язык | русский |
| Дата добавления | 20.11.2013 |
| Размер файла | 550,9 K |
Отправить свою хорошую работу в базу знаний просто. Используйте форму, расположенную ниже
Студенты, аспиранты, молодые ученые, использующие базу знаний в своей учебе и работе, будут вам очень благодарны.
Размещено на http://www.allbest.ru/
Ташкентская Медицинская Академия
на тему: «Определение явления абсорбции и его применение»
Выполнила: Пак Наталья
Промышленное проведение абсорбции может сочетаться или не сочетаться с десорбцией. Если десорбцию не производят, поглотитель используется однократно. При этом в результате абсорбции получают готовый продукт, полупродукт или, если абсорбция проводится с целью санитарной очистки газов, отбросный раствор, сливаемый (после обезвреживания) в канализацию.
В некоторых случаях (при наличии малоценного поглотителя) в процессе проведения десорбции отказываются от многократного применения поглотителя. Пои этом регенерированный в десорбере поглотитель сбрасывают в канализацию, а в абсорбер подают свежий поглотитель. Поглотители, абсорбция в которых сопровождается необратимой химической реакцией, не поддаются регенерации путем десорбции. Регенерацию таких поглотителей можно производить химическим методом. При абсорбционных процессах массообмен происходит на поверхности соприкосновения фаз. Поэтому абсорбционные аппараты должны иметь развитую поверхность соприкосновения между газом и жидкостью. Исходя из этого, абсорбционные аппараты можно подразделить на следующие группы:
а) Поверхностные абсорберы, в которых поверхностью контакта между фазами является зеркало жидкости (собственно поверхностные абсорберы) или поверхность текущей пленки жидкости (пленочные абсорберы). К этой же группе относятся насадочные абсорберы, в которых жидкость стекает по поверхности загруженной в абсорбер насадки из тел различной формы (кольца., кусковой материал и т. д.), и механические пленочные абсорберы. Для поверхностных абсорберов поверхность контакта в известной степени определяется геометрической поверхностью элементов абсорбера (например, насадки), хотя во многих случаях и не равна ей.
б) Барботажные абсорберы. в которых поверхность контакта развивается потоками газа. распределяющегося в жидкости в виде пузырьков и струек. Тaкое движение газа (барботаж) осуществляется путем пропускания его через заполненный жидкостью аппарат (сплошной барботаж) либо в аппаратах колонного типа с колпачковыми, ситчатыми или провальными тарелками. Подобный характер взаимодействия газа и жидкости наблюдается также в насадочных абсорберах с затопленной насадкой. В эту же группу входят барботажные абсорберы с перемешиванием жидкости механическими мешалками. В барботажных абсорберах поверхность контакта определяется гидродинамическим режимом (расходами газа и жидкости).
в) Распыливающие абсорберы, в которых поверхность контакта образуется путем распыления жидкости в массе газа на мелкие капли. Поверхность контакта определяется гидродинамическим режимом (расходом жидкости). К этой группе относятся абсорберы, в которых распыление жидкости производится форсунками (форсуночные, или полые, абсорберы), в токе движущегося с большой скоростью газа (скоростные прямоточные распыливающие абсорберы) или вращающимися механическими устройствами (механические распыливающие абсорберы).
Приведенная классификация абсорбционных аппаратов является условной, так как отражает не столько конструкцию аппарата, сколько характер поверхности контакта. Один и тот же тип аппарата в зависимости от условий работы может оказаться при этом в разных группах. Например, насадочные абсорберы могут работать как в пленочном, так и в барботажном режимах В аппаратах с барботажными тарелками возможны режимы, когда происходит значительное распыление жидкости и поверхность контакта образуется в основном каплями.
Области применения абсорбционных процессов в химической и смежных отраслях промышленности весьма обширны. Некоторые из этих областей указаны ниже:
1. Получение готового продукта путем поглощения газа жидкостью. Примерами могут служить: абсорбция SO3 в производстве серной кислоты; абсорбция НCl с получением соляной кислоты; абсорбция окислов азота водой (производство азотной кислоты) или щелочными растворами (получение нитратов) и т.д. При этом абсорбция проводится без последующей десорбции.
2. Разделение газовых смесей для выделения одного или нескольких ценных компонентов смеси. В этом случае применяемый поглотитель должен обладать возможно большей поглотительной способностью по отношению к извлекаемому компоненту и возможно меньшей по отношению к другим составным частям газовой смеси (избирательная, или селективная, абсорбция). При этом абсорбцию обычно сочетают с десорбцией в круговом процессе. В качестве примеров можно привести абсорбцию бензола из коксового газа, абсорбцию ацетилена из газов крекинга или пиролиза природного газа, абсорбцию бутадиена из контактного газа после разложения этилового спирта и т. п.
3. Очистка газа от примесей вредных компонентов. Такая очистка осуществляется прежде всего с целью удаления примесей, не допустимых при дальнейшей переработке газов (например, очистка нефтяных и коксовых газов от H2S очистка азотоводородной смеси для синтеза аммиака от СО2 и СО, осушка сернистого газа в производстве контактной серной кислоты и т. д.). Кроме того, производят санитарную очистку выпускаемых в атмосферу отходящих газов (например, очистка топочных газов от SO2; очистка от Сl2 абгаза после конденсации жидкого хлора; очистка от фтористых соединений газов, выделяющихся при производстве минеральных удобрений, и т.п.). В рассматриваемом случае извлекаемый компонент обычно используют, поэтому его выделяют путем десорбции или направляют раствор на соответствующую переработку. Иногда, если количество извлекаемого компонента очень мало и поглотитель не представляет ценности, раствор после абсорбции сбрасывают в канализацию.
4. Улавливание ценных компонентов из газовой смеси для предотвращения их потерь, а также по санитарным соображениям, например рекуперация летучих растворителей (спирты, кетоны, эфиры и др.).
Следует отметить, что для разделения газовых смесей, очистки газов и улавливания ценных компонентов наряду с абсорбцией применяют и иные способы: адсорбцию, глубокое охлаждение и др. Выбор того или иного способа определяется технико-экономическими соображениями. Обычно абсорбция предпочтительнее в тех случаях, когда не требуется очень полного извлечения компонента.
Характеризует термодинамическое равновесие раствора с паро-газовой смесью, а также материальный и энергетический балансы процесса. При физической абсорбции с образованием идеального раствора для растворителя и растворенного газа во всем интервале изменения состава в соответствии с законом Рауля растворимость газа:
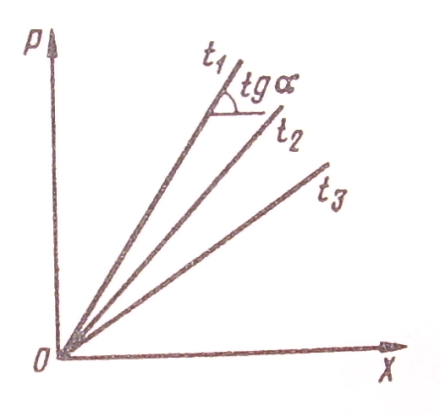
Зависимость растворимости газов х*2 от их парциального давления при физ. абсорбции в бесконечно разбавленном растворе (х2 >0) и при низких давлениях Р в системе описывается законом Генри (рис. 1, прямые 1-3):
Абсорбция
Абсо́рбция (лат. absorptio от absorbere — поглощать) — поглощение сорбата всем объёмом сорбента. Является частным случаем сорбции.
В технике и химической технологии чаще всего встречается абсорбция (поглощение, растворение) газов жидкостями. Но известны и процессы абсорбции газов и жидкостей кристаллическими и аморфными телами (например, абсорбция водорода металлами, абсорбция низкомолекулярных жидкостей и газов цеолитами, абсорбция нефтепродуктов резинотехническими изделиями и т.п.).
Часто в процессе абсорбции происходит не только увеличение массы абсорбирующего материала, но и существенное увеличение его объема (набухание), а также изменение его физических характеристик – вплоть до агрегатного состояния.
На практике абсорбция чаще всего применяется для разделения смесей, состоящих из веществ, имеющих различную способность к поглощению подходящими абсорбентами. При этом целевыми продуктами могут быть как абсорбировавшиеся, так и не абсорбировавшиеся компоненты смесей.
Обычно в случае физической абсорбции абсорбировавшиеся вещества могут быть вновь извлечены из абсорбента посредством его нагревания, разбавления неабсорбирущей жидкостью или иными подходящими способами. Регенерация химически абсорбированных веществ также иногда возможна. Она может быть основана на химическом или термическом разложении продуктов химической абсорбции с высвобождением всех или некоторых из абсорбированных веществ. Но во многих случаях регенерация химически абсорбированных веществ и химических абсорбентов бывает невозможной или технологически/экономически нецелесообразной.
Следует отличать абсорбцию (поглощение в объёме) от адсорбции (поглощения в поверхностном слое). Из-за схожести написания и произношения, а также близости обозначаемых понятий эти термины часто путают.
Содержание
Виды абсорбции
Различают физическую абсорбцию и хемосорбцию.
При физической абсорбции процесс поглощения не сопровождается химической реакцией.
При хемосорбции абсорбируемый компонент вступает в химическую реакцию с веществом абсорбента.
Абсорбция газов
Всякое плотное тело сгущает довольно значительно прилегающие непосредственно к его поверхности частицы окружающего его газообразного вещества. Если такое тело пористо, как, например, древесный уголь или губчатая платина, то это уплотнение газов имеет место и по всей внутренней поверхности его пор, а тем самым, следовательно, и в гораздо более высокой степени. Вот наглядный пример этого: если взять кусок свежепрокалённого древесного угля, бросить его в бутылку, содержащую углекислый или другой газ, и закрыв её сейчас же пальцем, опустить отверстием вниз в ртутную ванну, то мы вскоре увидим, что ртуть поднимается и входит в бутылку; это прямо доказывает, что уголь поглотил углекислоту или иначе наступило уплотнение, абсорбция газа.
При всяком уплотнении выделяется тепло; поэтому, если уголь растереть в порошок, что, например, практикуется при фабрикации пороха, и оставить лежать в куче, то от происходящего здесь поглощения воздуха масса так нагревается, что может произойти самовоспламенение. На этом именно согревании, зависящем от абсорбции, основано устройство платиновой горелки Дёберейнера. Находящийся там кусок губчатой платины уплотняет так сильно кислород воздуха и направленную на него струю водорода, что сам постепенно начинает накаливаться и наконец воспламеняет водород. Вещества, которые абсорбируют — поглощают из воздуха водяной пар, сгущают его тоже в себе, образуя воду, и от этого становятся влажными, как, например, нечистая поваренная соль, поташ, хлористый кальций и т. п. Такие тела зовутся гигроскопическими.
Абсорбция газов пористыми телами была впервые замечена и изучена почти одновременно Фонтаном и Шееле в 1777 г., а затем подвергалось исследованию многими физиками, а особенно Соссюра в 1813 г. Последний, как на самых жадных поглотителей, указывает на буковый уголь и пемзу (морская пенка). Один объём такого угля при атмосферном давлении в 724 мил. поглотил 90 объёмов аммиака, 85 — хлористого водорода, 25 — углекислоты, 9,42 — кислорода; пемза при таком же сравнении оказала немного менее поглотительной способности, но во всяком случае это тоже один из лучших абсорбентов.
Чем легче газ сгущается в жидкость, тем сильнее он поглощается. При малом наружном давлении и при нагревании — уменьшается количество поглощаемого газа. Чем мельче поры поглотителя, т. е. чем он плотнее, тем большею, в общем, он обладает поглотительной способностью; слишком однако же мелкие поры, как например графита, не благоприятствуют абсорбции. Органически уголь поглощает не только газы, но и мелкие твёрдые и жидкие тела, а потому и употребляется для обесцвечивания сахара, очистки алкоголя и т. д. Вследствие абсорбции всякое плотное тело окружено слоем уплотнённых паров и газов. Эта причина, по Вайделю, может служить для объяснения открытого Мозером в 1842 г. любопытного явления так называемых потовых картин, то есть получаемых при дыхании на стекло. А именно, если приложить клише или какой-нибудь рельефный рисунок к полированной стеклянной плоскости, затем, отняв её, подышать на это место, то на стекле получается довольно точный снимок рисунка. Это происходит от того, что при лежании на стекле клише газы близ поверхности стекла распределились неравномерно, в зависимости от нанесённого на клише рельефного рисунка, а потому и водяные пары, при дыхании на это место, распределяются тоже в таком порядке, а охладившись и осев, и воспроизводят данный рисунок. Но если нагреть предварительно стекло или клише, и рассеять таким образом уплотнённый близ них слой газов, то уже таких потовых рисунков получить нельзя.
По закону Дальтона из смеси газов каждый газ растворяется в жидкости пропорционально своему парциальному давлению, вне зависимости от присутствия остальных газов. Степень растворения газов в жидкости определяется коэффициентом, показывающим, сколько объёмов газа поглощается в одном объёме жидкости при температуре газа 0° и давлении в 760 мм. Коэффициенты абсорбции для газов и воды вычисляются по формуле α = А + Вt + Ct², где α — искомый коэффициент, t — температура газа, А, В и С — постоянные коэффициенты, определяемые для каждого отдельного газа. По исследованиям Бунзена коэффициенты важнейших газов имеют такие
| Газы | А | В | С | Действительны при t° |
|---|---|---|---|---|
| Сl | +3,0361 | -0,046196 | +0,0001107 | от 0° до 40° |
| СО | +1,7967 | -0,07761 | +0,0016424 | от 0° до 20° |
| О | +0,4115 | -0,00108986 | +0,000022563 | от 0° до 20° |
| H2S | +4,3706 | -0,083687 | +0,0005213 | от 0° до 40° |
| N | +0,020346 | 0,0000538873 | +0,000011156 | от 0° до 20° |
| H | +0,0193 | — | — | от 0° до 20° |
Кроме твёрдых тел поглощать могут и жидкости, особенно если их смешать вместе в каком-нибудь сосуде. 1 объём воды может при 15 °C и 744 мил. давления растворить в себе, абсорбировать 1/50 объёма атмосферного воздуха, 1 объём углекислоты, 43 объёма сернистого газа и 727 объёмов аммиака. Объём газа, который при 0 °C и 760 мил. барометрического давления поглощается единицею объёма жидкости, называется коэффициентом поглощения газа для этой жидкости. Коэффициент этот для различных газов и различных жидкостей — различен. Чем выше наружное давление и ниже температура, тем больше растворяется в жидкости газа, тем больше коэффициент поглощения. Твёрдые и жидкие тела абсорбируют в данное время различные количества газов, а потому и можно вычислить количества поглощаемого газа для каждой отдельной жидкости. Изучение абсорбции газов жидкостями начато было Анри (1803) и затем двинуто дальше Соссюром (1813) и В. Бунзеном («Gasometrische Methoden», Брауншвейг, 1857, 2 изд., 1877). — Причина абсорбции состоит во взаимном притяжении молекул тел абсорбирующего и абсорбируемого.
См. также
Ссылки
Абсорбция на примере абсорбционной колонны на сайте «Горной энциклопедии».
Сущность процессов абсорбции



Процесс выделения из абсорбента поглощенных компонентов газовой смеси называется десорбцией.
Газовые смеси могут быть разделены также ректификацией, однако это требует произвести их ожижение, что обычно связано с большими затратами энергии на охлаждение и сжижение или адсорбцией, т.е. путем контактирования газа с твердым поглотителем адсорбентом.
В нефте- и газоперерабатывающей промышленности процесс абсорбции применяют для разделения, осушки и очистки углеводородных газов. Из природных и попутных газов извлекают этан, пропан, бутан и компоненты бензина, сероводород, разделяют газы термокаталитических процессов.
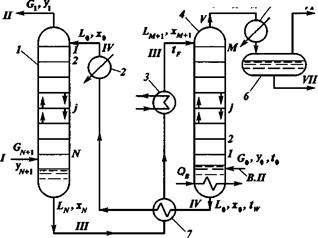
Схематически процесс абсорбции представлен (рисунок 18.1)
Поскольку парциальное давление компонента пропорционально его концентрации, движущую силу при абсорбции можно измерять также разностью концентраций в газовой и жидкой фазах:
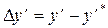
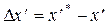
Рис. 18.1. Принципиальная схема абсорбционно-десорбционной установки:
/ — абсорбер; 2 — холодильник; 3 — подогреватель; 4 — десорбер; 5 — конденсатор; 6 — емкость; 7 — теплообменник. Потоки: I — сырой газ; II — сухой (тощий) газ; III — насыщенный абсорбент; IV — регенерированный абсорбент; V — извлеченные компоненты; V7 — несконденсированные газовые компоненты; VII — жидкий продукт
ФИЗИЧЕСКИЕ ОСНОВЫ АБСОРБЦИИ



Процессы и аппараты пищевых производств.
Абсорбация. Физические основы процесса. Материльный баланс при абсорбации и рабочая линия процессов абсорб.аппаратов
Абсорбцией называют процесс поглощения газов или паров (абсорбтивов) из газовых или паровых смесей жидкими поглотителями — абсорбентами. Этот процесс является избирательным и обратимым, что позволяет применить его с целью получения растворов газов в жидкостях, а также для разделения газовых или паровых смесей.
После абсорбции одного или нескольких компонентов из газовой или паровой смеси, как правило, проводят десорбцию, т. е. выделение этих компонентов из жидкости. Таким образом осуществляют разделение газовой смеси.
Имеют место физическая абсорбция и хемосорбция. При физической абсорбции при растворении газа не происходит химической реакции. При хемосорбция абсорбируемый газ вступает в химическую реакцию в жидкой фазе.
Процессы абсорбции в технике применяют для разделения углеводородных газов и получения соляной и сернистой кислот, аммиачной воды, очистки отводящих газов с целью улавливания ценных продуктов или обезвреживания газосбросов.
Аппаратурно-технологическое оформление абсорбции несложно, поэтому процессы абсорбции широко используют в технике.
Аппараты для проведения процессов абсорбции называются абсорберами.
ФИЗИЧЕСКИЕ ОСНОВЫ АБСОРБЦИИ
При взаимодействии газа с жидкостью возникает система, состоящая из двух фаз (Ф=2) и трех компонентов — распределяемого вещества и двух веществ носителей (К=3).
Согласно правилу фаз такая система имеет три степени свободы
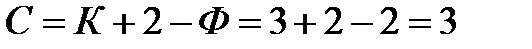
Тремя основными параметрами, определяющими фазовое равновесие в системе, являются давление, температура и концентрация.
В этом случае можно произвольно изменять общее давление 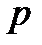
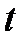
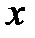
В условиях равновесия при 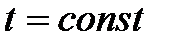
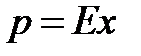
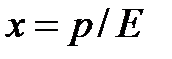
где: 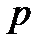
Константа Генри зависит от природы растворяющегося вещества (абсорбтива), абсорбента и температуры:
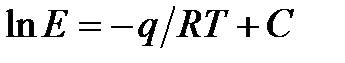
где: q – теплота растворения газа, кДж/кмоль; R =8,325 кДж/(кмоль*К) – универсальная газовая постоянная: Т – абсолютная температура растворения, К; С – постоянная, зависящая от природы газа и жидкости и определяемая опытным путём.
Из равенства (13.2) видно, что с ростом температуры растворимость газов в жидкостях уменьшается. Парциальное давление растворяемого газа в газовой фазе, соответствующее равновесию, может быть заменено равновесной концентрацией. Согласно закону Дальтона парциальное давление компонента в газовой смеси равно общему давлению, умноженному на мольную долю этого компонента в смеси, т. е.
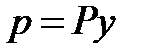
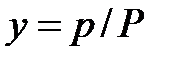
где: Р — общее давление газовой смеси; 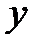
Сопоставляя уравнения (13.3) и (13.1), найдем
или, обозначая константу фазового равновесия 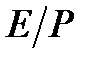
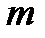
Уравнение(13.4) показывает, что зависимость между равновесными концентрациями распределяемого компонента в газовой смеси и в жидкости выражается прямой линией, проходящей через начало координат, тангенс угла наклона которой равен 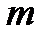
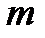
Рис.13.1. Зависимость между растворимостью газов в жидкости и парциальным его давлением над раствором при различных температурах (t1>t2>t3)
Процессы абсорбции можно рассчитывать в относительных мольных концентрациях. В этом случае при малой концентрации газа х в жидкости закон Генри записывается так:
Отметим, что закону Генри подчиняются сильно разбавленные растворы, а также растворы при небольших давлениях, которые по своим свойствам приближаются к идеальным. Для концентрированных растворов и больших давлений зависимость между равновесными концентрациями выражается кривой линией, вид которой определяют экспериментально