Для чего клеткам кислород
Для чего клеткам кислород
Для обеспечения жизнедеятельности любого живого организма необходимо постоянно поддерживать определенный уровень обмена веществ как между органами и тканями внутри организма, так и с внешней средой. Из внешней среды организм получает питательные вещества, которые он частично превращает в собственные ткани, во внешнюю среду отдает продукты своей жизнедеятельности ненужные или даже вредные для организма. Таким образом, наличие обмена веществ определяет сам факт жизни организма.
Для обеспечения обмена веществ необходима энергия. В организме высших животных энергия образуется в результате сложных биохимических реакций, основу которых составляют процессы окисления.
Основным субстратом, подвергающимся окислению, являются углеводы. Доля углеводов как субстрата для выработки энергии среди других веществ, составляет более 80%. В процессе окисления принимают участие также жирные кислоты и амиокислоты.
Единственным окислителем является кислород (аэробный гликолиз). При недостатке кислорода начинает функционировать более древний механизм выработки энергии — анаэробный гликолиз, эффективность которого в 18 раз меньше.
В процессе сложных биохимических преобразований вещества, участвующие в обменных процессах, расщепляются в основном до воды, двуокиси углерода (углекислый газ) и мочевины, которые и удаляются из организма соответствующими органами. В здоровом организме этот окислительный процесс сопровождается выделением энергии, составляющей приблизительно 3000-3500 Ккал.
Поскольку выработка энергии является одним из наиболее важных критериев жизнедеятельности организма, то постоянный контроль (мониторинг) этого параметра может быть существенным фактором получения информации. Особенно актуальной регистрация энергетики является у больных в критических состояниях при проведении реанимации и интенсивной терапии.
Основной проблемой для поддержания обмена веществ является проблема кислорода, т.к. его запасы столь незначительны, что позволяют осуществлять жизнедеятельность организма всего лишь несколько минут.
Содержание кислорода в крови при дыхании атмосферным воздухом составляет 850 мл., при дыхании 100% кислородом — 950 мл. Запасы кислорода в легких содержатся в их функциональной остаточной емкости (ФОЕ) и при дыхании воздухом составляют 450 мл, а при дыхании 100% кислородом — 3000 мл. В незначительных количествах (250-300 мл) кислород содержится в тканях в растворенном или связанном состоянии. Таким образом, общие запасы кислорода в организме составляют около 1,5 литров при дыхании воздухом и несколько больше четырех литров при дыхании 100% кислородом.
Если учесть, что в покое человек потребляет около 250 мл кислорода в 1 минуту, а при физической нагрузке и различных патологических состояниях потребление 02 увеличивается в несколько раз, то становится очевидным, что запасов кислорода может хватить не более, чем на 5-6 минут.
Именно поэтому в процессе эволюции высших организмов появились системы органов, призванных обеспечить в организме непрерывное поступление кислорода.
Это прежде всего система крови, в которой кислород аккумулируется в виде раствора в плазме и химической связи с гемоглобином.
Это система органов дыхания (ротовая полость, глотка, гортань, трахея, бронхи и легкие), в которой осуществляется переход кислорода из внешней среды в кровь и углекислого газа из крови во внешнюю среду (газообмен).
Это система органов кровообращения, которая обеспечивает транспорт кислорода к органам и тканям и выведение углекислого газа.
Оксигенотерапия повреждает микробиом легких: новое звено патогенеза Covid-19
Несмотря на то, что легкие считаются относительно «чистыми и свободными» от бактерий, в них существует определенный баланс микробиоты, который может нарушаться при проведении оксигенотерапи
Одним из ключевых признаков Covid-19 является одышка, которая вызывается значительным снижением уровня кислорода в крови. Во время госпитализации такие пациенты получают оксигенотерапию для нормализации уровня кислорода.
Несмотря на то, что легкие считаются достаточно «чистыми и свободными» от бактерий, в них существует определенный баланс микробиоты. Новое исследование указывает на то, что оксигенотерапия может негативным образом воздействовать на этот баланс.
«Кислород в избыточном виде является токсином. Если поместить лабораторное животное в среду с 100% кислородом, то оно погибнет в течение 5 дней, при этом будут развиваться повреждения легких, схожих с таковыми при Covid-19 или легочной недостаточности другой этиологии», – рассуждают авторы исследования.
Пациенты в интенсивной терапии получают высокие дозы кислорода на протяжении длительного времени. Ученые решили исследовать, как при этом меняется состав и жизнедеятельность микроорганизмов легких. Различные бактерии достаточно слабо различаются в том, как они реагируют на высокие дозы кислорода.
Была проведена серия экспериментов на здоровых лабораторных мышах. Изменения оказались ровно такими, как предполагали ученые: кислород-толератные бактерии, такие как стафилококки, распространялись в этой среде куда активнее остальных.
Следующий вопрос заключался в том, какое из изменений происходит первым – повреждение легочной ткани или изменения микробиомных взаимоотношений? Оказалось, что микробиом реагировал на оксигенотерапию уже в течение первого дня, в то время как повреждения легких развивались только после 3 дня.
В последнем эксперименте ученые сравнили 2 группы генетически идентичных мышей, получавших оксигенотерапию: со стерильными легкими и с обычным легочным микробиомом. Первая группа не демонстрировала легочных повреждений, характерных для второй группы с естественной микрофлорой в легких.
Это исследование указывает на то, что в патогенезе легочных повреждений при Covid-19 у пациентов, получающих оксигенотерапию, по-видимому, определенную роль играет легочный микробиом.
Тем не менее, результаты использования антибиотиков оказались неожиданными: применение ванкомицина, обладающего эффективностью против грамположительных стафилококков, не повлияло на возникновение легочных повреждений, в отличие от цефтриаксона, направленного на грамотрицательные бактерии.
Авторы работы настаивают на том, чтобы на основании их данных не проводилось никаких изменений актуальных протоколов лечения, в особенности оксигенотерапии. Необходимо проведение рандомизированных контролируемых исследований для получения уверенных клинических рекомендаций.
Что делают клетки, когда им нечем дышать
Могут ли клетки «измерять» количество кислорода? Зачем им это нужно? И как они реагируют в зависимости от его содержания? Долгое время механизм адаптации животной клетки к различной концентрации кислорода в окружающей среде был не понятен. Ясность в эти вопросы внесли работы Питера Рэтклифа, Уильяма Келина-младшего и Грегга Семенцы, которые в 2019 году удостоились Нобелевской премии по физиологии и медицине за исследования этого механизма. Что значит эта работа для современной науки и какие возможности для разработки новых стратегий в борьбе с раком и другими болезнями она открывает, рассказывает Екатерина Умнякова, старший научный сотрудник ФГБНУ «Институт экспериментальной медицины». Лекция ученого состоялась накануне в Центральной библиотеке имени Лермонтова в рамках проекта «Нобелевка в Открытой гостиной 2019».
Почему мы не можем жить без кислорода
Все знают, что кислород — важный химический элемент для всего живого. В атмосфере содержится до 21% О2, и жизнь и для нас, и для животных, которые населяют нашу планету, без него фактически не представляется возможной.
Но почему мы без него не можем? Дело в том, что под воздействием этого важнейшего газа происходит конвертирование энергии. Насколько бы полезной и вкусной ни была наша еда, мы не можем использовать ее, не преобразовав в те формы, благодаря которым мы «расплатимся» за энергетические процессы внутри нас. Грубо говоря, наши клетки не умеют воспринимать еду, которую мы видим у себя на столе. Они могут получать энергию в форме молекулы АТФ (аденозинтрифосфат). Это, своего рода, энергетическая валюта нашего организма — все в итоге сводится к ней. Наш организм получает энергию в виде этой молекулы. И чтобы осуществить какие-то процессы, тоже затрачивается АТФ.
Под действием кислорода происходит выработка большого количества АТФ. Без кислорода это тоже возможно, но этот процесс идет гораздо менее эффективно и этого не хватит, чтобы обеспечить нашу жизнедеятельность. Да, конечно, есть много живых организмов, которым кислород не нужен — они нашли для себя другой окислитель, который можно использовать, и прекрасно себя чувствуют. Мы так не умеем, и я думаю, вряд ли когда-либо сумеем.
Без АТФ невозможно существование клеток, поэтому давно было понятно, что каким-то образом они должны реагировать на недостаток кислорода. Но до работ Питера Рэтклифа, Уильяма Келина и Грегга Семенцы было неясно, как именно наши клетки понимают, что в какой-то момент кислорода в среде становится недостаточно. Примечательно, что эти ученые представляют довольно разные области. Но, работая в своих направлениях, они параллельно пришли к одному и тому же и смогли изучить эти механизмы.

С чего все началось
Как известно, в эритроцитах находится гемоглобин, и именно он связывает кислород и доставляет его к тканям. Но здесь необходимо упомянуть о таком гормоне, как эритропоэтин. Он выбрасывается в кровь почками (некоторым образом его могут синтезировать также клетки печени) и служит сигналом для организма, чтобы вырабатывалось большее количество эритроцитов. Это, в свою очередь, приводит к тому, что ткани и клетки больше снабжаются кислородом.
Исследователи, которым была присуждена Нобелевская премия по физиологии и медицине в 2019 году, как раз изучали, как происходит образование этого гормона в организме, а именно — в каких случаях запускается его синтез. Грегг Семенца обнаружил регуляторный элемент — энхансер (небольшой участок ДНК, который после связывания с ним факторов транскрипции стимулирует транскрипцию с основных промоторов гена или группы генов — прим.ред.), который усиливает производство эритропоэтина. Параллельно такую работу проводил и Питер Рэтклиф.
Послебыло обнаружено, что именно с этим регуляторным элементом связывается какой-то белковый фактор, Грег Семенца назвал его HIF-фактор (Hypoxia-inducible factor). Далее выяснилось, что этот белок на самом деле не один. HIF состоит из двух частей: HIF-alpha, содержание которого зависит от концентрации кислорода, и HIF-beta, содержание которого не зависит от концентрации кислорода.
Таким образом, ученые обнаружили, что есть последовательность, с которой связывается регуляторный фактор и которая запускает гены в ответ на недостаток кислорода. В дальнейшем они показали, что это касается не только эритропоэтина, этот процесс запускается повсеместно, поскольку всем клеткам жизненно важно отвечать на недостаток кислорода.
«Миксер для белков», «метки смерти» и HIF: как наш организм запускает или не запускает программу по выживанию
В наших клетках есть специальная молекулярная машина — протеасома. Фактически она работает как «миксер для белков»: обнаруживается белок, который по каким-то причинам уже не нужен, он получает «метки смерти» (не каждый белок отправляется в «миксер»), после в протеасоме его размолачивает на последовательности, и далее из этих аминокислот можно построить уже что-то другое. Уильям Келин обнаружил, что, когда кислорода достаточно, с HIF-alpha так и происходит.
Стоит отметить, что до исследования, связанного с HIF, Уильям Келин работал с другим объектом: он занимался исследованием довольно редкого синдрома под названием болезнь Гиппеля–Линдау. Ученый обнаружил, что при нарушении работы гена VHL (Von Hippel–Lindau) запускалось образование различных опухолей, как правило, это были опухоли спинного, головного мозга. Таким образом стало понятно, что этот ген очень важен для того, чтобы опухоли не развивались.
Также в процессе исследования обнаружилось, что в организме людей, у которых была нарушена работа белка, кодируемого этим геном, также было много различных продуктов, которые запускают фактор HIF. То есть он есть у них в больших количествах, и при этом никуда не убирается организмом, даже несмотря на нормальное количество кислорода в среде. Это натолкнуло на мысль, что VHL и HIF связаны. Эту загадку ученые разгадывали уже совместно, и вот к чему они пришли.
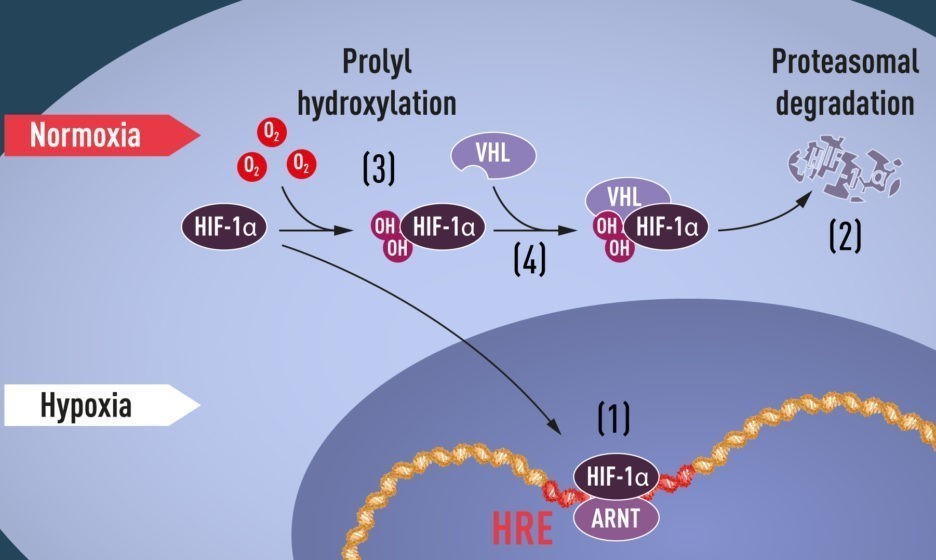
Если в среде недостаточно кислорода, то HIF-фактор уходит в ядро и связывается с той самой регуляторной последовательностью, которую обнаружил Грегг Семенца. Таким образом, запускается работа генов, которые нужны при ответе на гипоксию – низкое содержание кислорода в среде.
В случае же нормального содержания кислорода HIF-alpha разрушается. Как это происходит? Этот фактор имеет две аминокислоты, которые в присутствии кислорода и фермента пролилгидроксилазы преобразуются. В этом процессе задействованы очень сложные химические реакции, которые были расшифрованы этими тремя учеными. После этого, если у HIF-alpha появляются две этих гидроксильные группы, он может взаимодействовать с белком VHL. VHL-белок, в свою очередь, позволяет «меткам смерти» прикрепиться к фактору HIF1-alpha, и это, в свою очередь, отправляет его на разрушение в протеасому. Так что при нормальном содержании кислорода этот фактор не работает. И действительно, зачем? Ведь в этом случае не нужно отвечать на гипоксию и экстренно запускать программу по «выживанию».
Что еще показали ученые
Какие еще гены, помимо эритропоэтина, регулируются этим фактором? Это гены, которые запускаются при ангиогенезе, то есть при образовании и росте сосудов. Кроме того, это характерно для всех ферментов, которые участвуют в метаболизме. И наконец, это те гены, которые тем или иным образом способствуют выживанию или, наоборот, смерти клетки.
При активации генов, которые находятся под контролем фактора HIF-alpha, происходит усиление процессов гликолиза: глюкоза расщепляется, что в итоге дает нам энергию, или, иными словами, ту самую АТФ, которая нужна клетке. В нормальных условиях клетка может получить 36 молекул, а без кислорода — всего лишь две. То есть в таких условиях гены под контролем HIF-фактора пытаются сделать хоть что-то.
HIF-фактор может служить защитой от гибели клетки, если организм находится в условиях гипоксии короткое время. Но, если процесс хронический, они, напротив, запускают гибель клетки.
На что могут повлиять эти открытия на практике
На практике эти результаты открывают новые возможности по дальнейшему изучению адаптации организма к условиям, для которых характерно низкое содержание кислорода. Это не только высокогорье или морские глубины, но и космос.
Кроме того, это может стать причиной серьезного пересмотра патогенеза многих заболеваний. Учитывая новые знания, можно более эффективно лечить заболевания, связанные с нарушением снабжения органов и тканей кислородом. Можно также улучшить состояния пожилых людей, которые не могут в полной мере ответить на гипоксию тканей.
Нобелевка за “управление кислородом”. Как организм спасается от гипоксии и при чем тут допинговые скандалы
Члены Нобелевского комитета подчеркнули фундаментальную важность открытия: способность усваивать кислород критически важна для всех животных организмов на Земле, включая человека. Мы можем долго прожить без еды, достаточно долго – без воды, но мы не можем не дышать. Это связано с тем, что кислород, который мы вдыхаем, постоянно вовлечен в фундаментальные процессы извлечения энергии, которая необходима для жизни нашего организма. Сегодняшние лауреаты обнаружили генетический механизм, который позволяет организму регулировать уровни кислорода в разных частях тела и управлять ими.
«Эта система, которая требуется, чтобы наше тело нормально работало. Уровни кислорода отличаются в разных частях тела, например, в мышцах во время физических упражнений его уровни очень низкие – нам знакомо выражение «анаэробные тренировки». И нашему телу нужна система, чтобы выравнивать и регулировать уровень кислорода. Лауреаты обнаружили ее — эта система также отвечает за регулирование красных кровяных телец, которые могут переносить кислород. Она позволила нам, так сказать, колонизировать нашу планету во всем ее разнообразии – например, уровни кислорода в горах, на высоте, куда ниже, чем привычные нам и все равно люди смогли приспособиться к ним, такова адаптивная сила организма», — подчеркнул другой член Нобелевского комитета, профессор Патрик Эрнфорш, специалист по нейронаукам.
“Это может прозвучать банально, но открытие сегодняшних лауреатов – то, что войдет в учебники биологии. Дети в возрасте 12-13 лет будут изучать это, потому что это очень, очень базовый аспект работы клеток“, — сказал член Нобелевского комитета профессор Рэндон Джонсон.
Зачем вообще нужен кислород
Наверное, каждому очевидно, что кислород (O 2 ) очень нужен. Перекрытие его поступления в организм – при инфаркте, утоплении, повешении, сильном задымлении — приводит к быстрой смерти. Без кислорода невозможна жизнь не только такого сложного организма, как человеческий, но и куда более простых организмов и клеток. Кислород внутри клеток на самом базовом уровне участвует в процессах извлечения энергии из питательных веществ. Будь то углеводы или жиры, кислород нужен, чтобы окислить их – в этом процессе выделяется энергия, необходимая для всех без исключения процессов в нашем организме – биосинтеза белков, из которых состоит все внутри нас, их транспорта и всех более сложных функций, включая иммунитет и само дыхание.
Этот процесс протекает в специальных «органах» клетки – митохондриях. В 1931 году Отто Варбург получил Нобелевскую премию по физиологии и медицине за объяснение процесса генерирования энергии – для этого необходим сложный набор ферментов.
Еще одна важная мысль – наш организм никак не может производить кислород сам. Растения – могут, они выделяют его в ходе фотосинтеза (кстати, для жизнедеятельности растения расходуют кислород, они тоже дышат – но выделяют они его больше), а человек и животные – нет. Поэтому нам критически важно «уметь» стабильно получать его из окружающей среды, а получив – «грамотно» распределять внутри организма. Это не такая простая задача.
В разных условиях в окружающей среде содержится разное количество кислорода, поэтому при его недостатке телу нужно, во-первых, перераспределять его так, чтоб он шел на самое необходимое, а во-вторых, — сигнализировать нам о том, что кислорода мало и его нужно искать. То же касается уровней кислорода в разных частях тела и органах – иногда его сильнее расходует мозг, иногда – мышцы. Тогда нужно лучше снабжать их, выравнивать уровень.
В 1938 году Нобелевскую премию получил Корней Хейманс – он обнаружил так называемся каротидные тельца. Это специальные рецепторы («датчики») в сонной артерии, которые «измеряют» уровень кислорода и сообщают мозгу, если с ними что-то не так. Это механизм адаптации/реакции на недостаток кислорода – гипоксию.
Что сделали нобелиаты
Здесь важно понять, как же реагирует на гипоксию организм. Кислорода мало, значит, его нужно лучше переносить и извлекать, а для этого нам нужно больше красных кровяных тех – эритроцитов (тех самых, что содержат гемоглобин, который измеряют врачи – низкий гемоглобин означает проблемы со снабжением органов кислородом). Чтобы эритроцитов стало больше, при гипоксии организм выделяет гормон эритропоэтин, который и запускает их синтез. Слово эритропоэтин тоже знакомо – в связи с допинговыми скандалами. Больше кислорода в мышцах – больше спортивные успехи, поэтому спортсменами становятся те, у кого изначально хороший гемоглобин и много эритропоэтина.
И здесь на помощь приходит генетика. Грегг Семенза и Питер Рэтклифф независимо обнаружили, что в ДНК есть особые участки рядом с теми, что кодируют сам эритропоэтин. Они-то и являются чувствительными к кислороду и «толкают» в нужный момент «соседа» по ДНК, который запускает синтез эритропоэтина.
Теперь предстояло понять, кто «приносит» к ДНК информацию о недостатке кислорода. Семенза обнаружил соответствующий белковый комплекс, он получил название HIF (hypoxia inducible factor, индуцируемый гипоксией фактор – здесь фактор означает группу белков). Два разных белка в случае гипоксии связывались с ДНК и запускали молекулярный механизм, описанный выше.
Уильям Кэлин, занимаясь исследованием определенных типов рака, нашел еще один ген – VHL, который в нужный момент останавливает работу HIF, чтобы организм не произвел слишком много эритропоэтина и красных кровяных телец. Это механизм можно сравнить с весами – если кислорода слишком мало, HIF включается, чтоб выровнять равновесие, а VHL контролирует его работу, чтоб не допустить «перевеса» в другую сторону.
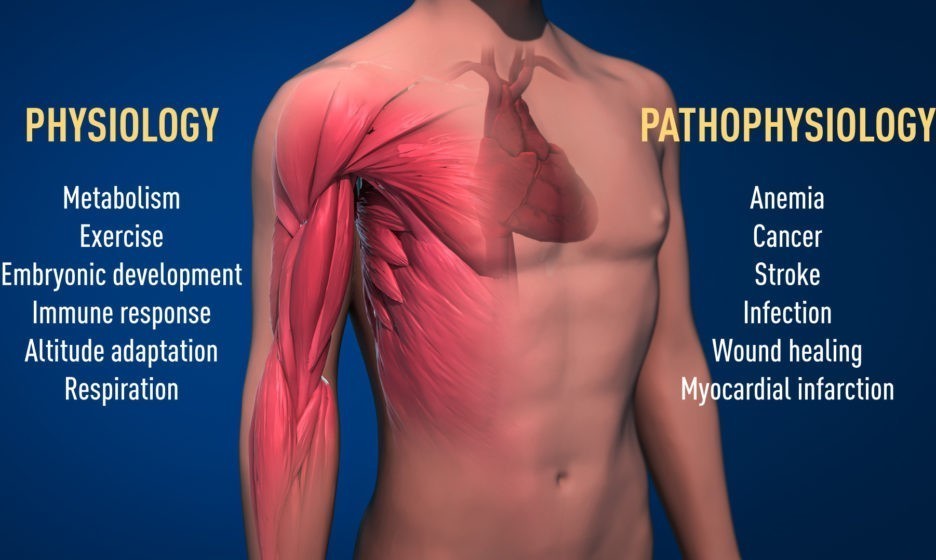
У здорового человека этот механизм критичен для метаболизма вообще – процесса выработки энергии из пищи, для компенсации при физических нагрузках, адаптации к горам, развитию эмбриона и контролю иммунитета. Он также важен при болезнях – анемии, инсультах, инфарктах, инфекциях и ранах, — везде, где необходимо локальное усиленное снабжение кислородом. Есть исследования, которые на основании этого механизма пытаются бороться с раковыми опухолями – если опухоль “посадить” на кислородный голод, она не сможет развиваться и расти.
“Рак питается и растет достаточно активно, в том числе опухоль выращивает дополнительные кровеносные сосуды, чтобы снабжать себя необходимым количеством кислорода. Исследования показывают, что эти белки гиперэкспрессированы в солидных опухолях (то есть их там больше чем необходимо). Предполагается, что регуляция уровня снабжения кислородом через работу с HIF позволит замедлить рост опухоли. Кроме этого, некоторые исследователи предполагают, что отслеживание уровня насыщения кислородом тканей может стать одним из способов обнаруживать рак, прогнозировать реакцию опухоли на лечение и ее развитие в целом”, говорит Любовь Барабанова, медицинский директор Севергрупп Медицина (сеть клиник «Скандинавия»).
О ком речь
Кэлин и Семенза родились в Нью-Йорке. Кэлин работает в медицинском институте Ховарда Хьюджеса, Семенза – в Университете Джонса Хопкинса. Сэр Питер Рэтклифф родился в Ланкашире и сейчас работает в Оксфорде.
Во время пресс-конференции, посвященной оглашению премии, секретарь Нобелевского комитета по физиологии и медицине Томас Перлманн рассказал, что ему удалось пообщаться со всеми тремя лауреатами.
«Профессор Рэтклифф уже был в офисе, а Грегг Семенза и Билл Кэлин живут в США, они еще спали, и мне пришлось их разбудить. Последний, кому я дозвонился, был Билл. У нас не было его телефона, поэтому мне сначала удалось поговорить с его сестрой. Она дала мне два номера телефона, я позвонил по первому из них и спросил, говорю ли я с Биллом Кэлином, и получил отрицательный ответ. Второй номер оказался правильным. Билл Кейлин был очень счастлив, не находил слов. Все трое были очень рады и подчеркнули, что для них большая честь разделить этот приз друг с другом, именно в этом коллективе», — рассказал Перлманн.
Иногда на пресс-конференции организуют телефонные интервью с лауреатами, однако в этот раз никого из них на связи не было, на вопросы отвечал только Нобелевский комитет.
Размера премии в этом году составляет девять миллионов крон, и они будут разделены поровну между всеми тремя лауреатами.
Немного истории
В прошлом году лауреатами по физиологии и медицине стали японец Тасуку Хондзё и американец Джеймс Эллисон «за открытие терапии рака ингибированием негативной иммунной регуляции».
Всего с 1901 года было присуждено 109 Нобелевских премий в физиологии и медицине – премии не всегда вручались во время мировых войн и в нескольких других случаях. Лауреатами стали 216 человек – правила Нобелевского комитета позволяют каждый год наградить от одного до трех человек. Среди них всего 12 женщин. Самым молодым лауреатом был Фредерик Бантинг – он получил премию в 1923 году в возрасте 32 лет за открытие инсулина. Самым старым – Пейтон Роус, он получил премию в 1966, когда ему было 87 лет.