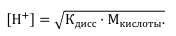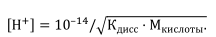Для чего при титровании раствора применяются индикаторы
Индикаторы в кислотно-основном титровании. Техника титрования
В реакции нейтрализации при достижении точки эквивалентности происходит изменение значения рН раствора. Поэтому для фиксирования точки эквивалентности используют вещества – индикаторы, окраска которых меняется в зависимости от изменения рН. Наиболее часто используемые индикаторы приведены в таблице 3.1.
↑ Таблица 3.1 Характеристики перехода кислотно-основных индикаторов
↑ Изменение окраски
Приготовление растворов индикаторов. Метиловый оранжевый (0,1% в воде): 0,01 г красителя растворяют в 10 мл воды; применяют в количестве 3-4 капель на 25 мл титруемого раствора.
Метиловый красный (0,2% в 60% этаноле): 0,02 г красителя растворяют в 10 мл 60% этанола; применяют в количестве 2-3 капель.
Фенолфталеин (1% в 60% этаноле): 0,1 г красителя растворяют в 10 мл 60 % этанола; применяют в количестве 2 капель.
Бромтимоловый синий (0,1% в 20% этаноле). 0,01 г красителя растворяют в 10 мл 20% этанола.
↑ Техника титрования
Титрование производится в конических колбах. Размер колбы подбирается так, чтобы общий объем жидкости в конце титрования не превышал половину объема колбы. Сам процесс титрования состоит в прибавлении титранта из бюретки к анализируемому раствору, находящемуся в колбе. Раствор из бюретки прибавляют до тех пор, пока количество прибавленного вещества не будет эквивалентно количеству вещества, находящемуся в колбе. Этот момент называется конечной точкой титрования (КТТ).
Рис. 3.3. Положение колбы при титровании.
Перед началом титрования заполняют бюретку раствором и доводят уровень жидкости до нулевой черты. В коническую колбу помещают точный объем анализируемого раствора, и добавляют нужное количество индикатора. Затем проверяют правильность установки уровня жидкости в бюретке на нулевое деление. Это надо делать обязательно перед самым началом титрования.
Подставляют колбу с титруемым раствором под бюретку. Правильное положение при титровании показано на рис. 3.3. Под колбу кладут лист белой бумаги, чтобы точнее заметить момент изменения цвета раствора. Колбу держат в правой руке, а левой открывают и закрывают кран, выпуская жидкость из бюретки.
При титровании раствор должен вытекать по каплям, сначала быстро, а вблизи конечной точки очень медленно. Во время титрования раствор в колбе следует все время перемешивать вращательными движениями.
Если при титровании нельзя сказать с уверенностью, что достигнута конечная точка, то следует записать показания бюретки, прибавить еще одну каплю раствора и наблюдать, происходит ли изменение в окраске титруемого раствора.
Записывают результаты титрования с точностью до второго десятичного знака, например: 10,53 мл; 11,20 мл; 9,00 мл.
Необходимо брать такое количество анализируемого раствора, чтобы объем рабочего раствора, затраченного на титрование, составлял не менее 1/3 объема бюретки. Наиболее точные результаты получаются в том случае, когда при титровании из бюретки вместимостью 25 мл прибавляют от 10 до 20 мл рабочего раствора, а из бюретки вместимостью 50 мл—от 20 до 40 мл рабочего раствора.
Чтобы убедиться в правильности результатов титрования проводят параллельное определение. Для этого в другую коническую колбу помещают такое же количество титруемого раствора, наполняют бюретку рабочим раствором и повторяют титрование. Если результаты двух определений расходятся не более чем на 0,1 мл для бюреток вместимостью 25 или 50 мл, то их можно считать правильными. В случае расхождения полученных результатов титрование повторяют. В ответственных случаях проводят 3 параллельных определения. Для расчета берут среднее арифметическое полученных результатов.
Вычисление результатов по методу отдельных навесок. В этом случае взвешивают на аналитических весах точную навеску m ( A ) вещества А, переносят ее в колбу для титрования, растворяют, прибавляя в колбу некоторое количество растворителя, и тируют полученный раствор.
Индикаторы. Основные этапы титриметрического анализа. Кислотно-основное и ок-восст-ное титрование и прим-е его для контроля качества продукции.
Индикаторы в титриметрии применяют для визуальной индикации КТТ. В зависимости от реак-ции, лежащей в основе их действия, индикаторы подразделяют на: 1) кислотно-основные, которые реагируют на значение рН.
— смешанные индикаторы— смеси двух индика- торов или индикатора и красителя
— Флуорецентные индикаторы – применяют для мутных или сильно окрашен- ных растворов, у которых при освещении ультрафиолетовыми лучами при определенном значении рН появляется или исчезает флуоресценция или изменяется цвет либо оттенок
— Хемилюминесцентные индикаторы – это группа веществ, которая высвечивает видимым светом в конечной точке титрования. Их применяют для титрования сильноокрашенных растворов при протекании окислительно-восстановительных и кислотно-основных реакций.
—Универсальные индикаторы –при изменении значения рН в широких пределах происходят заметные на глаз изменения окраски (индикат.бумага)
2) окислительно-восстановительные, которые представляют собой органические соединения, окисляющиеся при определѐнном значении потенциала.
3) комплексонометрические, представляющие собой хорошо растворимые в воде органические красители, способные образовывать с ионами металла интенсивно окрашенные комплексные соединения
4) адсорбционные. В случае применения таких индикаторов в КТТ происходит изменение цвета образующегося осадка.
Требования к индикаторам:1. Должен обладать высоким светопоглощением;
2Переход окраски д.б. контрастным;3Область перехода окраски д.б. к.м уже.
Основные этапы титриметрического анализа.
– подготовка пробы (зависит от природы аналита и матрицы пробы; наличия мешающих компонентов, и может включать следующие операции: раство-рение, разбавление или концентрирование, экстрагирование, переведе-ние аналита в определенную степень окисления и др
– приготовление растворов титрантов;
– построение кривых титрования (при необходимости);
– обработку и расчет результатов анализа.
Кислотно-основное титрование. Данный метод титрования применяется для определения кислот, оснований, а также многих солей слабых кислот: карбонатов, боратов, сульфитов, и т. д.
Кривая кислотно-основного титрования представляет собой зависимость: рН раствора от объема добавленного титранта или его концентрации или рН раствора от степени оттитро- ванности определяемого вещества.
Установление КТТ в данном методе можно производить инструментальным методом, непосредственно измеряя рН раствора при помощи рН–метра, но чаще для этих целей используют кислотно- основные индикаторы.
– кислотного и щелочного чисел нефтепродуктов;– щелочности хоз. и туалетного мыла.и т.д.
Окислительно-восстановительное титрование. В основе ме- тода лежит изменение потенциала окислительно-восстановительной системы в процессе титрования обусловленное изменением соотношения концентраций окисленной и восстановленной форм. Кривая титрования, отражающей зависимость окислительно-восстановительного потенциала системы от объѐма прибавляемого титранта.
– при помощи окислительно-восстановительных индикаторов.
Основные видыОВ титрования (перманганатометрия, йодометрия, дихроматометрия и т.д.) различают по окислителю, используемому в реакции.
В пищевой промышленности: – массовую долю сахара и сахарозы в кондитерских изделиях ;– содержание сахаров в виноградных, плодовых, шампанских, иг-ристых винах, виноматериалах и коньяках (методом Бертрана )
– содержание витамина С в молочных продуктах для детского пи-тания
– содержание этилового спирта в продуктах переработки плодов и овощей
Титриметрия. Посуда, титрованные растворы, способы и методы
» data-shape=»round» data-use-links data-color-scheme=»normal» data-direction=»horizontal» data-services=»messenger,vkontakte,facebook,odnoklassniki,telegram,twitter,viber,whatsapp,moimir,lj,blogger»>
ТИТРИМЕТРИЯ
Основные понятия титриметрии
Титриметрический анализ основан на точном измерении реактива, израсходованного на реакцию с определяемым веществом. Раньше этот вид анализа называли объемным, так как в расчетах используют объем раствора, пошедшего на реакцию. Титриметрия отличается от гравиметрии малой трудоемкостью, простотой аппаратурного оформления. Титриметрический анализ в отношении скорости выполнения дает огромное преимущество по сравнению с гравиметрическим, являющимся, однако, наиболее точным химическим методом анализа.
Титриметрия возникла в середине XVIII века. Многие ученые внесли вклад в ее развитие. У. Льюис (1767) дал определение понятия «точки насыщения», т. е. точки эквивалентности. Благодаря работам Ж. Гей-Люссака титриметрия превратилась из метода анализа в самостоятельный раздел науки. Э. Мор разработал много методик по данному виду анализа, написал учебник по химико-аналитическому методу титрования (1856); В. Оствальд и А. Ганч развили теорию индикаторов (1894).
Титриметрия широко применяется в настоящее время для научных исследований и при контроле технологических процессов.
Титруемое вещество — вещество, количество которого определяется непосредственно в процессе титрования.
Титрант — вещество, вступающее в реакцию с титруемым веществом. Концентрация стандартного раствора титранта должна быть определена перед началом анализа с точностью не менее трех значащих цифр после запятой.
Аликвота — объем раствора, точно отмеренный при помощи калиброванной пипетки.
Титрование — прибавление титрованного раствора к анализируемому с целью определения точно эквивалентного его количества. Отсюда ясно, что при титровании необходимо достаточно точно установить момент наступления эквивалентности или, как говорят, фиксировать точку эквивалентности.
Реакция, используемая в титриметрическом анализе, должна протекать количественно, т. е. должны выполняться следующие условия:
Если не выполняется хотя бы одно условие, то метод титриметрии непригоден. Для этого метода необходимо:
В титриметрии концентрации растворов веществ выражают в молях эквивалентов вещества в одном кубическом дециметре или в одном литре раствора. Нормальная концентрация, используемая в аналитической химии, учитывает то, что эквиваленты веществ для разных реакций различаются, поэтому следует указывать (в скобках) фактор эквивалентности. Например, 0,1н КМnО4 (f экв = 1/5).
В полуреакции восстановления участвуют 5 электронов, следовательно, f экв (КМnО4) = 1/5, а эквивалент перманганата калия равен 1/5 молярной массы КМnО4.
Химическая лабораторная посуда и ее назначение
Для точного определения объемов используются бюретки, пипетки и мерные колбы (рис. 3.1).
Рис. 3.1. Мерная посуда а — цилиндры; б — мерные колбы; в — химический стакан; г — бюретки с краном; д — пипетка Мора
Бюретка — цилиндрическая трубка с суженым концом, к которому с помощью резинового шланга присоединена стеклянная трубка с оттянутым кончиком. На резиновый шланг надет зажим, либо вставлен в него стеклянный шарик. Если для титрования применяют агрессивные для резины растворы, то используют полностью стеклянную бюретку (пермангонатометрия). Бюретка градуиронана на миллилитры и десятые их доли. В титриметрии используют бюретки объемами 10, 25 и 50 мл. Заполненная раствором бюретка имеет вогнутую поверхность (мениск). По правилам показания по бюретке берут по нижнему краю мениска; глаз должен находиться на уровне этого нижнего края (рис. 3.2).
Рис. 3.2. Правила определения результатов исследований
Показания по бюретке могут быть с существенными погрешностями. Такие погрешности являются источником ошибок в объемном анализе.
Бюретка должна быть тщательно промыта и обезжирена (хромовой смесью — смесь концентрированной серной кислоты и бихромата калия или смесью раствора перманганата калия со щелочью). Затем бюретку многократно промывают водопроводной водой, 2−3 раза — дистиллированной водой и 2−3 раза — небольшими порциями раствора, которым заполняют бюретку для анализа. Затем заполняют бюретку раствором для титрования через воронку. При промывании бюретки нельзя затыкать ее сверху пальцами, так как пальцы никогда не бывают химически чистыми.
Пипетка используется для измерения точного объема раствора для метода титриметрии. Это стеклянная длинная узкая трубка с расширением или без него в середине. В верхней узкой части пипетки имеется черта, до которой и нужно заполнять пипетку раствором 5, 10, 20, 25, 50, 100 мл. На пипетке указана ее вместимость и температура, при которой градуирована пипетка. При необходимости используют измерительные пипетки (с градуировкой). Такие пипетки особенно необходимы для работы с небольшими объемами растворов (до 5 мл).
Рис. 3.3. Мерные стеклянные колбы
Используют мерные колбы для приготовления титрованных, стандартных растворов, а также для их разбавления. Моют колбы так же, как пипетки и бюретки, но не споласкивают рабочим раствором. Вначале раствор заливают через воронку в колбу, а затем доводят объем до черты прикапыванием воды из пипетки. Правило заполнения — по нижнему мениску.
Калибровка объемов мерной посуды идет при температуре 20–25 о С, точное значение температуры приготовления растворов указано на ней.
Приготовление титрованных растворов
Большая разница значений температур, при которых идет приготовление растворов, недопустима. Есть вещества, которые можно растворить только в горячей воде. Например, бура Na2B4O7 ∙10H2O. Растворение ее ведут в горячей воде, в половине объема, затем охлаждают до комнатной температуры и доводят объем водой до метки.
Существуют два способа приготовления титрованных растворов.
Вещество, удовлетворяющее указанным требованиям, называется первичным стандартом.
Второй способ — с установленным веществом. Если вещество не удовлетворяет требованиям, указанным выше, то используют установочные вещества. Например, для установления точной концентрации раствора NaOH используют в качестве установочного вещества щавелевую кислоту Na2C2O4 ∙2H2O, для соляной кислоты — буру Na2B4O7 ∙10H2O. Очень удобно использовать фиксаналы, выпускаемые промышленностью.
Фиксанал — запаянные ампулы с веществом для приготовления, как правило, 1 л раствора концентрации 0,1 н.
Основные способы и методы титрования
1. Способ прямого титрования. Определяемое вещество непосредственно реагирует с титрантом. Например, для определения концентрации кислоты ее титруют щелочью.
2. Способ обратного титрования (или титрование по остатку). Для этого способа необходимы два рабочих раствора, в раствор определяемого вещества вносят избыток основного рабочего раствора, а остаток оттитровывают вспомогательным рабочим раствором.
Например, в кислый раствор хлорида добавляют
AgNO 3 Ag + + Cl – = AgCl.
Затем избыток серебра оттитровывают роданидом Ag+ + CSN – = AgCSN.
3. Титрование по замещению, или косвенное титрование. К определяемому веществу (например, Cu +2) добавляют специальный реагент (I −) для проведения реакции, образовавшийся йод оттитровывают тиосульфатом натрия. Конец реакции определяют по крахмальному индикатору (исчезновение синей окраски).
Титрование проводят по следующим правилам:
Различают методы титриметрического анализа по типу основной реакции, протекающей при титровании. Выделяют следующие методы титриметрического анализа кислотно-основное взаимодействие, реакция нейтрализации; окисление-восстановление (оксидиметрия); комплексообразование; осаждение.
Расчеты в титриметрии основаны на законе эквивалентов. Вещества реагируют между собой в эквивалентных количествах. Поэтому наиболее удобный способ выражения концентрации — нормальная концентрация. Объемы [V(A) и V(B)] и нормальные концентрации реагирующих веществ [СN(А) и CN(В)] в точке эквивалентности выражается соотношением
СN(А) и V(A) известны, а V(B) был определен после титрования раствором (А). Тогда:
Масса вещества m(B), содержащего в объеме V(B), находится по формуле:
Методы разделения и концентрирования
Процесс разделения состоит в выделении компонентов, составляющих исходную смесь. Процесс концентрирования состоит в увеличении концентрации микрокомпонентов в пробе анализируемого вещества. Концентрирование является частным случаем разделения. Эти методы чрезвычайно многочисленны и разнообразны. Методы разделения гомогенных и гетерогенных систем отличаются друг от друга по своей сущности.
Система — совокупность находящихся во взаимодействии веществ, обособленных мысленно или фактически.
Компонент — составная часть системы.
Фаза — однородная часть системы, отделенная от других частей поверхностью раздела. Гомогенная система состоит из одной фазы (например, истинный раствор). Гетерогенная система состоит из двух и более фаз (например, вода + лед, раствор + осадок).
Разделение гетерогенных систем происходит следующими методами:
Для разделения гомогенных систем используют следующие методы:
Кислотно-основное титрование. Индикаторы, техника титрования
» data-shape=»round» data-use-links data-color-scheme=»normal» data-direction=»horizontal» data-services=»messenger,vkontakte,facebook,odnoklassniki,telegram,twitter,viber,whatsapp,moimir,lj,blogger»>
Кислотно-основное титрование
Основные понятия кислотно-основного титрования
Индикаторы метода кислотно-основного титрования. Теории индикаторов
Техника титрования
Основные понятия кислотно-основного титрования
Метод кислотно-основное титрование базируется на реакциях взаимодействия между кислотами и основаниями, т. е. на реакции нейтрализации:
Рабочими растворами метода являются растворы сильных кислот (HCl, H2S, НNО3 и др.) или сильных оснований (NaOH, КОН, Ва(ОН)2 и др.). В зависимости от титрованного раствора (титранта) кислотно-основное титрование подразделяют на ацидиметрию, если титрантом является раствор кислоты, и алкалиметрию, если используют в качестве титранта раствор основания.
Согласно правилу эквивалентности титрование необходимо продолжать до тех пор, пока количество прибавленного реагента не станет эквивалентным содержанию определяемого вещества. Наступающий в процессе титрования момент, когда количecтвo вещества в растворе титранта становится строго эквивалентным количеству определяемого вещества согласно уравнению химической реакции, называют точкой эквивалентности.
Точку эквивалентности устанавливают различными способами. В методах ручного анализа преимущественно используют изменение окраски индикатора, добавляемого в титруемый раствор. Момент, при котором происходит наблюдаемое изменение цвета индикатора, называют конечной точкой титрования. Очень часто конечная точка титрования не совсем совпадает с точкой эквивалентности. Как правило, они отличаются друг от друга не более чем на 0,04 мл (2 капли) титранта. Это то количество вещества в растворе титранта, которое необходимо для взаимодейcтвия его с индикатором.
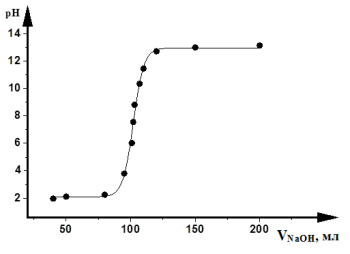
Кривые кислотно-основного титрования выражают зависимость изменения рН раствора от объема добавленного титранта (рис. 3.4).
Рис. 3.4. Кривая кислотно-щелочного титрования
При расчете рН необходимо знать состав титриметрической смеси. Для упрощения вычислений (что не приводит к заметным ошибкам) не учитывают разбавление раствора в процессе титрования и используют понятие «концентрация», а не «активность». Кривые титрования представляют в виде графика зависимости рН от объема добавленного титранта или объема избытка определяемого вещества и избытка титранта.
В начале титрования рН изменяется очень медленно. Кривая (см. рис. 3.4) показывает, в частности, что если оттитровать половину имеющегося количества кислоты (50 мл), рН раствора изменится незначительно по сравнению с исходным, если оттитровать 90 % (90 мл), то и тогда уменьшение рН составит лишь одну единицу. С уменьшением концентрации оставшейся кислоты изменение рН при титровании становится более резким. Оттитровывание кислоты от 90 до 99 % вызывает изменение рН на три единицы. Также на единицу возрастает рН при оттитровывании от 99 до 99,9 %, т. е. на 0,9 %. Титрование остатка кислоты (0,1%) приводит к изменению рН на целых 3 единицы. Введение избытка в 0,1 % NaOH по сравнению с эквивалентным количеством вызывает изменение рН также на 3 единицы, и рН раствора становится равным 13,0.
Кривая титрования сильного основания сильной кислотой представляет собой зеркальное отображение кривой титрования сильной кислоты сильным основанием. При титровании сильной кислотой сильного основания и наоборот до точки эквивалентности рН раствора определяется концентрацией неоттитрованной щелочи или кислоты, а после точки эквивалентности — концентрацией добавленной кислоты или щелочи. В точке эквивалентности раствор нейтрален.
Скачок титрования — это резкое изменение рН в области точки эквивалентности. Факторы, влияющие на величину и положение скачка титрования (на величину скачка титрования влияют все факторы, от которых зависят значения рН):
Чем меньше концентрация титруемого вещества и титранта, тем меньше скачок. Практически невозможно оттитровать сильные протолиты концентрацией 10 –4 М, а слабые — концентрацией 10 –2 М. При изменении температуры сильно изменяется константа автопротолиза воды, входящая во многие формулы расчета рН. В результате при увеличении температуры скачок уменьшается и смещается в более кислую область. Ионная сила влияет незначительно.
В рассматриваемом случае расчет рН проводят по следующим формулам:
● Для сильной кислоты, например HCl, рН определяется концентрацией ионов водорода: [H+] = M кислоты.
● Для сильного основания, например КОН [H+] = 10 –14 / Mщелочи. Часто проводят титрование с использованием слабых электролитов.
При титровании слабой кислоты сильным основанием чем слабее кислота, тем больше значение рН в начале титрования. Следовательно, ветвь кривой титрования (рис. 3.5) до точки эквивалентности смещается в щелочную область. После достижения точки эквивалентности образуется сильное основание, следовательно, значение рН резко смещается в щелочную область. При дальнейшем титровании кривая изменяется незначительно.
В ходе титрования раствора уксусной кислоты сильным основанием значение pH все время остается выше, чем при тех же концентрациях соляной кислоты. В результате этого скачок на кривой начинается с более высокого значения рН. Заканчивается он, как и в первом случае, при рН = 10, так как титрование производят тем же раствором 0,1 моль/л NaOH.
Рис. 3.5. Ход титрования слабой кислоты сильным основанием
При титровании слабой кислоты сильным основанием pH раствора кислоты вычисляют с учетом ее константы диссоциации:
Интервал скачка рН на кривой титрования 0,1 мольл уксусной кислоты раствором 0,1 мольл NaOH значительно уже предыдущего случая. Он простирается от рН = 7,8 до рН = 10.
При титровании слабого основания сильной кислотой интервал скачка уменьшается в щелочной области рН. Рассчитывается рН в этом случае следующим образом:
При титрование слабой кислоты слабым основанием (или наоборот) сужение интервала скачка рН происходит и в кислотной, и в щелочной областях рН. Вследствие этого интервал скачка рН на кривой вовсе исчезает. Пример — нейтрализация раствора 0,1 моль/л СН3СООН раствором 0,1 моль/л NН4ОН. Кривая титрования не имеет скачка рН. Поэтому нельзя ожидать и резкого изменения окраски индикаторов. Титрование слабой кислоты слабым основанием вообще невозможно.
Индикаторы метода кислотно-основного титрования. Теории индикаторов
Индикаторы — вещества, которые резко реагируют на изменение концентрации определяемого компонента или титранта вблизи точки эквивалентности. В методах кислотно-основного титрования для определения конечной точки титрования используют кислотноосновные индикаторы (табл. 3.1). Это органические вещества, способные видимо и обратимо изменять свою окраску в растворе при изменении рН среды.
Кислотно-основные индикаторы изменяют свою окраску в области интервала перехода независимо от того, достигнута ли точка эквивалентности. Правильно выбранный индикатор изменяет окраску в области скачка титрования. У неправильно выбранного индикатора изменение окраски может происходить задолго до наступления точки эквивалентности или после нее.
Таблица 3.1 Характеристики кислотно-основных индикаторов
Выбирают индикатор с помощью кривой титрования. Для этого на график наносят интервал перехода индикатора. У правильно выбранного индикатора интервал перехода полностью или частично перекрывается скачком титрования. Если такого перекрывания нет, то индикатор для данного титрования не подходит. Значение рН, при котором заканчивается титрование с данным индикатором, называют показателем титрования и обозначают рТ. Показатель титрования находится обычно в середине интервала перехода индикатора. Существуют различные теории индикаторов, каждая из которых по-своему объясняет поведение кислотно-основных индикаторов в кислых и щелочных средах.
Ионная теория индикаторов. В связи с тем, что кислотно-основные индикаторы представляют собой слабые кислоты или слабые основания, любой индикатор диссоциирует в растворе согласно уравнению:
HInd = Н+ + Ind — (бесцветный — малиновый).
Изменение окраски индикаторов происходит при прибавлении к любому раствору любой кислоты или щелочи влечет за собой изменение концентрации ионов Н+ в нем, а следовательно, и величины рН. Перемена окраски у индикаторов также связана с изменением рН раствора. Однако каждый индикатор изменяет окраску только в определенном, характерном для него интервале значений рН. Объясняется это тем, что окраска индикатора зависит от соотношения концентраций его диссоциированной и недиссоциированной форм, т. е.
Если к раствору фенолфталеина прибавить щелочь и довести рН раствора до 8, то соотношение [HInd] / [Ind−] = 10 –8 /10 –9 уменьшится в 10 раз и раствор станет бледно-розовым. При рН = 9 соотношение [HInd] / [Ind−] = 10 –9 /10 –9 = 1,0, т. е. в растворе присутствуют равные количества бесцветных молекул индикатора и окрашенных в красный цвет ионов, при этом раствор приобретает розовую окраску. Следовательно, цвет водного раствора индикатора определяется соотношением концентрации его молекулярной и ионной форм, отличающихся различной окраской, и зависит от [Н+].
Техника титрования
Правильное определение точки эквивалентности при титровании зависит не только от выбора индикатора, но и от порядка титрования. По методу нейтрализации титруют растворы кислот растворами оснований или наоборот. Этот порядок следует учитывать при выборе индикатора. Например, если титруют кислоту основанием и в качестве индикатора используют метиловый оранжевый (или метиловый красный), то розовая окраска индикатора от избыточной капли щелочи должна перейти в желтую.
Такое изменение окраски гораздо хуже улавливается глазом, чем переход ее из желтой в розовую. Поэтому с метиловым оранжевым (или метиловым красным) рекомендуют титровать растворы оснований растворами кислот. С фенолфталeином удобнее титровать растворы кислот растворами оснований, так как при этом бесцветный раствор становится малиновым.
Следует заметить, что при использовании индикаторов для фиксирования конечной точки титрования возможно появление индикаторной ошибки. Она образуется в случае несовпадения рН раствора в точке эквивалентности и рТ индикатора. Если такое несовпадение имеет место, то раствор обычно либо несколько перетитровывают, либо, наоборот, недотитровывают. Для уменьшения индикаторной ошибки титрование проводят с так называемым свидетелем. В запасную коническую колбу (или стакан) наливают дистиллированную воду в количестве, приблизительно равном объему жидкости, получающейся в конце титрования. Прибавляют к воде столько же капель индикатора, например метилового оранжевого, сколько и к титруемому раствору, и приливают из бюретки 1−2 капли кислоты, вызывающей слабое порозовение раствора. Приготовленный таким образом свидетель используют в качестве образца при титровании, добиваясь, чтобы окраска анализируемого раствора и свидетель была одинакова. С помощью свидетель вводят также поправку в результаты титрования на прибавленный избыток кислоты, т. е. из затраченного ее объема вычитают объем двух капель (0,04 мл), использованных на окрашивание индикатора в свидетель.
Правильное определение точки эквивалентности зависит от количества прибавленного индикатора. Иногда стараются прилить побольше индикатора, полагая, что большая интенсивность окраски раствора облегчит определение точки эквивалентности. Но чем больше прибавлено индикатора, тем труднее заметить изменение окраски, так как оно будет происходить медленнее. Для установления конечной точки титрования имеет значение не столько яркость окраски раствора, сколько четкость ее изменения. Опытным путем найдено, что на 10–15 мл анализируемого раствора следует брать одну каплю раствора индикатора, а на 25 мл — не более двух капель.
Таким образом, результат объемного определения зависит не только от выбора индикатора, но также от его взятого количества и от принятого порядка титрования.