Для чего сдавать кровь на биопсию
Биопсия в диагностике рака
Рак представляет собой группу заболеваний. Их объединяет общий признак: клетки в организме начинают бесконтрольно делиться. В результате развивается злокачественная опухоль, так или иначе влияющая на окружающие ткани.

Когда развивается рак, этот упорядоченный процесс нарушается. Клетки становятся аномальными, старые или поврежденные продолжают функционировать, а новые формируются, даже когда в этом нет необходимости. Иммунная система по каким-то причинам не успевает реагировать и блокировать такое деление. Так дополнительные клетки размножаются без остановки и объединяются в опухоли.
Некоторые виды рака – это злокачественные образования, они представляют собой определенный массив ткани, который может прорастать в соседние органы или давить на них, что и дает клинические проявления. Также по мере роста клетки могут отделяться от первичной опухоли, распространяться по лимфатическим или кровеносным сосудам и формировать новые очаги – близлежащие или отдаленные метастазы.
В отличие от злокачественных доброкачественные опухоли не распространяются или не проникают в близлежащие ткани. Однако они могут достигать значительных размеров. После их удаления возможно развитие рецидивов.
Что такое биопсия при раке
Для подтверждения диагноза онкозаболевания необходимо сделать анализ на наличие раковых клеток, которые отличаются от нормальных строением, степенью дифференцировки и размерами.
Биопсия клеток – это базовое исследование при подозрении на рак. Заключается в изъятии образца ткани для ее изучения. Для такого анализа возможен забор небольшого фрагмента иглой или хирургическим путем.
Большинство биопсий выполняются в амбулаторных условиях, без особой подготовки. Обычно это делается под контролем ультразвука, рентгена, КТ или МРТ. Такая визуализация делает исследование прицельным и безопасным.
Когда назначают биопсию
Процедура показана при обнаружении подозрительного образования. Она позволяет определить степень его злокачественности, природу и структуру. В отдельных случаях помогает выявить другие состояния: инфекции, воспалительные и аутоиммунные нарушения.
Исследовать возможно практически любой орган или ткань:
Как выполняется процедура
Биопсия различается по методам забора материала (биоптата):
Обычно биопсия проходит в амбулаторных условиях под местной анестезией. Иногда выполняется в процессе оперативного вмешательства (интраоперационная). Ее результаты могут повлиять на дальнейшую тактику ведения пациента.
Хотите мы вам перезвоним?
Как исследуется материал
После того, как ткань собирается, ее отправляют в лабораторию для анализа. Там проводят гистологическое (если возможно) и цитологическое исследование.
Подготовка к исследованию
Перед тем, как сделать биопсию, проводят лабораторные и инструментальные методы исследования, которые помогают в диагностике заболевания.
Если предполагается амбулаторная процедура, то специальная подготовка и пребывание в стационаре не требуется. Пациенту рекомендуют не есть и не пить до исследования, если нужна будет анестезия.
Временно отменяются противосвертывающие средства и другие препараты, которые могут вызвать кровотечение в послеоперационном периоде. Также врач может назначить седативные препараты.
Противопоказания к биопсии
Преимущества пункционной или игольной биопсии
Это надежный метод получения образцов тканей, который помогает определить, развивается ли опухоль и какова ее природа.
Пункционная биопсия менее травматична, чем хирургическое вмешательство, которое предполагает разрезы на коже, а также местную или общую анестезию.
Как правило, процедура безболезненная, а результаты такие же точные, как при удалении образца ткани хирургическим путем.
Время восстановления небольшое, пациенты не нуждаются в госпитализации.
Биопсия рака в онкологическом центре «СМ-Клиника»

Биопсия как заключительное диагностическое исследование назначается после консультации онколога и изучения результатов дополнительных обследований. Возможно как самообращение, так и по направлению из других медицинских учреждений.
Большой опыт наших врачей позволяет провести исследование максимально точно и профессионально. Для этого клиника оснащена всем необходимым специальным оборудованием, включая лапароскопы и эндоскопы. Гистологическое и цитологическое исследование образцов проводится в собственной лаборатории, поэтому результаты онкологи получают без задержек.
Чаще всего, это амбулаторная процедура. Но при необходимости пациент может оставаться под наблюдением еще несколько часов.
Если показано лапароскопическое или хирургическое вмешательство, то оно проводится в условиях стационара.
После того, как диагноз установлен, определяется тактика дальнейшего наблюдения и лечения. В нашем онкологическом центре возможно комплексное лечение опухолевых заболеваний, а также реабилитация.
Онкологический центр «СМ-Клиника» проводит диагностическую биопсию в Москве, но принимает жителей и других городов. Достаточно позвонить и записаться на консультацию к онкологу.
Почему назначили биопсию и нужно ли специально к ней готовиться?
Биопсию просто так пациенту не назначают. Обычно основной причиной, почему она требуется, является наличие патологических изменений в тканях или органах человека. Различное оборудование и расходные материалы для проведения этой процедуры вы можете купить на сайте Биопси Медикал.
Когда назначают биопсию пациенту?
Биопсия – это взятие образца ткани подозрительного с медицинской точки зрения участка с целью проведения его комплексной диагностики (могут использоваться методы компьютерной томографии, магнитно-резонансной томографии).
Чаще всего биопсию назначают именно для подтверждения или опровержения диагноза онкология. Только после проведения анализа ткани медицинские специалисты могут говорить о природе образования, подтвердить или опровергнуть факт его злокачественности. При этом часто этот вид исследования назначается на стадии ранней диагностики. Своевременное исследование позволяет предупредить дальнейшее развитие болезни.
Какие есть причины проведения биопсии?
Медики выделяют несколько основных причин, по которым требуется проведение биопсии. В частности, это:
· Подтверждение или опровержение факта злокачественности новообразования.
· Определение локализации опухоли, ее природы.
· Рассмотрение вопроса: насколько «агрессивно» ведет себя опухоль.
· Определение процессов патологического характера в различных органах: легких, молочной железе, пищеварительном тракте, а также в мягких тканях и так далее.
Нужно ли готовиться к проведению биопсии?
Ответ на этот вопрос однозначный – да. Перед процедурой врач обычно выписывает направление на проведение анализа мочи и крови. В некоторых случаях дополнительно назначается ультразвуковое или магнитно-резонансное обследование – зависит от особенностей болезни.
Специалисты отмечают, что очень важно исключить различные препараты, способствующие разжижению крови. Но самостоятельно нарушать комплексное лечение не стоит. Необходимо проконсультироваться с лечащим специалистом по этому вопросу. Если не получается по каким-то причинам оставить прием препаратов, то процедура биопсии будет проводится под еще большим контролем врачей. Также необходимо исключить примем спиртных напитков, курение, прием жирной пищи хотя бы за несколько дней до проведения биопсии. Не рекомендовано заниматься активно спортом и в целом перетруждаться.
Что такое биопсия под УЗИ-навигацией?
Что такое биопсия?
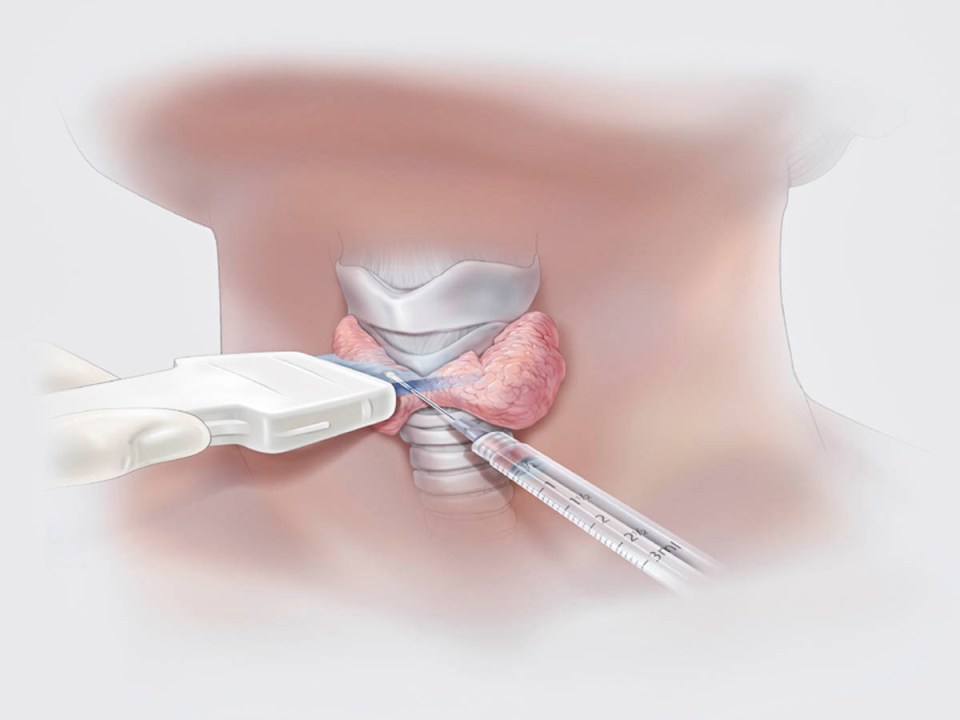
Биопсия – это взятие образцов тканей и клеток человека для последующей диагностики. Биопсия назначается пациентам в случае подозрения на онкологическое заболевание. Во время исследования врач вводит в подозрительное новообразование тонкую иглу, именно с ее помощью осуществляется забор исследуемого материала.
В большинстве случаев биопсия проводится под ультразвуковым наблюдением, т.е. игла вводится под контролем УЗИ-аппарата. Это позволяет точно визуализировать патологическое новообразование, а также кровоток вокруг него (чтобы не повредить сосуды и предотвратить образование гематом).
Когда пациента направляют на биопсию?
Если в ходе приема врач любой специализации обнаруживает у человека образование, то он направляет пациента к онкологу. Специалист определит характер новообразования – доброкачественное или злокачественное. В этом ему поможет ряд исследований, среди них – имуногистохимическое, гистологическое (тканевое) и/или цитологическое (клеточное). Чтобы это осуществить, онколог направит пациента на биопсию, т.е. забор клеток и тканей новообразования.
Какие виды биопсии бывают?
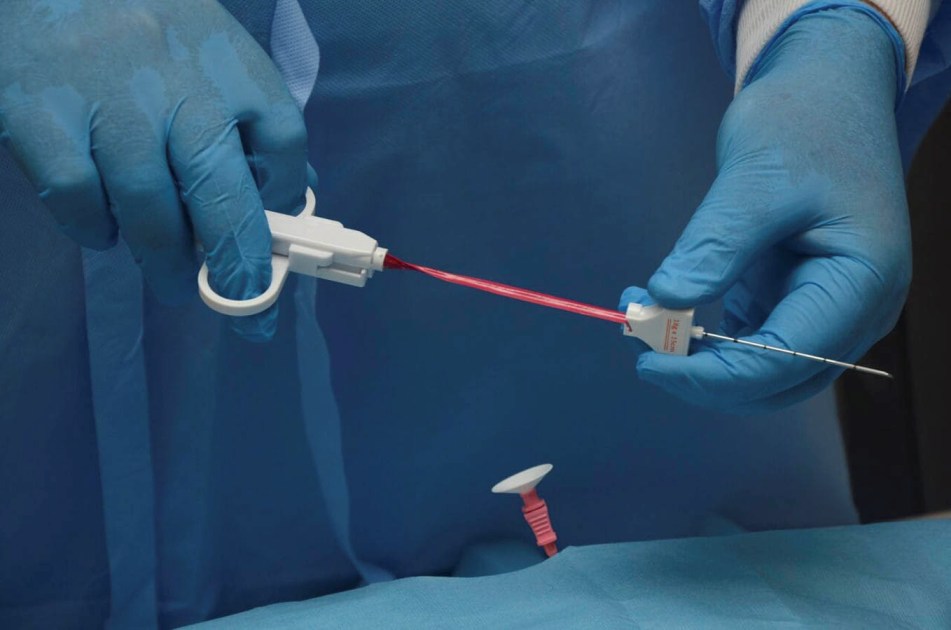
Пункционная тонкоигольная. Во время манипуляции в новообразование вводится тонкая игла и производится забор материала для цитологического (клеточного) исследования.
Трепан-биопсия. Выполняется под местной анестезией. Во время манипуляции врач вводит в новообразование специальную трепан-иглу и выполняет забор гистологического (тканевого) материала.
Стереотаксическая биопсия. Это более сложная манипуляция, которая проводится в операционной. С помощью специальных аппаратов врачи делают снимки исследуемой локализации. Снимки накладываются друг на друга, что позволяет получить объемное изображение. На его основе специалисты выбирают место введения иглы.
На каких органах проводится биопсия под УЗИ-навигацией?
Данная манипуляция проводиться на молочной железе, щитовидной железе, лимфоузлах различной локализации. Ее применяют для пункции патологических очагов в глубоко расположенных органах (печень, поджелудочная железа, селезенка, почки, опухоли грудной клетки, малого таза, забрюшинного пространства).
Как осуществляется биопсия?
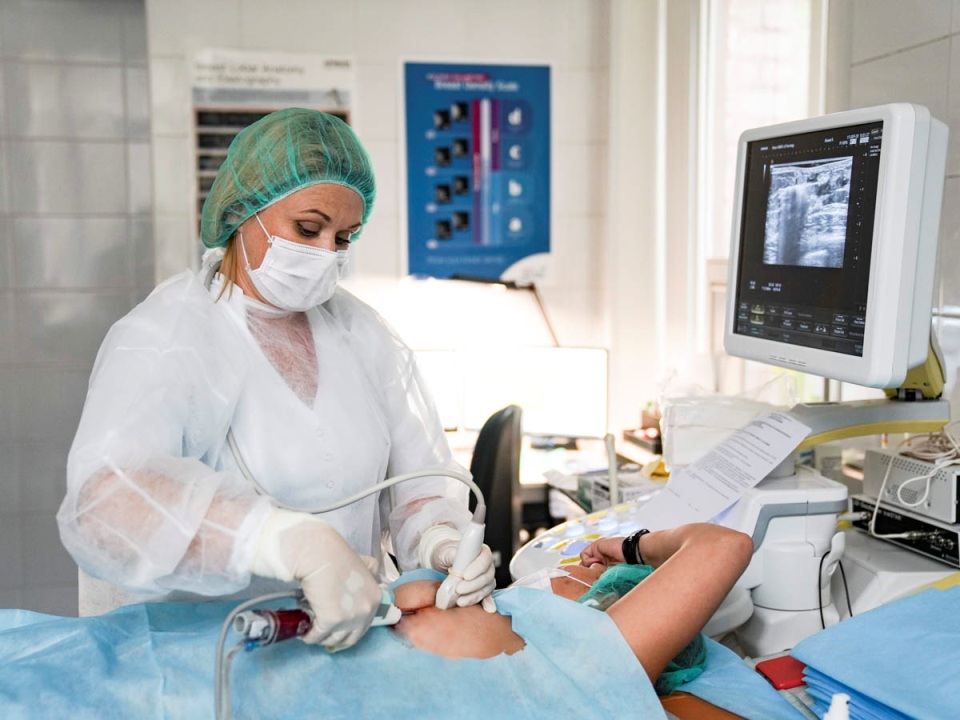
Пациент во время манипуляции находится в положении лежа. Предварительно врач выполняет обезболивание. В большинстве случаев достаточно местной анестезии. Специалист проводит контрольное УЗИ, определяет точное месторасположение новообразования. После того, как анестезия подействует, врач осуществит забор тканей патологического участка. Чаще всего пациент не испытывает болезненные ощущения, но может чувствовать легкое надавливание, жжение, покалывание. Когда забор материала произведен, врач извлекает иглу, а место прокола обрабатывает анестетиком. В некоторых случаях рекомендуется приложить холод на 30-40 минут.
Как быстро заживет прокол?
Разрез от иглы заживает быстро – около 2-3 дней. Один-два дня после манипуляции лучше избегать сильных физических нагрузок и занятий спортом.
Куда направляется биоматериал, полученный во время биопсии?
После выполнения биопсии полученные фрагменты тканей направляют в лабораторию, где проводится их гистологический(тканевый) и/или цитологический(клеточный) анализ. Исследование выполняется в срок от 14 до 45 дней. На основе полученного гистологического и/или цитологического исследования, лечащий врач выберет дальнейшую тактику лечения или наблюдения.
Список литературы:
Hederstorm E, Forsberg L, Floren CH et al. Liver biopsy complications monitored by ultrasound. Hepatol. 1989. Vol. 8. P. 94.4.
Ткачев В.Д., Логинов А.Г., Аруин Л.И. Современные представления о роли чрескожной биопсии печени в клинической практике. Хронический гепатит. Сб. науч. тр. М., 1988. С. 71.
Алауи Аль-Асс Абдулмаджид. Ультразвуковая диагностика и мини-инвазивные вмешательства при объемных образованиях брюшной полости. Автореф. дис. … канд. мед. наук. Саранск, 2004. С. 17.
Авторская публикация:
Мамедова Сабина Камрановна, врач ультразвуковой диагностики консультативно-диагностического Центра ФГБУ «НМИЦ онкологии им. Н.Н. Петрова» Минздрава России
Для чего сдавать кровь на биопсию
Жидкая биопсия в персонализированном лечении онкологических пациентов
Жидкая биопсия является неинвазивным методом для характеристики генома опухоли пациента на основании периферической крови путем анализа циркулирующей опухолевой ДНК (ctDNA). Жидкие биопсии имеют огромный потенциал для молекулярного профилирования, прогнозирования и мониторинга опухолей. Они может обеспечить значительное улучшение персонализированного ведения пациентов с онкологическими заболеваниями. В настоящее время эта область находится в интересном периоде трансформации, когда анализ ctDNA начинает применяться в клинической практике, хотя о его биологии еще предстоит узнать многое. В данной обзорной статье кратко представлены современные технологии и появляющиеся новые концепции, которые могут способствовать дальнейшему развитию области применения жидкой биопсии.
Сравнение жидкой биопсии и тканевой биопсии, которые дополняют друг друга в молекулярно- патологической диагностике
Параметры
Техника выполнения
— возможно проведение серии анализов
— более высокий риск, в зависимости от места забора материала
— сложное проведение серийных анализов
Биология
— отсутствие морфологического коррелята
— репрезентативность всей опухоли
— наличие морфологического коррелята
— репрезентативность для отдельных мелких участков опухоли
Предварительная методика анализа
— возможность простой стандартизации
— отсутствие квалификационных испытаний, специальной обработки
— установленная процедура обработки и анализа тканей
Клиническая значимость
— репрезентативность при наличии нескольких очагов опухоли
— отсутствие информативности в случае отсутствия мутации
— отсутствие репрезентативности при гетерогенности опухоли
— информативность даже при отсутствии мутации
Что такое жидкая биопсия?
Возможности использования и потенциал жидких биопсий
Метод жидкой биопсии используется в онкологии и связанной с ней молекулярной диагностике опухолей для различных целей. Биопсия крови у онкологических пациентов позволяет получить потенциально полезную информацию о диагностических, предикативных и, возможно, прогностических биомаркерах. Важнейшими областями применения являются определение терапевтических структур-мишеней и механизмов резистентности. Хотя наблюдение за прогрессированием заболевания (мониторинг опухоли) все еще находится на ранней стадии, в настоящее время оно становится многообещающим методом наблюдения за онкологическим пациентом, например, для оценки состояния ремиссии и раннего выявления и лечения пациентов с рецидивом или прогрессированием заболевания. Еще не полностью подтвержденные применения жидкой биопсии включают оценку риска опухолевых заболеваний, скрининг здоровых людей для раннего выявления рака, дифференциальную диагностику обнаруженных злокачественных новообразований, определение прогноза и анализ всего спектра гетерогенности опухолей.
В целом, анализы цоДНК в идеале должны проводиться в случае клинически выраженного прогрессирования заболевания, а не до тех пор, пока пациент все еще реагирует на целевую терапию. Если опухоль реагирует на терапию, концентрации цоДНК в крови пациента обычно снижаются, и поэтому обнаружение цоДНК становится намного более сложным.
Предиктивная диагностика мутаций на основе крови для оценки таргентной терапии («сопутствующая диагностика»)
Перед использованием таргентной терапии настоятельно рекомендуется диагностика молекулярных мутаций («сопутствующая диагностика»). Анализ с помощью жидкой биопсии подходит для этой цели, если обычная биопсия или цитологический материал недостаточны из-за низкого содержания опухолевых клеток для диагностики генеза опухоли. Кроме того, этот метод может использоваться в труднодоступных очагах опухоли или у пациентов с сопутствующими заболеваниями, которые делают невозможным инвазивное взятие проб. В ходе заболевания и при прогрессировании опухоли часто встречаются множественные опухолевые участки и метастазы, которые могут быть генетически гетерогенными. В данном случае жидкая биопсия обладает преимуществом отграничения освобожденной цоДНК от всех проявлений опухоли и, таким образом, обеспечения репрезентативного молекулярно-генетического профиля опухоли даже в случае генетической гетерогенности (см. таблицу).
Оценка клинической пользы анализа цоДНК по сравнению с обычными биопсиями опухолевой ткани для комплексного генотипирования опухоли еще не является окончательной, поскольку отсутствуют проспективные данные клинических исследований. В настоящее время применение на практике жидких биопсий ограничивается выявлением мутаций рецептора эпидермального фактора роста (EGFR) у пациентов с немелкоклеточным раком легких и мутаций саркомы Кирстен-рат (KRAS) у пациентов с колоректальной карциномой.
Жидкие биопсии имеют высокую положительную, но низкую отрицательную прогностическую ценность. Например, обнаружение мутации EGFR из крови можно использовать в качестве прогностического маркера для прогнозирования ответа на таргентную терапию ингибиторами тирозинкиназы, но при отсутствии мутации EGFR в крови образец ткани обязательно должен быть дополнительно изучен. Случаи, в которых мутация EGFR не обнаруживается при жидкой биопсии, но обнаруживается при биопсии тканей опухоли, относительно распространены, и, следовательно, при отсутствии признаков мутации в крови обязательно следует искать подтверждение ее наличия в опухолевой ткани.
Жидкая биопсия в молекулярной диагностике в условиях резистентности
Интересной и многообещающей областью применения жидкой биопсии является выявление возникающих мутаций резистентности при прогрессировании опухоли после терапии с целью адаптации дальнейшего лечения. Жидкая биопсия играет важную роль в поиске мутации резистентности к p.T790M в гене EGFR при таргентной терапии немелкоклеточного рака легких. Дополнительный молекулярный тест для обнаружения этой мутации устойчивости к p.T790M-EGFR может быть выполнен быстро и надежно на основе цоДНК из плазмы крови. Однако чувствительность этого метода составляет всего около 60-70%, поэтому в этой ситуации при отсутствии доказательств мутации устойчивости к EGFR следует сделать повторную биопсию или забор цитологического материала из прогрессирующего очага опухоли.
Молекулярный мониторинг опухолей
Мониторинг опухолей с помощью жидкостной биопсии особенно интересен, поскольку, с одной стороны, он может обнаруживать рецидивы очень рано, а с другой стороны, он также может быть использован для расшифровки факультативно измененного молекулярно-генетического профиля рецидивирующей опухоли. Если во время терапии обнаруживаются мутации резистентности, прогноз пациента может быть улучшен путем изменения таргентной терапии. Примерами использования жидкой биопсии в мониторинге являются контроль терапии у пациенток с раком молочной железы и у пациентов с раком легких. Для этих опухолевых образований удалось продемонстрировать, что увеличение известной драйверной мутации в крови сопровождается рецидивом. Таким образом, использование жидких биопсий позволяет осуществлять мониторинг терапии в режиме реального времени. Однако клиническая значимость жидкой биопсии в этом контексте все еще слишком ограничена, чтобы оправдать ее широкое использование в практической диагностике.
Жидкая биопсия как прогностический параметр
Преимущества жидкой биопсии
Наиболее важное преимущество жидкой биопсии очевидно: вместо инвазивного забора образца достаточно взять образец крови для мутационного анализа опухоли (см. таблицу). По сравнению с классической биопсией ткани, жидкие биопсии гораздо более просты в заборе и, следовательно, менее рискованны и менее обременительны для пациента, особенно когда необходимо периодически исследовать образцы тканей, прежде всего, в рамках последующего наблюдения. Таким образом, данный метод особенно подходит для видов рака, при которых биопсия иглой сопровождается риском, например, при опухолях легких. Благодаря простой процедуре забора проб жидкая биопсия может быть проведена последовательно без каких-либо проблем и, таким образом, позволяет документировать процесс. Теоретически, такие жидкие биопсии дают полную информацию об опухолевой нагрузке у пациента, так как этот метод может использоваться для исследования всей опухолевой ДНК, присутствующей в кровотоке пациента. Это еще одно преимущество по сравнению с биопсией ткани, при которой в конкретном анатомическом месте исследуется только одна область поражения, которая не обязательно является репрезентативным из-за неоднородности опухоли.
Жидкие биопсии и биопсии тканей сравнимы с точки зрения технической сложности, так что никакого существенного увеличения затрат на их проведение не возникает.
Проблемы и ограничения жидкой биопсии
Жидкая биопсия в настоящее время используется в рутинной диагностике только для решения отдельных клинических задач, поскольку данный метод еще имеет некоторые неточности, препятствующие его широкому использованию.
Бесклеточная циркулирующая опухолевая ДНК обнаруживается только примерно у 75% пациентов с метастатической опухолевой болезнью, при этом имеются значительные различия между различными формами опухоли и стадиями опухоли. Концентрация цоДНК особенно низка при карциномах почечных клеток, предстательной и щитовидной железы, а также при опухолях головного мозга (из-за гематоэнцефалического барьера) даже при метастазировании, поэтому диагностировать ее не всегда удается. Даже у пациентов с локализованным опухолевым поражением (стадия I) частота обнаружения цоДНК значительно ниже.
Другая проблема с анализом цоДНК в обычной молекулярной патологии заключается в том, что до сих пор не существует маркера, который мог бы надежно отличить цоДНК из опухолевых клеток от сцДНК из здоровых клеток. Только обнаружение мутации, известной по первичной опухоли, дает уверенность в том, что исследование сработало, и результат теста имеет клиническую значимость. Однако если в жидкой биопсии не обнаружено никакой известной мутации, то либо в крови отсутствует цоДНК, либо чувствительность метода анализа слишком низкая для обнаружения существующей цоДНК. Также проблематичным в этом контексте является потенциальное высвобождение мутированной ДНК из доброкачественных, воспалительных наслаивающихся поражённых участков (например, меланоцитарный невус кожи, кишечный полип). Третье ограничение заключается в том, что обнаружение цоДНК в крови не позволяет сделать выводы о том, где располагается опухоль и какой орган поражен. Это должно быть дополнительно изучено при помощи визуализационной диагностики.
Открытые вопросы в исследовании
Обнаружение транслокаций (слияний генов) лучше всего проводить на уровне мРНК из крови. Однако циркулирующая мРНК свободной опухоли в крови состоит из очень коротких фрагментов (в среднем 40 базовых пар), которые не подходят для выявления мутаций. Таким образом, анализ мРНК опухоли в настоящее время проводится на экзосомах, но этот метод еще не готов для использования в клинической практике. Все это показывает, что, хотя метод ликвидной биопсии имеет много применений, он еще не созрел и все еще находится на стадии тестирования. Из-за методологических ограничений жидкие биопсии, предположительно, никогда не достигнут качества и информативности исследований опухолевой ткани, но дополняют их и имеют свое значение в персонализированной молекулярной диагностике и мониторинге опухолевых заболеваний. Другим критическим аспектом все еще является отсутствие стандартизации технологий выделения и анализа цоДНК и управления качеством обработки образцов (см. таблицу).
Резюме и перспективы
Жидкая биопсия и классическая биопсия ткани дополняют друг друга в молекулярном анализе опухолей. В будущем метод жидкой биопсии может даже частично заменить классические биопсии тканей. Однако в настоящее время эта процедура еще недостаточно разработана для широкого использования в рутинной диагностике. В частности, клиническая интерпретация результатов представляет серьезные проблемы для использования данного метода в повседневной клинической практике. Однако ожидается, что растущее понимание биологической основы цоДНК и других многообещающих биомаркеров периферической крови, а также новых методов анализа прочно утвердит жидкую биопсию в повседневной клинической практике, что значительно улучшит ведение онкологических пациентов.
Следует запомнить
По этим причинам используемые в настоящее время технологии жидкой биопсии все еще слабо стандартизированы и, следовательно, пока не подходят для широкого использования в рутинной диагностике.