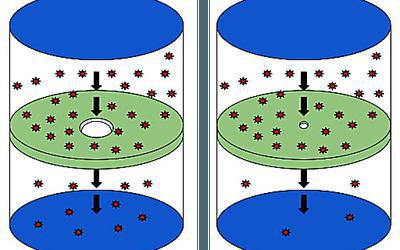
Доказать что молекулы движутся
Какие явления подтверждают движение молекул: диффузия
Научные опыты, с давних пор проводимые учеными всего мира, однозначно доказали, что частицы, из которых состоят все тела, находятся в постоянном движении.
Учение об этих мельчайших частичках, из которых состоит любое вещество (твердое, жидкое, газообразное), возникло в эпоху расцвета древних культур задолго до нашей эры. Знаменитые ученые и философы Демокрит, Эпикур, Анаксагор, Лукреций и другие сходились во мнении, что все состоит из мельчайших неделимых атомов, и разнообразные атомы образуют соответствующие разнообразные вещества. Ответ на вопрос: «Какие явления подтверждают движение молекул?» был найден позднее. В современную молекулярно-кинетическую теорию эти зародыши идей начинают оформляться только в XVIII веке нашей эры.
Какие явления подтверждают движение молекул?
Догадываться о том, что молекулы хаотично движутся, ученые начали давно. Но чтобы догадки стали чем-то более серьезным и получили научное обоснование, физики должны были себе и всему миру ответить на вопрос: «Какие явления подтверждают движение молекул?»
Диффузия
Диффузия — это взаимное проникновение молекул одного вещества в межмолекулярные пустоты другого вещества. В переводе с латыни термин «диффузия» обозначает «растекание, распространение».
Частицы, из которых состоят тела (газообразные, жидкие, твердые), находятся на определенном расстоянии друг от друга и постоянно движутся.
Интересно, что большую часть объема всякого тела занимает свободное пространство. Чтобы понять масштаб, можно представить ядро атома в виде небольшого лесного ореха, тогда орбиты электронов этого атома будут приблизительно равны размерам большого катка или огромного бассейна.
Диффузия в газах
Быстрее всего происходит движение молекул в газах. При этом частицы движутся хаотично.
Диффузия в жидкостях
Связь между молекулами жидкостей более прочная, чем в газах.
Диффузия в твердых телах
Движение молекул в твердых телах протекает очень медленно. Но все же, если, например, наплавить небольшое количество золота на свинцовый стержень и оставить его так при температуре не менее 300 градусов, то по прошествии суток молекулы золота проникнут в межмолекулярные пустоты свинца примерно на сантиметр.
Диффузия в условиях нагревания
При нагревании диффузия происходит намного быстрее, следовательно, можно сделать вывод, что чем выше поднимается температура тела, тем выше становится скорость движения молекул. Соответственно, чем быстрее движутся молекулы, тем выше поднимается температура тела. При температуре, близкой к абсолютному нулю, скорость движения частиц максимально снижается.
Примеры диффузии
Примеры диффузии встречаются в быту, в промышленности, в жизни человека и животных:
Диффузия: тест
Ответы: I — а; II — б; III — а; IV — а; V — в; VI — б; VII — б.
Тепловые явления, в принципе, можно объяснить и
без гипотезы движения молекул.
Броуновское движение НЕ доказывает, а только позволяет
ПРЕДПОЛОЖИТЬ, что причиной хаотического движения
частиц служит движение молекул. Размер броуновских
частиц может быть больше, чем размер микроорганизмов
или простейших, которые тоже могут толкать эти частицы.
самый простой. в кружку с горячим чаем кинь сахар и оставь. сахар со временем растворится.
тепло и тепловыделение
Диффузия происходит и в твердых телах. Это доказывает такой опыт: две отполированные плоские пластинки из золота и свинца, положенные друг на друга, выдерживались при комнатной температуре в течение 5 лет. За это время пластинки срослись, образовав единое целое, причем молекулы золота проникли в свинец, а молекулы свинца — в золото на глубину до 1 см.
Скорость диффузии зависит от агрегатного состояния вещества и температуры. С повышением температуры скорость диффузии возрастает, а с понижением — уменьшается.
Диффузия, как и броуновское движение, является наглядным доказательством непрерывного движения молекул во всех веществах
тело двигается и молекулы в мести с ни тоже двигаются.
Броуновское движение
7 класс, без форм заявки
Молекулярно-кинетическая теория
Мы состоим из клеток, клетки состоят из молекул, молекулы из атомов, атомы из… Ладно, пока достаточно атомов. И молекулы, и атомы подчиняются законам, которые описаны в молекулярно-кинетической теории.
В основе молекулярно-кинетической теории лежат три основных положения:
Броуновское движение
Во второй половине ХIХ века в научных кругах разгорелась нешуточная дискуссия о природе атомов. На одной стороне дискуссии утверждали, что атомы — просто математические функции, удачно описывающие физические явления и не имеющие под собой реальной физической основы.С другой стороны настаивали, что атомы — это реально существующие физические объекты.
Самое смешное в этих спорах то, что за десять лет до их начала ботаник Роберт Броун уже провел эксперимент, который доказал физическое существование атомов. Вот, как это было:
Как Броун проводил эксперимент
Броун изучал поведение цветочной пыльцы под микроскопом и обнаружил, что отдельные споры совершают абсолютно хаотичные движения.
Представьте себе, что мы издалека наблюдаем, как плотная толпа людей толкает над собой большой мяч. Причём каждый толкает мяч, куда хочет. Мы не видим отдельных игроков, потому что поле далеко от нас, но мяч мы видим — и замечаем, что перемещается он очень беспорядочно.
Мяч постоянно меняет направление своего движения, и пойти в какую-нибудь определенную сторону не желает. Предсказать его местоположение через заданное время — нельзя.
Вот что-то похожее на это Броун увидел при изучении пыльцы.
В первую очередь он начал грешить на движение потоков воды или ее испарение, но проверив эту гипотезу, отмел ее. Проведя множество экспериментов, Броун установил, что такое хаотичное движение свойственно любым микроскопическим частицам — будь то пыльца растений, взвеси минералов или вообще любая измельченная субстанция. Но причины этого явления он выяснить не смог (не в обиду ботаникам, но все же, это не его специализация).
А теперь угадайте, кто смог применить этот эксперимент в доказательстве атомной теории строения вещества. Альберт Эйнштейн, кто же еще. Он объяснил его примерно так: взвешенная в воде спора подвергается постоянной «бомбардировке» со стороны хаотично движущихся молекул воды.
В среднем, молекулы воздействуют на нее со всех сторон с равной интенсивностью и через равные промежутки времени. Однако, как бы ни мала была частица, в силу чисто случайных отклонений сначала она получает импульс со стороны молекулы, ударившей ее с одной стороны, а затем — со стороны молекулы, ударившей ее с другой. И так далее.
Чуть позже, через 3 года после открытия Эйнштейна, в 1908 году французский физик Жан Батист Перрен провел серию опытов, которые подтвердили правильность эйнштейновского объяснения броуновского движения. Стало окончательно ясно, что наблюдаемое «хаотичное» движение броуновских частиц происходит вследствие межмолекулярных соударений. Поскольку вывод о том, что несуществующие в природе математические функции не могут привести к физическому взаимодействию, напрашивается сам собой, стало окончательно ясно, что спор о реальности атомов окончен: они существуют в природе.
Также, если еще раз посмотреть на второе положение молекулярно-кинетической теории, можно заметить, что броуновское движение очень хорошо его доказывает: Атомы и молекулы находятся в непрерывном хаотическом движении.
Диффузия
Явление, которое доказывает первое и второе положения молекулярно-кинетической теории называется диффузия.
Диффузия в газах
Если в комнате открыть флакон с духами или зажечь ароматизированную свечу, то запах вскоре будет чувствоваться во всей комнате. Распространение запахов происходит из-за того, что молекулы духов проникают между молекулами воздуха. На самом деле, в этом процессе очень большую роль играет такой вид теплопередачи, как конвекция, но и без диффузии не обошлось.
На самом деле, молекулы вокруг нас движутся очень быстро — со скоростью в сотни метров в секунду — это напрямую зависит от температуры.
Давайте проверим это сами несложным экспериментом:
Замерьте температуру воздуха в помещении. Распылите освежитель воздуха в одном углу, встаньте в другой и включите секундомер. А лучше проведите эксперимент вдвоем, чтобы один человек распылял, а другой включал секундомер — так не будет погрешности, но будет веселье 😉
Как только почувствуете аромат освежителя в противоположном от места распыления, выключите секундомер. Запишите результат измерения. А потом проветрите помещение и проделайте все то же самое. Время, через которое до вас дойдет запах, будет другим. Во втором случае аромат будет распространяться медленнее.
То есть, чем выше температура, тем больше скорость диффузии.
Диффузия в жидкостях
Если диффузия в газах происходит быстро — чаще всего за считанные секунды — то диффузия в жидкостях занимает минуты или в некоторых случаях часы. Зачастую это зависит от температуры (как и в эксперименте выше) и плотности вещества.
С диффузией в жидкостях вы встречаетесь, когда, например, размешиваете краску. Или когда смешиваете любые две жидкости, например, газировку с сиропом. Также из-за диффузии происходит загрязнение рек (да и в целом окружающей среды).
Ну или вот пример диффузии в жидкостях, с которым вы точно не встречались — акулы ищут свою жертву по запаху крови, который распространяется в океане за счет диффузии.
Диффузия в твёрдых телах
Диффузия в твёрдых телах происходит очень медленно. Например, при комнатной температуре (около 20 °С) за 4-5 лет золото и свинец взаимно проникают друг в друга на расстояние около 1 мм.
Кстати, если вы проведете такой эксперимент, то увидите, что в свинец проникло малое количество золота, а свинец проник в золото на глубину не более одного миллиметра. Такое различие обусловлено тем, что плотность свинца намного выше плотности золота.
Этот процесс можно ускорить за счет нагревания, как в жидкостях и газах. Если на тонкий свинцовый цилиндр нанести очень тонкий слой золота, и поместить эту конструкцию в печь на неделю при температуре воздуха в печи 200 градусов Цельсия, то после разрезания цилиндра на тонкие диски, очень хорошо видно, что свинец проник в золото и наоборот.
Презентация по физике на тему: «Доказательства существования и движения молекул»
Описание презентации по отдельным слайдам:
Движение молекул. Скорость движения молекул и температура тела. Диффузия.
Цель урока Расширить знания о строении вещества. Дать представление о процессе диффузии. Сформировать представление о диффузии в различных состояниях вещества. Продолжить формирование общих умений коммуникаций
Почему это происходит? Если в комнату внести какое-нибудь пахучее вещество, например эфир, то его запах через некоторое время будет ощущаться по всей комнате.
Распространение запаха объясняется движением молекул. Это движение носит непрерывный и беспорядочный характер.
Почему мы не можем почувствовать запах мгновенно?
Сталкиваясь с молекулами газов, входящих в состав воздуха, молекулы эфира много раз меняют направление своего движения и, беспорядочно перемещаясь, разлетаются по всей комнате.
Диффузия – это самопроизвольное перемешивание веществ.
Рассмотрите рис. 23 на стр. 21 в учебнике
То, что молекулы всех тел непрерывно и беспорядочно движутся, подтверждается и другими многочисленными опытами. Рассмотрим один из них.
ГАЗЫ Частицы газа далеко удалены друг от друга. Между ними существуют большие промежутки. Сквозь эти промежутки легко перемещаются частицы другого вещества. Поэтому диффузия в газах протекает быстро.
ЖИДКОСТИ Частицы в жидкости «упакованы» так, что расстояние между соседними частицами сравнимы с их размерами. Сами частицы могут скачкообразно перемещаться по всему занимаемому жидкостью объему сосуда. Перемешивание жидкостей происходит медленно.
ТВЕРДЫЕ ТЕЛА В твердых телах расстояния между частицами совсем маленькие. Они такие же, как размеры самих частиц. Проникновение через такие малые промежутки частиц другого вещества крайне затруднено и поэтому диффузия происходит очень медленно.
Давайте сделаем вывод о том, какова скорость диффузии в различных состояниях вещества.
Скорость протекания диффузии увеличивается с ростом температуры. От чего зависит скорость протекания диффузии?
1 Между частицами имеются промежутки Частицы вещества находятся в постоянном движении Явление диффузии можно объяснить лишь в том случае, если считать, что: Все вещества состоят из частиц 3 2
Воздух, как известно, представляет собой смесь газов. Однако вследствие диффузии на одной высоте от Земли состав атмосферы оказывается достаточно однородным.
Она широко используется в пищевой промышленности при консервировании овощей и фруктов, при засолке огурцов.
Диффузия в природе: Поддерживается однородный состав атмосферного воздуха вблизи поверхности Земли. Диффузия растворов различных солей в почве способствует нормальному питанию растений и т.д.
В чем состоит явление диффузии? Знаете ли вы какой-либо пример диффузии кроме тех, что были приведены на уроке?
Сформулируйте гипотезу о том, почему засолку производят горячей, а не холодной водой. Дать объяснение вашему предположению
вывод Скорость протекания диффузии увеличивается с ростом температуры
Рассмотрите рисунки и объясните – это явление.
Что общего между рисунком с игроками на футбольном поле и явлением диффузии?
Домашнее задание § 9, домашний эксперимент (стр. 23, задание 2)
Курс повышения квалификации
Дистанционное обучение как современный формат преподавания
Курс профессиональной переподготовки
Физика: теория и методика преподавания в образовательной организации
Курс профессиональной переподготовки
Методическая работа в онлайн-образовании
Ищем педагогов в команду «Инфоурок»
Номер материала: ДБ-1212751
Не нашли то что искали?
Вам будут интересны эти курсы:
Оставьте свой комментарий
Авторизуйтесь, чтобы задавать вопросы.
В России планируют создавать пространства для подростков
Время чтения: 2 минуты
Петербургский Политех создал отдельное меню для вегетарианцев в своих столовых
Время чтения: 1 минута
ДНР полностью перешла на стандарты и программы России в образовании
Время чтения: 1 минута
Путин поручил не считать выплаты за классное руководство в средней зарплате
Время чтения: 1 минута
В России предложили учредить День семейного волонтерства
Время чтения: 2 минуты
Учителям предлагают 1,5 миллиона рублей за переезд в Златоуст
Время чтения: 1 минута
Подарочные сертификаты
Ответственность за разрешение любых спорных моментов, касающихся самих материалов и их содержания, берут на себя пользователи, разместившие материал на сайте. Однако администрация сайта готова оказать всяческую поддержку в решении любых вопросов, связанных с работой и содержанием сайта. Если Вы заметили, что на данном сайте незаконно используются материалы, сообщите об этом администрации сайта через форму обратной связи.
Все материалы, размещенные на сайте, созданы авторами сайта либо размещены пользователями сайта и представлены на сайте исключительно для ознакомления. Авторские права на материалы принадлежат их законным авторам. Частичное или полное копирование материалов сайта без письменного разрешения администрации сайта запрещено! Мнение администрации может не совпадать с точкой зрения авторов.
Конспект урока «Молекулы. Движение молекул»
Выбранный для просмотра документ 8 класс_Урок №2_Молекулы. Движение молекул.doc
Молекулы. Движение молекул.
Цель урока: ввести понятие атома и молекулы, рассмотреть их движение в веществе; продемонстрировать опыт Штерна.
Повторение. Проверка домашнего задания.
Какие представления о строении вещества имели древнегреческие мыслители Демокрит и Эпикур?
Какие представления о строении вещества отражены в поэме Лукреция Кара «О природе вещей»?
Почему представления древнегреческих учёных о строении вещества долгое время оставались гипотезой и не могли превратиться в теорию?
Какие явления и опыты, описанные в параграфе, доказывают, что тела состоят из мельчайших частиц? Приведите свои примеры.
Какие опыты доказывают, что между частицами, из которых состоят тела, существуют промежутки?
Изучение нового материала.
Из опытов, которые были рассмотрены в предыдущем параграфе, следует, что вещество можно разделить на отдельные частицы. Возникает вопрос: до каких пор можно производить это деление? Оказывается, существует определённый предел деления вещества. Иными словами, существует самая маленькая частица, которая сохраняет свойства вещества.
Наименьшую частицу вещества, которая сохраняет его химические свойства, называют молекулой.
Слова «химические свойства» не являются новыми; они известны вам из курсов естествознания и химии. Рассмотрим, что значит «сохраняет химические свойства», на примере мела. Мел — это вещество, представляющее собой соединение кальция Са, углерода С и кислорода О (СаСО3). Это соединение имеет определённые химические свойства, в частности, оно может вступать в реакцию с каким-либо другим веществом. При этом и кусок мела, и молекула этого химического соединения будут вести себя в реакции одинаково. В этом смысле и говорят, что молекула сохраняет химические свойства данного вещества.
Слово «молекула» происходит от латинского слова «молекуле», что значит «маленькая масса».
Таким образом, можно сказать, что вещество состоит из молекул: мел состоит из молекул соединения кальция, сахар — из молекул сахара, вода — из молекул воды и т. д.
О 
Поскольку молекулы такие маленькие, то в теле их содержится очень много. Так, в 1 см 3 воздуха содержится 27∙10 18 молекул.
Для того чтобы получить представление о числе молекул в единице объёма и соответственно об их размерах, предположим, что имеется стакан воды и молекулы воды, находящейся в нём, определённым образом помечены. Выльем эту воду в Чёрное море. Будем считать также, что вода в море равномерно перемешалась. Зачерпнём из моря в любом месте стакан воды и увидим, что в нём окажутся сотни меченых молекул воды.
Возникает вопрос: можно ли молекулу разделить на отдельные частицы? Оказывается, можно! Молекула воды, например, состоит из водорода и кислорода. Однако водород и кислород уже другие вещества, и они обладают свойствами, отличными от свойств воды. Разделить молекулу воды на такие вещества можно в процессе химической реакции.
Частицы, из которых состоят молекулы веществ, называют атомами.
Атом — наименьшая частица вещества, не делящаяся при химических реакциях.
Так, молекула воды состоит из двух атомов водорода и одного атома кислорода; молекула поваренной соли — из одного атома натрия и одного атома хлора. Молекула сахара, который мы обычно употребляем в пищу, более сложная: она состоит из 12 атомов углерода, 22 атомов водорода и 11 атомов кислорода, а молекула белка состоит из тысячи атомов.
Существуют вещества, молекулы которых содержат однородные атомы. Например, молекула водорода состоит из двух атомов водорода, молекула кислорода — из двух атомов кислорода.
Таким образом, можно сказать, что вещества состоят из молекул и атомов.
Определённое вещество, независимо от того, как оно получено, состоит из одних и тех же молекул и атомов. Например, молекула воды, полученной при таянии льда, или из сока ягод, или налитой из-под крана, содержит два атома водорода и один атом кислорода. Молекула кислорода, извлечённая из атмосферного воздуха или полученная в ходе какой-либо химической реакции, состоит из двух атомов кислорода.
Движение молекул. Диффузия
Вы уже знаете, что все вещества состоят из молекул и атомов, между которыми есть промежутки. Возникает вопрос: покоятся молекулы вещества или они движутся? Чтобы ответить на него, обратимся к явлениям, хорошо вам знакомым.
Если бы молекулы были неподвижны, то бельё не высыхало бы и запахи не распространялись бы по комнате. Остаётся предположить, что молекулы движутся. Сложность экспериментальной проверки этого предположения заключается в том, что молекулы малы и само их движение наблюдать невозможно. Однако можно изучить явления, которые являются следствием движения молекул. Рассмотрим одно из них.
В 1827 г. английский ботаник Роберт Броун (1773— 1858) изучал с помощью микроскопа поведение частичек цветочной пыльцы, взвешенных в воде. Он заметил, что частички совершают беспорядочное движение; они как бы дрожат в воде. Такое движение называют броуновским.
На рисунке 7 показана в увеличенном масштабе траектория движения частицы.
П
Лишь значительно позже поняли истинную причину броуновского движения. Эта причина — движение молекул воды. Молекулы воды, в которой находится частица пыльцы, движутся и ударяются о неё. При этом с разных сторон о частицу ударяется неодинаковое число молекул, что и приводит к её перемещению.
Пусть в момент времени t 1 под действием ударов молекул воды частица переместилась из точки А в точку В (см. рис. 7). В следующий момент времени большее число молекул ударяется о частицу с другой стороны, и направление её движения изменяется, она перемещается из точки В в точку С. Таким образом, движение частицы пыльцы является следствием движения молекул воды, в которой пыльца находится.
Подобное явление можно наблюдать, если поместить в воду частицы краски или сажи. Броуновское движение частиц можно наблюдать и в газах.
Выясним, каков характер движения молекул.
По траектории движения частицы пыльцы (см. рис. 7) видно, что направление её движения всё время меняется. Поскольку движение частицы — следствие движения молекул воды, то можно сделать вывод, что молекулы движутся беспорядочно (хаотически). Иными словами, нельзя выделить какое-то определённое направление, в котором движутся все молекулы.
Движение молекул никогда не прекращается. Можно сказать, что оно непрерывно. Итак,
молекулы находятся в непрерывном беспорядочном (хаотическом) движении.
Положение тела, совершающего равномерное механическое движение, можно определить, если известны его начальное положение, скорость и время движения. Иначе обстоит дело в случае движения молекул.
Вы уже знаете, что тела состоят из большого числа молекул. Поскольку движение молекул беспорядочно, то нельзя точно сказать, сколько ударов будет испытывать та или иная молекула со стороны других. Поэтому говорят, что положение молекулы и её скорость в каждый момент времени случайны. Однако это не означает, что движение молекул не подчиняется никаким законам. В частности, хотя скорости молекул в любой момент времени различны, у большинства из них значения скорости близки к некоторому определённому значению. Обычно, говоря о скорости движения молекул, имеют в виду среднюю скорость ( v c р).
С
У
Пока цилиндры были неподвижны, атомы осаждались напротив щели. Осадок имел форму полоски (рис. 10, а). Когда цилиндры приводили во вращение, то атомы серебра осаждались не напротив щели, а на некотором расстоянии от полоски атомов, образовавшейся в случае неподвижных цилиндров. При этом в зависимости от скорости движения атомов они оседали на разных расстояниях от полоски. Поэтому полоска не имела чётких границ, как бы размывалась. При этом центральная её часть была толще, чем края (рис. 10, б). Это означает, что скорость большей части атомов близка к некоторому определённому значению.
Если известны путь, пройденный молекулой (атомом), и время, за которое он пройден, то можно определить скорость молекулы. Из опыта Штерна найдено, что скорости большинства атомов серебра при температуре 1200 °С лежат в интервале от 500 до 625 м/с.
Актуализация знаний. Закрепление материала.
Каков предел деления вещества?
Что называют молекулой?
Каковы размеры молекул?