Доказательная медицина это что простыми словами
Что такое доказательная медицина
Доказательная медицина — это относительно новый подход к лечению, профилактике и реабилитации, основанный на научных выводах и фактах. То есть, используются препараты, который участвовали в многочисленных исследованиях и доказали свою эффективность и безопасность.
Образно говоря, классическая медицина скорее искусство, а доказательная — наука. Сама по себе доказательная медицина только инструмент для сравнения разных способов лечения и не отрицает предыдущих методов, если их можно научно обосновать.
Долгое время врачи лечили пациентов на основе своего личного опыта и опыта старших коллег. Если лекарство помогало одному пациенту, то специалисты делали выводы, что оно работает. Позиция доказательной медицины в этом случае — сначала выяснить, на самом деле помогло это лекарство или это стечение обстоятельств. Ведь если лечить насморк, то он пройдёт за неделю, а если не лечить, то за 7 дней.
Поэтому применять жаропонижающие препараты при ОРВИ можно в любом случае, а ставить горчичники или обтирать кожу спиртом могут порекомендовать педиатры старой школы, но не «доказательные» врачи. Ведь это может быть опасно для ребёнка и никак не поможет выздоровлению, как показывают исследования.
Как она появилась
После множества подобных историй стало ясно, что традиционный подход не эффективен и приносит страдания пациентам, которые стали невольными участниками медицинских экспериментов.
В 1972 году Кокрейн написал книгу, в которой указал на недостатки традиционных методов лечения и важности проведения исследований. А в 1990 году появился термин «доказательная медицина» и утвердились её принципы.
Принципы доказательной медицины
В этой системе врачи опираются на два пункта:
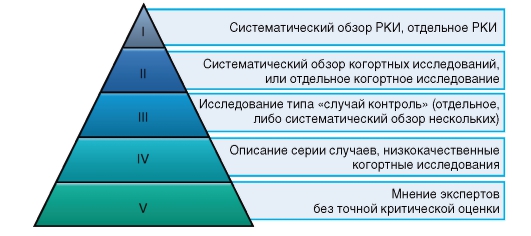
Как определяется доказательность
Она определяется по уровню исследований.
Основная задача врача, работающего по стандартам доказательной медицины, назначить препарат из первой группы. Но если такого нет, то из второй, а в крайнем случае из третьей. Лекарства из группы D, назначаются только если больше нет никаких вариантов лечения.
Какие организации принимают решения
Мировыми центрами доказательной медицины считаются «Кокрейновское сотрудничество» и «Клинические руководства на основе доказательной медицины» — гайдлайны.
Они создают и обновляют базу медицинских исследований, на которые опираются доказательные врачи всего мира.
В России главными документами считаются клинические рекомендации Минздрава. Только 20% российских специалистов пользуются Кокрейновской библиотекой и гайдлайнами, поэтому в нашей стране доказательная медицина не так распространена. Тем ценнее такие врачи.
Введение в доказательную медицину
Почему именно доказательная медицина
Сухую формулировку термина «доказательная медицина» Вы найдете на страницах нашей базы знаний, а в рамках этой статьи я попытаюсь объяснить более доступно суть этого подхода.
Краткое определение одного из отцов-основателей концепции медицины, основанной на доказанном, дано в 1996 году:
Думаю, каждый из нас сталкивался с тем, что на одно и то же заболевание или состояние врачи имеют различный, а иногда просто противоположный взгляд на обследование и лечение. И пациент (а за этим словом скрываются здоровье и даже жизнь вполне конкретного человека) оказывается перед выбором: кому верить? Как лечиться? Куда бежать? И посещение врача вместо ответов порождает новые вопросы.
Как ни странно, но с такой же ситуацией сталкиваются и врачи, сталкиваются ежедневно и даже ежечасно. При всей анатомо-физиологической схожести люди могут отличаться по полу, возрасту, сопутствующим заболеваниям, и даже одно заболевание может иметь разные варианты течения.
Долгие годы в подобных случаях врачи опирались на личный опыт, мнения более опытных врачей, коллегиальные решения, но и это не гарантировало благоприятного исхода. Поэтому долгое время медицина считалась более искусством, чем наукой.
ИСТОРИЧЕСКАЯ СПРАВКА: 12 декабря 1799 года Джордж Вашингтон, объезжая свои фермы, заболел. Судя по всему, у него развился паратонзиллярный абсцесс (или эпиглоттит). Врачи пришли к выводу, что лечить пациента следует кровопусканием (8 пинт, т.е. более 3х литров крови), несмотря на то, что трахеостомия, как метод лечения, была известна уже много сотен, если не тысяч лет. В итоге пациент скончался острой кровопотери.
Как появилась доказательная медицина
Началось все в 70 годах ХХ века, когда группа докторов, анализируя результаты клинических исследований, ввела термин «критический подход». Не вдаваясь в историю и терминологию, скажу, что суть критического подхода заключается в следующем:
прежде чем применить тот или иной метод профилактики, диагностики или лечения, необходимо иметь доказательства эффективности используемого метода.
И здесь важно не путать: не нужно доказывать неэффективность, нужно доказать именно эффективность.
ЭТО ИНТЕРЕСНО: в 1952 году, Бертран Рассел, английский математик и философ, в своей статье “Существует ли Бог?” привел аналогию, известную с тех пор как ЧАЙНИК РАССЕЛА. Эта аналогия используется для объяснения принципа, согласно которому необходимость доказывать что-либо следует на утверждающем.
ЦИТАТА: Многие верующие ведут себя так, словно не догматикам надлежит доказывать общепринятые постулаты, а наоборот — скептики обязаны их опровергать. Это, безусловно, не так. Если бы я стал утверждать, что между Землёй и Марсом вокруг Солнца по эллиптической орбите вращается фарфоровый чайник, никто не смог бы опровергнуть моё утверждение, добавь я предусмотрительно, что чайник слишком мал, чтобы обнаружить его даже при помощи самых мощных телескопов. Но заяви я далее, что, поскольку моё утверждение невозможно опровергнуть, разумный человек не имеет права сомневаться в его истинности, то мне справедливо указали бы, что я несу чушь. Однако если бы существование такого чайника утверждалось в древних книгах, о его подлинности твердили каждое воскресенье и мысль эту вдалбливали с детства в головы школьников, то неверие в его существование казалось бы странным, а сомневающийся — достойным внимания психиатра в просвещенную эпоху, а ранее — внимания инквизитора.
Таким образом, если кто-то утверждает, что какой-либо метод эффективен в лечении заболевания, то он не может требовать доказательств неэффективности своего метода, а должен доказать его эффективность.
Второй немаловажный пункт:
предлагаемое пациенту вмешательство должно иметь наибольшую эффективность и наименьший риск, к сожалению, этот пункт не всегда достижим, но из этого не следует, что к этому не нужно стремиться.
Сравнение! Каждый день, принимая решения, мы сравниваем, соотносим, оцениваем. Покупая продукты, мы соотносим цену и вес; приобретая автомобиль, мы сравниваем скоростные характеристики, расход топлива, стоимость покупки и владения, после чего выбираем наиболее оптимальную именно для нас марку и модель.
Как ни странно, но до появления инструментов, которые мы сейчас называем доказательной медициной, ни врачи, ни тем более пациенты, не могли сравнивать методы диагностики и лечения при наличии нескольких вариантов. Оперироваться или лечиться таблетками? Если оперироваться, то у кого и по какой из методик? Если таблетками, то какими и как долго? А что будет, если вообще не лечиться (как ни странно, но это очень важный вопрос)? Мы не могли сколько-нибудь достоверно ответить на эти простые, но важнейшие вопросы.
ИСТОРИЧЕСКАЯ СПРАВКА: концепция контролируемого клинического исследования была впервые описана в 1662 году Яном Баптистом ван Гельмонтом в отношении кровопускания. [2] Ван Гельмонт писал:
Первый опубликованный отчет с описанием проведения и результатов контролируемого клинического испытания был сделан Джеймсом Линдом, шотландским военно-морским хирургом, который проводил исследования цинги во время пребывания на борту HMS Salisbury на флоте Ла-Манша во время патрулирования Бискайского залива. Линд разделил моряков, участвовавших в его эксперименте, на шесть групп, чтобы можно было справедливо сравнить эффекты различных методов лечения и обнаружил улучшение симптомов и признаков цинги в группе мужчин, принимавших лимоны или апельсины. [3] Он опубликовал трактат с описанием результатов этого эксперимента в 1753 году.
Рассмотрим несколько простых примеров, которые позволят лучше понять, что такое доказательная медицина. Конечно же, в приведенных примерах мы многое упростим, но и это даст представление о том, что дает нам возможность сравнивать.
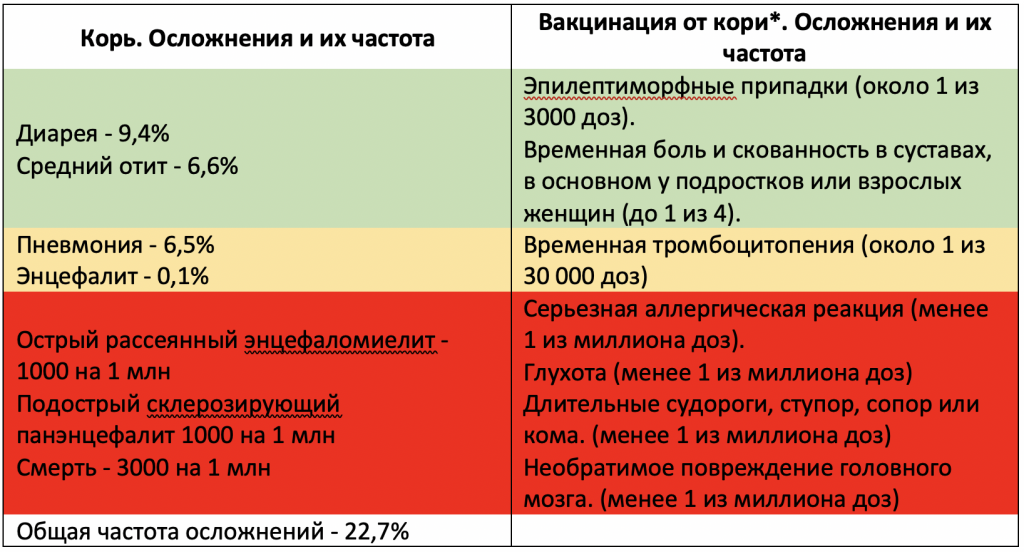
Пример №1. Сакраментальный вопрос, прививаться от кори или нет?
А давайте посмотрим как соотносятся на графике опасные и смертельно-опасные осложнения кори и прививок от кори
Итак, изучив таблицы, мы делаем вывод, что серьезных (смертельных и смертельно опасных) осложнений от вакцинации менее 4 на 1 млн прививок. В случае заболевания риск смертельных и смертельно опасных осложнений 5000 на 1 млн заболевших.
Но может быть риск заболеть корью не очень высок? В довакцинальную эпоху к 15 годам корь переносили 90% детей, с минимальным уровнем смертности в 2,5% и частотой осложнений не менее 22,5%. После введения вакцинации ряд стран был свободен от кори. Теперь у нас значительно больше данных для сравнения, остается сделать выбор.
Результат прекрасный, экстрасистолия проходила у большинства, у остальных существенно уменьшалась. Провели исследование, где одной группе пациентов после инфаркта миокарда давали плацебо (контрольная группа), а второй группе антиаритмик класса 1С (группа исследования). Подтвердили, что действительно, экстрасистолия уменьшается или даже проходит, но проблема оказалась в том, что в группе исследования пациенты умирали настолько чаще, что исследование пришлось прекратить.
Заметим, что кроме всего прочего, пример №2 иллюстрирует ситуацию, когда пациенты, а иногда даже врачи, в качестве доводов в защиту того или иного метода лечения заявляют: “мы же видим результат. ”. Те врачи, что лечили экстрасистолию у пациентов после инфаркта миокарда соответствующими антиаритмиками, тоже видели результат, он был очевиден и пациентам и легко фиксировался результатами обследований. А вот проблему увеличения смертности не видели. Практикующему врачу проанализировать и увидеть такую проблему, мягко говоря, непросто.
И примеров подобных множество. Далеко не все, что ранее считалось очевидным, получило соответствующее подтверждение в исследованиях. Как не все новое, что теоретически обещает стать прорывом в лечении чего-либо, оказывается таким прорывом в действительности.
Какие Ваши доказательства (с)
А – данные получены в нескольких рандомизированных клинических исследованиях;
В – данные получены в небольшом числе рандомизированных клинических исследований или в нерандомизированных исследованиях, или в наблюдениях;
C – рекомендации основаны главным образом на согласованном мнении специалистов.
Класс I: достоверные доказательства и/или единогласие экспертов в том, что данная процедура или вид лечения полезны и эффективны.
Класс II: противоречивые доказательства или различные мнения экспертов относительно полезности/эффективности данной процедуры или вида лечения.
Класс IIa: большая часть доказательств или мнений склоняется в пользу полезности/эффективности данной процедуры или вида лечения.
Класс IIb: меньшая часть доказательств или мнений склоняется в пользу полезности/эффективности данной процедуры или вида лечения.
Предлагаем Вам ознакомиться с лекцией Антона Владимировича Родионова, посвященной доказательной медицине. Лекция ориентирована на врачей, но будет интересна и широкой аудитории.
В чем преимущество доказательной медицины?
Пациент получает наиболее эффективную и безопасную на сегодняшний день терапию, врач может рассчитать соотношение риск/польза для каждого вмешательства.
Но ведь мне помогает.
Обычно, доводы: “но ведь мне помогает” или “ну я же вижу результат” приходится слышать от пациентов. Правда, последний довод нередко и от врачей. Тут следует заметить следующее:
Приведем еще один пример: долгое время родители при прорезывании зубов у детей использовали кремы на основе лидокаина. Часто отмечался благоприятный результат, т.е. ребенок успокаивался, боль стихала. Но в результате исследований оказалось, что использование данных средств нередко приводит к передозировке и было зафиксировано 22 смерти на несколько миллионов использований. В итоге имеем: состояние (боль при прорезывании зубов), от которого никто не умер, и метод лечения, который хоть и очень редко, но приводит к смерти. Стоит ли его применять? Думаю, ответ очевиден.
Можно ли было бы это выяснить, не используя инструменты доказательной медицины? Безусловно, нет.
Таким образом, мы предлагаем и призываем перед принятием решения оценить имеющуюся информацию о имеющихся методах диагностики и лечения, и только после сравнения, оценки ожидаемой пользы и предполагаемого риска принять взвешенное и осознанное решение.
Выводы
О том, какие исследования принимаются за доказательства в рамках доказательной медицины, а какие нет, мы поговорим отдельно, сейчас же попытаемся резюмировать то, что уже узнали:
Доказательная медицина это что простыми словами
В лексике современных врачей, фармацевтов и организаторов здравоохранения появился новый термин — «медицина, основанная на доказательствах (доказательная медицина)». Философский смысл этого понятия можно пояснить дуалистическим тезисом, издавна дискутируемым в медицинских кругах: медицина — это наука или искусство?
Для примера сравним европейскую и американскую модели деятельности врача. Американская модель считается формализованной, находящейся в жестких рамках стандартов медицинской помощи. Преимущество и слабость такой модели состоит в жесткой запрограммированности действий врача, что, с одной стороны, уменьшает количество врачебных ошибок (достаточно лишь точно следовать стандартам), а с другой — ограничивает возможности в выборе терапевтической тактики. Таким образом, американская модель медицины напоминает конвейер — высокопроизводительный, но неповоротливый.
Европейская модель напоминает скорее искусство, поскольку предоставляет врачу простор для творчества. Эта модель более гибкая, но менее производительная и менее устойчивая к ошибкам, нежели американская.
Тем не менее, в последнее время разница между двумя моделями медицины нивелируется за счет применения на практике принципов медицины, основанной на доказательствах.
Доказательная медицина (evidence-based medicine) — это раздел медицины, основанный на доказательствах, предполагающий поиск, сравнение, обобщение и широкое распространение полученных доказательств для использования в интересах больных (Evidence Based Medicine Working Group, 1993).
Доказательная медицина — это новый подход, направление или технология сбора, анализа, обобщения и интерпретации научной информации. Доказательная медицина предусматривает добросовестное, объяснимое и основанное на здравом смысле использование наилучших современных достижений для лечения каждого пациента (Sackett D.L. et al., 1996). Основная цель внедрения принципов доказательной медицины в практику здравоохранения — оптимизация качества оказания медицинской помощи с точки зрения безопасности, эффективности, стоимости и др. значимых факторов.
ИЗ ИСТОРИИ ТЕРМИНА
КОМУ И ЗАЧЕМ ЭТО НУЖНО?
Ни один практический врач не обладает достаточным опытом, позволяющим свободно ориентироваться во всем многообразии клинических ситуаций. Можно полагаться на мнения экспертов, авторитетные руководства и справочники, однако это не всегда надежно из-за так называемого эффекта запаздывания — перспективные терапевтические методы внедряются в практику спустя значительное время после получения доказательств их эффективности (Antman E.T. et al., 1992). С другой стороны, информация в учебниках, руководствах и справочниках зачастую устаревает еще до их публикации, а возраст проводящего лечение опытного врача отрицательно коррелирует с эффективностью лечения (Sackett D.L. et al., 1991). Эти заключения были получены с помощью основного статистического инструмента доказательной медицины — метаанализа (В.А. Горьков и соавт., 1998).
Основные тенденции развития биомедицинских наук определяют следующие факторы:
глобализация информационных процессов;
большое количество проводимых биомедицинских исследований;
широкий спектр лекарственных средств (ЛС) на фармацевтических рынках;
увеличение потока медицинской информации (издается около 40 000 биомедицинских журналов, публикующих примерно 2 млн статей ежегодно) (Oxman A., Guyall G., 1988);
Эти основные тенденции определяют следующие потребности практической медицины:
необходимость критической оценки информации, предназначенной для практических врачей и руководителей здравоохранения;
выбор системных подходов для принятия решений в медицине (лечебных, диагностических, управленческих и др.).
Следовательно, существует необходимость обобщения биомедицинских знаний и широкого информирования медицинской общественности о результатах новейших исследований.
Потенциальные возможности применения принципов доказательной медицины в практике здравоохранения — значительны. В первую очередь, их применение позволяет использовать объективные критерии ко всем аспектам фармакотерапии. Принципы доказательной медицины дают возможность с учетом новейшей и достоверной информации оптимизировать влияние на принятие решения таких во многом субъективных факторов, как интуиция и квалификация врача, мнения авторитетных экспертов, рекомендации популярных руководств и справочников. Таким образом, доказательная медицина предполагает объединение индивидуального клинического опыта врача с наилучшими доступными независимыми клиническими доказательствами из систематизированных исследований (Юрьев К.Л., Логановский К.Н., 2000).
При этом принципы доказательной медицины позволяют разрабатывать наиболее эффективные, безопасные и экономичные современные терапевтические стратегии, которые могут быть реализованы на государственном, региональном, популяционном, субпопуляционном и индивидуальном уровнях, способствуя выбору оптимального варианта в каждом конкретном клиническом случае.
Остановимся на некоторых аспектах практического применения принципов доказательной медицины. Прежде всего они применимы для повышения качества оказания медицинской помощи: это разработка клинических рекомендаций для практических врачей и внедрение систем стандартизации в здравоохранение.
Клинические рекомендации для практических врачей позволяют усовершенствовать работу врача в отношении следующих аспектов:
определение задач, стоящих перед врачом;
описание заболевания (этиология, распространенность, клиническая картина и т.д.);
алгоритмы диагностических процедур (программа обследования, показания и противопоказания к назначению диагностических манипуляций);
лечение (тактика, описание конкретных ЛС и лечебных мероприятий, критерии эффективности и прекращения лечения);
Внедрение систем стандартизации в здравоохранении:
сфера обращения ЛС;
разработка и применение медицинской техники;
разработка формулярной системы (протоколы ведения и лечения больных);
разработка и использование протоколов в страховой медицине;
определение относительной ценности различных источников информации применительно к поиску ответа на клинические вопросы.
ДОСТОВЕРНО ИЛИ НЕТ?
Важным аспектом доказательной медицины является определение степени достоверности информации: результатов исследований, которые берут за основу при составлении систематических обзоров. Центр доказательной медицины в Оксфорде разработал следующие определения степени достоверности представляемой информации:
A. Высокая достоверность — информация основана на результатах нескольких независимых клинических испытаний (КИ) с совпадением результатов, обобщенных в систематических обзорах.
B. Умеренная достоверность — информация основана на результатах по меньшей мере нескольких независимых, близких по целям КИ.
C. Ограниченная достоверность — информация основана на результатах одного КИ.
D. Строгие научные доказательства отсутствуют (КИ не проводились) — некое утверждение основано на мнении экспертов.
Согласно мнению Шведского совета по методологии оценки в здравоохранении, достоверность доказательств из разных источников не одинакова и убывает в следующем порядке (Li Wan Po, 1998):
1) рандомизированное контролируемое КИ;
2) нерандомизированное КИ с одновременным контролем;
3) нерандомизированное КИ с историческим контролем;
4) когортное исследование;
5) исследование типа «случай—контроль»;
7) результаты наблюдений;
8) описание отдельных случаев.
ПОИСК И АНАЛИЗ ДОКАЗАТЕЛЬНОЙ ИНФОРМАЦИИ
Информационный поиск в области доказательной медицины требует от исследователя соответствующего опыта и использования системного подхода. Для успешного поиска необходимой информации по вопросам доказательной медицины большое значение имеют выбор доступных баз клинических данных (MedLine, Cochrane Library, Adonis и др.) и разработка адекватной методологии поиска (по ключевым словам или словосочетаниям, именам авторов и т.д.).
Но даже при самом тщательном и квалифицированном поиске не всегда удается найти необходимую информацию о проведенных КИ (например, из-за некачественного индексирования или нежелания фирм-спонсоров публиковать отрицательные результаты КИ) (Hetherington O. et al., 1989). Таким образом, данные некоторых необходимых КИ могут быть не охвачены.
По этой причине при поиске доказательной информации компьютерный отбор необходимо дополнять другими методами поиска: «ручным» поиском информации о КИ, описание которых отсутствует в электронных базах данных; изучением списков литературы в найденных статьях; запросами исследователям и производителям ЛС (Юрьев К.Л., Логановский К.Н., 2000).
Для анализа доказательной информации используют такие специальные методы работы с информацией, как систематический обзор и метаанализ.
Метаанализ (meta-analysis) — применение статистических методов при создании систематического обзора (см. ниже) в целях обобщения результатов, включенных в обзор исследований. Систематические обзоры иногда называют метаанализом, если этот метод применялся в обзоре (Davies H., Crombie I., 1999).
Метаанализ проводят для того, чтобы обобщить имеющуюся информацию и распространить ее в понятном для читателей виде. Он включает определение основной цели анализа, выбор способов оценки результатов, систематизированный поиск информации, обобщение количественной информации, анализ ее с помощью статистических методов, интерпретацию результатов (Юрьев К.Л., Логановский К.Н., 2000).
Метаанализ — это статистический метод, позволяющий объединить результаты независимых исследований. Чаще всего его используют для оценки клинической эффективности терапевтических вмешательств; для этого объединяют результаты двух и более рандомизированных контролируемых исследований. Информативность метаанализа зависит от качества систематического обзора, на основании которого он проводится. Качественный метаанализ предполагает изучение всех исследований, посвященных соответствующей проблеме, оценку неоднородности и определение информативности основных результатов путем анализа чувствительности.
Существует несколько разновидностей метаанализа (Юрьев К.Л., Логановский К.Н., 2000).
Кумулятивный метаанализ позволяет построить кумулятивную кривую накопления оценок при появлении новых данных.
Проспективный метаанализ — попытка разработки метаанализа планируемых испытаний. Такой подход может оказаться приемлемым в областях медицины, где уже существует сложившаяся сеть обмена информацией и совместных программ.
Метаанализ индивидуальных данных основан на изучении результатов лечения отдельных больных. В ближайшем будущем метаанализ индивидуальных данных, вероятнее всего, будет ограничиваться изучением основных заболеваний, лечение которых требует крупномасштабных централизованных капиталовложений.
получение достоверных результатов;
устранение возможных ошибок;
выявление и отбор исследований;
неоднородность представленной информации;
вероятность потери важной информации;
неадекватный анализ сравниваемых подгрупп;
неадекватный анализ чувствительности метода.
Главным требованием к информативному метаанализу является наличие адекватного систематического обзора. Результаты метаанализа обычно представляют в виде графика и отношения шансов (оdds ratio), суммарного показателя, отражающего выраженность эффекта (H. Davies, Crombie I., 1999).
Систематический обзор (systematic review, systematic overview) — особый вид научного исследования, выполненный по специально разработанной методике, объектом которого являются результаты других, оригинальных научных исследований. Анализ и обобщение результатов исследований, включенных в обзор, можно проводить с применением статистических методов и без них.
Систематические обзоры позволяют провести адекватное обобщение результатов научных исследований. Целью систематического обзора является взвешенное и беспристрастное изучение результатов ранее проведенных исследований. Часто в систематическом обзоре проводится количественная оценка суммарного эффекта, установленного на основании результатов всех изученных исследований (метаанализ) (H. Davies, Crombie I., 1999).
Примечательна история одного из первых систематических обзоров. Результаты первого КИ, посвященного эффективности недорогого короткого курса кортикостероидов, который назначали беременным с высоким риском преждевременных родов, были опубликованы в 1972 г. Было установлено, что кортикостероиды снижают вероятность смерти новорожденных от осложнений, обусловленных недоношенностью. К 1991 г. были опубликованы сообщения еще о 7 КИ, посвященных той же теме, подтвердивших и уточнивших результаты первого КИ. Было доказано, что риск смерти у таких детей можно снизить на 30–50%. Схематическое изображение результатов этого исследования стало эмблемой Кокрановского Сотрудничества (см. заголовок).
Поскольку до 1989 г. не было опубликовано ни одного систематического обзора данных КИ, большинство врачей считали такую терапию неэффективной. Таким образом, прошло около 20 лет со времени публикации первых результатов исследования до широкого их внедрения в практику. По приблизительной оценке десятки тысяч детей пострадали и умерли от отсутствия необходимой терапии. Это впечатляющая иллюстрация необходимости внедрения принципов доказательной медицины в практику (The Cochrane Collaboration, 2001).
Систематические обзоры — главный результат деятельности Кокрановского Сотрудничества — регулярно публикуются в электронном виде под названием «The Cochrane Database of Systematic Reviews» (Кокрановская база данных систематических обзоров).
Основой современной доказательной медицины является так называемое Кокрановское Сотрудничество — международная организация, целью которой является поиск и обобщение достоверной информации о результатах медицинских вмешательств (Юрьев К.Л., Логановский К.Н., 2000). Составление систематических обзоров — весьма трудоемкая работа, требующая совместных усилий исследователей. Кокрановское Сотрудничество — наиболее активная организация, созданная с этой целью в 1992 г. Дж. Чалмерсом (Chalmers J. et al. 1994), в настоящее время насчитывающая около 3000 организаций-участников. Кокрановское Сотрудничество действует в виде сети сообщающихся центров в различных странах. Цель Кокрановского Сотрудничества — создать исчерпывающий регистр всех рандомизированных КИ, необходимых для составления систематических обзоров.
1973 г. — английский эпидемиолог Арчи Кокран (Cochrane A.L.) составил первый систематический обзор.
1992 г. — открыт первый Кокрановский центр в Оксфорде.
ПРИНЦИПЫ КОКРАНОВСКОГО СОТРУДНИЧЕСТВА
За годы, прошедшие с момента образования, Кокрановское Сотрудничество претерпело значительные изменения, не отступив при этом от провозглашенных задач и принципов. Основная задача этой международной организации — создание, обновление и распространение систематических обзоров результатов медицинских вмешательств, которые должны облегчить заинтересованным лицам принятие решений в различных областях медицины.
Кокрановское Сотрудничество основано на 8 принципах:
отсутствие дублирования в работе;
минимизация предвзятости и систематических ошибок;
постоянное обновление данных;
постоянное повышение качества работы.
Кокрановские центры поддерживают деятельность подразделений Кокрановского Сотрудничества. Профиль каждого центра определяется с учетом интересов его участников и уровнем финансирования, но все они должны координировать свои действия и оказывать поддержку Кокрановскому Сотрудничеству (Юрьев К.Л., Логановский К.Н., 2000).
Кокрановские центры облегчают работу всех, кто намерен составлять систематические обзоры по отдельным областям клинической медицины и системы здравоохранения в целом. Условием такого сотрудничества является публикация в Кокрановской базе данных систематических обзоров, распространяемых также на компакт-дисках (The Cochrane database of systematic reviews, 1995) и в сети Интернет. Получить такую информацию можно, например, воспользовавшись услугами сервера Московского центра доказательной медицины и фармакотерапии: http://evbmed.fbm.msu.ru/index-r.html и официальным сайтом Российского отделения Кокрановского Сотрудничества: http://www.cochrane.ru/
МЕЖДУНАРОДНЫЕ ПРОБЛЕМНЫЕ ГРУППЫ ПО СОСТАВЛЕНИЮ СИСТЕМАТИЧЕСКИХ ОБЗОРОВ
Международные проблемные группы по составлению систематических обзоров занимаются составлением и обновлением Кокрановских обзоров.
В помощь членам проблемных групп Кокрановское Сотрудничество подготавливает обучающие материалы, а Кокрановские центры и в отдельных случаях сами проблемные группы проводят семинары. При обучении лиц, участвующих в проведении Кокрановских обзоров, по возможности используются примеры реально проведенных исследований (Юрьев К.Л., Логановский К.Н., 2000).
В работе групп участвуют исследователи, врачи, представители организаций потребителей — все, кто заинтересован в получении надежной, современной и актуальной информации в области профилактики, лечения и реабилитации при различных заболеваниях.
Отдельные мультидисциплинарные группы организованы для анализа и обобщения данных, относящихся к различным клиническим разделам медицины и областям медицинской деятелности.
КОКРАНОВСКИЕ РАБОЧИЕ ГРУППЫ ПО МЕТОДОЛОГИИ ОБЗОРОВ
ГРУППЫ ПО ОБЛАСТЯМ ИНТЕРЕСОВ
Группы по областям интересов — это Кокрановские подразделения, объединенные не по нозологическим формам, а по таким аспектам медицины, как условия оказания медицинской помощи (например, догоспитальной), оказание помощи определенным группам больных (например, старческого возраста), различные уровни медицинской помощи (например, сестринский уход) или по определенному типу вмешательств (например, по физиотерапии). Работает отдел координации различных обзорных групп по интересам и сетям (например, потребительская сеть).
КОКРАНОВСКАЯ ЭЛЕКТРОННАЯ БИБЛИОТЕКА
Кокрановская база данных систематических обзоров содержит завершенные обзоры и протоколы готовящихся обзоров.
Кокрановский регистр контролируемых испытаний представляет собой библиографическую базу данных всех выявленных публикаций контролируемых испытаний.
Реферативная база данных обзоров по эффективности медицинских вмешательств содержит структурированные рефераты тех систематических обзоров, которые прошли критическую оценку сотрудниками Йоркского Центра по составлению и распространению обзоров (Великобритания) либо сотрудниками журналов «American College of Physicians’ Journal Club» и «Evidence-Based Medicine».
Кокрановская база данных по методологии обзоров представляет собой библиографию статей, посвященных методам синтеза и анализа результатов клинических исследований. В Кокрановскую электронную библиотеку также включены: учебное пособие по методологии составления систематических обзоров, словарь методологических и специфических терминов, принятых в организации, адреса проблемных групп и других подразделений Кокрановского Сотрудничества.
Кокрановский подход является основой развития идей доказательной медицины. В настоящее время органы управления здравоохранением и страховые организации промышленно развитых стран, принимая большинство своих решений, руководствуются заключениями и рекомендациями Кокрановского Сотрудничества (Юрьев К.Л., Логановский К.Н., 2000).
Владимир Мальцев,
доктор медицинских наук,
заведующий сектором координации
и контроля клинических испытаний ГП ГФЦ
Татьяна Ефимцева,
кандидат медицинских наук,
ведущий научный сотрудник ГП ГФЦ
Alain Li Wan Po. Evidence-Based Pharmacotherapy. The Pharmaceutical J. Vol. 256, March 2, 1996: 308–312.
Antman E.T., Lau J., Kupelnick В., Mosteller F., Chalmers T.C. A comparison of Results of Meta-analyses of Randomized Control Trials and Recomendations of Clinical Experts. Treatment for Myocardial Infarction. JAMA, July 8, 1992. — Vol. 268, № 2, 240–248.
Chalmers J., Dickersin K., Chalmers T.C. Getting to grips with Archie Cochrane’s agenda. Br. Med. 1994:305:786–8.
Davies H., Crombie I., Что такое мета-анализ?// Клиническая фармакология и фармакотерапия № 8, 1999 г.
Hetherington O., Chalmers L. Dickersin К, Meinert С. Retrospective and prospective identification of controlled trials: lessons from a survey of obstetricians and paediatricians. Pediatrics 1989:84:374–80.
Sackett D.L., Haynes R.B., Guyatt G.H., Tugwell P. Clinical Epidemiology: a Basic Science for Clinical Medicine. V Edn, Little, Brown & Co., 1991: 305–306.
The Cochrane Collaboration. Preparing, maintaining and promoting the accessibility of systematic reviews of the effects of health care interventions, 2001.
The Cochrane database of systematic reviews. London: BMJ Publishing Group and Update Software, 1995.
Юрьев К.Л., Логановский К.Н. Доказательная медицина. Кокрановское сотрудничество.//Укр. мед. часопис, 2000, № 6/20.
Alain Li Wan Po. Evidence-Based Pharmacotherapy. The Pharmaceutical J. Vol. 256, March 2, 1996: 308–312.
Antman E.T., Lau J., Kupelnick В., Mosteller F., Chalmers T.C. A comparison of Results of Meta-analyses of Randomized Control Trials and Recomendations of Clinical Experts. Treatment for Myocardial Infarction. JAMA, July 8, 1992. — Vol. 268, № 2, 240–248.
Chalmers J., Dickersin K., Chalmers T.C. Getting to grips with Archie Cochrane’s agenda. Br. Med. 1994:305:786–8.
Davies H., Crombie I., Что такое мета-анализ?// Клиническая фармакология и фармакотерапия № 8, 1999 г.
Hetherington O., Chalmers L. Dickersin К, Meinert С. Retrospective and prospective identification of controlled trials: lessons from a survey of obstetricians and paediatricians. Pediatrics 1989:84:374–80.
Sackett D.L., Haynes R.B., Guyatt G.H., Tugwell P. Clinical Epidemiology: a Basic Science for Clinical Medicine. V Edn, Little, Brown & Co., 1991: 305–306.
The Cochrane Collaboration. Preparing, maintaining and promoting the accessibility of systematic reviews of the effects of health care interventions, 2001.
The Cochrane database of systematic reviews. London: BMJ Publishing Group and Update Software, 1995.
Юрьев К.Л., Логановский К.Н. Доказательная медицина. Кокрановское сотрудничество.//Укр. мед. часопис, 2000, № 6/20.
Alain Li Wan Po. Evidence-Based Pharmacotherapy. The Pharmaceutical J. Vol. 256, March 2, 1996: 308–312.
Antman E.T., Lau J., Kupelnick В., Mosteller F., Chalmers T.C. A comparison of Results of Meta-analyses of Randomized Control Trials and Recomendations of Clinical Experts. Treatment for Myocardial Infarction. JAMA, July 8, 1992. — Vol. 268, № 2, 240–248.
Chalmers J., Dickersin K., Chalmers T.C. Getting to grips with Archie Cochrane’s agenda. Br. Med. 1994:305:786–8.
Davies H., Crombie I., Что такое мета-анализ?// Клиническая фармакология и фармакотерапия № 8, 1999 г.
Hetherington O., Chalmers L. Dickersin К, Meinert С. Retrospective and prospective identification of controlled trials: lessons from a survey of obstetricians and paediatricians. Pediatrics 1989:84:374–80.
Sackett D.L., Haynes R.B., Guyatt G.H., Tugwell P. Clinical Epidemiology: a Basic Science for Clinical Medicine. V Edn, Little, Brown & Co., 1991: 305–306.
The Cochrane Collaboration. Preparing, maintaining and promoting the accessibility of systematic reviews of the effects of health care interventions, 2001.
The Cochrane database of systematic reviews. London: BMJ Publishing Group and Update Software, 1995.
Юрьев К.Л., Логановский К.Н. Доказательная медицина. Кокрановское сотрудничество.//Укр. мед. часопис, 2000, № 6/20.
Alain Li Wan Po. Evidence-Based Pharmacotherapy. The Pharmaceutical J. Vol. 256, March 2, 1996: 308–312.
Antman E.T., Lau J., Kupelnick В., Mosteller F., Chalmers T.C. A comparison of Results of Meta-analyses of Randomized Control Trials and Recomendations of Clinical Experts. Treatment for Myocardial Infarction. JAMA, July 8, 1992. — Vol. 268, № 2, 240–248.
Chalmers J., Dickersin K., Chalmers T.C. Getting to grips with Archie Cochrane’s agenda. Br. Med. 1994:305:786–8.
Davies H., Crombie I., Что такое мета-анализ?// Клиническая фармакология и фармакотерапия № 8, 1999 г.
Hetherington O., Chalmers L. Dickersin К, Meinert С. Retrospective and prospective identification of controlled trials: lessons from a survey of obstetricians and paediatricians. Pediatrics 1989:84:374–80.
Sackett D.L., Haynes R.B., Guyatt G.H., Tugwell P. Clinical Epidemiology: a Basic Science for Clinical Medicine. V Edn, Little, Brown & Co., 1991: 305–306.
The Cochrane Collaboration. Preparing, maintaining and promoting the accessibility of systematic reviews of the effects of health care interventions, 2001.
The Cochrane database of systematic reviews. London: BMJ Publishing Group and Update Software, 1995.
Юрьев К.Л., Логановский К.Н. Доказательная медицина. Кокрановское сотрудничество.//Укр. мед. часопис, 2000, № 6/20.