Дюспаталин или ганатон в чем разница
Эффективность применения препарата Ганатон в лечении больных ГЭРБ
О.Н. Минушкин, Ю.Н. Лощинина
УНМЦ управления делами Президента РФ
Гастроэзофагеальная рефлюксная болезнь (ГЭРБ) является заболеванием, обусловленным нарушением перистальтики органов эзофагогастродуоденальной зоны, часто повторяющимися забросами в пищевод желудочного или дуоденального содержимого, удлинением времени экспозиции рефлюктата в пищеводе, приводящих к повреждению дистальной части пищевода.
Из определения болезни видно, что основным патогенетическим механизмом, формирующим условия для раздражения, воспаления, повреждения слизистой, является расстройство моторики. Тем не менее, основным направлением терапии, используемым в лечении ГЭРБ, является блокада желудочной секреции. Это связано в значительной степени с тем, что эффективных препаратов, восстанавливающих нарушенную перистальтику, до настоящего времени не было, а те, которые присутствовали на фармакологическом рынке, обладали значительным количеством побочных эффектов.
Следует отметить, что в клинической практике блокада желудочной секреции не всегда эффективно решает задачу контроля над симптомами ГЭРБ. В таких случаях (а это, например, сочетание изжоги с симптомами диспепсии, резистентность к ингибиторам протонной помпы или ночные прорывы кислотности на фоне терапии этими препаратами, щелочной рефлюкс и др.) значение восстановления нормальной двигательной функции пищевода и желудка увеличивается.
В 2007 году в России зарегистрирован новый прокинетик с комбинированным механизмом действия – Ганатон (Ganaton – своеобразная аббревиатура от «gastric natural tone», т.е. восстанавливающий нормальный тонус желудка; международное название – итоприда гидрохлорид).
Ганатон (итоприда гидрохлорид) является одновременно антагонистом допаминовых рецепторов и блокатором ацетилхолинэстеразы. Препарат активирует освобождение ацетилхолина и препятствует его деградации.
Ганатон обладает минимальной способностью проникать через гематоэнцефалический барьер в центральную нервную систему, включая головной и спинной мозг. Метаболизм препарата позволяет избежать нежелательного лекарственного взаимодействия при приеме препаратов, метаболизирующихся ферментами системы цитохрома Р 450.
Взрослым Ганатон назначают внутрь по 1 таблетке (50 мг) 3 раза в сутки до еды. Рекомендуемая суточная доза составляет 150 мг.
В Японии, где Ганатон (итоприда гидрохлорид) применяется с 1995 г., было проведено многоцентровое двойное слепое сравнительное исследование эффективности применения в течение 2 недель у больных хроническим гастритом с симптомами диспепсии. Итоприд гидрохлорида назначался в дозе 50 мг 3 раза в сутки (у 111 пациентов), цизаприд – в дозе 2,5 мг 3 раза в сутки (у 114 пациентов) (3). Умеренное или значительное клиническое улучшение наблюдалось у 79,3% больных, получавших итоприда гидрохлорид, и у 71,9% пациентов, получавших цизаприд. Авторы сделали вывод о высокой эффективности применения итоприда гидрохлорида в лечении больных хроническим гастритом с симптомами диспепсии. Был отмечен также хороший эффект итоприда гидрохлорида у больных хроническим гастритом с сопутствующими симптомами гастроэзофагеальной рефлюксной болезни (2), а также у пациентов с диабетическим гастропарезом (5).
Во всех клинических исследованиях Ганатон (итоприда гидрохлорид) зарекомендовал себя как препарат, характеризующийся хорошей переносимостью и отсутствием серьезных побочных эффектов. Основными побочными эффектами при приеме итоприда гидрохлорида явились: диарея (0,7% случаев), боли в животе (0,3%), головная боль (0,3%). Проведенные постмаркетинговые исследования подтвердили безопасность итоприда гидрохлорида (1). Результаты применения этого препарата более чем у 10 млн больных не выявили ни одного случая удлинения интервала Q-T. При назначении препарата в обычных терапевтических дозах повышение уровня пролактина в крови встречается редко.
На специальном симпозиуме по лечению функциональной диспепсии, который проходил в 2005 г. в Монреале в рамках Всемирного конгресса гастроэнтерологов, Ганатон (итоприда гидрохлорид) был охарактеризован как высокоэффективный и безопасный представитель нового класса прокинетиков, который может с успехом применяться при лечении функциональной диспепсии, а в будущем, возможно, займет важное место и в лечении других гастроэнтерологических заболеваний, протекающих с нарушением двигательной функции желудка (идиопатического гастропареза, гастроэзофагеальной рефлюксной болезни и др.) (4).
На кафедре гастроэнтерологии ФГУ УНМЦ УД Президента РФ в период с апреля по июнь 2008 г. Было проведено изучение клинического применения, предусматривающее курсовое лечение Ганатоном по стандартной схеме в течение 4 недель больных ГЭРБ.
Цель изучения – оценка эффективности 4-недельного курса терапии Ганатоном в стандартном режиме в купировании симптомов ГЭРБ и влияния на качество жизни больных, а также на тонус ВНС (устранение дисфункции по симпатическому и парасимпатическому типу).
Критериями включения больных явились: наличие у пациентов умеренной или сильной изжоги (≥ 2 баллов по шкале Лайкерта), по крайней мере 1-2 раза в неделю, наличие дисфункции ВНС по симпатическому или парасимпатическому типу.
Всего к изучению было принято 20 пациентов мужского пола с ГЭРБ 0 – I стадии, в возрасте от 20 до 25 лет (средний возраст 22,8 ± 0,33 года), соответствующих критериям включения.
Перед включением проводились клинический анализ крови и мочи, ЭГДС. До и после лечения оценивали интенсивность и частоту симптомов, эндоскопическую картину у пациентов с эрозивной формой ГЭРБ и уровень качества жизни по данным опросника SF-36 и визуальной аналоговой шкалы (ВАШ).
Больные принимали Ганатон в дозе 1 таблетка 3 раза в день, за 15 минут до приема пищи в течение 25 дней.
Тип течения ГЭРБ имел рецидивирующий характер в 100% случаев. Средняя продолжительность ЭНРБ (эндоскопически негативной рефлюксной болезни) составляла 3,4 ± 0,65 лет.
Все пациенты на момент включения в группу лечения испытывали изжогу и другие симптомы ГЭРБ, значительно ухудшающие качество жизни.
Изжога оценивалась с помощью расчетного показателя в баллах (таблица 1).
Среднее значение изжоги составляло 7,0 ± 0,2 балла.
Эндоскопическая характеристика больных до начала лечения представлена в таблице 2.
Таблица 1. Оценка изжоги изученных больных
| Параметр | Характеристика | Балл |
|---|---|---|
| Частота | Отсутствует Менее 2 раз в неделю 2-6 раз в неделю Ежедневно | 0 1 2 3 |
| Время возникновения | Отсутствует Только днем Только ночью Днем и ночью | 0 1 1 2 |
| Интенсивность | Отсутствует Легкая Средняя Тяжелая | 0 1 2 3 |
| Продолжительность | Отсутствует Несколько минут Длительно | 0 1 2 |
Таблица 2. Результаты эндоскопического исследования до начала терапии
| Эндоскопический признак | Количество пациентов, N (%) |
|---|---|
| Отсутствие изменений слизистой | 8 (40%) |
| Катаральный эзофагит | 6 (30%) |
| Эрозивный эзофагит | 6 (30%) |
| Недостаточность кардии | 17 (85%) |
| ГПОД | 1 (2%) |
Исследование вегетативного статуса проводилось по данным специального вопросника (Вейн А.М., 1993 г.), объективного осмотра и по вычислению индекса Кердо: ВИ = (1 – Д/Р) × 100,
где ВИ – вегетативный индекс; Д – диастолическое давление; Р – частота сердечных сокращений в 1 минуту.
Результаты лечения больных
На фоне проводимой монотерапии препаратом Ганатон изжога уменьшилась на 1 и более баллов к 7 ± 0,62 дню лечения у всех больных и была полностью купирована на 8,5 ± 1,1 день терапии в 90% случаев. У 2 пациентов купирования симптомов ГЭРБ (изжога, отрыжка воздухом) по окончании терапии не наступило. Это может быть связано с тем, что механизм формирования клинических проявлений у них был иным – не связанным с расстройством моторики.
У пациентов с эрозивной формой ГЭРБ (6 пациентов) после окончания терапии проводилась контрольная ЭГДС, при которой была выявлена полная эпителизация эрозий пищевода в 100% случаев.
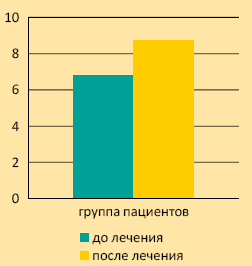
При оценке самочувствия визуальноаналоговой шкалы исходные данные ВАШ составили 6,8 ± 0,38 см, после курсовой терапии – 8,7 ± 0,19 см (р
График 1. Динамика самочувствия пациентов (оценка по ВАШ) до и после лечения
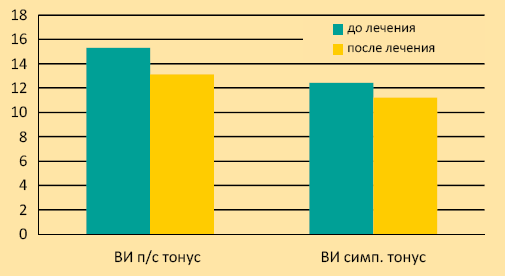
Было получено отчетливое влияние на вегетативный статус, что выражается в улучшении клинической симптоматики. Так, вегетативный индекс Кердо у пациентов с дисфункцией нервной системы по парасимпатическому типу до лечения составил 15,3 ± 1,8, после лечения – 13,1 ± 0,9. У пациентов с дисфункцией ВНС по симпатическому типу индекс Кердо до лечения – 12,4 ± 1,8, после лечения – 11,2 ± 1,2. Результаты представлены в графике 2.
График 2. Динамика вегетативного индекса Кердо до и после лечения Ганатоном
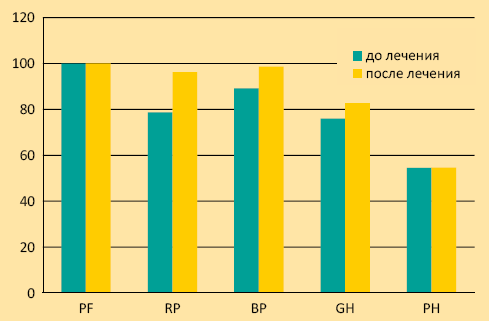
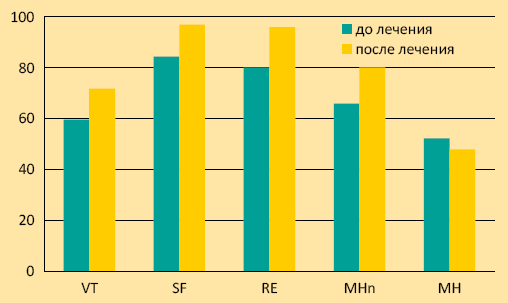
Динамика уровня качества жизни по данным опросника SF-36 показала, что среди показателей физического компонента здоровья (график 3) достоверно улучшились ролевое функционирование (RP), интенсивность боли (BP), общее состояние здоровья (GH). Среди показателей психологического компонента здоровья (график 4) наблюдалось достоверное улучшение жизненной активности (VT), социального (SF) и ролевого (RE) функционирования, психического здоровья (MHn).
График 3. Динамика уровня качества жизни (физическое здоровье) по данным опросника SF-36
График 4. Динамика уровня качества жизни (психическое здоровье) по данным опросника SF-36
Оценка безопасности и п ереносимости препарата Ганатон
За время лечения каких-либо побочных эффектов зарегистрировано не было. Препарат хорошо переносился и не вызывал органолептических неудобств.
Обсуждение
Изучена эффективность лечения 20 больных ГЭРБ (у 70% – НЭРБ, у 30% – эрозивный вариант). Больные характеризовались выраженным клиническим вариантом болезни (интенсивность изжоги составила 7 баллов), снижен уровень качества жизни; изменен вегетативный статус (поровну с преобладанием симпатического и парасимпатического отделов ВНС), причем у больных с преобладанием парасимпатического отдела – фиксировались более выраженные изменения слизистой пищевода – эрозивные и катаральные.
Больные получали только Ганатон и непродолжительным курсом (25 дней), при этом в обычные сроки были купированы клинические проявления и наступала эпителизация эрозий. Ни один больной ни потребовал усиления терапии антацидами или блокаторами секреции.
Эти результаты вселяют надежду, что новый (для нашей страны) прокинетик Ганатон может занять достойное место в лечении ГЭРБ.
Можно предположить, что для части больных Ганатон окажется препаратом выбора (не только в лечении, но и в поддержании ремиссии), для части – его использование поможет уменьшить дозу блокаторов секреции; сократить сроки лечения.
Препарат нуждается в дальнейшем изучении с целью определения его места в лечении наиболее распространенного гастроэнтерологического заболевания – ГЭРБ, которая и в условиях России становится болезнью № 1.
Выводы
Функциональные расстройства кишечника и желчевыводящих путей. Лечебные подходы, выбор спазмолитика

Рассмотрены виды функциональных расстройств кишечника и билиарного тракта, общие клинические проявлениям при разных формах таких расстройств, алгоритм диагностики и подходы к лечению пациентов с применением спазмолитиков.
Types of functional dysfunctions of bowels and biliary have been reviewed, general clinic preparations for different forms of such dysfunctions, diagnostic algorithm and approaches to treatment with antispasmodic agents application.
К функциональным расстройствам органов пищеварения относятся различные устойчивые комбинации хронических или рецидивирующих гастроинтестинальных симптомов, не объяснимых на сегодняшний день структурной, органической или известной биохимической патологией.
Согласно рекомендациям Римского консенсуса III (2006 г.) к функциональным расстройствам кишечника и билиарного тракта относят [1]:
I. Функциональные кишечные нарушения:
II. Дисфункциональные расстройства билиарного тракта:
По характеру моторных расстройств билиарного тракта их подразделяют на гиперфункциональные и гипофункциональные.
Общими клиническими проявлениями при разных формах функциональных расстройств желчевыводящей системы и кишечника являются: абдоминальные боли, метеоризм, изменения частоты и характера стула.
В регуляции двигательной активности кишечника и билиарной системы принимают участие парасимпатический и симпатический отделы вегетативной нервной системы, обеспечивающие их сбалансированное влияние с последующей передачей импульсов на интрамуральные сплетения.
Сокращение гладкой мускулатуры желудочно-кишечного тракта (ЖКТ) возникает при стимуляции ацетилхолином мускариновых рецепторов на поверхности мышечной клетки. Это приводит к открытию натриевых каналов и входу Na + в клетку. Появившаяся деполяризация клетки, в свою очередь, способствует открытию кальциевых каналов и входу Са 2+ в клетку. Увеличившийся внутриклеточный уровень Са 2+ способствует фосфорилированию миозина и, соответственно, сокращению мышцы. В зависимости от интенсивности сигнала может возникнуть мышечный спазм, который формирует боль.
В свою очередь симпатические импульсы содействуют выходу К + из клетки и Са 2+ из кальциевого депо, закрытию кальциевых каналов и расслаблению мышцы [2, 3].
Таким образом, учитывая тот факт, что в формировании боли при билиарной дисфункции и функциональных расстройствах кишечника лежит чрезмерное сокращение гладкой мускулатуры, в купировании их основное место должны занимать антиспастические средства.
В настоящее время для купирования боли используют релаксанты гладкой мускулатуры, которые включают в себя следующие группы:
1. Миотропные спазмолитики:
2. Нейротропные спазмолитики (блокируют процесс передачи нервных импульсов в вегетативных ганглиях и нервных окончаниях, стимулирующих гладкомышечные клетки):
3. Прокинетики — группа препаратов, нормализующих моторную активность ЖКТ; усиливают пропульсивную активность верхних отделов ЖКТ за счет антагонизма с дофаминовыми рецепторами (метоклопромид, домперидон (Мотилиум) и итоприд (Ганатон), который помимо блокады дофаминовых рецепторов ингибирует активность холинэстеразы, подавляя разрушение ацетилхолина, расширяя зону регуляции).
4. Универсальные модуляторы моторики ЖКТ (блокаторы µ-, δ-рецепторов и активаторы κ-рецепторов) — тримебутин (Тримедат).
Таким образом, в основе функциональных расстройств ЖКТ лежат расстройства моторики, а представленная выше группа препаратов так или иначе влияет на тонико-перистальтическую активность, причем спектр этих влияний очень разнообразный и нередко, используя их, мы сталкиваемся с эффектами, нежелательными в данной конкретной ситуации. Так, нейротропные спазмолитики имеют широкий спектр «побочных» эффектов, ограничивающих их длительное применение, а у отдельных категорий больных их применение вообще нецелесообразно. Основным недостатком миотропных спазмолитиков являются отсутствие селективности и возможность развития гипомоторной дискинезии и гипотонии всего сфинктерного аппарата ЖКТ [4].
Подводя итог всего вышеизложенного, можно констатировать, что на сегодняшний день мы располагаем большим арсеналом препаратов, действующих на разные патогенетические звенья спазма гладкой мускулатуры, формирующие боль. Наша задача состоит в том, чтобы выбрать наиболее адекватный спазмолитик, свести к минимуму побочные эффекты, максимально быстро купировать боль, ограничить, не допустить ее возврата.
Почему боль является главным проявлением, определяющим выбор препарата? Потому что она нередко является единственным симптомом, свидетельствующим о функциональном расстройстве, а остальные проявления требуют доказательного обследования.
Как же выбрать наиболее рациональный препарат для лечения? Мы предлагаем следующий алгоритм выбора препарата:
I. В зависимости от степени выраженности и зоны распространения спазмолитического эффекта (табл. 1).
II. В зависимости от сочетания зон спазма:
а) желудок + мочеполовая сфера;
б) пищевод, желудок + кишечник;
в) пищевод + мочевой пузырь;
г) желчевыводящие пути + мочеточники (почки);
д) желчевыводящие пути;
е) кишечник (без определенной локализации);
ж) кишечник (правые отделы);
з) кишечник + сфинктер Одди;
и) «спастическая дискинезия» + патология предстательной железы;
к) спастическая дискинезия + пожилой и старческий возраст.
III. В зависимости от интенсивности боли (острая — парентеральный вариант введения препарата).
IV. В зависимости от возраста.
V. В зависимости от издержек использования спазмолитиков:
а) «стирание» симптоматики;
б) распространение зон действия;
в) отрицательные эффекты при сочетании с другими фармпрепаратами;
г) вариант исходного состояния вегетативной нервной системы.
Предложенный алгоритм выбора препарата не является догмой — он только показывает ориентиры, которые помогают в выборе. Выбрав и начав лечение, мы оцениваем эффективность:
Но главным в лечении является диагностика «клинической ситуации», которая позволяет говорить либо об органической патологии и вторичном характере функциональных расстройств, либо о функциональной патологии (рис.).
Таким образом, диагностика функциональной патологии на сегодняшний день является диагностикой исключения органической патологии. Установив это, мы оцениваем характер функциональных расстройств и определяем комплекс расстройств в целом.
Мы решили представить результаты лечения 60 больных препаратом Дицетел: 30 из них страдали синдромом раздраженного кишечника (по 10 — вариант с запором, вариант с диареей, болями и вздутием живота). Возраст больных от 18 до 60 лет; преобладали женщины — 2:1. Диарейный синдром характеризовали отсутствием диареи ночью; позывы к стулу возникали утром, после завтрака, стулу предшествовали боли «спастического» характера, которые проходили после стула. Запоры носили постоянный характер (у 8), у 2 больных — периодический. Вариант СРК с болями и вздутием у 7 больных носил постоянный характер, у 3 — характер приступообразного вздутия.
Исследование исключало органическую патологию (ирригоскопия, колоноскопия). Контролем за моторикой явилась: электромиография, «карболеновая проба» в динамике. Лечение Дицетелом проводили на протяжении 4 недель в суточной дозе 150 мг. Если эффект оценивали как недостаточный, доза могла быть увеличена до 300 мг/сутки; если не удавалось справиться с диареей, то лечение дополнялось Смектой; если не удавалось справиться с запором, то назначали Форлакс. Эффективность лечения оценивалась по динамике клинических симптомов, по скорости и полноте купирования болей.
Результаты лечения
На фоне проводимой терапии Дицетелом в течение 2 недель общая эффективность составила 63% (при этом боли купированы полностью у всех больных). Запоры, в основном, были купированы на дозе 150 мг/сутки — у 77% больных, у 5 больных потребовалось увеличение дозы Дицетела до 300 мг/сутки и у одного больного потребовалось назначение Форлакса. При варианте с диареей эффект составил 74%, у 5 больных (15%) потребовалось назначение Смекты, хотя общее количество послаблений уменьшилось до 1–2 раз в сутки; у 1 больного исчезли императивные позывы, хотя утренний (жидкий, полуоформленный) стул сохранился. При изучении «карболеновой пробы» было зарегистрировано удлинение времени пассажа по кишечнику с 14,3 часа до 18,1 часа. В группе больных с болями и метеоризмом в течение первых двух недель лечения достигнуто уменьшение степени вздутия и болей у 63% больных и только увеличение дозы Дицетела до 300 мг/сутки привело к регрессии симптоматики у 83% больных; 17% больных нуждались в лекарственной коррекции дисбиоза, и только после этого был достигнут полный эффект у 87% больных (4 больных сохранили умеренную степень вздутия живота, постоянную или приступообразную).
Таким образом, использование Дицетела для лечения больных СРК (разные варианты) в дозе 150 мг/сутки оказалось эффективным у 63% больных, увеличение дозы препарата до 300 мг/сутки позволило добиться эффекта в целом у 77% больных; у 17% больных потребовался сочетанный вариант лечения (Смекта у больных с послаблением; Форлакс — у больных с запором и Бактисубтил — у больных с вздутием и болями).
У 2 больных (6%) достаточный эффект получен не был, и мы рассмотрели их в плане более сложного генеза функциональных расстройств, хотя боли значительно уменьшились.
Вторую группу составили 30 больных в возрасте от 20 до 74 лет с различными дискинезиями желчевыводящих путей. 10 больных имели гипокинетическую дискинезию желчного пузыря (ГДЖП), 10 — дисфункцию сфинктера Одди 3-го типа (ДСО), 10 — гиперкинетическую дискинезию желчного пузыря (ГрДЖП). Средний возраст больных составил 54,6 года. Мужчин было — 3, женщин — 27.
Все пациенты предъявляли жалобы на боли различного характера, диспепсические проявления и кишечные расстройства. Боли локализовывались, в основном, в правом подреберье, не иррадиировали, провоцировались едой, интенсивность была умеренной.
Результаты изучения диспепсического синдрома и характер стула представлены в табл. 2.
Как видно из таблицы, диспепсические проявления регистрировались у 70% больных (с разной частотой в разных группах, максимально у больных с гипокинезией желчного пузыря и ДСО) и практически у половины больных фиксировались те или иные нарушения стула.
Рандомизированные в группы больные получали монотерапию Дицетелом в суточной дозе 50 мг × 3 раза. Общая продолжительность лечения составила 20 дней.
Результаты лечения
В целом положительный эффект в отношении диспепсического синдрома достигнут у 80% больных.
Нормализация работы кишечника и при запорах (6 больных), и при полосах (5 больных) наступила к 10–14 дню лечения у всех больных.
Среди побочных эффектов — у 2 пациентов наблюдали усиление болей в верхних отделах живота — в одном случае в начале лечения, а в другом на 6–9 дни лечения, что послужило причиной отмены препарата.
Таким образом, положительный эффект в отношении болевого синдрома получен в 83% случаев, диспепсического — в 80% случаев и синдрома кишечной дисфункции — в 100% случаев.
Было оценено также влияние Дицетела на состояние желчного пузыря, при этом отмечено преимущественное влияние препарата на гипертонус желчного пузыря и восстановление нормокинезии у 80% больных, что, по всей вероятности, связано с восстановлением градиента давления и нормализацией опорожнения желчного пузыря в связи с этим.
При оценке влияния Дицетела на функциональную патологию кишечника (СРК) и дискинезию желчевыводящих путей на основании проводимого исследования следует отметить эффект у 80% больных. Это хороший показатель, при этом фиксируется небольшое количество «побочных» эффектов, что связано, по всей вероятности, с селективным эффектом его действия, реализующимся только на уровне кишечника. Недостаточность эффекта у отдельной категории больных может быть усилена дозой (максимальные дозы не использовались) или сочетанным вариантом лечения на отдельные симптомы кишечной диспепсии.
Отсутствие эффекта у небольшой части больных (6–10%) связано, скорее всего, с нарушением других регулирующих систем (опиодных, вегетативной нервной системы, гормональной системы), которые подлежат использованию в случаях неуспеха лечения.
Заключение
В настоящем сообщении представлены данные о функциональных расстройствах кишечника и желчевыводящих путей, а также лекарственные препараты, влияющие на тонус и сократительную способность ЖКТ. На основании собственных данных предложен алгоритм выбора препарата, влияющего на дисфункциональные расстройства и результаты лечения больных с разными вариантами СРК и дисфункциональными расстройствами желчевыводящих путей (всего 60 больных). В лечении использован представитель миотропных спазмолитиков — селективный блокатор кальциевых каналов Дицетел. Показана высокая эффективность препарата в лечении (83% — эффективность в лечении СРК и 80% — в лечении функциональных расстройств желчевыводящих путей).
Селективность препарата обеспечила небольшое количество побочных эффектов (3,3%). В отношении дисфункции кишечника препарат обладает прямым спазмолитическим эффектом, в отношении дисфункции желчевыводящих путей — преимущественно непрямым эффектом, связанным с уменьшением внутрипросветного давления в кишечнике, восстановлением градиента давления и пассажа желчи. Препарат может быть рекомендован для лечения указанных расстройств.
Литература
О. Н. Минушкин, доктор медицинских наук, профессор
ФГБУ УНМЦ Управления делами Президента РФ, Москва
_550.gif)
.gif)
.gif)