Если интервал больше ритма что простаивает
Научная электронная библиотека
Прекина В И, Самолькина О Г,
1.2. Интервал QT
Изменения интервала QT обусловлены преимущественно нарушением процесса реполяризации, то есть процессом восстановления ионного баланса клеток миокарда желудочков, начинающимся сразу после деполяризации. Сильное укорочение или удлинение интервала QT cвидетельствует о нарушении синхронизации процесса реполяризации, что является сильным аритмогенным фактором, приводящим к возникновению желудочковых аритмий, чаще по типу «torsades de pointes», имеющим большой риск внезапной смерти. Полиморфная желудочковая тахикардия «torsades de pointes», составляет 13 % в структуре причин внезапной аритмической смерти у больных с синдромом удлиненного QT [113].
Наиболее важным ионным сдвигом во время реполяризации является выходящий поток ионов калия, которые возвращают потенциал действия к исходному состоянию отрицательной поляризации. Идентифицировано, по крайней мере, шесть различных калиевых «токов»; они функционируют в разное время потенциала действия и модулируются несколькими факторами (ионами кальция, мускариновыми рецепторами, ацетилхолином, аденозиндифосфатом) [141]. В сложном процессе деполяризации и реполяризации клеток участвуют ионы (натрий, калий, кальций, хлор, магний), каналы, рецепторы и насосы. При нарушении в одном или нескольких механизмах возможны изменения интервала QT.
На ЭКГ интервал QT часто бывает неразделим с интервалом Q-T-U. Поэтому, когда речь идет о удлиненном QT, подразумевают Q-T-U. У здоровых зубец U регистрируется на ЭКГ в 11,5–50 %, а на ЭКГ высокого разрешения и до 70 % случаев [67, 101]. В последние годы, обсуждается гипотеза постпотенциалов (автопотенциалов). Удлинение интервала QT согласно этой гипотезе является отражением замедленной реполяризации и наличием постдеполяризации (ранней или поздней). При этом ранняя постдеполяризация характерна для развития бради-зависимых, а поздняя – для тахи-зависимых аритмий. Идея медленной постдеполяризации подтверждена обнаружением связи этого феномена с освобождением и выходом ионизированного кальция из саркоплазматического ретикулума [204].
В настоящее время изучено два патогенетических механизма аритмий при синдроме удлиненного интервала QT или QTU. Первый механизм «внутрисердечных нарушений» реполяризации миокарда, а именно, повышенная чувствительность миокарда к аритмогенному эффекту катехоламинов. Второй патофизиологический механизм – дисбаланс симпатической иннервации (снижение правосторонней симпатической иннервации вследствие слабости или недоразвития правого звездчатого ганглия) [170, 177, 180, 190]. Недооценка удлинения интервала QT может существенно повысить риск развития у больных угрожающих жизни тахиаритмий и внезапной смерти [55, 86].
Наследственные варианты синдрома следует дифференцировать от приобретенного, в том числе лекарственно-индуцированного удлинения интервала QT [166]. Вклад генетических факторов в возникновение вторичного удлинения интервала QT нельзя недооценивать. В значительной части случаев, у больных с вторичным удлинением интервала QT выявляются, так называемые «молчащие мутации», или функциональные полиморфизмы в тех же генах, которые отвечают за первичные формы синдрома удлиненного интервала QT. Изменения в строении ионных каналов кардиомиоцитов в таких случаях минимальны и могут долго оставаться бессимптомными. По данным разных авторов, более 30 % лиц с мутациями в заинтересованных генах, не имеют никаких признаков заболевания (в том числе, электрокардиографических) [214]. Однако сочетание генетических особенностей строения калиевых каналов и вторичных причин может вызывать кли-
нически значимые аритмии.
В последние годы растет интерес к влиянию лекарственных препаратов на интервал QT. Структурные заболевания сердца, такие как гипертрофия, ишемия миокарда, а также сердечная недостаточность, нарушения метаболизма (ацидоз, гипокалиемия, гиперкальциемия), могут сопровождаться удлинением интервала QT на ЭКГ [247].
Инсульт и продолжительность интервала QT взаимосвязаны. Риск возникновения инсульта у лиц с удлиненным QTc был почти в 3 раза выше, чем у лиц с нормальным QTc [257]. В исследовании японского населения риск возникновения инсульта и ИБС при удлинении интервала QTc cреди мужчин был выше, среди женщин такой связи не было [225].
У больных с острым инсультом на ЭКГ выявляется удлинение интервала QT, при этом обратная динамика более выражена при благоприятном течении геморрагического инсульта и субарахноидального кровоизлияния, а при ИИ изменения носят более стойкий характер [53]. Удлинение интервала Q-T чаще наблюдается при очагах в левом полушарии головного мозга [54]. В экспериментах на кошках при раздражении области гиппокампа и задне-боковой зоны возникало удлинение интервала QT, появлялся желудочковый ритм, переходящий в мерца-
ние желудочков [46].
При ИИ смертность в течение 90 дней была выше при удлинении интервала QTc более 440 мс у женщин и более чем 438 мс у мужчин, по сравнению с пациентами без удлинения интервала [258]. Увеличение постинсультной кардиальной смерти связано с удлинением интервала QT [172] и коррелирует с индексом массы миокарда левого желудочка, АД и снижением ВРС [272].
АГ оказывает непосредственное влияние на величину дисперсии QTc независимо от наличия гипертрофии миокарда ЛЖ и величины индекса массы миокарда ЛЖ. Удлиненная дисперсия QTc у больных с повышенным АД, в сравнении с лицами без АГ, встречается достоверно чаще [106]. У больных АГ с наличием концентрических типов ремоделирования ЛЖ значения дисперсии QTc были достоверно выше, чем у больных АГ с эксцентрическим ремоделированием [148].
Показана связь продолжительности интервала QT с такими факторами, как пол, возраст, состояние нейрогормональной регуляции, психоэмоциональное и физическое напряжение [97]. ХМ позволяет выявить эпизодическое удлинение интервала QT, оценить реакцию интервалов QT на изменение частоты ритма [103, 157, 240].
1.2.1. Интервал QT в острейшем периоде инсульта
В последние годы широко изучаются причины вторичного (приобретенного) удлинения интервала QT, а в электрофизиологии – новые направления, связанные с определением длительности QT, дисперсии QT, вариабельности и циркадности QT и связи с фатальными аритмиями. Так как эти исследования требуют длительного наблюдения за динамикой QT, невозможно провести их без длительного мониторирования ЭКГ с автоматическим вычислением продолжительности QT. Однако при холтеровском мониторировании методики определения длительности QT более сложные, чем при анализе ЭКГ покоя, и поэтому недостаточно разработаны их нормативные параметры. Противоречиями в методиках и оценках возможности точного определения длительности интервала QT во многом объясняется осторожное отношение некоторых исследователей к клинико-прогностическому значению данного параметра по ХМ [200].
Поэтому, с целью изучения сопоставимости результатов измерений интервала QT, мы провели сравнительный анализ длительности интервала по ЭКГ покоя методом ручного измерения в отведении V5 и по данным холтеровского мониторирования методом автоматического анализа в том же отведении при тех же значениях интервала RR (или ЧСС) у 26 пациентов.
Средняя длительность интервала QT по ЭКГ покоя и данным ХМ существенно не различались и составили 400,00 ± 14,28 и 390,0 ± 13,76 мс
соответственно. Корреляционная взаимосвязь была прямая и сильная (r = 0,972; Р 460 мс и > 440 мс (пограничные значения) [87]. За минимальный эпизод удлиненного интервала QTс принимали эпизод продолжительностью не менее 20 с. Оценивали суммарную продолжительность эпизодов удлиненного интервала QTс за сутки, период бодрствования и сна.
Анализ показателей интервала QT показал, что стойкого удлинения интервала QT у пациентов, включенных в исследование, не было. Наблюдались лишь транзиторные эпизоды его удлинения. При этом эпизоды удлиненного интервала QTс более 460 мс встречались у больных ОГ на 16,57 % (P 440 мс не было.
Средние показатели интервала QT в ОГ достоверно превышали таковые в ГК: QTмакс – на 14,04 мс (на 3,27 %) (P ОГ ( n = 106)
Удлинение интервала QT
Статья посвящена врождённому и приобретённому ЭКГ-синдрому удлинённого интервала QТ, а также Амиодарону, как наиболее частой медикаментозной причине данного состояния.
Синдром удлинения QT интервала представляет собой сочетание удлиненного интервала QT стандартной ЭКГ и угрожающих жизни полиморфных желудочковых тахикардий (torsade de pointes – «пируэт»). Пароксизмы желудочковых тахикардий типа «пируэт» клинически проявляются эпизодами потери сознания и нередко заканчиваются фибрилляцией желудочков, являющихся непосредственной причиной внезапной смерти.
Длительность интервала QT зависит от частоты сердечных сокращений и пола пациента. Поэтому используют не абсолютную, а корригированную величину интервала QT (QTc), которую рассчитывают по формуле Базетта:
где: RR – расстояние между соседними зубцами R на ЭКГ в сек. ;
К = 0, 37 для мужчин и К = 0, 40 для женщин.
Удлинение интервала QT диагностируют в том случае, если длительность QTc превышает 0, 44 с.
Установлено, что как врожденные, так и приобретенные формы удлинения интервала QT являются предикторами фатальных нарушений ритма, которые, в свою очередь, приводят к внезапной смерти больных.
Так, отсутствует единое мнение о верхней границе нормальных значениях дисперсии корригированного интервала QT. По мнению одних авторов, предиктором желудочковых тахиаритимий является QTcd более 45, другие исследователи предлагают считать верхней границей нормы QTcd 70 мс и даже 125 мс.
Cуществуют два наиболее изученных патогенетических механизма аритмий при синдроме удлиненного QT интервала. Первый – механизм «внутрисердечных нарушений» реполяризации миокарда, а именно, повышенная чувствительность миокарда к аритмогенному эффекту катехоламинов. Второй патофизиологический механизм – дисбаланс симпатической иннервации (снижение правосторонней симпатической иннервации вследствие слабости или недоразвития правого звездчатого ганглия). Эта концепция подтверждается на моделях с животными (удлинение QT интервала после правосторонней стеллэктомии) и результатами левосторонней стеллэктомии в лечении резистентных форм удлинения QT интервала.
Частота выявления удлинения интервала QT у лиц с пролапсами митрального и/или трикуспидального клапанов достигает 33%. По мнению большинства исследователей, пролапс митрального клапана является одним из проявлений врожденной дисплазии соединительной ткани. Среди других проявлений «слабости соединительной ткани» – повышенная растяжимость кожи, астенический тип телосложения, воронкообразная деформация грудной клетки, сколиоз, плоскостопие, синдром гипермобильности суставов, миопия, варикозное расширение вен, грыжи. Рядом исследователей выявлена взаимосвязь увеличенной варибельности QT интервала и глубины пролабирования и/или наличия структурных изменений (миксоматозная дегенерация) створок митрального клапана. Одной из главных причин формирования удлинения интервала QT у лиц с пролапсом митрального клапана является генетически предопределенный или приобретенный дефицит магния
Приобретенное удлинение QT интервала может возникнуть при атеросклеротическом или постинфарктном кардиосклерозе, при кардиомиопатии, на фоне и после перенесенного мио– или перикардита. Увеличение дисперсии интервала QT (более 47 мс) может также являться предиктором развития аритмогенных синкопальных состояний у больных с аортальными пороками сердца.
Удлинение интервала QT может наблюдаться и при синусовой брадикардии, атриовентрикулярной блокаде, хронической цереброваскулярной недостаточности и опухоли головного мозга. Острые случаи удлинения интервала QT могут также возникать при травмах (грудной клетки, черепно–мозговых).
Автономная нейропатия также увеличивает величину интервала QT и его дисперсию, поэтому данные синдромы имеют место у больных сахарным диабетом I и II типов.
Удлинение интервала QT может иметь место при нарушениях электролитного баланса с гипокалиемией, гипокальциемией, гипомагнезиемией. Подобные состояния возникают под воздействием многих причин, например, при длительном приеме диуретиков, особенно петлевых (фуросемид). Описано развитие желудочковой тахикардии типа «пируэт» на фоне удлинения интервала QT cо смертельным исходом у женщин, находившихся на малобелковой диете с целью снижения массы тела.
Общеизвестно удлинение QT при острой ишемии миокарда и инфаркте миокарда. Стойкое (более 5 дней) увеличение интервала QT, особенно при сочетании с ранними желудочковыми экстрасистолами, прогностически неблагоприятно. У этих пациентов выявлено значительное (в 5–6 раз) повышение риска внезапной смерти.
В патогенезе удлинения QT при остром инфаркте миокарда, несомненно, играет роль гиперсимпатикотония, именно этим многие авторы объясняют высокую эффективность b–блокаторов у этих пациентов. Кроме того, в основе развития данного синдрома лежат и электролитные нарушения, в частности, дефицит магния. Результаты многих исследований свидетельствуют о том, что до 90% больных с острым инфарктом миокарда имеют дефицит магния. Выявлена также обратная корреляционноая взаимосвязь уровня магния в крови (сыворотке и эритроцитах) с величиной интервала QT и его дисперсией у пациентов с острым инфарктом миокарда.
У пациентов с идиопатическим пролапсом митрального клапана лечение следует начинать с применения пероральных препаратов магния (Магнерот по 2 табл. 3 раза в день в течение не менее 6 месяцев), поскольку тканевой дефицит магния считают одним из основных патофизиологических механизмов формирования как синдрома удлинения QT интервала, так и «слабости» соединительной ткани. У этих лиц после лечения препаратами магния не только нормализуется величина интервала QT, но и уменьшаются глубина пролабирования створок митрального клапана, частота желудочковых экстрасистол, выраженность клинических проявлений (синдрома вегетативной дистонии, геморрагических симптомов и др. ). Если лечение пероральными препаратами магния через 6 месяцев не оказало полного эффекта показано добавление b–блокаторов.
Другой важной причной удлинёния интервала QT является приём специальных медикаментов, одним из таких препаратов, чаще всего используемых в клинической практике является Амиодарон (Кордарон).
Амиодарон относится к III классу антиаритмических препаратов (класс ингибиторов реполяризации) и обладает уникальным механизмом антиаритмического действия, так как помимо свойств антиаритмиков III класса (блокада калиевых каналов) он обладает эффектами антиаритмиков I класса (блокада натриевых каналов), антиаритмиков IV класса (блокада кальциевых каналов) и неконкурентным бета-блокирующим действием.
Кроме антиаритмического действия у него имеются антиангинальный, коронарорасширяющий, альфа- и бета-адреноблокирующий эффекты.
Антиаритмические свойства:
— увеличение продолжительности 3-ей фазы потенциала действия кардиомиоцитов, в основном за счет блокирования ионного тока в калиевых каналах (эффект антиаритмика III класса по классификации Вильямса) ;
— уменьшение автоматизма синусового узла, приводящее к уменьшению частоты сердечных сокращений;
— неконкурентная блокада альфа- и бета- адренергических рецепторов;
Описание
— замедление синоатриальной, предсердной и атриовентрикулярной проводимости, более выраженное при тахикардии;
— отсутствие изменений проводимости желудочков;
— увеличение рефрактерных периодов и уменьшение возбудимости миокарда предсердий и желудочков, а также увеличение рефрактерного периода атриовентрикулярного узла;
— замедление проведения и увеличение продолжительности рефрактерного периода в дополнительных пучках предсердно-желудочкового проведения.
Другие эффекты:
— отсутствие отрицательного инотропного действия при приеме внутрь;
— снижение потребления кислорода миокардом за счет умеренного снижения периферического сопротивления и частоты сердечных сокращений;
— увеличение коронарного кровотока за счет прямого воздействия на гладкую мускулатуру коронарных артерий;
— поддержания сердечного выброса за счет снижения давления в аорте и снижения периферического сопротивления;
— влияние на обмен тиреоидных гормонов: ингибирование превращения Тз в Т4 (блокада тироксин-5-дейодиназы) и блокирование захвата этих гормонов кардиоцитами и гепатоцитами, приводящее к ослаблению стимулирующего влияния тиреоидных гормонов на миокард.
Терапевтические эффекты наблюдаются в среднем через неделю после начала приема препарата (от нескольких дней до двух недель). После прекращения его приема амиодарон определяется в плазме крови на протяжении 9 месяцев. Следует принимать во внимание возможность сохранения фармакодинамического действия амиодарона в течение 10-30 дней после его отмены.
Каждая доза амиодарона (200 мг) содержит 75 мг йода.
Показания к применению
Профилактика внезапной аритмической смерти у больных группы высокого риска
Для больных хронической сердечной недостаточностью амиодарон является единственным разрешенным к применению антиаритмиком. Это связано с тем, что прочие препараты у этой категории пациентов или увеличивают риск внезапной середечной смерти, или угнетают гемодинамику.
При наличии ишемической болезни сердца препаратом выбора является соталол, на 1/3 являющийся, как известно, b–адреноблокатором. Но при его неэффективности в нашем распоряжении вновь только амиодарон. Что же касается больных с артериальной гипертензией, то из их числа, в свою очередь, выделяются пациенты с выраженной и невыраженной гипертрофией левого желудочка. Если гипертрофия невелика (в Руководстве 2001 г. – толщина стенки левого желудочка менее 14 мм), препарат выбора – пропафенон, но при его неэффективности – как всегда, амиодарон (наряду с соталолом). Наконец, при выраженной гипертрофии левого желудочка, как и при хронической сердечной недостаточности, амиодарон – единственный возможный препарат.
Источник: Остроумова О. Д. Удлинение интервала QT. РМЖ №18 2001 С 750-54
Статья добавлена 11 апреля 2015 г.
Выявления нарушения сердечного ритма при помощи холтеровского мониторирования ЭКГ
Аксельрод А.С., заведующая отделением функциональной диагностики
Клиники кардиологии ММА им. И.М. Сеченова
Каждый практикующий кардиолог согласится, что ощущение перебоев в работе сердца является одной из самых частых жалоб пациентов кардиологического стационара и кардиологического поликлинического отделения. При этом даже самый опытный врач никогда не будет полностью уверен, какие именно нарушения сердечного ритма стоят за этими жалобами. Именно поэтому на сегодняшний день суточное мониторирование ЭКГ по Холтеру по-прежнему является обязательным исследованием у таких пациентов.
При выявлении нарушений ритма стоит обратить внимание на три основных вопроса:
• какова минимальная и максимальная длительность мониторирования ЭКГ для регистрации нарушений ритма?
• двух-, трех- или двенадцатиканальные регистраторы (мониторы) ЭКГ – что выбрать для оценки эктопической активности?
• каков минимальный и достаточный перечень программных возможностей?
Продолжительность мониторирования ЭКГ: как долго?
Этот вопрос задается наиболее часто. Наиболее правильным является мониторирование ЭКГ не менее 24 и не более 72 часов. При этом можно использовать как
24-часовой (чаще и предпочтительнее), так и 72-часовой регистратор. При отсутствии нарушений ритма за первые сутки после 30-минутного отдыха пациента проводится повторное мониторирование. При отсутствии значимых нарушений ритма за вторые сутки регистрации мониторирование продолжается до 72 часов. В дальнейшем повторная суточная регистрация ЭКГ производится на усмотрение лечащего врача.
Важным является также вопрос необходимости 72-часового регистратора. Такой регистратор может быть удобен, если пациент описывает связь ощущений перебоев в работе сердца с конкретными стереотипными физическими усилиями при длительных переездах, т.е. в ситуации, когда больной не может вернуться в клинику через 24 часа.
Если у пациента с жалобами на перебои в работе сердца нарушения ритма не выявлены в течение 3 суток мониторирования ЭКГ, стоит попытаться их индуцировать во время нагрузочного ЭКГ теста.
Выбор мониторов для анализа нарушений ритма.
При покупке двухканального регистратора дополнительных вопросов при анализе суточной ЭКГ, как правило, не возникает. Некоторое преимущество в редких случаях имеют трехканальные регистраторы: наличие дополнительного канала позволяет более четко дифференцировать желудочковые и суправентрикулярные аберрантные нарушения ритма.
Использование двенадцатиканальных регистраторов для выявления нарушений ритма не является целесообразным: исследование становится менее комфортно, но наличие отведений не вносит дополнительной информации о нарушениях сердечного ритма.
Использование двенадцатиканального монитора оправдано лишь в том случае, когда возникает необходимость оценить динамику сегмента ST и связать нарушения сердечного ритма с эпизодами ишемии миокарда.
Необходимые возможности программного обеспечения.
Правильный выбор возможностей программного обеспечения позволяет значительно облегчить и ускорить анализ холтеровской регистрации. Кроме того, врач, имеющий весь необходимый перечень программных возможностей, будет чувствовать себя гораздо увереннее и всегда будет знать, что ничего не пропустил во время анализа регистрации. Именно поэтому к выбору возможностей программного обеспечения необходимо подойти серьезно.
Нередко ощущения перебоев в работе сердца возникают у подростков и лиц молодого возраста с выраженной синусовой аритмией. При этом мы обычно обращаем внимание на ее выраженность и связь с фазами дыхания, которая наиболее отчетливо будет видна при использовании как стандартного выделения фрагмента для печати (рис.1, А), так использования «обзора ЭКГ» (рис. 1, Б).
Рис.1. Пациент К., 17 лет. Дыхательная аритмия в ночное время: стандартное выделение фрагмента для печати (А) и использование «обзора ЭКГ» (Б).
Именно «обзор ЭКГ» позволяет четко дифференцировать дыхательную и недыхательную синусовую аритмию с пароксизмальными суправентрикулярными нарушениями ритма: можно увидеть паузы после пароксизмов ускоренных суправентрикулярных ритмов и стереотипные периоды «гармошкообразного» рисунка с постепенным началом и постепенным окончанием при дыхательной аритмии, как это было представлено на рисунке 1.
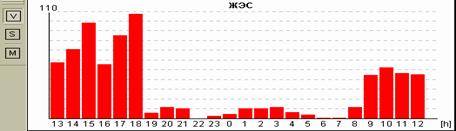
У пациентки Н. на фоне блокированных предсердных экстрасистол выявлена эктопическая желудочковая активность. Особенно важно, что желудочковые экстрасистолы регистрируется именно ночью и только на фоне указанных эпизодов. Взаимосвязь этих событий крайне важна для правильного подбора терапии, поскольку проясняет механизм эктопической желудочковой активности. Именно поэтому предпочтительно, чтобы Ваше программное обеспечение позволяло автоматически построить графики распределения событий по часам.
Некоторые программы вместо графика распределения событий по часам предоставляют пользователям таблицу распределения по часам. На наш взгляд, такая таблица является гораздо менее удобной и наглядной и не позволяет врачу «с первого взгляда» оценить преобладание выявленных нарушений в то или иное время суток.
Важной является также возможность изменения вольтажа полученного ЭКГ-сигнала. Такая возможность особенно необходима, если регистрируется слабо выраженный, низкоамплитудный зубец Р. Так, например, при смене положения тела в ночное время изменение вольтажа может облегчить диагностику феномена миграции водителя ритма по предсердиям и смены источника автоматизма (рис. 3).
Рис. 3. Пациент А., 77 лет: смена источника автоматизма (короткий эпизод нижнепредсердного ритма из 3 сокращений).
Увеличение общей амплитуды ЭКГ-сигнала приводит к более отчетливой визуализации зубца Р и, следовательно, достоверной диагностике описанных изменений. Кроме того, увеличение вольтажа важно при дифференциальной диагностике пароксизмальных суправентрикулярных нарушений ритма. Так, на рисунке 4, представлена хаотическая предсердная тахикардия с наложившимися на зубцы Т зубцами Р. При отсутствии возможности увеличения вольтажа врачом распечатанные фрагменты тахикардии будут гораздо менее наглядными и вызовут большее количество вопросов у других врачей.
Рис. 4. Больная У., 75 лет: пароксизм хаотической предсердной тахикардии
Обязательной является также возможность выделения цветом нарушений ритма различной топографии. На рисунке 5 представлены суправентрикулярные (выделены синим) и желудочковые (выделены красным) групповые экстрасистолы.
Нередко в холтеровской регистрации встречаются ранние экстрасистолы двух видов: с коротким интервалом сцепления без наслоения на предыдущий зубец Т, а также с коротким интервалом сцепления с наслоением на нисходящее колено зубца Т, т.е. классические экстрасистолы типа R на Т. Способность программ выделять ранние желудочковые экстрасистолы (особенно с классификацией в отдельную группу «R на Т») также значительно облегчают работу врача: используя ее, можно быстро просмотреть запись и подсчитать количество таких экстрасистол.
Рис. 6. Ранние желудочковые экстрасистолы.
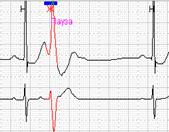
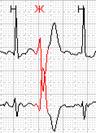
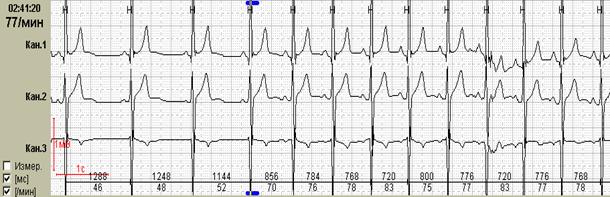
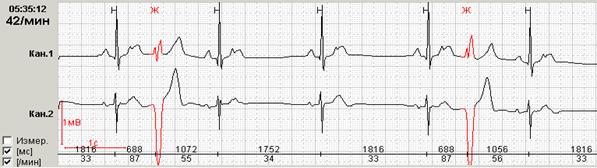
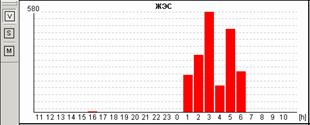
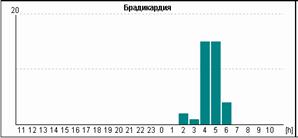
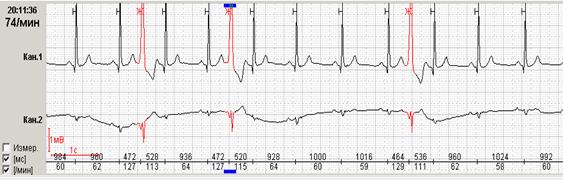
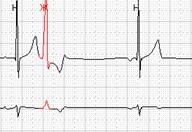
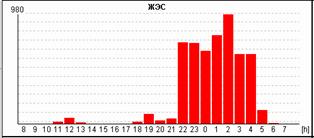
Если ранние желудочковые экстрасистолы возникают на фоне синусовой брадикардии, то последующая компенсаторная пауза может превышать 2 секунды (рис. 7А). При этом подсчет RR-пауз в течение суток и график их распределения по часам (рис. 7Б) стоит отразить в заключении и распечатать стереотипные фрагменты.
Рис. 7. Ранняя желудочковая экстрасистола «R на Т» на фоне синусовой брадикардии у пациента с ишемической болезнью сердца: А – стереотипный фрагмент регистрации; Б – график распределения таких фрагментов в течение суток с выраженным преобладанием в ночные часы.
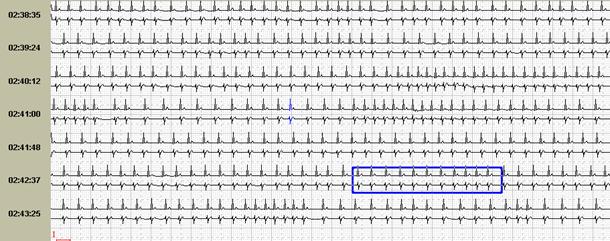
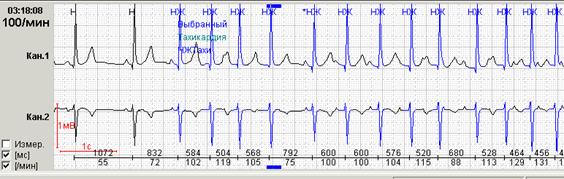
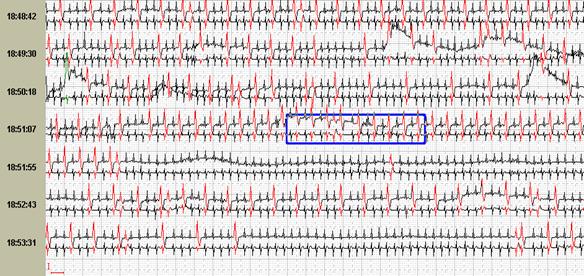
Способность программы при первичном автоматическом анализе выявлять эктопические пароксизмальные нарушения сердечного ритма и производить их количественный подсчет является одной из самых главных возможностей. При их значительном количестве в течение суток имеет большое значение количественный подсчет пароксизмов до и после лечения. Именно поэтому приобретение программного обеспечения без возможности выявления и/или количественного подсчета пароксизмальных нарушений ритма крайне нежелательно (рис.8).
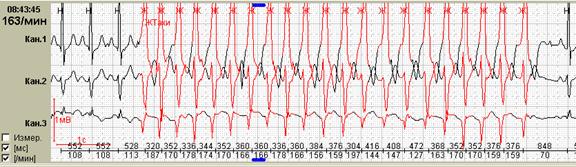
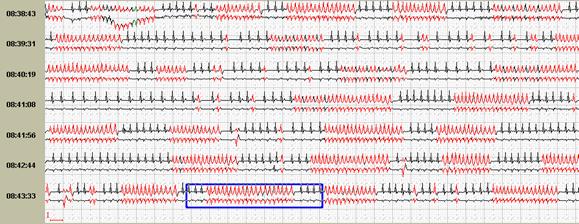
Рис. 8. Больная Г., 60 лет, страдает аритмогенной дисплазией правого желудочка: во время холтеровского мониторирования зарегистрированы частые пароксизмы правожелудочковой тахикардии на фоне аритмогенной дисплазии правого желудочка: А-стереотипные фрагменты желудочковой тахикардии; Б-опция «обзор ЭКГ» наглядно иллюстрирует частоту пароксизмов.
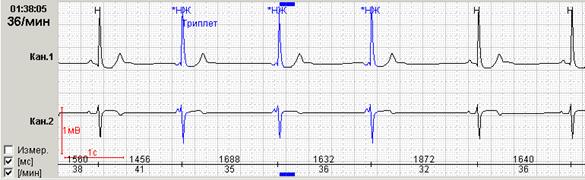
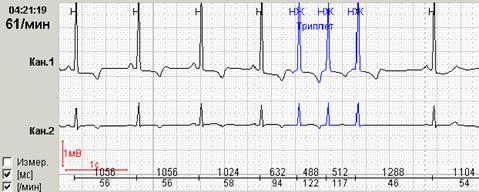
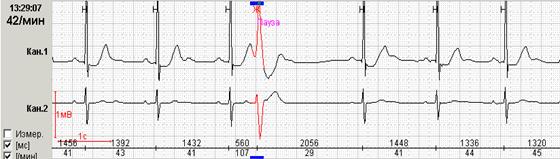
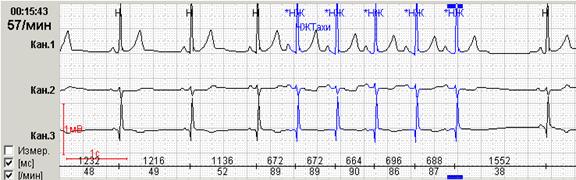
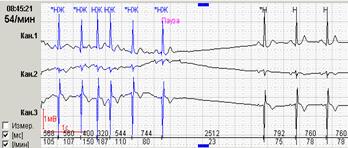
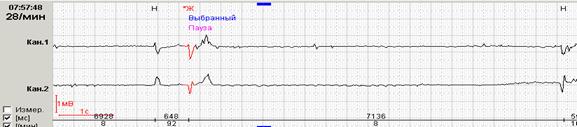
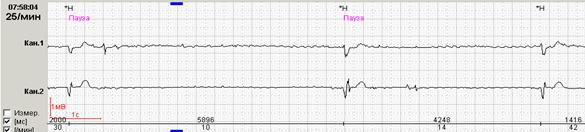
Кроме того, для пациентов с пароксизмальными эктопическими нарушениями ритма крайне важной является возможность выявления пауз, выведение их на экран и разметка во фрагменте абсолютного значения пауз с их количественным подсчетом. Особенности «выхода» из очередного пароксизма – через значимые или незначимые паузы – нередко предопределяют особенности клинического течения заболевания с развитием так называемых «аритмогенных синкоп». Так, на представленном ниже рисунке 9, короткий пароксизм ускоренного суправентрикулярного ритма заканчивается незначимым удлинением RR-интервала до 1552 мсек, а у больного с пароксизмами фибрилляции предсердий пауза превышает 2 секунды и при нарастании этого значения может стать причиной синкопального состояния.
Рис. 9. Короткий незначимый пароксизм ускоренного суправентрикулярного ритма у пациентки с гипертонической болезнью (А) и больного с идиопатической пароксизмальной фибрилляцией предсердий (Б).
Рис. 10. Гемодинамически значимые паузы у пациента с синдромом Фредерика. Переход ФП в идиовентрикулярный ритм через RR-паузу=7.14 сек (А), далее (Б) – идиовентрикулярный ритм с паузами до 5.9 сек.
Большинство программ, представленных различными фирмами-производителями, предоставляют возможность врачу отредактировать в ручном режиме количество и продолжительность как RR-пауз, так и максимального RR-интервала. Возможность такой редакции является крайне полезной при повторном мониторировании одного и того же пациента (например, при динамическом наблюдении больного с мерцательной аритмией, принимающего β-адреноблокатор).
Программное обеспечение также должно давать врачу возможность установить абсолютное значение RR-интервалов, которые будут называться паузами. Это важно, поскольку понятие «пауза» будет различаться у взрослых и детей. У взрослых как на фоне синусового ритма, так и на фоне фибрилляции/трепетания предсердий паузами являются RR-интервалы более 2 секунд. У детей абсолютные значения пауз зависят от возраста.
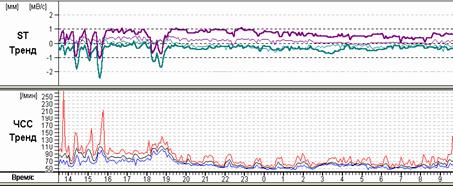
Сопоставление различных возможностей графического изображения друг с другом нередко существенно меняют взгляд лечащего врача на тактику ведения пациента. Так, например, на рисунке 11 представлены различные экраны программы, расширяющие представления о генезе имеющихся нарушений ритма. Стереотипные фрагменты аллоритмии (А), отчетливо видной и в «обзоре ЭКГ» (Б), по времени четко соответствуют периодам ходьбы, описанным в дневнике пациентки. При этом можно видеть ишемическую динамику сегмента ST по трендам (В) и преобладание желудочковой экстрасистолии в периоды бодрствования на графике распределения по часам (Г).
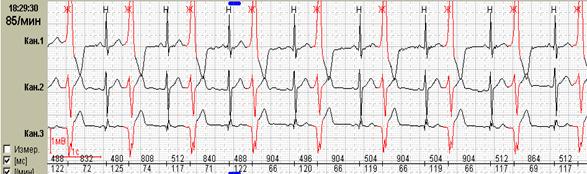
Рис. 11. Больная А., 75 лет. Диагноз: стенокардия напряжения II функционального класса. Представлены стереотипные фрагменты желудочковой бигеминии (А), их большое количество в «обзоре ЭКГ» (Б), тренды динамики сегмента ST, ЧСС (В) и график распределения по часам желудочковой экстрасистолии (Г).
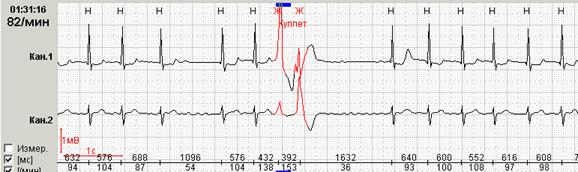
Рис. 12. Больной Н., 68 лет: желудочковый куплет на фоне фибрилляции предсердий.
Нередко Ваше программное обеспечение в автоматическом режиме выявляет фоновую фибрилляцию и/или трепетание предсердий (как и имеющиеся на фоне синусового ритма пароксизмы). Тем не менее, врачу стоит в обязательном порядке проверить в «обзоре ЭКГ», все ли пароксизмы выявлены при автоматическом анализе. В настоящее время практически все существующие программы не способны на полное автоматическое выявление как фоновой мерцательной аритмии, так и суправентрикулярных пароксизмов. К сожалению, не всегда декларируемые производителем возможности программы соответствуют реальности на практике.
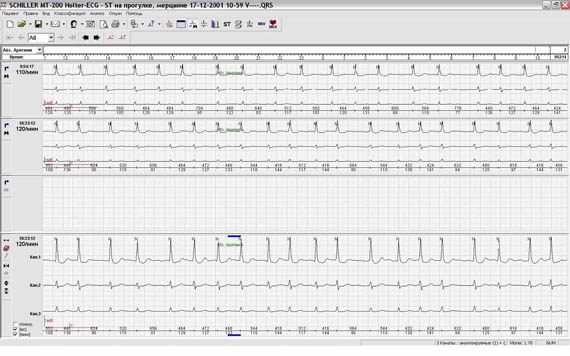
Рис. 13. Программа четко визуализирует мерцательную аритмию
В заключении хочется напомнить, что именно нарушения сердечного ритма являются наиболее частым показанием для проведения холтеровского мониторирования ЭКГ. Поэтому при выборе минимальных и оптимальных возможностей программного обеспечения Вам стоит изучить предлагаемое программное обеспечение особенно внимательно.