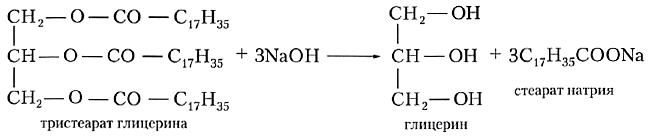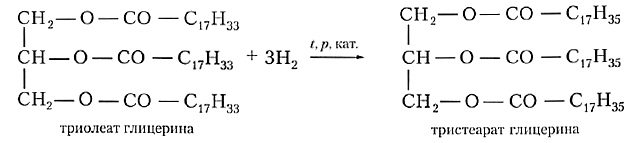Жир образуется в результате взаимодействия чего
Номенклатура жиров
Общее название жиров – триацилглицерины (триглицериды).
Существует несколько способов назвать молекулу жира.
Например, жир, образованный тремя остатками стеариновой кислоты, будет иметь следующие названия:
Физические свойства жиров
Жиры растворимы в органических растворителях и нерастворимы в воде. С водой жиры не смешиваются.
| Животные жиры — предельные | Растительные жиры (масла) — непредельные |
| Твёрдые, образованы предельными кислотами – стеариновой и пальмитиновой. Все животные жиры, кроме рыбьего – твёрдые. | Жидкие, образованы непредельными кислотами – олеиновой, линолевой и другими. Все растительные жиры, кроме пальмового масла – жидкие. |
Химические свойства жиров
1. Гидролиз (омыление) жиров
Жиры подвергаются гидролизу в кислой или щелочной среде или под действием ферментов.
1.1. Кислотный гидролиз
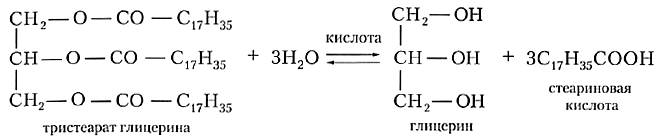
Под действием кислот жиры гидролизуются до глицерина и карбоновых кислот, которых входили в молекулу жира.
| Например, при гидролизе тристеарата глицерина в кислой среде образуется стеариновая кислота и глицерин |
1.2. Щелочной гидролиз — омыление жиров
При щелочном гидролизе жиров образуется глицерин и соли карбоновых кислот, входивших в состав жира.
2. Гидрирование (гидрогенизация) ненасыщенных жиров
Гидрогенизация жиров — это процесс присоединения водорода к остаткам непредельных кислот, входящих в состав жира.
При этом остатки непредельных кислот переходят в остатки предельных, жидкие растительные жиры превращаются в твёрдые (маргарин).
| Например, триолеат глицерина при гидрировании превращается в тристеарат глицерина: |
| Количественной характеристикой степени ненасыщенности жиров служит йодное число, показывающее, какая масса йода может присоединиться по двойным связям к 100 г жира. |
3. Мыло и синтетические моющие средства
При щелочном гидролизе жиров образуются мыла – соли высших жирных кислот.
Стеарат натрия – твёрдое мыло.
Стеарат калия – жидкое мыло.
Моющая способность мыла зависит от жесткости воды. Оно хорошо мылится и стирает в мягкой воде, плохо стирает в жёсткой воде и совсем не стирает в морской воде, так как содержащие в ней ионы Ca 2+ и Mg 2+ дают с высшими кислотами нерастворимые в воде соли.
| Например, тристеарат глицерина взаимодействует с сульфатом кальция |
Поэтому наряду с мылом используют синтетические моющие средства.
Их производят из других веществ, например из алкилсульфатов — солей сложных эфиров высших спиртов и серной кислоты.
Далее алкилсульфат гидролизуется щелочью:
Эти соли содержат в молекуле от 12 до 14 углеродных атомов и обладают очень хорошими моющими свойствами. Кальциевые и магниевые соли этих веществ растворимы в воде, а потому такие мыла моют и в жесткой воде. Алкилсульфаты содержатся во многих стиральных порошках.
А8. Жир образуется в результате взаимодействия 1) стеариновой кислоты и метанола 2) олеиновой кислоты и этиленгликоля 3) ацеталь
А8. Жир образуется в результате взаимодействия
1) стеариновой кислоты и метанола 2) олеиновой кислоты и этиленгликоля
3) ацетальдегида и глицерина 4) глицерина и пальмитиновой кислоты
А9. Оцените правильность суждений.
А. Фруктоза и крахмал при определенных условиях подвергаются гидролизу.
Б. Сахароза состоит из остатков глюкозы и фруктозы.
1) верно только А 2) верно только Б 3) верны оба суждения 4) оба неверны
А10. Более сильные основные свойства проявляет
1) метиламин 2) аммиак 3) глицерин 4) анилин
А11. Бензол можно получить
1) дегидрированием циклогептана 2) дегидрированием циклогексана
3) тримеризацией этилена 4) крекингом метана
А12.Уксусную кислоту можно получить в реакции
1) ацетата натрия с концентрированной серной кислотой
2) восстановления ацетальдегида
3) хлорэтана и раствора щелочи
4 )щелочного гидролиза метилацетата
Часть В
В 3. Установите соответствие между веществом и реагентами, с которыми оно взаимодействует.
ФОРМУЛА ВЕЩЕСТВА РЕАГЕНТЫ
А) СН3 – СООН 1) H2, Zn, KOH
Б) СН3 – СОН 2) O2, H2, Ag2O(аммиач. р-р)
В) СН2 = СН – СООН 3) CH3OH, Mg, Ag2O(аммиач. р-р)
Г) Н – СООН 4) NaOH, Na2CO3, Cl2(hν)
В4. Из 34,5 г этанола получили 11,2 л (н. у.) этилена. Рассчитайте объемную долю выхо¬да продукта реакции.
Часть С
С1.Написать уравнения реакций, с помощью которых можно осуществить превращения
Этанол—- этилен —-1, 2 –дибромэтан —-ацетилен —-бензол
С2.Решить задачу
При сжигании углеводорода объемом 2,24л образовался оксид углерода (IV) массой 13,2г и вода массой 7,2г. Относительная плотность паров этого вещества по водороду равна 22. Найдите молекулярную формулу углеводорода.
А8. Жир образуется в результате взаимодействия
1) стеариновой кислоты и метанола 2) олеиновой кислоты и этиленгликоля
3) ацетальдегида и глицерина 4) глицерина и пальмитиновой кислоты
А9. Оцените правильность суждений.
А. Фруктоза и крахмал при определенных условиях подвергаются гидролизу.
Б. Сахароза состоит из остатков глюкозы и фруктозы.
1) верно только А 2) верно только Б 3) верны оба суждения 4) оба неверны
А10. Более сильные основные свойства проявляет
1) метиламин 2) аммиак 3) глицерин 4) анилин
А11. Бензол можно получить
1) дегидрированием циклогептана 2) дегидрированием циклогексана
3) тримеризацией этилена 4) крекингом метана
А12.Уксусную кислоту можно получить в реакции
1) ацетата натрия с концентрированной серной кислотой
2) восстановления ацетальдегида
3) хлорэтана и раствора щелочи
4 )щелочного гидролиза метилацетата
Часть В
В 3. Установите соответствие между веществом и реагентами, с которыми оно взаимодействует.
ФОРМУЛА ВЕЩЕСТВА РЕАГЕНТЫ
А) СН3 – СООН 1) H2, Zn, KOH
Б) СН3 – СОН 2) O2, H2, Ag2O(аммиач. р-р)
В) СН2 = СН – СООН 3) CH3OH, Mg, Ag2O(аммиач. р-р)
Г) Н – СООН 4) NaOH, Na2CO3, Cl2(hν)
В4. Из 34,5 г этанола получили 11,2 л (н. у.) этилена. Рассчитайте объемную долю выхо¬да продукта реакции.
Часть С
С1.Написать уравнения реакций, с помощью которых можно осуществить превращения
Этанол—- этилен —-1, 2 –дибромэтан —-ацетилен —-бензол
С2.Решить задачу
При сжигании углеводорода объемом 2,24л образовался оксид углерода (IV) массой 13,2г и вода массой 7,2г. Относительная плотность паров этого вещества по водороду равна 22. Найдите молекулярную формулу углеводорода.
А8. Жир образуется в результате взаимодействия
1) стеариновой кислоты и метанола 2) олеиновой кислоты и этиленгликоля
3) ацетальдегида и глицерина 4) глицерина и пальмитиновой кислоты
А9. Оцените правильность суждений.
А. Фруктоза и крахмал при определенных условиях подвергаются гидролизу.
Б. Сахароза состоит из остатков глюкозы и фруктозы.
1) верно только А 2) верно только Б 3) верны оба суждения 4) оба неверны
А10. Более сильные основные свойства проявляет
1) метиламин 2) аммиак 3) глицерин 4) анилин
А11. Бензол можно получить
1) дегидрированием циклогептана 2) дегидрированием циклогексана
3) тримеризацией этилена 4) крекингом метана
А12.Уксусную кислоту можно получить в реакции
1) ацетата натрия с концентрированной серной кислотой
2) восстановления ацетальдегида
3) хлорэтана и раствора щелочи
4 )щелочного гидролиза метилацетата
Часть В
В 3. Установите соответствие между веществом и реагентами, с которыми оно взаимодействует.
ФОРМУЛА ВЕЩЕСТВА РЕАГЕНТЫ
А) СН3 – СООН 1) H2, Zn, KOH
Б) СН3 – СОН 2) O2, H2, Ag2O(аммиач. р-р)
В) СН2 = СН – СООН 3) CH3OH, Mg, Ag2O(аммиач. р-р)
Г) Н – СООН 4) NaOH, Na2CO3, Cl2(hν)
В4. Из 34,5 г этанола получили 11,2 л (н. у.) этилена. Рассчитайте объемную долю выхо¬да продукта реакции.
Часть С
С1.Написать уравнения реакций, с помощью которых можно осуществить превращения
Этанол—- этилен —-1, 2 –дибромэтан —-ацетилен —-бензол
С2.Решить задачу
При сжигании углеводорода объемом 2,24л образовался оксид углерода (IV) массой 13,2г и вода массой 7,2г. Относительная плотность паров этого вещества по водороду равна 22. Найдите молекулярную формулу углеводорода.
Жир образуется в результате взаимодействия чего
Процесс получения сложных эфиров носит название реакции этерификации. Эта реакция с использованием общих формул описывается уравнением
Именно реакцией этерификации в 1759 г. в результате взаимодействия уксусной кислоты с этиловым спиртом был получен первый сложный эфир — этиловый эфир уксусной кислоты:
Обратите внимание на то, как строится название сложного эфира. Оно состоит из четырёх слов, указывающих на название углеводородного радикала и исходной кислоты. Например, продукт взаимодействия муравьиной кислоты с метиловым спиртом — метиловый эфир муравьиной кислоты:
Катион водорода в схеме реакции указывает на то, что реакция этерификации протекает в присутствии кислоты в качестве катализатора.
Сложные эфиры с небольшой молекулярной массой представляют собой легковоспламеняющиеся жидкости с характерным, часто приятным запахом. Они нерастворимы в воде, но прекрасно растворяют различные органические вещества.
Реакции этерификации обратимы. В присутствии кислот сложные эфиры разлагаются водой — гидролизуются, что можно рассматривать как реакцию, обратную их получению:
В присутствии щелочей гидролиз сложных эфиров необратим, так как образующаяся кислота связывается щёлочью с образованием соли, неспособной вступать в реакцию со спиртом:
Нахождение в природе и применение сложных эфиров
Сложные эфиры широко распространены в природе. Неповторимый аромат цветов и фруктов часто обусловлен присутствием веществ именно этого класса. Сложные эфиры с большой молекулярной массой представляют собой твёрдые вещества — воски. Пчелиный воск — это смесь сложных эфиров, образованных карбоновыми кислотами и спиртами с длинными углеводородными цепями.
Синтетические сложные эфиры используют в пищевой промышленности в качестве добавок для придания фруктовых запахов напиткам и кондитерским изделиям. Благодаря хорошей растворяющей способности сложные эфиры входят в состав растворителей лаков и красок.
Жиры, их строение и свойства
Люди стали использовать жиры в повседневной жизни значительно раньше, чем задумались об их химическом строении. Животные и растительные жиры — важные компоненты пищи. Жиры необходимы для построения клеточных мембран и как источник энергии, поскольку калорийность жиров в 2 раза выше, чем других питательных веществ — углеводов и белков. У позвоночных животных жиры откладываются в жировой ткани, сосредоточенной в основном в подкожной жировой клетчатке и сальнике. В растениях жиры содержатся в сравнительно небольших количествах, за исключением семян масличных растений, в которых содержание жиров может быть более 50%.
Жиры используют не только в пищевой промышленности. Их используют в качестве смазки, косметических и лекарственных средств, для приготовления масляных красок и олифы.
В 1779 г. шведский химик К. Шееле получил из оливкового масла вязкую жидкость, сладкую на вкус, — простейший трёхатомный спирт глицерин. Вскоре выяснилось, что глицерин входит в состав молекул любых жиров. Позднее французский химик М. Шеврёль доказал, что, помимо глицерина, при нагревании жиров в присутствии кислоты образуются и карбоновые кислоты.
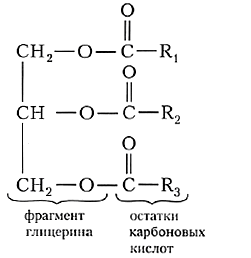
| Жиры представляют собой сложные эфиры трёхатомного спирта глицерина и высших карбоновых кислот. |
Общую формулу жиров можно представить в следующем виде:
В состав жиров чаще всего входят остатки карбоновых кислот, содержащих чётное число атомов углерода и неразветвлённую углеродную цепь. Наиболее часто в составе жиров встречаются остатки пальмитиновой, стеариновой и олеиновой кислот. В одной молекуле кислотные остатки могут быть различными, поэтому в общей формуле жиров углеводородные радикалы R обозначены разными цифрами.
Сравните состав стеариновой (С17Н35СООН) и олеиновой (С17Н33СООН) кислот. У стеариновой кислоты углеводородный радикал отвечает формуле СnН2n+1, т. е. является предельным. Следовательно, стеариновая кислота относится к предельным карбоновым кислотам. В углеводородном радикале олеиновой кислоты на два атома водорода меньше, поскольку в нём содержится одна двойная углерод-углеродная связь. Олеиновая кислота относится к непредельным карбоновым кислотам.
Жиры животного происхождения имеют твёрдую консистенцию (есть и исключения, например жидкий рыбий жир). В состав молекул твёрдых жиров входят остатки предельных кислот. Растительные жиры, которые часто называют растительными маслами, образованы остатками непредельных кислот, имеют жидкую консистенцию (исключение — твёрдое пальмовое масло). Кстати, название олеиновой кислоты произошло от латинского слова oleum — масло.
Жиры гидрофобны, т. е. нерастворимы в воде, но хорошо растворяются в органических растворителях: этиловом спирте, гексане, тетрахлорметане.
Жиры проявляют все характерные для сложных эфиров химические свойства. Главное из них — это гидролиз. Молекулы воды атакуют связи между кислотным остатком и фрагментом глицерина, в результате чего происходит распад молекулы жира:
Для жира, образованного стеариновой кислотой (такое вещество называют тристеаратом глицерина), уравнение реакции гидролиза выглядит следующим образом:
В качестве катализатора гидролиза жиров выступают кислоты. Такой гидролиз так и называют — кислотный гидролиз. Жирные руки трудно отмыть холодной водой, но стоит только протереть их ломтиком лимона, как они становятся заметно чище. Даже при таком непродолжительном контакте с лимонной кислотой жир частично гидролизуется.
Гидролиз жиров в присутствии щелочей называют щелочным гидролизом:
Щёлочь действует как катализатор, а также связывает образующиеся кислоты, превращая их в соли карбоновых кислот. Соли не способны вступать в реакцию этерификации с глицерином, и гидролиз становится необратимым. Неслучайно бытовые средства для удаления жира и засоров в раковинах более чем наполовину состоят из щёлочи.
Щелочной гидролиз жиров называют также омылением. Это название обусловлено тем, что образующиеся при этом натриевые и калиевые соли высших карбоновых кислот являются мылами.
Твёрдые жиры животного происхождения более ценны и дорогостоящи, чем жидкие растительные масла. Можно ли превратить жидкий жир в твёрдый химическим путём? Если вы вспомните, что растительные масла, в отличие от животных жиров, содержат остатки непредельных кислот, то нетрудно догадаться: гидрированием двойных связей С=С растительные масла превращают в аналог твёрдых жиров. Полученный продукт называют саломасом, его используют для приготовления маргарина и других продуктов питания:
Подобный процесс в больших масштабах проводят на жировых комбинатах.
Двойные связи непредельных кислот в жидких жирах сохраняют способность к реакциям полимеризации. Это свойство используют при изготовлении олифы — натуральной (на основе льняного или конопляного масла) или синтетической. При нанесении на деревянную поверхность олифа под действием кислорода воздуха полимеризуется с образованием прочной защитной плёнки. Олифу используют и при изготовлении и разбавлении масляных красок.
Справочная таблица «Сложные эфиры»
Конспект урока по химии «Сложные эфиры. Жиры». В учебных целях использованы цитаты из пособия «Химия. 10 класс : учеб, для общеобразоват. организаций : базовый уровень / О. С. Габриелян, И. Г. Остроумов, С. А. Сладков. — М. : Просвещение». Выберите дальнейшее действие: