Дазолик и трихопол в чем разница
Антихеликобактерные средства (ч. 2)
Схема эрадикации бактерии H. pylori подбирается в индивидуальном порядке в зависимости от чувствительности бактерии и реакции организма на выбранные препараты.
Преферанская Нина Германовна
Доцент кафедры фармакологии института фармации им. А.П. Нелюбина Первого МГМУ им. И.М. Сеченова (Сеченовский университет), к.фарм.н.
Амоксициллин (табл./капс. 250 мг, 500 мг) — полусинтетический антибиотик пенициллинового ряда широкого спектра действия, с умеренной активностью в отношении H. pylori. Биодоступность составляет 70–80%, растворимая лекарственная форма — 90%. В тканях достигается терапевтическая концентрация. Амоксициллин характеризуется широким спектром антимикробного действия, низким уровнем резистентности, хорошей всасываемостью в желудочно–кишечном тракте, высокой биодоступностью и кислотостойкостью. Блокада амоксициллином пенициллиносвязывающих белков приводит к остановке роста и гибели микробной клетки.
Период полувыведения — 1–1,5 ч. Выводится на 50–70% почками в неизмененном виде путем канальцевой секреции (80%) и клубочковой фильтрации (20%), печенью — 10–20%. В небольшом количестве выделяется с грудным молоком.
Противопоказаниями служит повышенная чувствительность к амоксициллину, детский возраст до 3 лет.
Важно! Вызывает аллергические реакции, тошноту, нарушения со стороны крови и лимфатической системы очень редко, диарею, очень редко кристаллурию.
Кларитромицин (табл. 250 мг, 500 мг; капс. 250 мг) — относится к группе полусинтетических макролидов, оказывает дозозависимый бактериостатический эффект за счет блокирования белковых систем микробной клетки, взаимодействует с 50S рибосомальной субъединицей, подавляет синтез белка бактерий. Однако при достижении концентрации, которая в 2–3 раза превышает минимальную ингибирующую концентрацию, оказывает бактерицидное действие. Бактерицидное действие оказывает в отношении H. pylori, данная активность Кларитромицина выше при нейтральном pH, чем при кислом. Кларитромицин по эффективности в отношению к H. pylori превышает все другие активные субстанции этой группы. Обладает широким спектром действия и является одним из наиболее эффективных и распространенных макролидов. При приеме внутрь хорошо всасывается, концентрация его в тканях намного превышает сывороточную. Максимальное накопление также наблюдается в слизистой ЖКТ.
Препарат хорошо проникает внутрь клеток (моноцитов, макрофагов, фагоцитов), создавая высокие внутриклеточные концентрации. Высокие концентрации в очаге воспаления делают его средством выбора при H. pylori — ассоциированной патологии желудка и 12-перстной кишки. Благодаря лиофильности способен проникать в клетки и накапливаться в высоких концентрациях в слизистой оболочке желудка и двенадцатиперстной кишки, что имеет большое значение при эрадикации H. pylori.
Также нельзя не вспомнить позитивный эффект санации, присущий Кларитромицину. Широкий спектр активности данного антибиотика по отношению к грампозитивным и грамнегативным бактериям позволяет элиминировать патогенные и условно–патогенные возбудители из полости ЖКТ, колонизация которых наблюдается в условиях хеликобактер–ассоциированных заболеваний. Препарат обладает собственной противовоспалительной активностью, что обусловлено угнетением продукции провоспалительных цитокинов и стимуляцией синтеза противовоспалительных гуморальных факторов. Однако самым главным его качеством является способность разрушать матрикс биопленки. 99% микроорганизмов, к которым относится и H. pylori, существуют не в виде отдельных микроорганизмов, а в составе сложно организованных сообществ — биопленок, которые представляют собой совокупность бактериальных клеток, которые окружены внеклеточным матриксом, который имеет полисахаридную природу. Матрикс выполняет защитную функцию и часто является причиной устойчивости микроорганизмов к действию антибиотиков, резистентность бактерий в составе биопленки возрастает в 10–1000 раз.
Важно! При применении препарата могут возникать диарея, гиперчувствительность, аллергические реакции, часто сыпь, очень редко может вызвать анафилактоидную реакцию, дерматит, нарушение слуха, звон в ушах (частота неизвестна), а также снижение числа лейкоцитов и тромбоцитов.
Метронидазол (ТН «Трихопол», «Флагил», табл. 250 мг) — противопротозойный препарат, относится к производным 5-нитроимидазола, активен в отношении микроаэрофилов H. pylori. Механизм действия заключается в биохимическом восстановлении 5-нитрогруппы внутриклеточными транспортными протеинами анаэробных микроорганизмов и простейших. Препарат оказывает избирательный бактерицидный эффект в отношении тех микроорганизмов, ферментные системы которых способны восстанавливать нитрогруппу. Восстановленная 5-нитрогруппа взаимодействует с дезоксирибонуклеиновой кислотой (ДНК) клетки микроорганизмов. Возникает ингибирование тканевого дыхание, нарушается репликация ДНК, синтез нуклеиновых кислот и синтез белка, что ведет к гибели бактерий.
Метронидазол быстро проникает в ткани (легкие, почки, печень, кожу, желчь, спинномозговую жидкость, слюну, семенную жидкость, вагинальный секрет), в грудное молоко и проходит через плацентарный барьер. Около 30–60 % метронидазола метаболизируется путем гидроксилирования, окисления и глюкуронирования.
Препарат медленно выводится из организма, период полувыведения 8–10 час., при повторных введениях кумулирует. Проникает в ткани и жидкости организма, обеспечивая терапевтические концентрации.
Важно! Вызывает темное окрашивание мочи, металлический привкус во рту, тошноту, рвоту, диарею, могут возникать аллергические реакции: крапивница, кожная сыпь, нарушения со стороны иммунной системы: ангионевротический отек, анафилактический шок.
КОМПЛЕКСНОЕ ПРИМЕНЕНИЕ ЛС
Успешная схема лечения основана на сочетании препаратов, которые предотвращают возникновение резистентности и настигают бактерию в различных участках желудка. Терапия должна гарантировать, что даже небольшая популяция микроорганизмов не останется жизнеспособной. В схемы терапии обязательно включают препараты висмута, химиотерапевтические препараты и ингибиторы протонной помпы (о последних препаратах мы писали в предыдущей статье).
Существуют стандартные схемы лечения двух-, трех- или четырехкомпонентной терапии в период лечения и обострения гастритов, язвенной болезни12-перстной кишки и желудка.
Используют:
√ БИТЕРАПИЮ: Ранитидин + Висмута цитрат (Пилорид);
Амоксициллин + Метронидазол (Хеликоцин);
√ ТРОЙНУЮ ТЕРАПИЮ:
Кларитромицин + Омепразол + Тинидазол (Пилобакт);
√ КВАДРОТЕРАПИЮ:
ЭРАДИКАЦИОННАЯ ТЕРАПИЯ H. pylori включает комплекс нескольких препаратов. Распространенная ошибка, которая зачастую приводит к непредсказуемым результатам, замена даже одного хорошо изученного препарата из стандартной схемы на другой препарат той же группы. Использование данных схем лечения значительно улучшает состояние больных и предупреждают развитие рецидивов.
Применение комбинированных лекарственных препаратов «Пилобакт», «Пилорид», «Хеликоцин» и др. значительно улучшает состояние больных и предупреждает развитие рецидивов. Как правило, терапия обязательно включает антисекреторные препараты, химиотерапевтические средства, гастропротекторы и препараты коллоидного висмута.
Интенсивную терапию проводят до достижения устойчивой ремиссии и отсутствия рецидивов у больных в течение 1,5–2 лет. При необходимости проводят профилактическую противорецидивную терапию. При применении комбинированной терапии необходимо убедиться в безопасном применении сочетанных препаратов, их переносимости и эффективности. При применении таких препаратов могут наблюдаться нежелательные побочные явления: тошнота, рвота (20%), диарея (10%), псевдомембранозный колит (1%), головокружение (2%), чувство жжения в ротовой полости, глотке, кандидоз (15%). Неэффективность лечения может быть обусловлена нарушением правил приема препаратов или развитием устойчивости бактерии к ним. Но несмотря на применение комбинированных схем лечения, у 10–20% пациентов, инфицированных H. pylori, не удается достичь элиминации возбудителя.
Повышают клиническую эффективность эрадикационной терапии комбинации ингибиторов протонной помпы (ИПП) с противомикробными препаратами.
Предполагается, что антисекреторные препараты из группы ИПП могут способствовать повышению концентрации антимикробных средств (Метронидазола и Кларитромицина) в просвете желудка. ИПП уменьшают объем желудочного сока, вследствие чего вымывание антибиотиков с поверхности слизистой уменьшается, а концентрация антибиотиков, соответственно, увеличивается. Кроме того, снижение объема соляной кислоты поддерживает стабильную терапевтическую концентрацию антимикробных препаратов. При проведении эрадикационной антихеликобактерной терапии совместно с ИПП является одним из необходимых условий.
Успешность комбинированных схем терапии определяется во многом правильным выбором антибактериального средства и обеспечением постоянно высокого уровня эрадикации бактерии. Удлинение курса лечения до 10–14 дней также повышает эффективность эрадикации в среднем на 5%, а назначение высоких (двойных) доз ИПП позволяет дополнительно получить 8% показателей эффективности эрадикации H. pylori.
Именно два антибактериальных агента Амоксициллин и Кларитромицин определяют высокую эффективность в отношении микроорганизмов, которые находятся в фазе деления. Поддержка уровня рН в желудке выше чем 3,0 при помощи антисекреторных препаратов резко тормозит процесс деградации Кларитромицина (при рН 1,0 в желудочном соке Т½ составляет 1 час, а при рН 7,0 205 час.), что обеспечивает полноценную эрадикацию H. pylori. На протяжении последних 20 лет в основных схемах эрадикационной терапии сохраняется стойкая комбинация указанных антибиотиков, что связано с фармакокинетическими и фармакодинамическими особенностями данных препаратов.
Схема эрадикации бактерии H. pylori подбирается в индивидуальном порядке в зависимости от чувствительности бактерии и реакции организма на выбранные препараты. Продолжительность курса лечения определяется лечащим врачом. Самолечение такого опасного заболевания, как хеликобактериоз, категорически противопоказано.
Применение метронидазола, тинидазола, ниморазола, тенонитрозола, орнидазола в лечении больных с хроническим урогенитальным трихомониазом
Опубликовано в журнале:
«ЗДОРОВЬЕ МУЖЧИНЫ», 2008, №1, с. 26-30
В.М. Kрасовский
Институт урологии АМН Украины (Kиев)
Изучена сравнительная эффективность использования препаратов Метронидазола, Тинидазола, Ниморазола, Тенонитрозола, Орнидазола в лечении 126 больных урогенитальным трихомониазом. Эффективность Метронидазола составила 40,4%, Тинидазола – 44,1%, Ниморазола – 85,7%, Тенонитрозола – 89,7%, Орнидазола – 93,3%, Орнидазола + Тенонитрозола – 97,7%. Препараты отличаются различной переносимостью и количеством побочных эффектов: Метронидазол – 23,3%, Тинидазол – 25%, Нимора-зол – 12,5%, Тенонитрозол – 12%, Орнидазол – 9,1%, Орнидазол + Тенонитрозол – 9,1%. Лучшие результаты получены в группах пациентов, которые получали: Орнидазол (93,3%), Тенонитрозол (89,7%), а также комбинация их последовательного применения Орнидазол + Тенонитрозол (97,7%). Результаты исследования можно использовать в клинической практике.
Kлючевые слова: хронический урогенитальный трихомониаз, лечение, Метронидазол, Тинидазол, Ниморазол, Тенонитрозол, Орнидазол.
Research of comparative efficiency of application of metronidazolum, tinidazolum, nimorazolum, tenonitrazolum, ornidazolum in treatment of patients with chronic urogenital trichmoniasis. V.M. Krasovsky
Keywords: chronic urogenital trichmoniasis, treatment, Metronidazolum, Tinidazolum, Nimorazolum, Tenonitrazolum, Ornidazolum.
В последние десятилетия трихомониаз получил широкое распространение. Чаще всего это заболевание диагностируют у мужчин и женщин молодого возраста – от 16 до 35 лет, из которых большой процент больных составляют лица с другими венерическими заболеваниями и те, кто часто меняют половых партнеров [1, 34].
Заражение трихомониазом происходит в основном половым путем, бытовым путем (плавая в бассейне или реке, в душе, в сауне) заразиться практически невозможно. Однако в сперме, моче и воде возбудитель остается жизнеспособным в течение 24 ч. У больных или у тех, кто перенес эту инфекцию, вырабатываются сывороточные и секреторные антитела, которые указывают на возбудителя, но иммунитет в отношении трихомонадной инфекции не развивается [1–5, 8, 11].
К главным особенностям заболевания следует отнести то, что возбудитель очень легко передается человеку, имевшему половую связь с инфицированным; наличие на поверхности микроорганизмов гиалуронидазы, каталазы, амилазы; способность повторять рельеф эпителиальной клетки и проникать в клетку хозяина; способность защититься от разрушительного действия организма с помощью фиксации на своей поверхности антитрипсина; наличие прямой зависимости вирулентности урогенитальных трихомонад от их гемолитической активности; способность прикрепляться к лейкоцитам, эритроцитам, эпителиальным клеткам за счет гликопротеида.
Выделяют несколько форм трихомониаза: свежая острая, подострая, торпидная; хроническая; трихомонадоносительство. Хроническая форма заболевания характеризуется малосимптомным течением, когда с момента заражения прошло более 2 мес. Периодические обострения могут быть спровоцированы снижением сопротивляемости организма, чрезмерным употреблением алкоголя, изменением рН содержимого мочеиспускательного канала. Трихомонадоносительство – форма заболевания, при которой отсутствуют какие-либо симптомы [2, 4, 5–10, 13].
Трихомониаз – многоочаговое заболевание. По данным Всемирной организации здравоохранения (1995), только у 10,5% больных трихомониаз протекает как моноинфекция, в 89,5% случаев выявляются смешанные трихомонадные инфекции в различных комбинациях: с микоплазмами – 47,3%; с гонококками – 29,1%; с гарднереллой – 31,4%; с уреаплазмой – 20,9%; с хламидиями – 20%; с грибами – 15%.
Диагностика трихомониаза осуществляется на основании клинических признаков и результатов лабораторных исследований. Для получения более точного результата используют сразу несколько методов, а материал для изучения берут из различных очагов воспаления. Применяют следующие лабораторные методы: латекс-агглютинация (используют для выявления трихомонадоносительства); культуральные (используют для диагностики атипичных форм); иммунологические; микроскопия нативного препарата (позволяет по грушевидной или овальной форме, а также характерным движениям микроорганизма определить наличие трихомонады); микроскопия окрашенного препарата (дает возможность проводить исследования, когда материал взят достаточно давно); люминесцентная микроскопия (основан на свечении микроорганизма в ультрафиолетовых лучах). Самый точный и современный метод – ДНK (ПЦР)-диагностика. Для ее проведения из биологического материала извлекают генетически уникальный кусочек ДНK микроорганизма. Все возможные ошибки данного метода составляют 5%. Этот метод отличается не только точностью, но и скоростью выполнения (1–2 дня) [2, 3, 5, 8–10, 12].
Лечение трихомониаза назначают обязательно после осмотра и лабораторного обследования с учетом количества очагов инфекции, тяжести заболевания и индивидуальных особенностей пациента. Кроме того, лечение трихомониаза по требованиям ВОЗ проводят всем половым партнерам, если у одного из них обнаружена инфекция (трихомонада). Особенностью заболевания является наличие множества очагов инфекции. Учитывая этот факт, больным назначают комплексную терапию, включающую: прротивопротозойные препараты; антибактериальные препараты; местное лечение; этиотропные методы; витамины; биостимуляторы; иммунокоррегирующие методы; симптоматическое лечение; гепатопротекторы; противогрибковые препараты. На фоне лечения половая жизнь и прием алкоголя не рекомендуются [2, 6–10,12, 13]. Выбор тактики лечения следует осуществлять индивидуально, с учетом клинико-анамнестических данных.
Лечение острой формы: этиотропная терапия; антибактериальные препараты по индивидуальным показаниям; ферменты, улучшающие пищеварение; витаминотерапия; противотрихомонадные препараты для местного применения в очагах воспаления. По окончании этиотропной терапии рекомендуется провести курс антиоксидантной терапии (перорально и местно) в сочетании с гепатопротекторными средствами.
Лечение хронической формы:
Первое контрольное обследование у мужчин проводят на 7–10-й день после окончания лечения трихомониаза: пальпаторное обследование предстательной железы и семенных пузырьков, микроскопическое исследование их секрета. Через 1 нед назначают провокацию. Если после провокации трихомонадная инфекция не обнаружена, то на последнее контрольное обследование пациент приходит через 1 мес.
Kритерии излеченности
Различают этиологическое и клиническое выздоровление от трихомониаза. Этиологическое выздоровление: при контрольных обследованиях после курса лечения трихомонады не обнаружены в течение 1–2 мес. у мужчин. Для контрольных обследований применяют культуральные и бактериоскопические лабораторные методы. Kлиническое выздоровление: исчезновение симптомов болезни. Нередко у мужчин после наступления этиологического выздоровления симптомы трихомониаза сохраняются. Посттрихомонадные воспалительные процессы бывают у пациентов с осложненными или хроническими формами болезни [9–13].
Этиотропную терапию трихомониаза проводят несколькими препаратами: это метронидазол, тинидазол, ниморазол, тенонитрозол, орнидазол, секнидазол, флюнидазол, карнидазол. Первых пять препаратов зарегистрированы и их применяют в Украине.
Лекарственная резистентность, ее механизмы и клиническое значение
В последние годы у микроорганизмов все чаще вырабатывается лекарственная резистентность к различными препаратам в связи с неконтролируемым, недостаточно интенсивным или длительным лечением, самолечением. Частота развития резистентности и уровень устойчивости существенно различаются в зависимости от вида микроорганизма, химического состава препарата, эффективности применяемых доз и схем лечения.
Развитие устойчивости связано в первую очередь со снижением активности нитроредуктаз микробной клетки и соответственно со снижением внутриклеточной биотрансформации препаратов. В результате уменьшается образование комплексов с ДНK, снижаются процессы образования свободных радикалов и концентрация цитотоксических продуктов метаболизма. Развитие устойчивости может быть обусловлено также нарушением транспортных систем клетки (снижение проницаемости клеточной стенки у анаэробов и микроаэрофилов и клеточной оболочки у простейших), включая феномен выброса.
Kроме того, главной проблемой в лечении трихомониаза сегодня выступает всевозрастающая резистентность трихомонады к антипротозойным препаратам. Так, согласно исследованиям, проведенным авторами в 1999 г., всего 35% штаммов трихомонад чувствительны к метронидазолу [4]. Согласно другим исследованиям, всего 55% трихомонад чувствительны к тинидазолу [5]. Соответственно изучение изменяющейся чувствительности трихомонад к современным антипротозойным препаратам является актуальной проблемой лечения трихомониаза и микст-инфекций половых путей.
В связи с этим была сделана попытка провести исследование сравнительной эффективности различных противотрихомонадных препаратов.
МАТЕРИАЛЫ И МЕТОДЫ
В отделении сексопатологии и андрологии Института урологии АМН Украины изучали клиническую эффективность различных противотрихомонадных препаратов: Метронидазола, Тинидазола, Ниморазола, Тенонитрозола, Орнидазола у больных хроническим урогенитальным трихомониазом. Кроме того, проводили ретроспективный анализ чувствительности влагалищной трихомонады к различным противопротозойным препаратам и оценивали их эффективность и безопасность.
Под наблюдением находились 370 пациентов с хроническим урогенитальным трихомониазом в возрасте от 21 до 48 лет и длительностью заболевания от 3 мес. до 8 лет. Диагноз урогенитального трихомониаза устанавливали на основании общепринятых принципов с выявлением трихомонад, что подтверждено микроскопией окрашенных мазков, исследованием нативного препарата, культуральным методом, а также методом ПЦР.
Все больные были разделены на группы:
1-я группа (52 пациента) получала в качестве противотрихомонадного препарата Метронидазол в стандартной дозе на протяжении 10 дней.
2-я группа (43 пациента) – Тинидазол по 0,5 г 4 раза в день с интервалом 15 мин 2 дня.
3-я группа (49 мужчин) – Орнидазол по 0,5 г 2 раза в день на протяжении 10 дней.
4-я группа (56 мужчин) – Ниморазол по 0,5 г 2 раза в день на протяжении 6 дней.
5-я группа (126 мужчин) – Тенонитрозол по 0,25 г 2 раза в день на протяжении 8 дней.
6-я группа (44 мужчин) – Орнидазол по 0,5 г 2 раза в день на протяжении 10 дней и Тенонитрозол по 0,25 г 2 раза в день на протяжении 8 дней.
С целью коррекции иммунного статуса назначали индуктор интерферона растительного происхождения кагоцел; как гепатопротектор использовали препарат легалон – 140 мг в день стандартных доз на курс лечения. Для получения антибактериального эффекта (ввиду наличия TANK-функции у трихомонады) назначали препарат группы макролидов кларитромицин в дозе по 500 мг 2 раза в сутки на протяжении 10 дней; пациенты также получали симптоматическое и физиотерапевтическое лечение.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЙ И ИХ ОБСУЖДЕНИЕ
Результаты комплексного курсового лечения пациентов в номинации «клиническое выздоровление» через 30 дней после окончания лечения приведено в табл. 1.
Таблица 1. Эффективность этиотропной терапии урогенитального трихомониаза различными препаратами
| Клиническая группа | Препарат | Количество больных | Клиническое выздоровление (абс. число) | Клиническое выздоровление, % |
| 1-я | Метронидазол | 52 | 21 | 40,4 |
| 2-я | Тинидазол | 43 | 19 | 44,1 |
| 3-я | Орнидазол | 49 | 45 | 93,3 |
| 4-я | Ниморазол | 56 | 48 | 85,7 |
| 5-я | Тенонитрозол | 126 | 113 | 89,7 |
| 6-я | Орнидазол + Тенонитрозол | 44 | 43 | 97,7 |
Результаты микроскопии секрета предстательной железы и молекулярно-генетического исследования соскоба слизистой оболочки мочеиспускательного канала мужчин в динамике приведено в табл. 3.
Таблица 3. Результаты микроскопии секрета предстательной железы при этиотропной терапии урогенитального трихомониаза различными препаратами
| Клиническая группа | Препарат | Количество больных | Микроскопия секрета ПЖ | ПЦР |
| 1-я | Метронидазол | 52 | 18 (34,6%) | 21 (40,4%) |
| 2-я | Тинидазол | 43 | 16 (37,2%) | 19 (44,1%) |
| 3-я | Орнидазол | 49 | 44 (89,8) | 45 (93,3%) |
| 4-я | Ниморазол | 56 | 44 (78,5%) | 48 (85,7%) |
| 5-я | Тенонитрозол | 126 | 121 (88,0%) | 113 (89,7%) |
| 6-я | Орнидазол + Тенонитрозол | 44 | 43 (97,7%) | 43 (97,7%) |
Kак видно из приведенных данных, лучшие результаты получены при использовании метода ПЦР в группах пациентов, которые получали: Орнидазол (93,3%), Тенонитрозол (89,7%), а также их комбинацию последовательного применения Орнидазол + Тенонитрозол (97,7%). Метод микроскопии показал несколько худшие результаты по всем группам пациентов, что обусловлено субъективностью самого метода и свойством мимикрии трихомонады. Но эффективность лечения в тех же группах была выше.
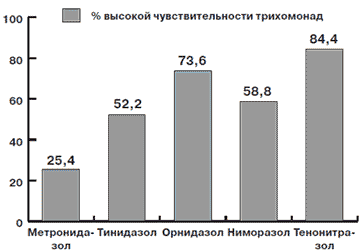
Рис 1. Процент высокой чувствительности трихомонады к различным препаратам
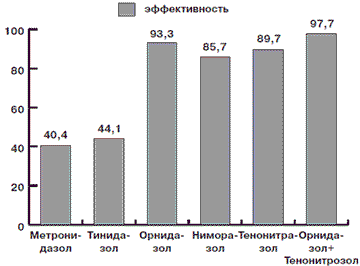
Кроме того, нами была оценена эффективность лечения различными препаратами больных, основываясь на полной эрадикации возбудителя, на что указывает молекулярно-генетический метод. Данные приведены на рис. 2.
Рис. 2. Эффективность терапии трихомониаза различными препаратами
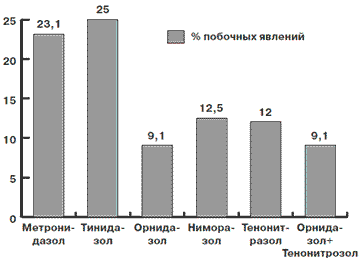
При определении количества побочных явлений при использовании различных противопротозойных препаратов выявлены результаты, которые приведены на рис. 3.
Рис. 3. Количество побочных явлений при использовании различных противопротозойных препаратов
ВЫВОДЫ