Диагноз мса что это
Диагноз мса что это
2. Спорадическая оливопонтоцеребеллярная атрофия (ОПЦА). При ОПЦА преобладает мозжечковая симптоматика (особенно атаксия и дизартрия), хотя редко бывает изолированной. Другими сопутствующими проявлениями могут быть паралич взора, гиперрефлексия, патологические стопные знаки и, что особенно важно, признаки паркинсонизма.
3. Синдром Шая-Дрейджера (Shy-Drager). При синдроме Шая-Дрейджера наблюдается дисфункция вегетативной нервной системы, что проявляется ортостатической гипотензией, нарушением функций тазовых органов, импотенцией.
Неясен вопрос о том, являются ли эти нарушения различными по сущности или только клиническими вариантами одного патологического состояния. Однако они обычно наблюдаются одновременно и имеют схожую патологическую картину. С диагностической точки зрения синдром МСА должен быть заподозрен у пациентов с гипокинезией, недостаточным эффектом леводопы при наличии значительных вегетативных или мозжечковых отклонений.
Методы нейровизуализации. МРТ головного мозга выявляет гипоинтенсивность в области скорлупы при СНД, вероятно, вследствие избыточного накопления железа в этой структуре. При ОПЦА можно наблюдать атрофию мозжечка.
Патоморфология. Общим признаком всех синдромов МСА является наличие характерных глиальных цитоплазматических включений. В дополнение к этому при синдроме Шая-Дрейджера обнаруживаются утрата нейронов и глиоз в двигательных ядрах блуждающего нерва и структурах спинного мозга, ответственных за вегетативную регуляцию.
4. Синдромы деменции. Болезнь Альцгеймера, болезнь Пика и болезнь с диффузными тельцами Леви —¦ это дегенеративные поражения ЦНС с преобладанием в клинической картине признаков деменции. Хотя дегенеративный процесс при этих заболеваниях затрагивает преимущественно некоторые области коры, могут быть вовлечены и подкорковые структуры, что приводит к развитию экстрапирамидных нарушений, включая паркинсонизм. Ключ к идентификации первичных дементных нарушений как причины паркинсонизма — это раннее появление признаков деменции, предшествующее развитию гипокинезии или ригидности.
Нейродегенеративные заболевания
Болезнь Вильсона — это аутосомно-рецессивное состояние, которое связано с нарушением экскреции меди, что приводит к накоплению ее в различных органах и системах, включая ЦНС, печень (цирроз), роговицу (кольца Кайзера-Флейшера), сердце и почки.
Болезнь Вильсона может начинаться в широком возрастном диапазоне — от 5 до 50 лет, но чаще всего в возрасте 8—16 лет. Неврологические расстройства присутствуют в начале заболевания примерно у 40 % больных. Такие экстрапирамидные симптомы, как дистония, ригидность и брадикинезия наиболее часто встречаются у детей, в то время как у взрослых более вероятно появление тремора и дизартрии. При болезни Вильсона могут наблюдаться разнообразные психические расстройства. Чрезвычайно важным для установления правильного диагноза является наличие печеночных расстройств (цирроз или хронический активный гепатит), особенно у молодых пациентов. Комбинация брадикинезии и тремора у этих больных позволяет предполагать болезнь Паркинсона. Однако слишком молодой возраст пациентов при появлении первых признаков заболевания, наличие психических расстройств, нарушений функций печени или дистонии являются основанием для поиска лабораторного подтверждения болезни Вильсона. Поскольку последствия этого заболевания предотвратимы при условии раннего назначения специфического лечения, возможность его наличия должна всегда учитываться при дифференциальном диагнозе вариантов атипичного паркинсонизма, особенно у людей моложе 50 лет.
Методы нейровизуализации. МРТ головного мозга выявляет расширение желудочков, а также атрофию в области коры и стволовых отделов. Базальные ганглии, особенно скорлупа, могут иметь гипо- или гиперинтенсивный характер в Т2-режиме исследования и гиподенсивный при КТ.
Иногда эти изменения в срезах среднего мозга при МРТ выглядят как «лицо гигантской панды».
Патоморфология. Наблюдается генерализованная атрофия мозгового вещества. Скорлупа, бледный шар и хвостатое ядро содержат кавитации и коричневый пигмент, что отражает накопление меди. d. Другие тесты. Наиболее информативный лабораторный тест —определение церулоплазмина плазмы, который обычно ниже 20 мг/дЛ (норма — 25—45 мг/дЛ). Уровень меди й плазме снижается, а выведение меди с мочой увеличивается. Исследование роговицы в свете щелевой лампы позволяет обнаружить кольца Кайзера-Флейшера почти у всех пациентов с неврологическими расстройствами, что является высокоспецифической, но не патогномоничной находкой. Если один или более из данных тестов в норме и диагноз вызывает сомнения, его следует подтвердить с помощью биопсии печени, которая позволяет констатировать увеличение содержания меди.
— Вернуться в оглавление раздела «Неврология.»
PsyAndNeuro.ru
Методы диагностики МСА на ранних стадиях
Мультисистемная атрофия (МСА) – это спорадическое фатальное нейродегенеративное заболевание с началом во взрослом возрасте, характеризующееся прогрессирующей вегетативной недостаточностью, паркинсонизмом, мозжечковым и пирамидным синдромами в различных комбинациях. МСА считается редким заболеванием (см. www.orpha.net ) : оно встречается в 3,4 – 4,9 случаях на 100 000 населения, но для группы старше 40 лет – 7,8.
Аутопсическим индикатором становится большое скопление α-синуклеина в олигодендроцитах вкупе со стриатонигральной дегенерацией или оливопонтоцеребеллярной атаксией.
МСА выделилась в отдельную нозологическую форму в 1969 г., обобщив три ранее отдельных диагноза. До начала XX века заболевание существовало под разными названиями: стриатонигральная дегенерация (СНД), оливомостомозжечковая атрофия (ОПЦА) и синдром Шая-Дрейджера (по имени исследователей Джорджа Милтона Шая и Глена Алберта Дрейджера).Термин МСА служит отныне отдельной клинико-патоморфической единицей для разнообразных сочетаний симптомов МСА. Термин «синдром Шая-Дрейджера» более не используется.
На данный момент заболевание имеет два подкласса: МСА-п (паркинсонического типа, или стратонигральная дегенерация, MSA-p – англ.) и МСА-ц (оливопонтоцеребеллярная атрофия, MSA-c – англ.). Различие двух типов становится ярче по мере прогрессирования заболевания.
Диагностика МСА очень затруднительна. Как правило, начало болезни приходится на шестой десяток жизни пациента. Продолжительность жизни варьируется от 6 до 15 лет после постановки диагноза.
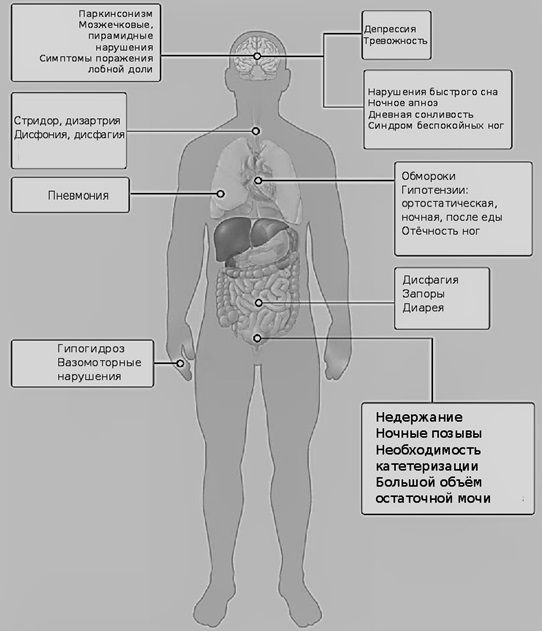
Симптоматика носит смешанный характер: помимо паркинсонизма, мозжечковой атаксии, двигательной атаксии, ортостатического коллапса , выявляются проблемы вегетативной системы (см. Табл. 1, и рис.1). Преобладание паркинсонизма или же мозжечковой атаксии предопределяет возможность (possible) или вероятность заболевания (probable, definite) и выбор подтипа.
Рис. 1 Мультидисциплинарное проявление МСА. Перевод на русский язык. Источник: Fanciulli, Alessandra, and Gregor K. Wenning. “Multiple-system atrophy.” New England Journal of Medicine 372.3 (2015): 249-263
В ходе лечения на первых порах можно отметить реакцию на леводопосодержащие медикаменты, но со временем их эффективность снижается. Для обоих типов МСА характерно драматически быстрое развитие болезни. Потеря автономности пациента сопровождается трудностями пищеварения, дыхания (стридор может вести к необходимости трахеостомии). По статистике, приведённой A. Фанчулли и Г. Веннингом, во время сна у 40% пациентов замечено ночное апноэ. На поздних стадиях заболевания следует избегать условий для развития пневмонии. Кроме того, МСА сопутствует гипертензия в позе лёжа. Во время сна у пациентов отмечается нарушение движений глазных яблок во время быстрого сна [5]. Также замечено уменьшение потоотделения, недержание (в т.ч. ночной полиурией), у мужчин – эректильная дисфункция. При этом следует учитывать, что последние два из перечисленных симптомов могут быть не связаны с МСА. Но в любом случае требуется превентивное и постоянное лечение инфекций мочевыводящих путей.
На более развитых стадиях болезни у 50% пациентов по статистике Фанчулли и Веннинга испытывают парализующую боль. Характерным условием для развития этого симптома была дистония. Симптом чаще наблюдается у женщин.
В обыденной жизни пациенты сталкиваются не только с ограничениями медицинского характера, но и с каждодневными трудностями, которые накладывает болезнь. Внешние проявления болезни выражаются в необычной походке, положении головы. Из-за спазмов на лице больных МСА иногда появляется “сардоническая улыбка”. При МСА-п непроизвольно происходит сильный наклон или вытягивание головы вперёд. Скованность и замедленность движений затрудняют выполнение рутинных задач.
Редкое заболевание известно далеко не всем, и порой вызывает непонимание окружающих. Поэтому в публичных местах из-за физических ограничений пациенты испытывают стресс, ограничивают себя в социализации, избегают людных мест, что создаёт дополнительные факторы для усугубления сопутствующей депрессии и психологического дискомфорта (см. «нейропсихологические проявления», Табл. 1).
Урология
2. Увеличенный объём остаточной мочи, недержание
Жалобы на хронический запор
Преобладает при МСА-п
4. Тремор покоя или движения
Преобладает при МСА-ц
Заметна скованность движений
2. Гиперрефлексия
5. Дневная сонливость (17%)
6. Неприятные ощущения в нижних конечностях (синдром беспокойных ног)
*Клинические проявления МСА среди 437 пациентов, EMSA-registry.
Карло Колозимо предлагает синтетическую таблицу основных и дополнительных критериев диагностики МСА (Таблица 3.5, глава “Multiple system atrophy”, Carlo Colosimo, David E. Riley, Gregor K. Wenning, Handbook of Atypical Parkinsonism, Cambridge University Press, 2011, P. 36.)
Основные критерии:
Дополнительные симптомы
Диагностика заболевания, как уже было сказано, затруднена. Нет единого критерия или сочетания симптомов, которые могли бы однозначно указать на МСА с самого начала болезни. Выход на финальный диагноз проводится методом исключения по мере её развития. При всех общих неизвестных, первостепенным аргументом для подтверждения МСА остаётся снимок МРТ (как минимум 1,5 тесла). Но анализ МРТ на начальных стадиях не даёт точной уверенности, поэтому как правило первоначальным диагнозом становится болезнь Паркинсона (БП). Более достоверное выявление потери нейронов возможно на снимках ПЭТ (PET, позитронно-эмиссионная томография) или ОЭМТ (SPECT,однофотонная эмиссионная компьютерная томография).
Подтипы МСА изображены на фиг. 1 и 2. [1]
Фиг. 1 А : двусторонняя атрофия в области скорлупы, гиперинтенсивность края (отмечено стрелочками). В-С : гиперинтенсивность двустороннего кортикопинального тракта в кортикальной и подкорковой предцентральной извилине и за пределом тракта (С).
Фиг. 2 A : “крест” в области варолиевого моста (“hot cross bun” (англ.) – по внешней схожести с пасхальным хлебом “мазанецем”, “крестовой булочкой”), B-C : гиперинтенсивность в области двустороннего кортикопинального тракта в подкорковой предцентральной извилине и за пределом тракта (С).
При МСА-п (паркинсонического типа, MSA-p)(характерный снимок-см. Фиг. 1) заметны проявления брадикинезии и ригидности; гипокинетической дизартрии; постуральная неустойчивость; часто – тремор покоя.
На 2003 г. случаи паркинсонического подтипа встречались вдвое-вчетверо раз чаще, чем МСА-ц в западном полушарии. Однако МСА-ц чаще встречается в Японии. По собранной на данный момент статистике МСА-п начинает уступать по частоте МСА-ц.
МСА-ц (оливоцеребеллярная атрофия, MSA-c)(характерный снимок – см. Фиг. 2) характеризуется прежде всего мозжечковой атаксией; постепенным, но неуклонным затруднением движения, речи и походки, а также движения глазных яблок и работы верхних век. У пациентов с МСА-ц чаще наблюдается тремор действия, например, при доставании предметов. Мышечная слабость при МСА-ц может привести к невнятной речи и попёрхиванию при глотании. Яркие проявления обнаруживаются среди ортостатических расстройств кровообращения: у пациента могут быть обмороки, слабость с головокружнием, тошнота, дрожь, боль области шеи и плеч. Мозжечковая дисфункция проявляется на более ранних стадиях и сочетается более заметным затруднением дыхания во время сна.
В статье французской исследовательской группы из Тулузы MRI Supervised and Unsupervised Classification of Parkinson’s Disease and Multiple System Atrophy приводится предварительный вывод многостороннего анализа снимков МРТ пациентов обоих подтипов МСА. На развитой стадии МСА (начало болезни наблюдаемых варьировалось между 5 и 7 годами) с высокой степенью вероятности можно отличить МСА от БП, опираясь только на МРТ-данные. Изменения отображаются на снимках в области:
1) лучистого венца верхнего отдела пирамидного пути (обе стороны),
2) верхней извилины лобной доли.
Для МСА-п характерны сокращение фракционной анизотропии в скорлупе, дополнительной моторной области и лучистом венце верхнего отдела пирамидного пути. Исходя из снимков МРТ, труднее отличить от бП МСА церебеллярного типа [7].
С помощью фтордеоксиглюкозы на снимках ПЭТ видны гипометаболизм в стриатуме, в основном в путамене, также стволе головного мозга и мозжечке при МСА-п. При МСА-ц – в основном в путамене, а также может быть заметна потеря допаминергических нейронов нигростриарного пути.
| Тест | Типичный результат |
| Кардиоваскулярные тесты | Ортостатическая гипотензия Низкий коэфициент при пробе Вальсавы Слабое выделение норадреналина в лимфе, слабое сосудосужение |
| Определение уровня глюкозы | Слабый релизинг гормона роста (спорный результат) |
| Тест терморегуляции и количественный тест вызванного судомоторного аксон-рефлекса | Судомоторная дисфункция, проявляющаяся гипо- ангидрозом |
| Электрофизиологические исследования (sympathetic skin response) | Кожный симпатический потенциал либо отсутвует, либо аномальный |
| Тест цереброспинальной жидкости | Повышенный уровень нейрофиламентов |
| Электромиография наружного сфинктера заднего прохода | Либо денервация, либо раздражение (нерелевантные результаты) |
| Транскраниальная сонография | Гиперэхогенность чечевицеобразного ядра и нормальная эхогенность чёрной субстанции |
| Компьютерная томография | Не дала результатов |
| МРТ на 1,5 тесла | Аномалии в базальных ганглиях, «крест» в области варолиевого моста, атрофия мозжечка или ствола мозга |
| ДВИ (диффузно-взвешенное изображение) | Диффузность в области путамена, варолиева моста и средней ножки мозжечка |
| Волюметрия | Потеря объёма в путамене при МСА-п, потеря объёма в стволе и мозжечке при МСА-ц |
| Cканирование с радиоактивным изотопом-метайодобензилгуанидином MIBG | В норме |
| Сканирование переносчиков Иофлупаном I123 (123I-FP-CIT SPECT imaging) | Недостаток транспортёров дофамина в полосатом теле |
| Сканирование переносчиков йодобензамидом I123 123I-IBZM-SPECT | Недостаток транспортёров дофаминового рецептора D2 в полосатом теле |
| ПЭТ с флуородопой | Недостаток захвата флуорисцентной леводопы |
| ПЭТ с раклопридом | Недостаток транспортёров дофаминового рецептора D2 в полосатом теле |
| ПЭТ с изохинолиновым карбоксамидом PK-11195 | Микроглиальная активация в области базальных ганглий и ствола мозга |
| ПЭТ с использованием радиофармпрепарата фтордеоксиглюкозы | Замедленный метаболизм |
Благодаря дополнительным тестам на данный момент выявлены несколько направлений, в которых будет развиваться диагностика. Они базируются не только на исключении других болезней или изучении снимков ПЭТ (см. Табл. 3, Типичные результаты дополнительных тестов.), но и на анализе офтальмологических особенностей МСА, терморегуляции, дисфункции вегетативной системы. Остановимся на результатах некоторых из них.
Офтальмологические особенности МСА
Целевое ретроспективное наблюдение больных МСА в клинике Мэйо (Рочестер, Миннесота, США) позволило выявить основные аномалии зрения, сопутствующие заболеванию. Из 285 рассмотренных случаев были отобраны 39 пациентов с подтверждённым диагнозом. Среди пациентов с МСА-п 14 человек жаловались преимущественно на синдром сухого глаза, у 13-ти были выявлены асинхронность глазных движений. У 7-х было отмечено смещение или ограничение движения глазного яблока, у одного пациента наблюдалась монокулярная диплопия (двоение изображения для одного глаза) из-за аномального роста ресниц. Единичными случаями стали двусторонняя атрофия зрительного нерва и синдром Холмса – Эйди (парасимпатическая денервация зрачка, проявляющаяся мидриазом со снижением, а иногда и полным исчезновением способности зрачка сужаться, реагируя на свет ).
Следует различать аномалии, которые по независимым причинам сопровождают МСА, и те, которые проистекают из заболевания. К последним относятся, по предположению учёных, атрофия глазного нерва и рубцевание конъюнктивы (рубцовый пемфогоид).
Среди наблюдаемых с МСА-ц офтальмологические особенности чаще всего проявляются в асинхронности движения и смещении глазного яблока. Особо выделена корреляция длительности жизни пациентов после установления диагноза и зрительными аномалиями, за исключением синдрома “сухого глаза”. В связи с этими наблюдениям медики призывают пациентов с МСА регулярно проходить офтальмологическое обследование с целью раннего выявления аномалий и предупреждения несчастных случаев по причине плохого зрения [2].
Особенности ортостатического давления и пульса при МСА
Среди критериев, указывающих на вероятное развитие болезни, отмечено падение ортостатического давления. Ортостатическая проба заключается в замере давления стоя. За три минуты в стоячем положении систолическое давление падает как минимум на 20-30 мм.рт.ст., а диастолическое – на 10-15 мм.рт.ст. при заниженном сердцебиении. Поэтому пациентам с МСА желательно носить абдоминальный бандаж, компрессионное бельё, увеличить частоту потребления воды и соли, а также медикаментов для повышения артериального давления.
Признаки тахикардии с гипотонией являются характерной особенностью пациентов с вегетативными нарушениями. Но диапазон нарушений пока ещё не изучен. В статье Orthostatic Heart Rate Changes in Patients with Autonomic Failure caused by Neurodegenerative Synucleinopathies сообщается о диапазоне ортостатических изменений сердечного ритма у пациентов с вегетативной недостаточностью, в том числе и при МСА.
При МСА речь идёт о вегетативной нервной системе. Ортостатическая гипотензия вызвана нарушением активации симпатических вазоконстрикторных нейронов. Сердечный пульс значительно выше у пациентов с МСА в отличие от других пациентов с заболеваниями, связанными с образованием телец Леви, и в частности БП. Заметное повышение сердечного ритма при МСА объясняется тем, что постганглионарные волокна и их аксоны остаются почти незатронутыми, однако при этом констатируется потеря вегетативных нейронов головного и спинного мозга [3]. Это, например, проявляется в том, что у пациентов с МСА очень низкая температура конечностей: холодные ладони и ступни [4].
Потоотделение при МСА
У пациентов с МСА, по сравнению с БП, значительно ниже показатели потоотделения ладоней и особенно ступней. Гипогидроз (пониженная потливость) или вовсе отсутствие потоотделения при МСА считается связанными с дегенерацией центральных предганлиев [6].
Изучение МСА затруднено редкостью заболевания, затруднённой диагностикой на начальной стадии и тем, что до сих пор не найдены способы эффективного торможения болезни. Интерес к разносторонним проявлениям болезни может в будущем привести к раннему выявлению заболевания, улучшенному лечению и повышению качества жизни пациентов.
Термины:
Проба Вальсальвы (напряжение по Вальсальве) — это форсированное выдыхание при закрытом носе и рте.
Гипокинетическая дизартрия — вид экстрапирамидной дизартрии, возникающий при поражении подкорковых узлов и их нервных связей.
Стриатонигральная дегенерация — спорадическое прогрессирующее нейродегенеративное расстройство, которое представляет собой одно из проявлений МСА. Проявляется, как правило, в снижении численности нейронов и глиозом в скорлупе, черной субстанции, стволе и мозжечке, а также в дегенерации клеток боковых рогов спинного мозга.
Оливопонтоцеребеллярные дегенерации — наследственные дегенеративные заболевания ЦНС, объединенные сходной локализацией патологического процесса в мозжечке, нижних оливах и мосте головного мозга.
Глазной рубцовый пемфигоид — заболевание, при котором происходит рубцевание конъюнктивы у пациентов пожилого возраста.
Монокулярная диплопия — ви́дение одним глазом двух или более изображений предмета.
Подготовила: Мартемьянова Е.О.
Помощь в редакции: Оськин С.
Carlo Colosimo, David E. Riley, Gregor K. WenningHandbook of Atypical Parkinsonism, Cambridge University Press (2011).
Fanciulli, Alessandra, and Gregor K. Wenning. “Multiple-system atrophy.” New England Journal of Medicine 372.3 (2015): 249-263.
Медицинские интернет-конференции
Языки
Мультисистемная атрофия или прогрессирующий надъядерный паралич?
Полянская О.В., Куташов В.А.
Резюме
Представлено описание клинического случая, в котором на ранней стадии заболевания встречались симптомы, характерные как для прогрессирующего надъядерного паралича, так и для мультисистемной атрофии. Представлено динамическое наблюдение за пациенткой в течение 4,5 лет.
Ключевые слова
Статья
Введение. Мультисистемная атрофия (МСА) и прогрессирующий надъядерный паралич (ПНП) – нейродегенеративные заболевания, которые раньше относились к группе болезней «паркинсонизм-плюс». В основе клинической картины – синдром Паркинсона с низкой эффективностью специфической терапии, когнитивные нарушения и дополнительные симптомы, на основании которых в дальнейшем и были определены отдельные нозологии [1]. И при МСА, и при ПНП поражаются подкорковые и стволовые структуры.
Оба заболевания, мультисистемная атрофия и прогрессирующий надъядерный паралич, встречаются в неврологической практике в основном как спорадические; мультисистемная атрофия имеет несколько типов развития и течения болезни, которые могут быть представлены как «чистыми», так и «смешанными» вариантами [2], для прогрессирующего надъядерного паралича также характерны различные клинические варианты дебюта, развития заболевания, описаны как традиционные, так и необычные и нетипичные сочетания симптомов [3,4], что приводит к существенным трудностям в диагностике каждого из этих заболеваний. На ранних стадиях, когда симптомы выражены еще неярко, а клинические синдромы находятся в процессе формирования, данные заболевания имеют значительное количество общих черт в виде синдрома паркинсонизма, вегетативной недостаточности, глазодвигательных нарушений, псевдобульбарного синдрома, когнитивных нарушений, эмоционально-личностных расстройств и нарушений сна, что вызывает существенные трудности в проведении дифференциальной диагностики.
В настоящее время проблема дифференциальной диагностики данных болезней представляет интерес как из-за различного прогноза в плане развития деменции и сохранения самостоятельности пациента [4], так и из-за выявления семейных случаев и при мультисистемной атрофии, и при прогрессирующем надъядерном параличе, в связи с чем предполагается, что генетические факторы могут влиять на патогенез и развитие этих заболеваний. По данным молекулярно-генетических исследований, один из вариантов мультисистемной атрофии связан с мутацией в гене COQ2, расположенном в области 4q21.22-q21.23 [5], семейный вариант прогрессирующего надъядерного паралича – с мутацией в гене МАРТ, расположенном в области 17q21.31 [6].
Описание клинического случая. В качестве иллюстрации сложности проведения дифференциального диагноза между мультисистемной атрофией и прогрессирующим надъядерным параличом приводим описание клинического случая динамического наблюдения за пациенткой М., 60 лет, несколько раз проходившей лечение в различных отделениях Воронежской городской клинической больницы скорой медицинской помощи № 1.
Впервые в поле зрения врача-невролога пациентка М. попала, когда находилась на лечении в гинекологическом отделении ВГКБМСП № 1 по поводу вульвовагинита и вульводинии. К неврологу была направлена на консультацию.
Жалобы и история развития заболевания.
Пациентка считает, что здоровье ее нарушилось около 3-х лет назад, когда больная самостоятельно выдавила и прижгла бриллиантовой зеленью фурункул во влагалище. Вскоре после этого появились дизурические жалобы: неприятные ощущения при мочеиспускании, ощущение, что в мочеиспускательном канале есть какое-то образование, инородное тело или воспалительный инфильтрат. Больная отметила также более частые позывы на мочеиспускание, акт мочеиспускания периодически бывал болезненным. Сначала лечилась самостоятельно «от цистита», принимала различные антибиотики, затем обращалась к урологам, был диагностирован острый, затем хронический цистит, который часто обострялся, что подтверждалось анализами мочи, ультразвуковым исследованием мочевого пузыря. Пациентка в течение последних двух лет по поводу гиперактивного мочевого пузыря по рекомендации урологов принимает препарат спазмекс. Начинала прием с минимальных доз, препарат давал положительный эффект, но периодически все равно приходилось увеличивать дозу лекарственного средства. В настоящее время пациентка отмечает существенное снижение эффективности препарата, особенно в течение последних нескольких месяцев, недель. Для поездок, работы пользуется прокладками, при прогулках по городу строит маршруты так, чтобы можно было зайти в какое-либо учреждение в туалет. Пациентка отмечает, что все позывы на мочеиспускание сильные, прохождение мочи по мочеиспускательному каналу чувствует хорошо. Количество принимаемой жидкости оценивает как небольшое или среднее, около 1,5-2 литров. Жажду отрицает.
Работает юристом, разведена, проживает с сыном, страдающим психическим заболеванием. У пациентки также есть дочь, живущая отдельно со своей семьей. Несколько лет назад был вывих ключицы в автоаварии, восстановилась быстро и хорошо, вернулась к работе. Онкологические, венерические заболевания, туберкулез, болезнь Боткина, отрицает. В течение ряда лет отмечались аллергические реакции на пыльцу растений. На продукты питания, медикаменты аллергию отрицает. Наблюдалась у ЛОР-врача с диагнозом аллергический ринит.
Неврологический статус. Больная в ясном сознании, контактна, адекватна, правильно ориентирована. Обращает на себя внимание телосложение и походка: пациентка астенического телосложения, высокая, плечи развернуты назад, голова также несколько запрокинута назад, спина прямая, практически не сгибается и не двигается при ходьбе. При этом несколько избыточны движения в области тазового пояса, походка «разболтанная», шаг широкий, ноги ставит далеко друг от друга. Ретроколлис.
Речь правильная, с богатым словарным запасом, эмоционально окрашенная, с яркими интонациями. Темп речи умеренный, ближе к медленному, речь несколько неплавная, тягучая. Голос хорошо модулирует, однако по тембру «надтреснутый, шероховатый», имеет носовой оттенок. При проверке когнитивных функций с помощью краткого исследования когнитивного состояния, теста рисования часов, монреальской шкалы оценки когнитивных функций и батареи лобных тестов получены нормальные результаты.
Зрачки равные, округлой формы, обычного диаметра, живо реагируют на свет. Глазные щели D=S, движения глазных яблок по горизонтали в полном объеме, по вертикали – с особенностями: затруднены следящие движения вверх и вниз, трудности с фиксацией взора в этих положениях, при длительном нахождении неврологического молоточка в этих позициях больная очень быстро отводит взор. Болезненность, тошноту, головокружение, двоение в этих положениях глаз отрицает. Затруднены также движения глаз в верхние и нижние косые положения. Возможно, имеет место формирование пареза взора вверх и вниз. Корнеальные рефлексы живые, симметричные. Чувствительность на лице не изменена, нижнечелюстной рефлекс оживлен, симметричный. Лицо симметричное. Глотание сохранено. Язык по средней линии, без атрофий и фасцикуляций, розовый, влажный. Определяются умеренно выраженные симптомы орального автоматизма: хоботковый, назолабиальный. Объем активных движений в конечностях полный, парезов нет. Мышечный тонус повышен по экстрапирамидному типу во всех группах мышц, в том числе в аксиальной мускулатуре. Выявляется феномен восковой гибкости, феномен Нойка-Ганева ярко представлен с 2-х сторон. Глубокие рефлексы с рук умеренные, без разницы сторон, с ног – ближе к низким, также симметричные. Чувствительность в области конечностей, живота не изменена. От проверки чувствительности в аногенитальной зоне больная отказалась. В позе Ромберга больная легко пошатывается вправо. Пальце-носовую пробу выполняет с легкой интенцией справа. Пяточно-коленную пробу выполняет с атаксией справа. Выявляются нерезко выраженные адиадохокинез, гиперметрия, дисметрия слева. Менингеальных знаков нет.
Таким образом, по результатам расспроса пациентки и первичного осмотра были выявлены следующие нарушения: гипокинетико-ригидный синдром с преобладанием тонуса мышц в аксиальной мускулатуре и формированием разгибательной позиции тела, псевдобульбарный синдром, глазодвигательные нарушения, нарушения походки, постуральная неустойчивость и падения, мозжечковые расстройства, нарушения сна, вегетативные расстройства в виде нарушений мочеиспускания и артериальной гипертензии. Большинство этих симптомов могут встречаться при обоих обсуждаемых заболеваниях (синдром паркинсонизма, псевдобульбарный синдром, нарушения сна). Тем не менее, некоторые из них более характерны для МСА (мозжечковые симптомы, вегетативные расстройства), тогда как другие – для ПНП (разгибательная поза при ходьбе, постуральная неустойчивость, парезы взора по вертикали, особенно вниз).
Пациентке было рекомендовано дообследование:
Через 3 месяца пациентка была осмотрена повторно (в период госпитализации в урологическое отделение по поводу обострения хронического цистита). На ЭЭГ – вариант возрастной нормы, на МРТ головного мозга – легкое расширение боковых желудочков, на глазном дне – ангиопатия сетчаток, отклонений со стороны биохимических показателей, в содержании гормонов и электролитов выявлено не было, эндокринолог не выявил заболеваний эндокринной системы. Согласно дневнику мочеиспусканий, их количество колебалось в различные дни от 8 до 27 за сутки, ночных – от 1 до 7. За эти 3 месяца у пациентки появились жалобы на ухудшение памяти на текущие бытовые события, профессиональная память не страдает. Беспокоит изменение почерка: стал более небрежным, неаккуратным. За последние 3 месяца похудела на 2 кг. В плане нарушений мочеиспускания отмечает, что бывают «хорошие дни», когда учащенное мочеиспускание беспокоит мало, и «ужасные», когда больная постоянно бегает в туалет. Пациентка обратила внимание на следующее: приняв анальгетик для снятия головной боли, заметила снижение количества походов в туалет в этот вечер, в дальнейшем несколько раз «экспериментировала», принимая анальгетик в те дни, когда мочеиспускание было особенно частым, прием лекарства приводил к некоторому урежению мочеиспускания.
В неврологическом статусе определяются следующие изменения: повторное исследование когнитивных функций выявило наличие умеренных когнитивных нарушений: по краткому исследованию когнитивного состояния (MMSE) – 26 баллов, по Монреальской шкале (MoCA) – 24 балла. В наибольшей степени нарушилось отсроченное воспроизведение запоминаемых слов и счет. Другие тесты выполнялись хорошо. Отмечается парез взора вверх, затруднение движений глазных яблок вниз, нарушение плавности горизонтальных движений глаз. В остальном в неврологическом статусе динамики нет.
Принимая во внимание, что учащенное мочеиспускание в данный период может быть связано с обострением хронического цистита, а также тот факт, что сформировался парез взора вверх, ухудшились движения глазных яблок вниз, появились умеренные когнитивные расстройства в виде нарушений памяти и счета, более правомочным представлялся диагноз прогрессирующего надъядерного паралича, при котором отмечается синдром паркинсонизма с преобладанием тонуса в аксиальной мускулатуре и формированием разгибательной позиции, отсутствует на ранней стадии изменение длины шага, скорости ходьбы, типичны глазодвигательные нарушения, особенно вертикальные парезы взора или офтальмоплегия, а когнитивные нарушения, достаточно быстро достигающие степени деменции. Соответственно данному диагнозу, ожидалось прогрессирование симптомов паркинсонизма, усиление постуральной неустойчивости, глазодвигательных нарушений, дальнейшее ухудшение когнитивных функций с последующим развитием деменции.
Через 10 месяцев состоялся следующий осмотр больной, когда пациентка попала в неврологическое отделение больницы с острой нейропатией лицевого нерва справа на фоне переохлаждения. Пациентка отмечает, что эпизоды неустойчивости случаются с той же частотой, однако падений стало меньше, объясняет это тем, что теперь «внимательно смотрит под ноги». Основной жалобой остается учащенное мочеиспускание с императивными позывами. В неврологическом статусе помимо выраженной асимметрии половины лица, усилились нарушения почерка, появились черты мегалографии, в остальном динамики нет: сохраняется повышение мышечного тонуса во всех группах мышц по экстрапирамидному типу, в том числе в аксимальной мускулатуре, ретроколлис, однако выраженность его та же, ограничены движения глазных яблок вверх, объем движений вниз и по горизонтали достаточный, но движения неплавные. Сохраняются имевшиеся мозжечковые расстройства, когнитивные нарушения не прогрессируют: MMSE 27 баллов, MoCA – 24 балла, другие тесты – норма. Принимая во внимание тот факт, что типичного для ПНП быстрого неуклонного прогрессирования заболевания не отмечается, когнитивные функции остаются сохранными, пареза взора вниз, тем более полной офтальмоплегии – нет, отмечается нарастание мозжечковых расстройств, стойкость вегетативных нарушений в виде резко учащенного мочеиспускания с императивными позывами уже вне обострения хронического цистита, диагноз ПНП, согласно критериям NINDS-SPSP [7], требует пересмотра.
В данной ситуации более вероятным представляется диагноз мультисистемной атрофии, при которой также могут иметь место глазодвигательные нарушения, но они, как правило, не достигают степени пареза взора или офтальмоплегии, часто встречаются когнитивные нарушения, которые, однако, не достигают степени деменции. Что же касается разгибательной позиции туловища, то она является частым, но не облигатным симптомом ПНП.
Заключение. Таким образом, на основании анализа представленного случая можно заключить, что клинический метод является ведущим в диагностике заболеваний, при которых отсутствуют патогномоничные симптомы, четко очерченные изменения при нейровизуализации, биохимические, инструментальные маркеры. Динамическое наблюдение за пациентами, у которых отмечаются симптомы, соответствующие нескольким заболеваниям со сходной клинической картиной, является крайне важным для уточнения диагноза. Как видно из описания данного случая, на более ранних этапах развития заболевания клиническая картина может больше соответствовать одному диагнозу, а на последующих – другому. В описанном наблюдении представляет интерес тот факт, что у пациентки сочеталось несколько симптомов, характерных для разных заболеваний, например, разгибательная позиция туловища и раннее развитие постуральной неустойчивости, более характерные для ПНП, и вегетативные нарушения и мозжечковые симптомы, более характерные для МСА. Возможно, это связано с некоторыми элементами патогенеза, общими для двух заболеваний [8].