Дидрогестерон и прогестерон в чем разница
Дидрогестерон или прогестерон микронизированный
Прогестерон, также называемый “гормоном беременности”, является распространенным женским гормоном, который естественным образом содержится в организме женщины. Он играет существенную роль как до, так и во время беременности. Когда предлагается исследование фертильности, есть два основных половых гормона, которые наблюдающий врач будет проверять: эстроген и прогестерон. Дидрогестерон или прогестерон микронизированный : что лучше?
Прогестерон (как предписанная гормональная добавка) часто необходим во время процедур вспомогательных репродуктивных технологий (ВРТ), таких как экстракорпоральное оплодотворение (ЭКО). Отчасти потому, что лекарства, которые вы можете использовать во время этих процедур, могут подавить способность вашего организма вырабатывать прогестерон. Некоторые процедуры могут даже непреднамеренно удалить клетки, продуцирующие прогестерон, из ваших яичников. Суть в том — что все женщины, которые хотят забеременеть, нуждаются в прогестероне, чтобы помочь своей матке подготовиться к беременности и поддерживать ее.
Иногда существуют и другие причины для использования препаратов прогестерона, такие как недостаточная или вообще отсутствующая выработка прогестерона из яичников или плохо развитые фолликулы.
Самопроизвольный выкидыш встречается примерно в 15-20% случаев беременности. Угроза выкидыша возникает, когда мать может потерять своего ребенка на сроке менее 20 недель беременности. Симптомами угрожающего выкидыша являются вагинальные кровотечения, с болями в животе или без них, в то время как шейка матки закрыта и ребенок внутри матки жив.
Прежде чем забеременеть.

Дидрогестерон или прогестерон микронизированный : что лучше? Во время беременности.
Баланс прогестерона во время беременности очень важен. Постоянное поступление прогестерона в эндометрий помогает поддерживать развивающийся плод на протяжении всей беременности. После успешной имплантации прогестерон также помогает поддерживать благоприятную среду для развивающегося плода. После 8-10 недель беременности плацента берет на себя выработку прогестерона из яичников и значительно увеличивает выработку прогестерона.
Различные формы прогестерона.
Не все формы прогестерона созданы равными. Существует несколько типов прогестерона, включая вагинальные продукты, которые доставляют прогестерон непосредственно в матку. Различные формы включают в себя следующее:
Что такое Дюфастон?
Таблетки дюфастона действуют как искусственная замена женскому гормону прогестерону, если его уровень низок. Дюфастон используется для лечения заболеваний, вызванных недостатком этого гормона, таких как нарушения менструального цикла (нерегулярные или пропущенные периоды), боли в животе во время беременности, трудности с зачатием и частые выкидыши. Другие признаки низкого уровня прогестерона включают снижение либидо, проблемы с желчным пузырем и увеличение веса.
Дюфастон или Утрожестан?
Таблетки дюфастона помогают регулировать гормональный баланс в женском организме, действуя как заменитель гормона, повышая уровень прогестерона. Он копирует то, что гормоны прогестерона делают для вашего организма в отношении регулирования овуляции и менструации. Он помогает стимулировать слизистую оболочку матки, чтобы она утолщалась и принимала оплодотворенную яйцеклетку, а также предотвращает мышечные сокращения в матке, чтобы яйцеклетка не была отвергнута.
Дюфастон или Утрожестан: что лучше? Давайте разберемся. Главное отличие Урожестана от Дюфастона заключается в том, что Дюфастон является искусственно синтезированным гормоном – дидрогестероном, являющийся аналогом прогестерона. А Утрожестан — содержит натуральный гормон прогестерон, который изготовлен из растительного сырья. Формакологические свойства и побочные эффекты практически одинаковы у обоих препаратов.
Какая добавка подходит именно вам?

Сравнительная характеристика прогестерона и синтетических прогестинов в аспекте клинического использования при терапии прогестерондефицитных состояний
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
МГМСУ им. Н.А. Семашко
Н аверное, ни у кого не вызывает сомнения, что клиническая практика врача–гинеколога совершенно невозможна без использования прогестинов. Спектр использования этих препаратов несравнимо велик – это проведение прогестероновой пробы, гормональный гемостаз, лечение недостаточности лютеиновой фазы менструального цикла, лечение и профилактика гиперпластических процессов эндометрия, а также устранение угрозы прерывания беременности. В настоящий момент на отечественном фармакологическом рынке существует множество препаратов данной группы, созданных в разное время, а потому имеющих свои недостатки и преимущества. Руководства по лечению гинекологических заболеваний, представляя схемы терапии тех или иных патологий, просто перечисляют ряд прогестинов, не делая акцента на особенностях каждого из препаратов. Вследствие этого у многих врачей складывается неправильное представление о полной идентичности и взаимозаменяемости различных прогестинов, что сказывается на эффективности и переносимости проводимого лечения. Кроме этого, одним из немаловажных аспектов проблемы является отсутствие у многих гинекологов данных об экстрагенитальных эффектах прогестинов.
Уже с середины 70–х годов было известно, что изолированное повышение концентрации эстрогенов в крови или экзогенное введение только эстрогенов в значительной степени повышает риск развития рака эндометрия. В связи с этим с начала 80–х годов основной целью клинического использования прогестерона стала защита эндометрия. В частности, был хорошо известен тот факт, что рецепторы эстрогенов, расположенные в ядрах клеток, контролируют клеточный цикл эпителия желез эндометрия, то есть эстрогены индуцируют начало клеточного цикла, а прогестерон блокирует этот процесс, при этом экзогенно введенные синтетические прогестины также обладают этой способностью, но только в другой дозе.
В процессе подбора оптимальной дозы прогестагенов основное значение придавалось их способности вызывать у женщины в постменопаузе такую же гамму морфологических и биохимических изменений в эндометрии, как во время лютеиновой фазы менструального цикла женщины пременопаузального возраста.
Начало кровотечения после 11 дней введения прогестагенов являлось доказательством эффективной защиты эндометрия и наилучшим свидетельством клинической эффективности.
Однако в процессе накопления опыта фармакологические критерии эффективности и надежности различных прогестагенов претерпели существенные изменения. В контролируемых исследованиях на животных и человеке было показано, что концентрация натурального прогестерона, находящаяся в физиологических рамках лютеиновой фазы менструального цикла, не приводит к развитию каких–либо побочных эффектов. В то же время множество рандомизированных контролируемых исследований, проведенных на животных и человеке, показали, что некоторые из наиболее часто использующихся в клинической практике синтетических прогестинов в обычных дозах вызывают значительные изменения в концентрациях липидов, метаболизме глюкозы, а также оказывают воздействие на стенку артериальных сосудов.
Для предсказания возможности развития побочных эффектов исследователи сконцентрировали свое внимание на анализе химической структуры стероидных молекул и их способности связываться с различными рецепторами, используя классические опыты на животных. Однако ценность полученной информации была относительно низкой, поскольку результаты было затруднительно экстраполировать на человеческую модель.
По своей сути прогестины являются препаратами, повышающими биодоступность прогестерона при пероральном приеме, сохраняя при этом его эффекты на эндометрий. Метаболизм прогестерона ферментами ЖКТ и печени начинается с редукции 5 a (в ЖКТ) и 5 b (в печени) кольца А, а на втором этапе – гидроксилирование С–20 и/или С–17. Любое изменение кольца В снижает аффиннитет 5 a или 5 b –редуктаз и поэтому используется для повышения биодоступности пероральных прогестагенов и улучшения их связывания с рецепторами прогестерона.
Эти изменения включают подавление С–19 (19 нор–тестостерон и прегнина дериватов), добавление 4,6–диеновой структуры (дидрогестерон, ципротерон ацетат) или метильного радикала к С–6 (медроксипрогестерон). Все эти препараты способны вызывать прогестагенные эффекты на организм в дозе, в 10 раз меньшей по сравнению с пероральным прогестероном.
Основным побочным эффектом различных синтетических прогестинов является остаточная андрогенная активность (дериваты 19–нор–тестостерона). Несмотря на уменьшение дневной дозы (по сравнению с прогестероном) некоторые прогестины, отличные по структуре от 19–нортестостерона, могут влиять на метаболизм глюкозы и холестерина, а также индуцировать дисфункцию эпителия. Имевшие место ранее предположения о том, что факторами, обеспечивающими надежность и эффективность прогестинов, могут быть более выраженный эффект при меньшей дозе и низкая андрогенная активность, в настоящий момент не могут быть использованы в качестве критерия для выбора оптимального прогестагена.
Прогестагены классифицируются на основании их способности связываться с рецепторами прогестерона в эндометрии, а также с рецепторами эстрогенов, кортизола, тестостерона и альдостерона. Однако эта классификация непригодна для предсказания основных побочных эффектов. К примеру, in vitro медроксипрогестеронацетат и прогестерон обладают приблизительно одинаковыми связывающими способностями, в то время как in vivo эти препараты имеют различные влияния на сердечно–сосудистую систему. Открытие рецепторов прогестерона в других тканях – эндотелии сосудов, гладкой мускулатуре артериальной стенки, рецепторов GABA (ГАМК) в головном мозге позволило пролить свет на эту ситуацию. Например, независимые исследования показали, что в сосудистой стенке и миокарде антагонистическое влияние на рецепторы альдостерона предпочтительнее, нежели подавление регуляции рецептора эстрадиола прогестинами.
В целом основные эффекты прогестерона на кожу, мозг и миометрий обусловлены его двумя метаболитами.
Частичный антиандрогенный эффект осуществляется посредством конкурентного ингибирования процесса метаболического превращения андрогенов в более активные формы (имеется в виду конкуренция за фермент 5- a редуктазу), а также за счет конкурентного ингибирования связывания наиболее активного андрогена – дигидротестостерона с его рецептором, что обусловлено действием 5- a прегнандиона (5- a редуцированного метаболита прогестерона). Надо отметить, что эти механизмы не способны оказывать влияние на прямые эффекты тестостерона, однако ингибирование 5- a редуктазы имеет большее значение, поскольку именно этот фермент играет ключевую роль в половой дифференцировке плода с 12 по 28 неделю гестации. Кроме этого, указанный выше фермент регулирует также синтез дигидротестостерона в мозговой ткани, который, в свою очередь, определяет такие эмоциональные явления, как злость и агрессивность.
Релаксирующий эффект (вероятнее всего имеет значение при высоких концентрациях эстрадиола в плазме крови) обусловлен активностью 5- a прегнанолона, который связывется с рецепторами ГАМК в головном мозге. Этот метаболит прогестерона обладает антидисфорической активностью, участвует в регулировании процессов сна и бодрствования и, возможно, оказывает нейропротективный эффект после повреждения мозговой ткани.
Токолитический эффект осуществляется 5- b метаболитом прогестерона (5- b прегнандион и прегнанолон).
В почках, и в особенности в миометрии и артериальной стенке, прогестерон проявляет антиальдостероновый эффект, основанный также на конкурентном механизме.
Немалое значение имеет способность прогестерона противодействовать эффектам эстрогенов на эндотелий сосудов, при этом синтетические прогестины (за счет своего более выраженного прогестагенного эффекта) способны в значительной степени усиливать проявление этого свойства прогестерона. В частности, известно, что прогестерон угнетает пролиферацию эндотелиальных клеток, таким образом, избыточный прогестагенный эффект, обусловленный действием синтетических прогестинов, приводит к нарушениям функций эндотелия (вазодилатация, отложение холестерина, адгезия различных молекул и т.д.) с последующим изменением морфологии сосудистой стенки.
В то же время прогестерон в своей физиологической концентрации оказывает благоприятный эффект на активность различных цитокинов, пролиферацию гладкомышечных клеток артерий и накопление липидов в макрофагах.
В настоящий момент не существует ни одного синтетического прогестагена, включая и дидрогестерон, который при введении в рекомендуемой дозе мог бы проявлять антиальдостероновый эффект (исключение составляет только дроспиренон). Кроме этого, ни один синтетический прогестин не способен генерировать в организме 5- a и 5- b редуцированные метаболиты, необходимые для реализации перечисленных выше физиологических эффектов прогестерона (частичный антиандрогенный, токолитический и анксиолитический).
При создании различных синтетических прогестинов особый акцент делался на более высокий, чем у прогестерона, аффинитет молекулы к рецептору прогестерона, что помимо положительных моментов несет в себе и отрицательный, обусловленный повышением риска развития сердечно–сосудистых заболеваний по механизму, описанному выше.
Указанные выше факты во многом подчеркивают очевидную целесообразность более широкого использования в клинической практике натурального прогестерона, который представлен на отечественном рынке препаратом Утрожестан.
Утрожестан представляет натуральный микронизированный прогестерон, выпускающийся в виде капсул для перорального и интравагинального применения.
При интравагинальном введении Утрожестана абсорбция микронизированного прогестерона происходит быстро, и высокий уровень прогестерона в плазме наблюдается уже через 1 час после введения капсулы. При введении более 200 мг Утрожестана концентрация прогестерона в плазме крови соответствует I триместру беременности и поддерживается около 24 часов.
Целый ряд гинекологических заболеваний требует восполнения недостаточности эндогенного прогестерона. Широко применяющиеся с этой целью препараты несут в себе достаточное количество неудобств для пациентки, проявляющихся наличием выраженных побочных эффектов, неудобством приема или высокой стоимостью, что во многом обусловлено недостаточным сродством входящих в них активных компонентов с натуральным прогестероном.
Утрожестан в отличие от синтетических аналогов имеет выгодные преимущества, заключающиеся в первую очередь в том, что входящий в его состав микронизированный прогестерон полностью идентичен натуральному, что обусловливает практически полное отсутствие побочных эффектов.
Физиологическое действие Утрожестана обусловлено сохранением в его молекуле первых двух колец и наличием между этими кольцами двойной связи между 4 и 5 атомами углерода. У всех остальных прогестинов имеют место изменения в расположении колец и двойных связей в молекуле, что отражается на их способности связываться с рецепторами. Уникальное строение молекулы Утрожестана позволяет ему воздействовать на метаболизм андрогенов по описанному выше механизму, что оказывает положительное воздействие на течение беременности и проявляется получением хорошего косметического эффекта. Воздействие на рецепторы андрогенов имеет большое значение в первые 3 месяца беременности.
В связи с этим назначение с целью поддержания беременности прогестинов, обладающих андрогенной активностью, опасно вследствие возможного отрицательного влияния на плод.
Применение Утрожестана в этом случае является наиболее приемлемым и целесообразным.
Может возникнуть логичный вопрос – существует ли угроза снижения уровня андрогенов на фоне приема Утрожестана за счет его антиандрогенного действия на плод мужского пола? Такой возможности нет, потому что существует конкурирующее взаимодействие между прогестероном и тестостероном.
Обычная доза Утрожестана составляет 200–300 мг в сутки, при этом может быть использован любой из двух путей введения препарата – интравагинальный или внутрь. При купировании угрозы прерывания беременности болеее предпочтительным и эффективным является сочетание интравагинального введения Утрожестана с приемом внутрь. Важно отметить, что первоначально доза Утрожестана при угрозе прерывания беременности составляет 400–600 мг одномоментно с последующей поддерживающей дозой – 400–600 мг в сутки. В случае неэффективности данной терапии доза Утрожестана может быть увеличена до 800–1000 мг в сутки.
Утрожестан имеет полное сходство с молекулой прогестерона, и именно это свойство обеспечивает целый ряд уникальных эффектов, выгодно отличающих его от других препаратов этой группы.
В целом Утрожестан аутентичен процессам инициации и поддержания беременности, полноценно соответствуя принципу «максимум пользы при минимуме вреда».
Менопаузальная гормонотерапия (МГТ)

Почему же процент женщин, принимающих МГТ, остается невысоким?
Крупное американское исследование WHI (Women’s Health Initiative, 2002 г.) вызвало драматический период в судьбе менопаузальной гормонзаместительной терапии, что способствовало резкому сокращению МГТ в большинстве стран мира, появлению страхов и сомнений в отношении пользы и рисков.
Преждевременное завершение части исследования по менопаузальной гормонзаместительной терапии (МГТ) привлекло к себе всеобщее внимание. Как женщины, так и врачи чувствовали себя обманутыми, так как терапия, которая до этого считалась полезной для здоровья в долгосрочной перспективе, теперь оказалась опасной. Отличающийся от фактического изложения пресс-релиз предварительной работы прогремел в СМИ за неделю до того, как сама статья стала доступна для большинства читателей. Сообщалось, что исследование было остановлено в связи с повышенным риском развития рака молочной железы, связанным с заместительной гормональной терапией. На самом деле, в скорректированном анализе связь МГТ и рака молочной железы не была статистически значима!
Последующий углубленный анализ результатов WHI показал, что МГТ характеризуется благоприятным профилем пользы/риска у более молодых женщин, которые начинают терапию в близкие к менопаузе сроки. Эти результаты характеризовались сходным защитным воздействием терапии в отношении ИБС и снижения общей смертности, которые были продемонстрированы ранее в крупномасштабных наблюдательных исследованиях с участием относительно молодых женщин. После WHI широкое распространение получила так называемая временная гипотеза или гипотеза «окна терапевтических возможностей», согласно которой существует различное влияние МГТ на атеросклероз и связанные с ним клинические события в зависимости от возраста женщины и времени начала использования МГТ по отношению к моменту наступления менопаузы.
Основными недостатки данного исследования являлись:
Что же происходит с женским организмом в 45-55 лет?
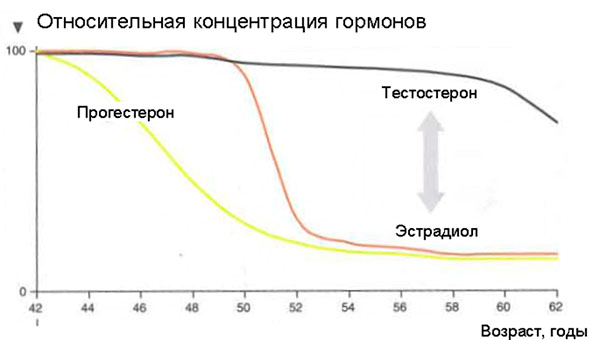
Что будет если МГТ не проводить?
А зачем нужно так «рисковать» и принимать «страшные» гормональные препараты при наступлении менопаузы? Ведь это естественный процесс, может, пусть все идет, как заведено природой? — Но тогда мы неизбежно столкнемся с заболеваниями, которые также предопределены природой.
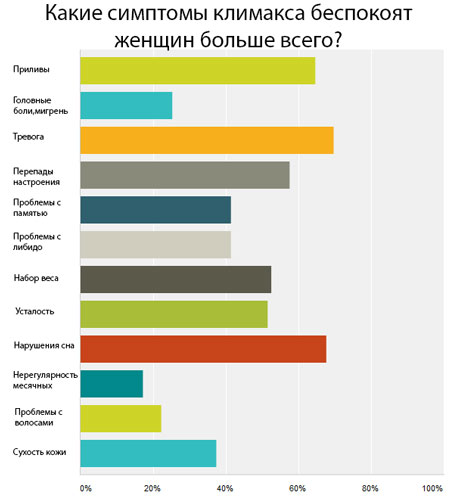
Сначала появляются ранние симптомы:
Через некоторое время появятся и поздние нарушения, связанные с длительным дефицитом половых гормонов:
Какое обследование проводится перед МГТ
Перед назначением менопаузальной гормональной терапии необходимо обследование (впрочем, которое необходимо проводить хотя бы раз в год и без терапии всем сознательным женщинам старше 45 лет).
Дополнительные обследования (при соответствующих данных анамнеза):
Когда пора начинать менопаузальную гормональную терапию?
Но проблема в том, что диапазон нормы ФСГ огромен, и для каждой женщины уровень свой. В идеале нужно сдать анализы крови на гормоны в период максимального расцвета – с 19 до 23 лет. Это и будет вашей индивидуальной идеальной нормой. А начиная с 45 лет ежегодно сверять с ней результаты. Но даже если вы впервые слышите о ФСГ – лучше поздно, чем никогда: в 30, 35, 40 лет имеет смысл выяснить свой гормональный статус, чтобы ближе к критическому возрасту было, на что ориентироваться.
Как самостоятельно понять, что пришло время МГТ?
Уровень эстрогенов снизился, если:
Препаратов огромное количество, какие из них наиболее безопасны?
Действует принцип «минимальности» и «натуральности»!
Для менопаузальной гормональной терапии применяются различные препараты, которые могут быть разделены на несколько групп:
«Натуральные» эстрогены – это препараты эстрогенов, которые по химической структуре идентичны эстрадиолу, синтезируемому в организме женщин. Благодаря современным технологиям создан синтетический эстрадиол, но по своей химической структуре он идентичен натуральному Эстрадиол–17b.
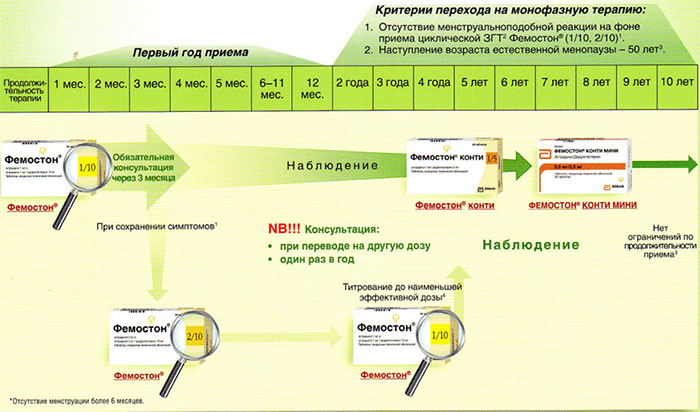
На сегодняшний день таким критериям более всего соответствует препарат Фемостон. Препараты линейки фемостона имеют различные дозировки, что укладывается в один из основных постулатов современной концепции МГТ – использование наименьшей возможной дозировки, которая сохраняет эффективность.
Препараты для двухфазной терапии – когда еще есть месячные
Фемостон 1/10 и Фемостон 2/10
В состав Фемостона 1/10 входят 28 таблеток. 14 белых, содержащих 1 мг Эстрадиола, и 14 серых, содержащих 1 мг Эстрадиола и 10 мг Дидрогестерона.
Состав Фемостона 2/10 отличается только количеством Эстрадиола
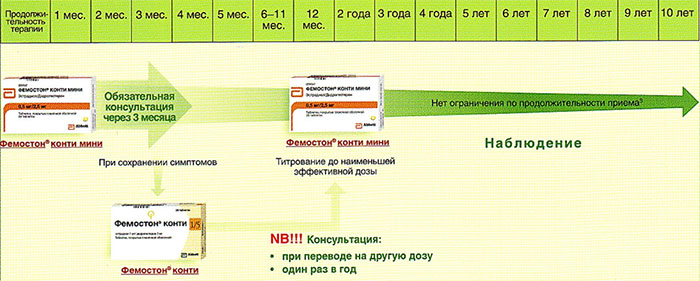
Препараты для монофазной терапии – когда месячные отсутствуют
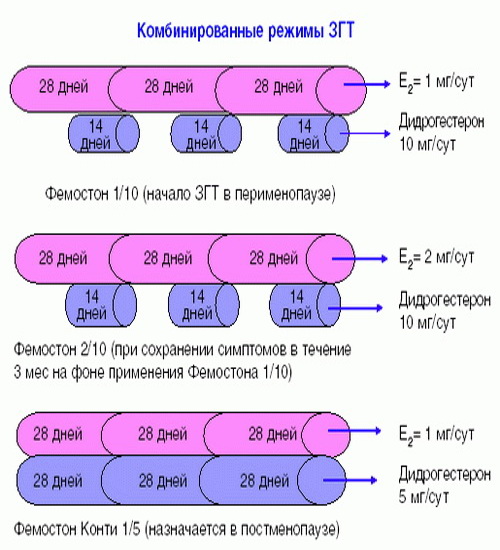
В состав Фемостона конти 1/5 входят 28 таблеток, содержащих 1 мг Эстрадиола и 5 мг Дидрогестерона.
В состав Фемостона мини 0,5/2,5 входят 28 таблеток, содержащих 0,5 мг Эстрадиола и 2,5 мг Дидрогестерона.
Ниже представлена более подробная схема первоначального назначения препаратов фемостон в пременопаузе (то есть до прекращения менструаций, но при наличии характерных климактерических симптомов). Пациенткам, у которых менструации не прекратились, рекомендуют начинать лечение в первый день менструального цикла. Пациенткам с нерегулярным менструальным циклом целесообразно начинать лечение после 10-14 дней монотерапии прогестагеном («химический кюретаж»).
Далее Вашему вниманию представлен алгоритм первоначального назначения препарата фемостон в постменопаузе (то есть когда уже прошел год и более после последней менструации).
Какой способ применения препаратов лучше?
Трансдермальное (накожное) нанесение позволяет избежать первой стадии печеночного метаболизма, благодаря чему колебания концентрации эстрадиола в плазме крови при применении накожных препаратов незначительны. Метаболизм и выведение эстрадиола при трансдермальном введении подобен метаболизму натуральных эстрогенов.
Большинству пациентов желательно использовать оптимальную и наиболее безопасную на сегодняшний день схему: Дивигель накожно + Утрожестан интравагинально.

Схема приема для женщин, у которых сохранена менструальная функция, назначается врачом. Обычно средство прописывают циклом с первого дня после окончания менструации (5 день цикла) в течение 25 дней, после овуляции (c 16 по 25 день цикла) нужно добавлять препараты гестагенов.
Утрожестан – содержит прогестерон микронизированный, существует в двух формах — 100 и 200 мг.
При МГТ в постменопаузе в непрерывном режиме препарат Утрожестан применяется в дозе 100 мг с первого дня приема эстрогенов.
При болях в молочной железе можно добавить прожестожель ежедневно по 1 дозе на каждую молочную железу 2-4 недели.
Противопоказаниями для заместительной гормонотерапии являются:
Нужен ли женщинам тестостерон?
Согласно рекомендациям Международного общества по менопаузе (International Menopause Society (IMS)) основное показание для применения тестостерона – лечение уменьшенного сексуального влечения, которое заставляет данную женщину испытывать значительные страдания. До рассмотрения вопроса о проведении терапии тестостероном необходимо решить вопросы, связанные с другими причинами нарушенного сексуального желания и/или возбуждения. К ним относятся диспареуния, депрессия, побочные эффекты лекарственных препаратов, проблемы взаимоотношений и другие проблемы со здоровьем, влияющие на женщину или ее партнера.
В настоящее время возможно применение трансдермальных препартов. На отечественном фармацевтическом рынке существует только один вариант – Андрогель, но его применение у женщин является «off-label», то есть не разрешено инструкцией. Обычно назначается 1/5 пакета в день (то есть 1 г геля/10 мг тестостерона).
Еще более перспективным может стать интравагинальная форма тестостерона, которая также может оказывать благоприятное действие при лечении вульвовагинальной атрофии.
Ключевые положения по применению препаратов тестостерона
Самые частые заблуждения:
А как же рак молочной железы, ведь это самая главная причина смерти у женщин?
В этом утверждении много заблуждений. На самом деле рак молочной железы – причина смертности в 4% случаев. Ведущая причина преждевременной смерти – сердечно-сосудистые заболевания (50%), которые запускает инсулинорезистентность. А она возникает на фоне гормональных нарушений.
Гормоны вызывают побочные эффекты и от них толстеют?
Новые низкодозированные и высокоселективные препараты направлены четко на мишень. Врачи на протяжении многих лет наблюдали за тысячами женщин, которые получали МГТ? Сегодня уже есть уникальные гестагены, метаболически нейтральные, они не приводят к ожирению и вместе с тем не понижают тестостерон, если у женщины нет его избытка. Выработаны и новые схемы лечения. Иногда при применении таблеток с эстрогенами, где-то в 10% случаев, бывают головные боли и боль в венах. В этом случае они заменяются на трансдермальные формы в виде геля.
Зачем мне принимать гормоны, если у меня нет приливов и отличное самочувствие?
Вместе с падением уровня гормонов возникает риск развития возрастных болезней: повышается артериальное давление, возникает ожирение, увеличивается риск развития сахарного диабета второго типа, подагры, остеопороза и онкологических заболеваний.
Вместо таблеток лучше принимать травы и различные фитоэстрогены?
Эффективность данных препаратов по устранению вазомоторных симптомов составляет 30%, что равно эффективности плацебо. При этом данная группа препаратов никаким образом не оказывает профилактического действия на возрастные заболевания (сердечно-сосудистые, онкологические заболевания, остеопороз, ожирение и сахарный диабет).