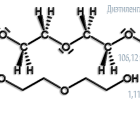
Диэтиленгликоль для чего используется
Диэтиленгликоль — востребованный промышленностью гликоль
Диэтиленгликоль — органическое соединение, 
Свойства
Дигликоль представляет собой густую прозрачную жидкость без запаха и цвета (допускается желтоватый оттенок), со слегка сладковатым вкусом. Впитывает влагу из окружающего воздуха, водорастворим в любых соотношениях. Водные растворы отличаются низкой температурой замерзания. Реактив смешивается с низшими спиртами, гликолями, целлозольвом, ацетоном, фенолом, хлороформом и некоторыми другими орг. веществами. Слабо растворяется в бензоле, стироле, толуоле, диэтиловом эфире, дибутилфталате, тетрахлорметане. Почти не растворяется в маслах.
Малолетуч, что выгодно отличает его от этиленгликоля. Токсичен. Горюч.
 |  |
| Этиленгликоль в/с техн | Полиэтиленгликоль 8000 |
ДЭГ — химически активное вещество, проявляет все свойства гликолей и простых эфиров. Реагирует с:
• водой и кислородом;
• карбоновыми кислотами, их ангидридами и хлорангидридами;
• альдегидами, кетонами, фосгеном, аминами.
В реакциях синтеза может отщеплять атомы водорода (реакция дегидрирования) и молекулы воды (дегидратация). В результате оксиэтилирования (воздействия оксида этилена) превращается в полиэтиленгликоль. Хорошо растворяет щелочи.
Меры предосторожности
Дигликоль считается менее токсичным, чем этиленгликоль; относится к 3-му классу опасности. Тем не менее, для человека он ядовит. Раздражает кожу, при проглатывании вызывает тяжелое отравление, негативно влияет на функционирование почек, печени и центральной нервной системы. Пожароопасен, может самовоспламеняться уже при нагревании до +132 °С. При горении не выделяет опасных соединений. Тушат горящий реактив водой, пенными или углекислотными огнетушителями.
В помещениях, в которых работают с диэтиленгликолем, следует применять строгие меры противопожарной безопасности. Оно должно быть вентилируемым; снабжено автоматической системой пожаротушения и ручными средствами для тушения локального очага возгорания. Работникам следует использовать средства защиты: спецодежду, перчатки, защитные очки или лицевые маски.
Хранят вещество на крытых неотапливаемых складах, в таре из нержавеющей стали, алюминия или алюминированной стали. Для герметичности емкости снабжаются химически стойкими прокладками.
Утилизацию реактива проводят с помощью ионно-обменных смол или сжиганием.
Применение
• В химпроме — сырье для синтеза сложных эфиров, полиуретанов, некоторых других сложных органических соединений; вспомогательных веществ для текстильпрома (набивочных, уплотняющих материалов).
• В качестве очень эффективного высокоизбирательного экстрагента для извлечения ароматических углеводородов в процессах каталитического риформинга, например бензола, ксилола, толуола.
• Пластификатор, стабилизатор, активатор синтеза полимеров; увлажнитель табака, бумаги и химических волокон.
• Осушитель газов; используется для удаления конденсата и влажных паров из трубопроводов для предотвращения образования ледяных пробок. Для очистки технических газов от разных примесей, например, от двуокиси углерода, сероводорода.
• Применяется при производстве целлофана, клеев, пленок.
• Входит в состав антифризов, тормозных и гидравлических жидкостей, смазок, взрывчатых веществ.
• Как растворитель полиэфирных и эпоксидных смол, нитратов целлюлозы.
• В качестве топлива для компактных переносных горелок (обладает высокой теплоемкостью).
Все, что нужно знать, о диэтиленгликоле и триэтиленгликоле
Диэтиленгликоль и триэтиленгликоль, основные сопродукты производства моноэтиленгликоля, за последние десятилетия нашли на рынке собственные узкие ниши, где их использование экономически выгодно, а ограниченные объемы производства – достаточны. Они используются как сырье и растворители в нефтехимической отрасли, а триэтиленгликоль даже можно добавлять в косметику и пищу.
Невольные попутчики
При выпуске моноэтиленгликоля методом гидратации окиси этилена формируется два сопродукта со схожими свойствами – диэтиленгликоль (ДЭГ) и триэтиленгликоль (ТЭГ). Они – прозрачная, бесцветная и вязкая жидкость без запаха со сладковатым привкусом, менее летучи и обладают более высокой температурой кипения.

ДЭГ менее токсичен, чем моноэтиленгликоль и относится к третьему классу опасности. ТЭГ еще более безопасен, но, несмотря на это, оба вещества остаются ядовитыми для человека, вызывая тяжелое отправление в случае проглатывания. Пары не токсичны и не представляют опасности даже при долговременном вдыхании.
Есть два наиболее распространенных варианта производства диэтиленгликоля:
На данный момент в России всего два крупных производителя ди- и триэтиленгликоля – «СИБУР-Нефтехим» и входящий в ТАИФ «Нижнекамскнефтехим». До 2011 года оба продукта также выпускал другой актив ТАИФа – «Казаньоргсинтез», но затем компания отказалась от производства триэтиленгликоля.
Внутренние объемы производства не покрывают растущий спрос, так что сопродукты, в основном – ТЭГ, российским потребителям приходится закупать в Европе. Основной импортер – немецкая корпорация BASF.
Достойная замена
Гликоли стали активно использоваться в промышленности только в начале 20 века, хотя впервые моноэтиленгликоль французский химик Шарль Адольф Вюрц синтезировал в 1859 году, а во время Первой мировой войны он использовался для производства взрывчатых веществ.
Сопродукты моноэтиленгликоля получили широкое распространение еще позже, чем исходный компонент. Гликоли заменили глицерин сначала в области производства динамита, а затем – как компонент охлаждающих жидкостей, так как были эффективней технически и экономически.
После 1936 года они выиграли конкуренцию у глицерина как абсорбент для осушки углеводородных газов.
Несмотря на свое более позднее распространение, ТЭГ имеет преимущества перед ДЭГ в нефтегазовой сфере за счет более низкого давления над раствором и более высокой температуры разложения.

Каждому – свое место
Отличия диэтиленгликоля и триэтиленгликоля от МЭГ определило специфику их использования. За счет более низкой летучести и более высокой температуры кипения и вязкости в некоторых сферах предпочтение производителей отдается именно диэтиленгликолю.
Он используется как:
Еще одной крупной сферой применения ДЭГ с его высокой гигроскопичностью является газовая отрасль. Там он выполняет роль осушителя газов и используется в трубопроводах для удаления конденсата и влажных паров, предотвращая образование ледяных пробок. Также он помогает убирать углекислый газ и сероводород.
Способность поглощать влагу делает его полезным для поддержания необходимой влажности табачных изделий и бумаги.
Диэтиленгликоль применяется при производстве целлофана, клеев, пленок. Также за счет высокой теплоемкости он может использоваться в качестве топлива для переносных горелок.
В то же время как компонент антифриза диэтиленгликоль хоть и применяется, но намного реже, чем моноэтиленгликоль. Но это никак не связано с конкретными свойствами веществ, так как параметры замерзания водных растворов МЭГ и ДЭГ серьезно не отличаются.

Просто объемы производства моноэтиленгликоля существенно выше, а сам компонент – более привычен в качестве сырья для нефтехимии. При этом в некоторых случаях использование в производстве охлаждающих жидкостей обоих веществ позволяет добиться их более высоких эксплуатационных показателей.
Ближе к людям
Сферы применения триэтиленгликоля во многом определяет его сниженная летучесть и относительная безопасность по сравнению с МЭГ и ДЭГ. Вещество используется в тех продуктах, с которыми потребитель контактирует напрямую или в течение долгого времени.
Например, триэтиленгликоль выступает растворителем и пластификатором для лаков и лакокрасочных материалов. Он также используется в качестве дезинфицирующего средства. Ограниченно применяется в фармацевтике и на предприятиях пищевой промышленности. Так, за счет более низкой токсичности, ТЭГ в некоторых странах разрешен к применению в малых дозах в косметических и лекарственных препаратах.
Относительная безопасность сопродуктов моноэтиленгликоля стала причиной «антифризного» скандала в сфере виноделия в Австрии. В 1985 году в ходе стандартной проверки винной продукции немецкая лаборатория обнаружила в некоторых видах австрийской продукции повышенное содержание диэтиленгликоля.
Выяснилось, что отдельные производители в Австрии добавляли ДЭГ, который маскирует в вине дополнительные объемы сахара, который виноделам приходилось добавлять в неудачные годы, когда виноград не успевал вызреть и набрать нужное количество природного сахара.
Помимо этого, диэтиленгликоль делал напитки более сладкими, а букет – более полным. После выявления ДЭГ в составе продажи австрийских вин рухнули во всем мире и еще более 15 лет не могли вернуться на прежние уровни, даже несмотря на то, что из-за их потребления не было жертв. По расчетам экспертов, отравиться насмерть можно было только аяв течение двух недель по 28 бутылок вина с ДЭГ ежедневно.
В целом, как отмечает глава Центра отраслевых исследований Андрей Костин, диэтиленгликоль и триэтиленгликоль со временем нашли свои определенные ниши потребления, хоть и не очень крупные. По его словам, это напрямую связано с небольшими объемами производства сопродуктов. Но, говорит эксперт, наращивать объемы этих продуктов отдельно – невозможно экономически оправданным способом, это реально только вместе с увеличением производства основного продукта – МЭГ.
Диэтиленгликоль
ДИЭТИЛЕНГЛИКOЛЬ (2,2′-дигидроксидиэтиловый эфир, дигликоль)
молярная масса 106,12
бесцветная, вязкая гигроскопичная жидкость, без запаха, со сладковатым вкусаом;
Смешивается с водой, низшими спиртами, карбитолами, гликолями, целлозольвами, ацетоном, анилином, фенолом, хлороформом.
Ограниченно — с бензолом, дибутилфталатом, толуолом, стиролом, диэтиловым эфиром, ССl4.
В диэтиленгликоле плохо растворяются минеральные и растительные масла. Диэтиленгликоль обладает химическими свойствами, характерными для гликолей и простых эфиров. При взаимодействии с карбоновыми компонентами и их ангидридами образует сложные моно- и диэфиры, с альдегидами и кетонами.
Диэтиленгликоль образует водородные связи также с водой, аминами. Диэтиленгликоль способен к автоокислению. Процесс автоокисления резко ускоряется при наличии в диэтиленгликоле, пероксидов, гидропероксидов. Антиокислители (гидрохинон или др.) сильно увеличивают стабильность диэтиленгликоля.
Получение диэтиленгликоля.
В промышленности диэтиленгликоль получают двумя способами:
1) оксиэтилированием этиленгликоля в присутсвии щелочи при 160-180°С, давлении 1,1-2,0 МПа и мольном соотношении этиленоксид : этиленгликоль = 1:2 (выход диэтиленгликоля 60%):
2) как побочный продукт в производств этиленгликоля, путем гидратации этиленоксида в присутсвии щелочи или кислето при температуре 160-200 °С, 1-2 МПа и мольном соотношении этиленоксид: вода = 1:10. При этом около 15% этиленоксида превращается в диэтиленгликоль. На производство 1 т диэтиленгликоля расходуется 1,0-1,1 т этиленоксида.
Применение диэтиленгликоля.
Диэтиленгликоль — применяется как сырье в производств сложных эфиров, полиуретанов, олигоэфиракрилатов, полиалкиленгликольмалеинатов. Используется как пластификатор, высокоселективный экстрагент ароматических углеводородов из катализатов риформинга, а также увлажнитель табака, осушитель газов, компонент антифризов, гидротормозных и гидравлических жидкостей. Является Растворитель нитратов целлюлозы и полиэфирных смол.
Мировое производство на 1975г. диэтиленгликоля около 400 тыс. т/год.
Диэтиленгликоль
Диэтиленгликоль марки А (ДЭГ, дигликоль А) поставляется в металлических бочках с массой нетто 242 кг или наливом в тару потребителя. Мы также поставляем этиленгликоль, пропиленгликоль, этилцеллозольв, глицерин и другое сырье для лакокрасочной промышленности.
Основные свойства
Отличия от этиленгликоля
Физические свойства близки. Диэтиленгликоль отличается от этиленгликоля лучшей растворимостью, меньшей летучестью, более высокой температурой кипения и вязкостью. Температура замерзания водного раствора несколько выше чем у этиленгликоля, хотя и незначительно.
Растворимость
Диэтиленгликоль превосходно смешивается с водой и большим количеством различных органических соединений: одноатомными спиртами, пропиленгликолем и другими гликолями, этилцеллозольвом и другими целлозольвами и карбитолами, этаноламином, ацетоном, фенолом, уксусной кислотой, фурфуролом, пиридином в широком интервале температур. Растворимость бензола при комнатной температуре составляет 45% по массе, что гораздо выше чем в этиленгликоле. В диэтиленгликоле не растворимы минеральные и многие растительные масла.
Применение
Диэтиленгликоль реже используется в качестве антифриза по сравнению с этиленгликолем. Однако скорее это связано не с тем, что он имеет менее подходящие для этой цели свойства (температура замерзания водных растворов и другие характеристики различаются не столь значительно) а с тем, что этиленгликоль является более привычным и доступным продуктом для и объем его производства больше. При этом в некоторых случаях применение диэтиленгликоля в смеси этиленгликолем позволяет получать антифризы с более высокими эксплуатационными свойствами.
Диэтиленгликоль используется в качестве избирательного (селективного) растворителя с целью экстракции различных веществ из нефти и нефтепродуктов, таких как ксилол, толуол, бензол, т.к. хорошо растворяет ароматические углеводороды и не способен к растворению парафиновых и нафтеновых углеводородов. Благодаря более высокой растворимости диэтиленгликоль предпочтительней этиленгликоля для этих целей. При этом получаются продукты высокой степени чистоты.
Благодаря высокой гигроскопичности диэтиленгликоль широко используется для удаления водяных паров из газов, прокачиваемых по трубопроводам. Удалять водяные пары необходимо с целью предотвращения образования в трубопроводах конденсата и ледяных пробок. Также с помощью диэтиленгликоля можно очищать газы и от других примесей, например сероводорода и углекислого газа.
Дигликоль применяется в качестве сырья при синтезе различных полимерных материалов: ненасыщенных полиэфирных смол, щелочестойких алкидных смол, термостойких и огнестойких полиуретанов, а также используется при синтезе различных модифицирующих компонентов для полимерных материалов: пластификаторов, стабилизаторов, антиоксидантов, активаторов полимеризации, отвердителей эпоксидных смол.
Технология производства
Наиболее распространенными технологиями производства диэтиленгликоля являются: совместный его синтез с этиленгликолем и получение из этиленгликоля. Эти две технологии близки и в качестве исходного реагента в них используется окись этилена.
Первая технология представляет собой не что иное как обычную технологию получения этиленгликоля по реакции гидратации окиси этилена, в которой всегда вместе с этиленгликолем получается и диэтиленгликоль. При этом варьируя соотношение исходных реагентов можно получать различный выход этих продуктов. Так, например при мольном соотношении воды и окиси этилена 17:1 соотношение получаемых этиленгликоля и диэтиленгликоля составляет 10:1. А при соотношении воды и окиси этилена 14:1 выход диэтиленгликоля составляет уже 20%. Дальнейшее уменьшение доли воды в реакционной смеси не приводит к увеличению выхода диэтиленгликоля, так как в этих условиях наряду с ним в заметных количествах образуются триэтиленгликоль, тетраэтиленгликоль и другие более высокомолекулярные гликоли. Образующийся при этом этиленгликоль после отделения от других гликолей может возвращаться обратно в реакционную смесь для следующего цикла синтеза.
По второй технологии диэтиленгликоль получается при взаимодействии этиленгликоля с окисью этилена. Процесс включает несколько стадий: совмещение окиси этилена и этиленгликоля в водном растворе, выдержка раствора с целью осуществления реакции, выпаривание воды из смеси продуктов реакции и разделение получившихся гликолей на отдельные продукты. При синтезе по данной технологии получается высокий выход диэтиленгликоля. При этом также образуются триэтиленгликоль, тетраэтиленгликоль, пентаэтиленгликоль, гексаэтиленгликоль и в небольших количествах другие гликоли.
Опасность
Токсичность диэтиленгликоля ниже чем этиленгликоля. Пары не представляют высокой опасности при вдыхании. Однако прием внутрь также чрезвычайно опасен.
Утилизация и регенерация
Отработанный продукт можно очищать с помощью ионно-обменных смол.
Диэтиленгликоль
бесцветная, без запаха, прозрачная жидкость
полностью смешивается с водой
оглавление
Производство
характеристики
Диэтиленгликоль образует легковоспламеняющиеся паровоздушные смеси при высоких температурах. Соединение имеет температуру вспышки 138 ° C. Диапазон взрывоопасности составляет от 1,7% по объему (75 г / м 3 ) в качестве нижнего предела взрываемости (НПВ) до 37% по объему (1635 г / м 3 ) в качестве верхнего предела взрываемости (ВПВ). Температура возгорания 355 ° C. Таким образом, вещество относится к температурному классу T2.
использовать
Случаи отравления
В 2007 году токсичное вещество было также обнаружено в китайской зубной пасте, продаваемой в дисконтном магазине в Панама-Сити. В результате зубная паста была снята с рынка в США и Канаде.
Отравление зубной пастой, загрязненной диэтиленгликолем, на сегодняшний день не известно и очень маловероятно при нормальном использовании из-за низкой дозы и токсикологических свойств диэтиленгликоля. Тем не менее, Федеральный институт оценки рисков и Научный комитет по пищевым продуктам Европейского союза рекомендуют максимальную суточную дозу 0,5 мг / кг массы тела для суммы диэтиленгликоля, моноэтиленгликоля и сложного эфира ди-, моно- и стеариновой кислоты. триэтиленгликоль «не должно быть превышено.
В Бразилии было несколько случаев отравления в 2019 и 2020 годах в связи с употреблением зараженного пива с пивоварни Backer. Были также расследованы несколько смертей, предположительно вызванных диэтиленгликолем. В результате в январе 2020 года вся продукция этой пивоварни была снята с рынка властями.