Дискинезия сердца что это такое
Аневризма левого желудочка сердца
Тел.: 8-800-25-03-03-2
(бесплатно для звонков из регионов России)
Санкт-Петербург, наб. реки Фонтанки, д. 154
Тел.: +7 (812) 676-25-25
Санкт-Петербург, В.О., Кадетская линия, д. 13-15
Тел.: +7 (812) 676-25-25
Санкт-Петербург, ул. Циолковского, д.3
Тел.: +7 (812) 676-25-10
В результате ткань истончается и растягивается, образуя выпячивание- аневризму. Чаще всего поражается левый желудочек в передней верхней части.
Аневризма левого желудочка сердца классифицируется по нескольким признакам:
1. По времени появления:
2. По форме проявления:
В практике более часто встречаются диффузные формы, реже диагностируют расслаивающуюся и грибовидную аневризмы.
Симптомы и причины появления
Основная причина появления аневризма — инфаркт миокарда. Так же появление истонченных, выпирающих участков ткани на сердце может быть спровоцировано такими причинами, как:
Симптоматически наличие аневризмы левого желудочка сердца определить невозможно, но поскольку она вызывает нарушения работы сердца то и, соответственно, вызывает общие признаки расстройства сердечной деятельности. Среди них:
Диагностировать аневризму желудочка сердца может врач-кардиолог. После осмотра пациента и получения результатов всех необходимых исследований, в том числе ЭКГ, УЗИ и МРТ. Своевременная диагностика поможет избежать тяжелейших осложнений, часто смертельных. Для определения плана лечения необходимо точно знать локализацию, структуру и размеры аневризмы.
Методы диагностики
Главные способы диагностирования аневризмы основаны на последовательном выявлении клинических и инструментальных признаков. Начинается обследование с опроса больного, сбора анамнеза, некоторых лабораторных исследований крови и мочи — эти данные позволяют обнаружить сопутствующие заболевания, наличие которые может повлиять на развитие аневризмы. Пациент также получает направление на ЭКГ, МРТ или УЗИ и другие исследования.
Традиционные методы диагностики и информация, которую они предоставляют:
Комплексное всестороннее обследование пациента позволяет получить полную картину деформации тканей желудочка, а значит, назначить точное и наиболее эффективное лечение. Помимо медикаментозной терапии, больным с выявленной аневризмой левого желудочка сердца может быть назначено хирургическое вмешательство. Обычно такое решение принимается лечащим врачом в случае, если размеры поврежденной ткани превышают 20% площади стенки.
Методы лечения
В связи с относительно благоприятным прогнозом при бессимптомных аневризмах левого желудочка (ЛЖ), показания к хирургическому лечению у таких пациентов относительны. Тем не менее, у пациентов, которым показана хирургическая реваскуляризация миокарда (АКШ), в некоторых случаях необходимо выполнять хирургическое восстановление правильной формы левого желудочка.
Хирургическое лечение абсолютно показано пациентам, у которых в результате инфаркта миокарда появилась дисфункция ЛЖ с участками акинезии и дискинезии его стенок и закономерным увеличением объема ЛЖ: > 80 мл / м 2 при сокращении и > 120 мл / м 2 в момент расслабления, а также при угрозе разрыва аневризмы и в случае тромбоэмболического синдрома при тромбированных аневризмах.
При правильном профессиональном подходе, внимательном изучении функции ЛЖ по данным ЭхоКГ, оценке формы и локализации аневризмы, фракции выброса сокращающейся (уцелевшей) части ЛЖ – операция по устранению левожелудочковой аневризмы является вполне оправданной, так как впоследствии снижается напряжение в стенке ЛЖ, мышечные волокна вновь направляются в правильную сторону, возрастает систолическая и улучшается диастолическая функция ЛЖ.
Относительные противопоказания: крайне высокий риск анестезии, отсутствие «живого» миокарда за пределами аневризмы, низкий сердечный индекс.
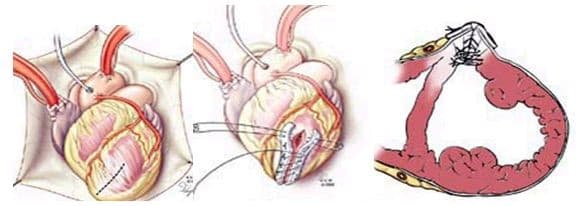
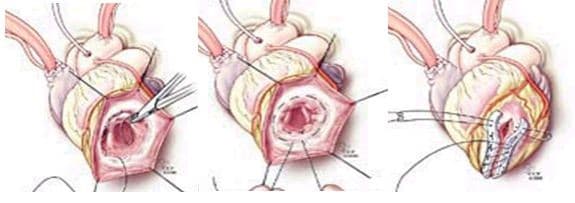
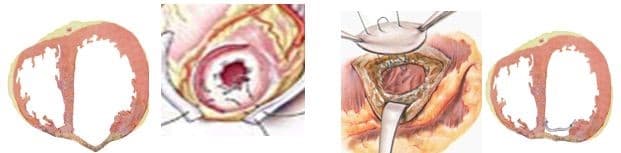
При хирургическом лечении аневризмы ЛЖ выполняется стандартный доступ путем срединной стернотомии. Аппарат искусственного кровообращения подключается как для АКШ, для удобства устанавливается дренаж ЛЖ через правые легочные вены. После кардиоплегии участок аневризмы выглядит как белесая, фиброзная площадка, впалая в полость левого желудочка. Выполняется разрез аневризмы вдоль передней нисходящей артерии, отступая от нее не менее 1,5 см. Имеющийся в полости тромб удаляется, исключая оставление даже очень мелких фрагментов. Часто такие операции сопровождаются вмешательством на митральном клапане, а также шунтированием передней нисходящей артерии и других артерий при наличии показаний. Оценив объем резецированного участка приступают к ремоделированию и восстановлению геометрии ЛЖ. Методик для этого предложено много, ниже мы приведем основные из них. После завершения хирургических манипуляций на сердце, выполняется важный процесс изгнания воздуха из полостей сердца, следом к сердцу пускают кровоток, снимая зажим с аорты, и через пару минут происходит восстановление сердечной деятельности. Окончание сеанса искусственного кровообращения для оперированного ЛЖ может стать настоящим испытанием и потребовать применение до трех инотропных и вазопрессорных препаратов, а также внутриаортальной баллонной контрапульсации.
Техники ремоделирования ЛЖ
Прогресс не стоит на месте, и методики постоянно совершенствуются, но основные хирургические принципы для лечения данной патологии представлены вашему вниманию и заключаются в стремлении к уменьшению полости ЛЖ за счет резекции нефункционального аневризматического мешка и восстановлению близкой к нормальной геометрической формы ЛЖ применяя разной формы заплаты и кисетные пластики.
Результаты хирургического лечения аневризмы левого желудочка сердца
Частым осложнением после операции по поводу аневризмы ЛЖ является синдром малого выброса, который развивается вследствие чрезмерного уменьшения размеров полости ЛЖ, а так же желудочковые нарушения ритма и легочная недостаточность.
30-ти дневная летальность в последние годы снизилась и составляет 3-7%. Факторы повышенного риска операции это: пожилой возраст, женский пол, операция в экстренном порядке, а так же операция дополненная протезированием митрального клапана, исходно низкая сократительная способность миокарда (ФВ менее 30%), умеренная и высокая легочная гипертензия, почечная недостаточность.
В нашей клинике успешно выполняются все виды операций на сердце включая хирургическое ремоделирование и пластику при аневризмах ЛЖ.
Какие нарушения сердца видны через ЭхоКГ
Сердце – особенный орган, и УЗИ для него тоже особенное. Называется – ЭхоКГ.
Почему нельзя делать УЗИ сердца на обычном ультразвуковом аппарате?
Можно, но только результат исследования окажется неполным. Дело в том, что у эхокардиографа есть дополнительные возможности и особые датчики, которые позволяют получить качественное изображение органа, постоянно находящегося в движении. Кроме того, любой аппарат способен проводить исследование с эффектом Доплера. Доплерография даёт возможность оценить скоростные показатели потока крови, его направление, наличие патологического сброса. Это принципиально важно при оценке состояния клапанов сердца и перегородок, расположенных между предсердиями и желудочками. Наконец, к эхокардиографу можно подсоединить специальный датчик для проведения чреспищеводной эхокардиографии, который внешне больше напоминает гастроскоп.
Говорят, что ЭхоКГ это золотой стандарт в окончательной диагностике инфаркта?
По сути именно ЭхоКГ ставит точку в решении вопроса, были инфаркт миокарда или всё-таки нет. Такую возможность даёт прицельное изучение стенок сердца – передней, боковой, задней или нижней, а также межжелудочковой перегородки. Если миокард в этих зонах получил некротическое повреждение и там сформировался рубец, на эхокардиографии будет выявлено нарушение его сократимости. Это значит, что стенка сокращаться хуже, отставать от рядом расположенных (гипокинезия), сокращаться в своем режиме, что называется, не попадая в ногу (дискинезия), или вообще не будет сокращаться, выбиваясь из общего марша (акинезия). Если подобные изменения обнаружены (а они нередко бывают случайной находкой, без указания на перенесённый инфаркт), то вероятность инфаркта в прошлом более 90%. Если же в диагнозе стоит инфаркт, а по данным ЭКГ и ЭхоКГ подтверждений этому обнаружить не удаётся, скорее всего, речь идет о гипердиагностике и инфаркта на самом деле не было.
Какие показатели ЭхоКГ можно назвать наиболее важными?
Силу сердечной мышцы показывает так называемая фракция выброса (ФВ). Если этот показатель снижен, речь может идти о хронической сердечной недостаточности. Наличие нарушений локальной сократимости миокарда стенок сердца (гипокинезия, дисикинезия, акинезия) свидетельствует о перенесённом инфаркте или ишемии. Оценка клапанов включает количество створок, размер отверстия, доплерографически определяется наличие обратного сброса крови (недостаточность клапана) или повышенного градиента давления на клапане, свидетельствующего о формировании сужения (стеноза) клапана. Недостаточность клапанов или регургитация измеряется в степенях: от первой до четвёртой. Если первую и вторую можно отнести к варианту нормы, то третью (выраженную,) а тем более четвёртую считают патологией, которая требует хирургической коррекции. Анализ перегородок сердца помогает выявить наличие патологических отверстий и сброса крови через них (дефектов межпредсердной и межжелудочковой перегородок). Важную информацию представляют размеры камер сердца, толщина миокарда и наличие его гипертрофии, тромбы в полости сердца.
Что такое стресс — ЭхоКГ?
Если у пациента подозревают ишемическую болезнь сердца, врач-кардиолог обычно назначает нагрузочный тест. Часто это велоэргометрия или тредмил, когда пациент крутит педали велосипеда или идёт по беговой дорожке, а у него постоянно фиксируют ЭКГ, дожидаясь появления ишемии. Но раньше появления изменений на ЭКГ появляются те самые изменения кинетики стенок, о которых мы уже говорили. Тем более, сразу можно точно обнаружить стенку сердца, которая страдает больше всего, и предположить, какая именно артерия сужена бляшками. Поэтому, стресс-тест с ЭхоКГ считается более информативным. Его проводят с помощью физической нагрузки, когда пациент крутит педали на специальном велосипеде в лежачем положении, либо стимулируя работу сердца с помощью введения в вену специальных лекарств. В результате сердце работает намного активнее, и фрагменты миокарда, испытывающие нехватку питания, сокращаются хуже остальных.
Зачем назначают чреспищеводное ЭхоКГ?
В некоторых случаях даже после проведения стандартного ЭхоКГ кардиологам требуется уточнение. То, что не удалось увидеть через грудную клетку с помощью обычного датчика, можно рассмотреть из пищевода с помощью датчика, больше напоминающего гастроскоп. Оказывается, изнутри лучше видно пороки клапанов сердца, состояние его перегородок и наличие тромбов в предсердиях. Исследование проводится в сознании под действием легких снотворных препаратов, по ощущениям приятным его не назовешь, но и слишком дискомфортным тоже, но напоминает проведение обычной гастроскопии.
Как подготовиться к ЭхоКГ?
Обычное исследование, которое называют трансторакальным, особой подготовки не требует. Если речь идёт о чреспищеводном исследовании, то предварительно нужно будет выполнить гастроскопию, чтобы убедиться, что в пищеводе нет эрозий, варикозно расширенных вен и других нарушений. Если в ходе исследования выясниться, что человек с трудом переносит введение «шланга» и в верхние отделы ЖКТ, чреспищеводное ЭхоКГ можно буде провести под внутривенной анестезий, как говорят пациенты «во сне».
Сегодня ЭхоКГ, как и все исследования, активно развивается. Теперь его делают не только из пищевода, но и непосредственно из полости сердца – так называемое внутрисердечное ЭхоКГ. Для этого датчик доводят до сердца от паховых сосудов. Результаты исследования представляют в виде трёхмерных двигающихся изображений такого качества, что врачу трудно отличить реконструкцию от реального бьющегося сердца.
Если у Вас остались вопросы, Вы можете задать их кардиологу онлайн в приложении Доктис.
Онлайн консультации врачей
в мобильном приложении Доктис
Дежурный терапевт и педиатр консультируют бесплатно
© 2016-2021, ООО «Диджитал Медикэл Оперейшнс»
Лицензия на осуществление мед деятельности ЛО-76-01-002757.
Адрес: 121205, г. Москва, Территория Сколково Инновационного Центра, бульвар Большой, д. 42, стр. 1, эт. 4, пом. 1594, раб. 2
Филиал в г. Ярославль: 150062, Ярославская область, г. Ярославль, ул. 5-я Яковлевская, д.17
Расстройства движения (дискинезии) причины, симптомы, методы лечения и профилактики
Расстройства движения (дискинезии) — заболевание, подразумевающее нарушение координации движения. Чаще гладких мышечных тканей внутренних органов. Самостоятельно заболевание не исчезает. Требует консультации врача.
Симптомы расстройства движения (дискинезии)
Врачи выделяют несколько проявлений болезни:
Статью проверил
Дата публикации: 24 Марта 2021 года
Дата проверки: 24 Марта 2021 года
Дата обновления: 10 Декабря 2021 года
Содержание статьи
Причины
Чаще болезнь прогрессирует на фоне частого эмоционального переутомления. Врачи выделяют несколько факторов развития первичной формы патологии:
Вторичная форма болезни развивается в следующих случаях:
Стадии развития расстройства движения (дискинезии)
Врачи выделяют несколько стадий:
Разновидности
В зависимости от области поражения выделяют следующие виды:
В зависимости от объёма выделяемой желчи выделяют следующие виды:
Диагностика
Невролог собирает жалобы пациенты, проводит визуальный и пальпаторный осмотр. Пациенту назначают инструментальные и лабораторные методы исследования. Для обнаружения дискинезии пищевода проводят эзофагоскопию, рентгенографию. С целью обнаружения осложнений больного направляют на анализ каловых масс. Для постановки диагноза нарушение движений желудочного тракта проводят электрогастрографию, рентгеноскопию и биопсию. Для обнаружения дискинезии желчевыводящих путей пациента направляют на ультразвуковое исследование, МРТ, биохимический анализ крови. Поражение кишечного тракта помогают диагностировать колоноскопия, обзорная рентгенография, исследование каловых масс. В сети клиник ЦМРТ используют следующие методы обследования:
Синдром «разбитого сердца» (синдром такоцубо)
Впервые этот синдром стал широко известен в 2006 году после обсуждения этой темы на Европейском конгрессе кардиологов в Барселоне. Однако до сих пор многие практические врачи и пациенты остаются плохо осведомленными о его существовании. В последние годы современная медицина все больше внимания уделяет изучению его причин, которые до сих пор неясны.
Как правило, типичные симптомы синдрома разбитого сердца – это боль в сердце и затрудненное дыхание, что совершенно идентично симптомам острого инфаркта миокарда и определяет драматизм ситуации и его актуальность.
В настоящее время считается, что синдром разбитого сердца, или стресс-индуцированная кардиомиопатия (она же — обратимая апикальная дискинезия) вызван сильными эмоциями и характеризуется преходящим нарушением работы левого желудочка сердца, что проявляет себя изменениями на электрокардиограмме и в крови, свойственными инфаркту миокарда.
Стресс-индуцированная кардиомиопатия впервые была описана в 1991 году в Японии и даже получила название такоцубо по названию ловушки для ловли осьминогов, которую используют японские рыбаки, так как при этом синдроме форма левого желудочка становится похожей на нее. При этом расстройстве, сердце больных, вернее его левый желудочек, принимает необычную –шарообразную форму. Оно как будто бы сдавлено невидимым обручем. Этот симптом помогает отличить это расстройство от инфаркта и правильно поставить диагноз.
Провоцирующим это заболевание фактором является сильный стресс и интенсивные эмоциональные переживания. Почти сразу же после этого у больных возникает сильная боль в сердце и серьезные проблемы с дыханием, что обычно диагностируется, как инфаркт миокарда, так как симптомы и данные электрокардиограммы не вызывают никаких сомнений. Загрудинные боли при этом синдроме более длительные, чем при инфаркте миокарда.
Механизмы возникновения этого заболевания до конца неясны. Явная связь его со стрессом и тяжелыми эмоциями заставляет медиков думать, что причина его кроется в эффекте катехоламинов – гормонов стресса. Исследовались и другие механизмы – спазм коронарных артерий, нарушение микроциркуляции крови в сердце и неврологические причины, но ни одна из них до сих пор не подтвердилась.
Проблема в диагностике этого расстройства в том, что как анализы крови, так и электрокардиограмма при синдроме разбитого сердца практически идентичны результатам диагностических проб при инфаркте миокарда. Отличить его возможно только посредством коронарографии, которая демонстрирует в этом случае совершенно здоровые артерии сердца.
Есть сообщения, что патоморфологические изменения при этом виде кардиомиопатии представлены фокальным миоцитолизом; ассоциированных микробиологических агентов не выявляется. В некоторых случаях обнаруживалась инфильтрация малыми мононуклеарами; эти патологические находки позволяют предположить, что стрессовая кардиомиопатия является вариантом воспалительного заболевания сердца, а не коронарной патологией. Также имеются сообщения о гистологическом повреждении миокарда без ишемической болезни сердца.
Более 90% случаев этого заболевания возникает у женщин в климактерическом периоде. Причина этого неясна, но существует несколько гипотез: большая чувствительность женщин к действию гормонов стресса и проблемы в сосудах и мышце сердца, спровоцированные низким уровнем женских половых гормонов.
При стресс-индуцированной кардиомиопатии необходима неотложная госпитализация больного в стационар. При этом синдроме часто возникает сердечная недостаточность, которая бесследно исчезает через нескольких дней.
Прогноз заболевания, обычно, очень хороший. Несмотря на изначально тяжелое состояние пациентов, почти все они полностью выздоравливают в течение нескольких дней или недель без всяких осложнений. Смертность составляет лишь 1, 1%. В очень редких случаях могут быть тяжелые осложнения: мерцательная аритмия в 4, 2% и кардиогенный шок в 1, 5% случаев.
Дискинезия сердца что это такое
а) Региональная сократимость. Так как в различных слоях миокарда волокна ориентированы по-разному, то движение стенки, видимое при ЭхоКГ, является суммой различно ориентированных сокращений в миокарде. При этом внутренняя (субэндокардиальная) половина стенки утолщается значительно сильнее, чем внешняя, субэпикардиальная. В итоге нормальные сегменты стенки желудочка выполняют в систолу движение, направленное внутрь желудочка, а сама стенка утолщается. При этом утолщение стенки является более надежным параметром, который можно использовать и, например, в случае асинхронного сокращения при блокаде ножки пучка Риса.
Утолщение стенки и направленное внутрь движение наименее выражены в области базальных сегментов. Особое место занимает базальная часть базального переднеперегородочного сегмента, которая во время систолы не совершает направленного внутрь движения или даже немного смещается наружу (прежде всего, это хорошо видно на парастернальном базальном сечении по короткой оси), что, предположительно, обусловлено «пульсовой волной» ударного объема в области выносящего тракта левого желудочка.
1. Качественная оценка. В первую очередь происходит качественная оценка региональной сократимости:
— нормокинезия: нормальное движение и утолщение стенки,
— гипокинезия: сниженное, но определяемое движение и утолщение стенки (это наиболее субъективно вариабельная категория),
— акинезия: отсутствие движения и утолщения стенки,
— дискинезия: систолическое движение стенки наружу,
— аневризма: выпячивание левого желудочка, отмечающееся и во время диастолы, с аномально тонким, не сокращающимся миокардом,
— гиперкинезия: движение и утолщение стенки превышают нормальные показатели, что встречается при клапанной регургитации, в качестве компенсации нарушения локальной сократимости в другой зоне (например, после инфаркта), во время нагрузки или при стимуляции катехоламинами. При этом в конце систолы почти вся полость может быть замещена сокращающимся миокардом (систолическая облитерация полости желудочка). Сама по себе гиперкинезия не имеет патологического значения, однако является указанием на одно из вышеназванных состояний.
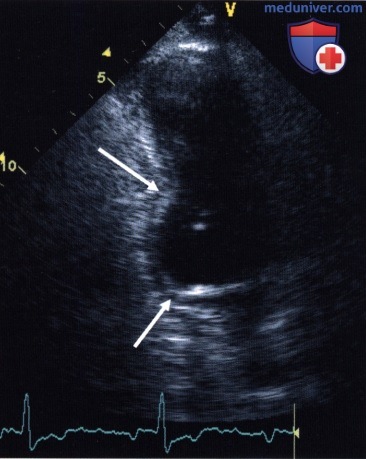

2. Количественный анализ. Многочисленные попытки количественного анализа локальной сократимости, в особенности автоматизации оценки, до сих пор не привели к созданию надежной методики, хотя бы приблизительно равнозначной визуальному заключению опытного исследователя. Поэтому сохраняется проблема субъективной вариабельности оценки локальной сократимости, которая лишь в ограниченной мере решается улучшением качества изображения, параллельным просмотром различных видеофрагментов, введением контрастных средств для левых отделов сердца и другими усовершенствованиями.
Недавно опубликованный систематический обзор различных методических подходов показал степень соответствия между различными визуализирующими методиками и определяемой при помощи согласованного клинического мнения «истиной» (степень соответствия выражалась в виде доверительного интервала значений каппы Кохена). Значение каппы, равное 1, означает полное соответствие бинарного события (нарушение локальной сократимости присутствует/отсутствует). Доверительные интервалы каппы с точки зрения выявления нарушений локальной сократимости составили:
— 0,5-0,7 для нативной ЭхоКГ,
— 0,6-0,8 для ЭхоКГ с контрастированием левых отделов,
— 0,5-0,8 для МРТ.
В рамках каждой из методик вариабельность между двумя исследователями составила:
— 0,3-0,5 для ЭхоКГ,
— 0,7-0,9 для ЭхоКГ с контрастированием левых отделов и
— 0,3-0,6 для МРТ.
Особенное значение эта проблема имеет в стресс-ЭхоКГ и при диагностике жизнеспособного миокарда в зонах с нарушенной сократимостью (см. соответствующие главы).
3. Анализ региональной деформации. В настоящее время наиболее перспективным подходом к количественной оценке локальной сократимости является анализ региональной деформации (strain/strain rate) при помощи тканевой допплерографии. Здесь можно локально и количественно оценить степень выраженности и временную динамику систолической и диастолической деформации (например, продольное укорочение и удлинение на апикальных сечениях). Но до сих пор получаемые данные чувствительны к артефактам, обременены шумовым сигналом, и их часто бывает трудно интерпретировать. Методика двумерного отображения деформации (20-strain), находящаяся ныне в начальной стадии апробации, должна существенно улучшить данный методический подход.
б) Причины нарушения сократимости:
1. Коронарная болезнь сердца. Чаще всего локальные нарушения сократимости развиваются на фоне коронарной болезни сердца:
— После инфаркта развивается необратимое, сохраняющееся в покое нарушение локальной сократимости. При этом большой постинфарктный рубец проявляется в виде акинезии или аневризмы, а после мелких инфарктов остается лишь гипокинезия или существенное нарушение локальной сократимости не определяется. Большие постинфарктные рубцы характеризуются уменьшением толщины стенки примерно на 30% и иногда несколько более высокой эхогенностью, чем окружающий миокард, что объясняется более высоким содержанием коллагена в рубце.
Надежное соотнесение нарушения локальной сократимости с гистологической зоной инфаркта осложняется связностью всех сегментов миокарда: как соседние, нормально сокращающиеся области миокарда могут «увлекать» акинетическую зону инфаркта, так и, наоборот, нарушения локальной сократимости в инфарктной зоне могут снижать амплитуду сокращений соседних здоровых сегментов («теттеринг-эффект»),
— В случае острой ишемии в покое или на фоне нагрузки (обратимые нарушения сократимости, диагностическое использование в стресс-ЭхоКГ).
— В покое в связи с оглушенным (станнинг) или гибернирующим миокардом, т.е. отсутствием (или снижением) сократимости в еще жизнеспособном миокарде.
2. Другие заболевания. Кроме КБС, нарушения локальной сократимости могут развиваться при следующих заболеваниях:
— ДКМП: хотя поражение часто имеет диффузный характер, но нередко обнаруживаются зоны гипокинезии различной степени выраженности. Однако аневризмы при этом заболевании не встречаются.
— Миокардиты: здесь изредка встречаются и более выраженные нарушения локальной сократимости, например, апикальная аневризма при болезни Чагаса (Trypanosoma cruzii).
— Нарушения локальной сократимости, поражающие только межжелудочковую перегородку, без вовлечения остальной перфузионной территории ПМЖВ, т.е. передней стенки: они встречаются относительно часто. С одной стороны, возможно развитие аномального временного паттерна сократимости с сохраненным утолщением перегородки в результате локального замедления механической систолы (например, при блокаде левой ножки пучка Гиса, правожелудочковом кардиостимуляторе, синдроме WPW, после кардиохирургического вмешательства), а также в результате взаимодействия левого и правого желудочков или наложения движения всего сердца в грудной клетке на процессы сокращения, например, после операции на сердце, при повышении нагрузки давлением или объемом на правый желудочек или в случае значительного перикардиального выпота.
Если в начале систолы происходит движение перегородки, направленное наружу, то такая ситуация обозначается термином «парадоксальная перегородка», что, будучи неспецифическим изменением, может встречаться при всех вышеназванных клинических ситуациях. С другой стороны, может развиваться истинное снижение амплитуды сокращений, как, например, при КБС (закупорка септальной ветви) или кардиомиопатии.
Редактор: Искандер Милевски. Дата публикации: 26.12.2019