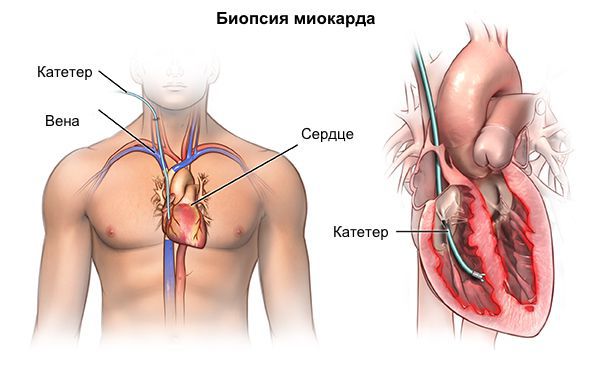
Диспластическая кардиопатия у ребенка что это значит
Кардиопатия у детей
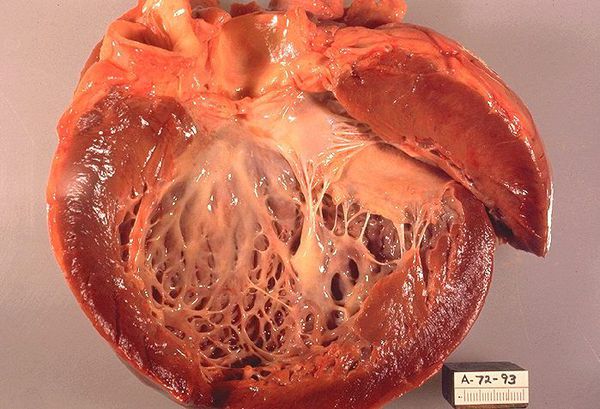
С каждым годом врачи все чаще и чаще диагностируют у своих пациентов заболевания, поражающие сердечно-сосудистую систему. С течением времени постепенно увеличивается и количество таких патологий у подростков и детей. Основная масса отклонений от нормального развития приходится на долю кардиопатий. Данная патология подразумевает совокупность заболеваний, связанных с нарушением развития миокарда. В переводе с греческого языка понятие «кардиопатия» дословно можно перевести как «нарушение сердца». Поэтому нередко любую сердечную патологию медики относят к этому понятию. Однако, все же принято кардиопатией называть ряд детских отклонений, имеющих определенную классификацию. Каждое изменение развития миокарда имеет свои характерные особенности.
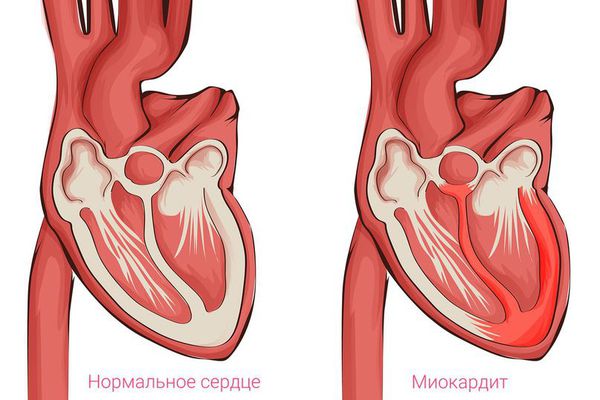
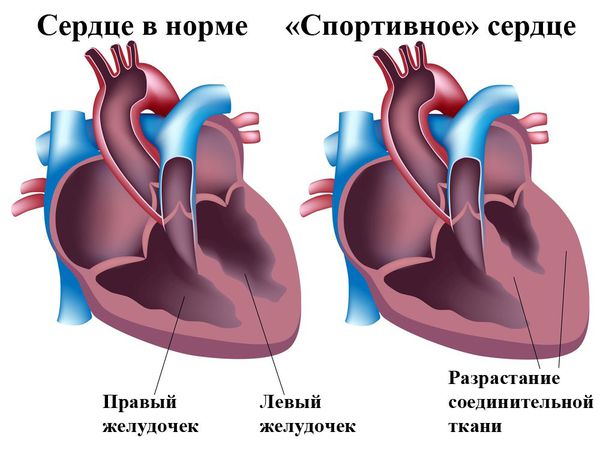
В зависимости от возраста, при котором обнаруживается данная патология, ее принято делить на приобретенную и врожденную. Врожденную кардиопатию диагностируют на первых неделях жизни ребенка. Такая патология чаще связана с врожденными пороками развития или с ревматоидными аутоиммунными заболеваниями новорожденных. Диагноз приобретенной кардиопатии врач может выставить ближе к подростковому возрасту. Это связано с тем, что в период с 9 до 12 лет ребенок активно растет. Нередко отклонения в развитии сердечно-сосудистой системы диагностируются в 15-16 лет. Это связано с изменением гормонального фона и половым созреванием. Чаще всего кардиопатия определяется при одном или нескольких следующих изменениях: аномалии развития крупных сердечных сосудов; увеличение межжелудочковой перегородки в сердце; нарушение сердечного ритма и проводимости нервного импульса; изменение электрической оси сердца; отклонения в развитии одного или обоих желудочков сердца; нарушение работы сердечных клапанов (их неполное открытие). Некоторые из вышеописанных изменений напрямую свидетельствуют о пороке развития сердца у ребенка. Иные являются общими признаками различных заболеваний. Именно по этой причине для достоверной постановки диагноза обязательно выполнение некоторых инструментальных исследований. Существует основные 4 вида кардиопатий у детей, которые классифицируются по варианту течения и причинам: Функциональная. Диспластическая. Дилатационная. Вторичная. Функциональная кардиопатия возникает в тех случаях, когда дети чрезмерно занимаются спортом и получают физические нагрузки выше возрастной нормы. Под их действием миокард пытается экстренно адаптироваться к такому режиму работы. В итоге возникают так называемые функциональные изменения в сердечной мышце. Ярким примером развития такой патологии являются регулярные занятия у спортсменов, которые проходят с нарушением режимов и регламентов. Суть заключается в том, что недостаточно квалифицированные тренеры и учителя физической подготовки заставляют детей выполнять большой объем работы, предварительно не подготовив детский организм к нему. Также подобная кардиопатия может наблюдаться у ребенка при его воспитании в неблагополучной семье. Диспластическая кардиопатия развивается как самостоятельное заболевание. Обычно патология не связана с какими-либо нарушениями других систем и органов в организме. Часть специалистов считают, что болезнь подразумевает наличие соединительной ткани в каком-либо участке сердца. Другая часть медиков такие изменения относит к функциональной кардиопатии. В детском возрасте не выставляется диспластическая кардиомиопатия в качестве самостоятельного диагноза. В некоторых странах данный термин все же используют, подразумевая под ним пролапс митрального клапана. Такая патология в своем большинстве вариантов не требует абсолютно никакого специального лечения. Понятие «диспластическая кардиопатия» используется еще и в том случае, когда в сердце обнаруживается какая-либо необъяснимая патология, причину которой понять невозможно. При таком варианте в качестве лечения обычно назначаются профилактические средства и манипуляции. Дилатационная кардиопатия – это расширение одного или нескольких отделов сердца. Такая патология развивается при действии на миокард токсинов, вирусов, бактерий. В результате при длительных воспалительных процессах снижается эластичность сердечной мышцы, вызывая расширение полости предсердия или желудочка. Доказана и наследственная теория возникновения этого заболевания, т.к. часто оно встречается у членов одной семьи из поколения в поколение. Вторичная кардиопатия развивается при наличии заболеваний, связанных не только с сердечно-сосудистой системой. Наибольшему риску, естественно, подвержены дети и подростки. Патология может появиться на фоне следующих болезней: воспалительные заболевания сердца (эндо- и миокардиты); заболевания легких (пневмонии, бронхиальная астма); нарушения обмена веществ; любые затяжные или хронические воспалительные заболевания. В последнем случае диагностировать патологию сердца достаточно просто, т.к. болеющий человек уже в момент лечения находится под постоянным контролем врача. Симптомы Основным проявлением кардиопатии у детей является болевой синдром. Ноющие или давящие ощущения чаще всего локализованы за грудиной в области сердца. Дискомфорт чаще кратковременный, хотя бывают случаи длительных болей. Другие симптомы полностью зависят от формы патологии и особенностей ребенка и его организма. При функциональной кардиопатии из-за того, что органы хуже обогащаются кислородом, могут возникнуть следующие симптомы: общее недомогание и слабость; повышенная утомляемость; одышка даже при небольших физических нагрузках. Диспластическая форма может сопровождаться нехваткой кислорода, приступами головокружения и ощущением нарушения нормального сердцебиения. При вторичной кардиопатии симптомы очень разнообразны, т.к. все проявления зависят от основного первичного заболевания.
Диагностика кардиопатий у детей
При плановых осмотрах педиатр может заподозрить наличие каких-либо изменений в сердечно-сосудистой системе. Обычно он направляет ребенка на консультацию детского кардиолога. Если врач определяет симптомы, похожие на какую-либо кардиопатию, то планируется дальнейшая диагностика для назначения правильного своевременного лечения. Иногда случается так, что патология сердца выявляется при обращении к врачам по причине другого заболевания, не связанного с сердцем. Однако в любом случае кардиолог, скорее всего, назначит следующие исследования: УЗИ сердца; электрокардиографию; эхокардиографию. Обычно этих трех исследований достаточно для определения заболевания и выбора способа лечения. Дополнительно может быть назначена рентгенография грудной клетки при помощи которой определяется расширение желудочка (при дилатационной кардиопатии). Особенности заболевания у новорожденных Новорожденные также могут страдать кардиопатиями. Заболевание часто развивается на фоне перенесенного недостатка кислорода. Притом не важно, когда возникла гипоксия, во время родов или еще во время беременности. Из-за дефицита кислорода нарушается регуляция работы сердца с изменением вегетативной нервной системы. Дисфункция миокарда возникает из-за нарушения процессов энергетического обмена. В среднем, 50-70 % перенесших гипоксию новорожденных страдают кардиопатиями. Тяжесть патологии во многом зависит от продолжительности перенесенной гипоксии. Если нехватка кислорода наблюдалась и после рождения, то с большей долей вероятности развивается патология сердца, которую нужно потом специфически лечить. Обычно подобные кардиопатии сохраняются от месяца и до трехлетнего возраста примерно у трети заболевших детей. Лечение кардиопатий Вся терапия полностью зависит от формы патологии. Функциональная кардиопатия лечится физиотерапевтически. Для этого используется специальный аппарат, который при помощи интерференционных токов действует на организм. По своему принципу данная процедура является в большей степени профилактической, чем лечебной. По механизму действия она такая же, как подобные процедуры, которые проводят в санаториях. Происходит улучшение всех обменных процессов, в том числе и кровообращения. Снижаются некоторые болевые ощущения. При других формах применяется медикаментозное лечение. Притом схема терапии подбирается строго индивидуально. Это связано с тем, что понятие «кардиопатия» очень обширное. Оно включает в себя огромное количество абсолютно разных изменений в сердце. При лечении крайне важно, чтобы пациентом соблюдался правильный образ жизни и распорядок дня. Необходимы регулярные прогулки и сбалансированное питание. Все инфекционные заболевания, включая банальную простуду, нужно своевременно лечить. Любое проявление и симптом, похожий на признак сердечной патологии нельзя игнорировать ни в коем случае. Во время диагностированное заболевание и начатое лечение всегда имеет высокий шанс на благоприятный исход. Практически любая кардиопатия в детском возрасте имеет очень высокую вероятность полного излечения.
Что такое кардиомиопатия? Причины возникновения, диагностику и методы лечения разберем в статье доктора Кузнецова Т. Н., кардиолога со стажем в 26 лет.
Определение болезни. Причины заболевания
Пусковым механизмом возникновения кардиомиопатии поначалу считали процесс воспаления в сердце, который мог быть спровоцирован вирусными, бактериальными и аутоиммунными повреждениями клеток. Исходя из этой теории, назначение антибиотиков, противовирусных и противовоспалительных препаратов должно было привести к регрессии повреждения и восстановлению функции сердца. Однако практика это не подтвердила.
Риск развития кардиомиопатий повышен у лиц с отягощённой наследственностью, а также после перенесённых острых инфекционных заболеваний. Для появления вторичных кардиомиопатий важно наличие системных аутоиммунных заболеваний, эндокринной патологии (сахарный диабет, тиреотоксикоз) и токсических факторов.
Первичные кардиомиопатии чаще выявляют в детском и молодом возрасте, вторичные же возможны в любом возрасте.
Симптомы кардиомиопатии
Специфических, характерных только для кардиомиопатии симптомов не существует. Именно эта особенность и затрудняет раннюю диагностику заболевания. Кардиомиопатия длительно протекает бессимптомно или малосимптомно, в развёрнутой стадии похожа по клинике на проявления ишемической болезни сердца, различных пороков сердца.
Первыми жалобами, с которыми пациенты обращаются к врачу, являются:
Патогенез кардиомиопатии
За последние годы благодаря возможностям генетики было установлено, что причиной многих кардиомиопатий являются генетические мутации, которые приводят к выработке дефектных белков кардиомиоцита. От того, какой белок рабочей клетки миокарда (кардиомиоцита) изменился, зависит развитие определённого вида кардиомиопатии.
Подобные изменения бывают также при наследственных нарушениях обмена веществ и лизосомальных болезнях накопления (редких заболеваниях, при которых нарушается функция внутриклеточных органелл лизосом). Из-за врождённой нехватки ферментов, перерабатывающих углеводсодержащие продукты, в организме накапливаются крупные молекулы гликогена, гликопротеина и др., которые повреждают организм. Таких заболеваний известно более сотни, но их распространённость невелика. Как правило, проявляются они в детском и молодом возрасте и помимо поражения сердца затрагивают практически весь организм: кости, мышцы, нервную систему, зрение и слух. Самыми изученными болезнями накопления являются гемохроматоз, болезнь Пике и болезнь Фабри.
Классификация и стадии развития кардиомиопатии
По мере накопления информации были выявлены самые распространённые типы кардиомиопатии и их семейные формы:
К редким формам кардиомиопатии относят также системные заболевания и патологические состояния, при которых возникают так называемые вторичные кардиомиопатии: диабетическая, тиреотоксическая, алкогольная, аутоиммунная и другие.
Исходя из причины развития болезни, становится ясным, что кардиомиопатии могут быть как изолированными – первичными, так и являться частью системного заболевания, т. е. быть вторичными.
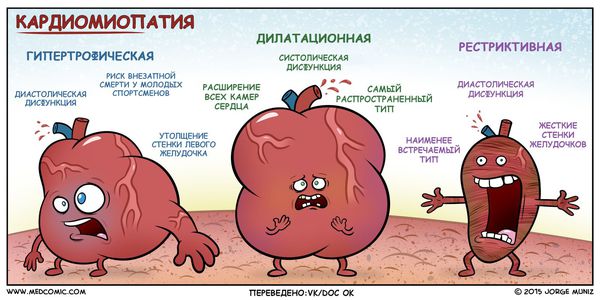
В России традиционно применяется клинико-морфологическая классификация первичных кардиомиопатий, где кардиомиопатии разделяются на:
Анатомическая классификация гипертрофической кардиомиопатии в зависимости от локализации:
I. Гипертрофия левого желудочка:
В зависимости от наличия обструкции выносного тракта левого желудочка (область между межжелудочковой перегородкой и передней створкой митрального клапана) в покое и при нагрузке выделяют два типа гипертрофической кардиомиопатии :
К тяжело выявляемым видам относится аритмогенная дисплазия правого желудочка, при которой происходят структурные изменения в строении стенки правого желудочка — замещение кардиомиоцитов фиброзно-жировой тканью и развитие аритмии.
Неклассифицируемые кардиомиопатии: некомпактный миокард, стресс-индуцированная кардиомиопатия.
Вторичные (специфические) кардиомиопатии: при имеющемся известном заболевании тяжесть поражения сердца более выражена и не соответствует причине:
Осложнения кардиомиопатии
Особенности течения кардиомиопатии представляют угрозу для жизни. Болезнь может дебютировать сразу внезапной смертью или жизнеугрожающими аритмиями : фибрилляцей желудочков, желудочковой тахикардией. Высокий риск внезапной сердечной смерти связан с такими факторами риска, как:
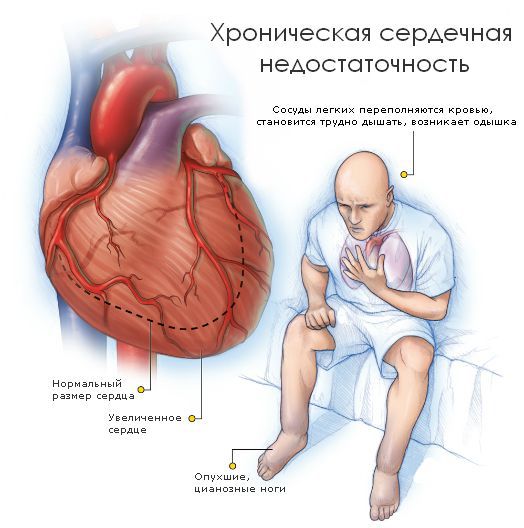
С утяжелением недостаточности все симптомы становятся более выраженными. Выделяют пять стадий сердечной недостаточности:
Диагностика кардиомиопатии
Особых признаков, характерных для этого заболевания, при сборе жалоб и осмотре пациента выявить не удаётся.
При клиническом осмотре обращают на себя внимание признаки сердечной недостаточности различной степени выраженности, аритмии, возможны тромбоэмболические осложнения.
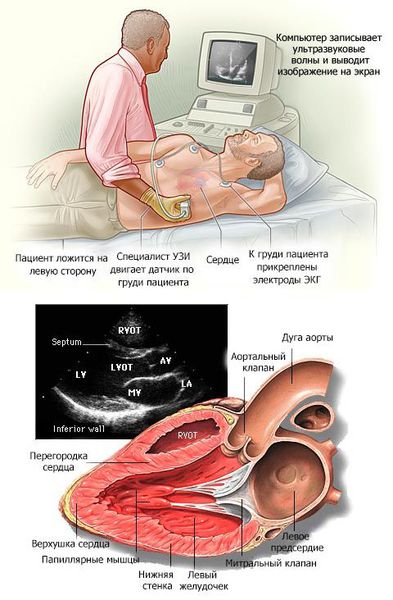
В основном кардиомиопатии выявляются при проведении эхокардиографии (ЭХОКГ) и электрокардиографии (ЭКГ). Дополнительно применяются рентгеноконтрастная вентрикулография и магнитно-резонансная томография (МРТ) с контрастированием гадолинием.
В современной кардиологии всё больше распространяются новые методы визуализации сердца и сосудов — например, магнитно-резонансная томография (МРТ). Но её недостатком является дороговизна оборудования и малая доступность методики из-за отсутствия качественного оборудовании и специалистов.
На стандартной ЭКГ также могут быть зарегистрированы изменения в виде признаков гипертрофии миокарда левого желудочка, а также признаки его перегрузки и различные нарушения ритма сердца.
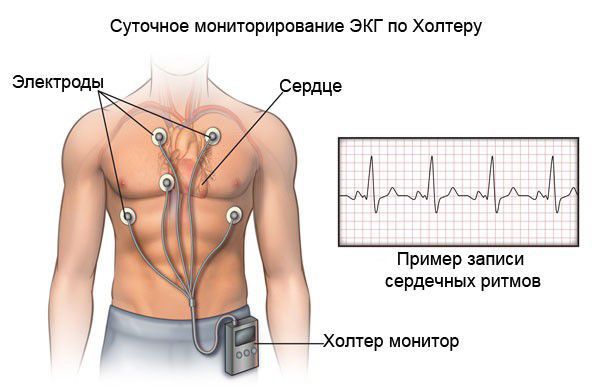
При холтеровском мониторировании ЭКГ также фиксируются нарушения ритма и проводимости практически в 100 % случаях. Выявление таких нарушении ритма сказывается на подборе базисной терапии кардиомиопатии.
В особых случаях для уточнения диагноза редких форм кардиомиопатии (например, при амилоидозе) возможна прижизненная биопсия миокарда. Методика инвазивная, потенциально опасная для пациента, требует использования уникального комплекса аппаратуры и высочайшей квалификации специалистов, что возможно только в нескольких научных кардиологических центрах РФ.
Из лабораторных методов диагностики помимо стандартных анализов крови (клинического и биохимического), необходимо отметить ДНК-диагностику. Она является «золотым стандартом» при подозрении на кардиомиопатию согласно мировым (европейским и американским) руководствам. Этот подход на данный момент является практически единственным, который применим для раннего выявления и прогнозирования риска развития семейных форм кардиомиопатии. В России такой уровень диагностики возможен в единичных лабораториях и является дорогостоящей процедурой из-за своей уникальности.
Лечение кардиомиопатии
По современным представлениям стратегия лечения пациента определяется в процессе разделения больных на категории в зависимости от типа кардиомиопатии.
Все больные с выявленной кардиомиопатией, независимо от течения заболевания (в том числе и бессимптомные), нуждаются в динамическом наблюдении. Кратность наблюдения и объём обследований определяются индивидуально. В обязательный перечень входят стандартные анализы (клинический и биохимический анализ крови), ЭКГ, ЭХОКГ и холтеровское мониторирование ЭКГ.
Лечебная тактика зависит от множества факторов и подбирается индивидуально. При этом учитываются анатомические особенности — обструкция выносного тракта левого желудочка, растяжение полостей сердца, наличие клапанной патологи, стадия сердечной недостаточности и также сопутствующие заболевания. Необходимо выявлять факторы, повышающие риск внезапной смерти и жизнеугрожающих аритмий [15]
При дилатационной кардиомиопатии необходимо лечить причину развития растяжения полостей сердца, если это возможно. В медикаментозной терапии сердечной недостаточности применяют все стандартные группы лекарств:
Помимо лекарств в ряде случаев прибегают к хирургическим методам лечения кардиомиопатии.
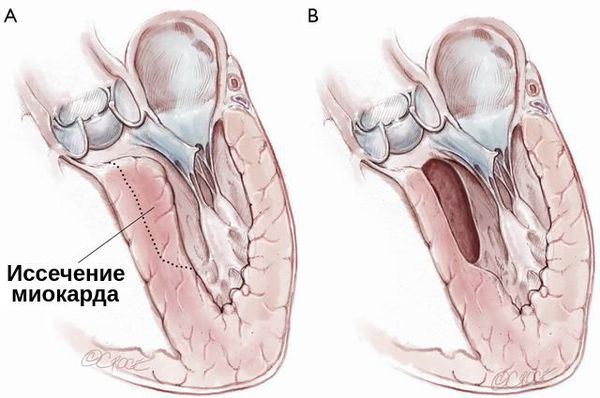
При гипертрофической кардиомиопатии применяется септальная миэктомия — иссечение миокарда, расположенного в основании межжелудочковой перегородки. Она может быть дополнена и вмешательством на изменённом митральном клапане: вальвулопластикой, протезированием митрального клапана и коррекцией кольца митрального клапана.
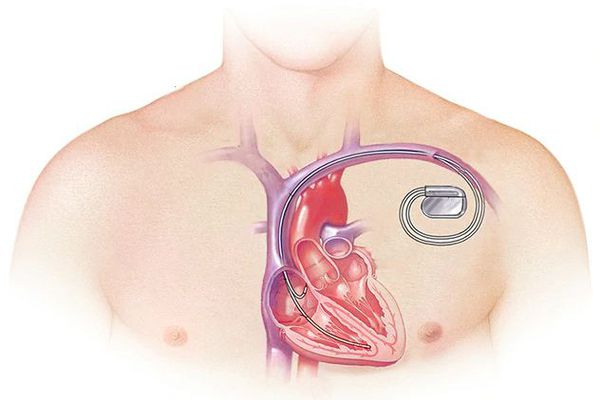
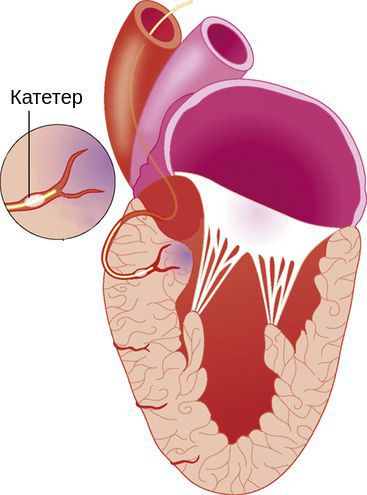
При тяжёлой обструктивной гипертрофической кардиомиопатии рассматривается проведение операции — иссечения части сердечной мышцы или более щадящая методика — чрескожная транслюминальная алкогольная абляция. При ней через катетер вводится до 3 мл 96 % спирта в зону максимальной гипертрофии миокарда и вызывается его инфаркт. Из-за этого мышца уменьшается в размере, исчезает препятствие (обструкция) току крови через митральное кольцо. Далее проводится установка кардиостимулятора для синхронизации работы всех отделов сердца. Эта процедура проводится кардиохирургами в специализированных отделениях.
Прогноз. Профилактика
Прогноз при гипертрофической кардиомиопатии также неблагоприятный, но смертность не такая высокая — в первый год умирают 1 % заболевших, чаще от внезапной смерти, обусловленной факторами риска (наследственностью, тахикардией, предшествующим обмороками, понижением давления).
При рестриктивной кардиомиопатии прогноз неблагоприятный, так как заболевание часто находят уже на поздней стадии развития. Лечение только симптоматическое и поддерживающее.
Для человека с выявленной кардиомиопатии частота посещений и обследований устанавливается индивидуально.
Дисплазия соединительной ткани: основные клинические синдромы, формулировка диагноза, лечение
Дисплазия соединительной ткани (ДСТ) (dis — нарушения, рlasia — развитие, образование) — нарушение развития соединительной ткани в эмбриональном и постнатальном периодах, генетически детерминированное состояние, характеризующееся дефектами волокнистых структур и основного вещества соединительной ткани, приводящее к расстройству гомеостаза на тканевом, органном и организменном уровнях в виде различных морфофункциональных нарушений висцеральных и локомоторных органов с прогредиентным течением, определяющее особенности ассоциированной патологии, а также фармакокинетики и фармакодинамики лекарств [15, 24].
Данные о распространенности собственно ДСТ разноречивы [5, 14, 17], что обусловлено различными классификационными и диагностическими подходами. Распространенность отдельных признаков ДСТ имеет половозрастные различия [3]. По самым скромным данным показатели распространенности ДСТ, по меньшей мере, соотносятся с распространенностью основных социально значимых неинфекционных заболеваний.
ДСТ морфологически характеризуется изменениями коллагеновых, эластических фибрилл, гликопротеидов, протеогликанов и фибробластов, в основе которых лежат наследуемые мутации генов, кодирующих синтез и пространственную организацию коллагена, структурных белков и белково-углеводных комплексов, а также мутации генов ферментов и кофакторов к ним [1, 12, 23]. Некоторые исследователи, основываясь на выявляемом в 46,6–72,0% наблюдений при ДСТ дефиците магния в различных субстратах (волосы, эритроциты, ротовая жидкость), допускают патогенетическое значение гипомагниемии.
Одна из основополагающих характеристик дисплазии соединительной ткани как дисморфогенетического феномена — фенотипические признаки ДСТ могут отсутствовать при рождении или иметь очень незначительную выраженность (даже в случаях дифференцированных форм ДСТ) и, подобно изображению на фотобумаге, проявляться в течение жизни. С годами количество признаков ДСТ и их выраженность нарастает прогредиентно.
Классификация ДСТ — один из самых дискутабельных научных вопросов. Отсутствие единой, общепринятой классификации ДСТ отражает разногласие мнений исследователей по данной проблеме в целом. ДСТ может классифицироваться с учетом генетического дефекта в периоде синтеза, созревания или распада коллагена [1, 12]. Это перспективный классификационный подход, который дает возможность обосновать генетически дифференцированную диагностику ДСТ [23], однако на сегодняшний день данный подход ограничен наследственными синдромами ДСТ.
Т. И.Кадурина (2000 г.) выделяет MASS-фенотип, марфаноидный и элерсоподобный фенотипы, отмечая, что именно эти три фенотипа являются наиболее частыми формами несиндромной ДСТ. Это предложение является очень заманчивым, благодаря своей простоте и исходной идее, что несиндромные формы ДСТ являются «фенотипическими» копиями известных синдромов. Так, «марфаноидный фенотип» характеризуется сочетанием «признаков генерализованной дисплазии соединительной ткани с астеническим телосложением, долихостеномелией, арахнодактилией, поражением клапанного аппарата сердца (а порой и аорты), нарушением зрения». При «элерсоподобном фенотипе» отмечается «сочетание признаков генерализованной дисплазии соединительной ткани с тенденцией к гиперрастяжимости кожи и разной степенью выраженности гипермобильности суставов». «MASS-подобному фенотипу» присущи «признаки генерализованной дисплазии соединительной ткани, ряд нарушений со стороны сердца, скелетные аномалии, а также кожные изменения в виде истончения или наличия участков субатрофии». На основе этой классификации предлагается формулировать диагноз ДСТ [12].
Учитывая, что классификация любой патологии несет важный «прикладной» смысл — используется как основа для формулировки диагноза, решение классификационных вопросов являются очень важным с точки зрения клинической практики.
Универсальных патологических повреждений соединительной ткани, которые бы формировали конкретный фенотип, не существует. Каждый дефект у каждого больного в своем роде уникален. При этом всеобъемлющее распространение в организме соединительной ткани определяет полиорганность поражений при ДСТ. В связи с этим предлагается классификационный подход с обособлением синдромов, связанных с диспластикозависимыми изменениями и патологическими состояниями [15, 24].
Синдром неврологических нарушений: синдром вегетативной дисфункции (вегетососудистая дистония, панические атаки и др.), гемикрания.
Синдром вегетативной дисфункции формируется у значительного числа пациентов с ДСТ одним из самых первых — уже в раннем детском возрасте и рассматривается как обязательный компонент диспластического фенотипа [11, 12, 14, 15, 17]. У большинства пациентов выявляется симпатикотония, реже встречается смешанная форма, в малом проценте случаев — ваготония [9, 23]. Выраженность клинических проявлений синдрома нарастает параллельно тяжести ДСТ [11, 23]. Вегетативная дисфункция отмечается в 97% случаев наследственных синдромов, при недифференцированной форме ДСТ — у 78% пациентов. В формировании вегетативных нарушений у пациентов с ДСТ, несомненно, имеют значение генетические факторы, лежащие в основе нарушения биохимизма обменных процессов в соединительной ткани и формировании морфологических субстратов, приводящих к изменению функции гипоталамуса, гипофиза, половых желез, симпатико-адреналовой системы.
Астенический синдром: снижение работоспособности, ухудшение переносимости физических и психоэмоциональных нагрузок, повышенная утомляемость.
Астенический синдром выявляется в дошкольном и особенно ярко — в школьном, подростковом и молодом возрасте, сопровождая пациентов с ДСТ на протяжении всей жизни. Отмечается зависимость выраженности клинических проявлений астении от возраста больных: чем старше пациенты, тем больше субъективных жалоб.
Клапанный синдром: изолированные и комбинированные пролапсы клапанов сердца, миксоматозная дегенерация клапанов.
Чаще он представлен пролапсом митрального клапана (ПМК) (до 70%), реже — пролапсами трикуспидального или аортального клапанов, расширением корня аорты и легочного ствола; аневризмами синусов Вальсальвы. В части случаев выявленные изменения сопровождаются явлениями регургитации, что отражается на показателях контрактильности миокарда и объемных параметрах сердца. Durlach J. (1994) предположил, что причиной ПМК при ДСТ может быть дефицит магния.
Клапанный синдром начинает формироваться также в детском возрасте (4–5 лет). Аускультативные признаки ПМК выявляются в различном возрасте: от 4 до 34 лет, однако наиболее часто — в возрасте 12–14 лет. Следует отметить, что эхокардиографические данные находятся в динамическом состоянии: более выраженные изменения отмечаются при последующих осмотрах, что отражает влияние возраста на состояние клапанного аппарата. Кроме того, на выраженность клапанных изменений влияет степень тяжести ДСТ и объем желудочков.
Среди пациентов с ДСТ наиболее часто встречается воронкообразная деформация грудной клетки, на втором месте по частоте — килевидная деформация и наиболее редко выявляется астеническая форма грудной клетки.
Начало формирование торакодиафрагмального синдрома приходится на ранний школьный возраст, отчетливость проявлений — на возраст 10–12 лет, максимальная выраженность — на период 14–15 лет. Во всех случаях воронкообразная деформация отмечается врачами и родителями на 2–3 года раньше, чем килевидная.
Наличие торакодиафрагмального синдрома определяет уменьшение дыхательной поверхности легких, деформацию просвета трахеи и бронхов; смещение и ротацию сердца, «перекрут» основных сосудистых стволов. Качественные (вариант деформации) и количественные (степень деформации) характеристики торакодиафрагмального синдрома определяют характер и выраженность изменений морфофункциональных параметров сердца и легких. Деформации грудины, ребер, позвоночника и связанное с ними высокое стояние диафрагмы приводят к уменьшению грудной полости, повышению внутригрудного давления, нарушают приток и отток крови, способствуют возникновению аритмий сердца [13, 15]. Наличие торакодиафрагмального синдрома может повлечь за собой повышение давления в системе малого круга кровообращения [23, 27].
Сосудистый синдром: поражение артерий эластического типа: идиопатическое расширение стенки с формированием мешотчатой аневризмы; поражение артерий мышечного и смешанного типов: бифуркационно-гемодинамические аневризмы, долихоэктазии удлиненных и локальных расширений артерий, патологическая извитость вплоть до петлеобразования; поражение вен (патологическая извитость, варикозное расширение вен верхних и нижних конечностей, геморроидальных и др. вен); телеангиоэктазии; эндотелиальная дисфункция.
Изменения сосудов сопровождаются повышением тонуса в системе крупных, мелких артерий и артериол, уменьшением объема и скорости наполнения артериального русла, снижением венозного тонуса и избыточным депонированием крови в периферических венах.
Сосудистый синдром, как правило, манифестирует в подростковом и молодом возрасте, прогрессируя с увеличением возраста пациентов.
Изменения артериального давления: идиопатическая артериальная гипотензия.
Торакодиафрагмальное сердце: астенический, констриктивный, ложностенотический, псевдодилатационный варианты, торакодиафрагмальное легочное сердце.
Формирование торакодиафрагмального сердца происходит параллельно манифестации и прогрессированию деформации грудной клетки и позвоночника, на фоне клапанного и сосудистого синдромов. Варианты торакодиафрагмального сердца служат отражением нарушения гармоничности взаимоотношений веса и объема сердца, веса и объема всего тела, объема сердца и объема больших артериальных стволов на фоне диспластикозависимой дезорганизации роста тканевых структур самого миокарда, в частности, его мышечных и нервных элементов.
У пациентов с типичной астенической конституцией формируется астенический вариант торакодиафрагмального сердца, характеризующийся уменьшением размеров камер сердца при «нормальной» систолической и диастолической толщине стенок и межжелудочковой перегородки, «нормальных» показателях миокардиальной массы, — формирование истинного малого сердца. Сократительный процесс в данной ситуации сопровождается увеличением циркулярного стресса и внутримиокардиального напряжения в циркулярном направлении в систолу, что свидетельствовало о гиперреактивности компенсаторных механизмов на фоне преобладавших симпатических влияний. Установлено, что определяющими факторами в изменении морфометрических, объемных, контрактильных и фазовых параметров сердца являются форма грудной клетки и уровень физического развития костно-мышечного аппарата [15].
У части больных с выраженной формой ДСТ и различными вариантами деформации грудной клетки (воронкообразная деформация I, II степени) в условиях уменьшения объема грудной полости наблюдается «перикардитоподобная» ситуация с развитием диспластикозависимого констриктивного сердца. Уменьшение максимальных размеров сердца с изменением геометрии полостей при этом носит гемодинамически неблагоприятный характер, сопровождаясь уменьшением толщины стенок миокарда в систолу. При уменьшении ударного объема сердца происходит компенсаторное повышение общего периферического сопротивления.
У ряда пациентов с деформацией грудной клетки (воронкообразная деформация III степени, килевидная деформация) при смещении сердца, когда оно «уходит» от механических воздействий костяка грудной клетки, ротируя и сопровождаясь «перекрутом» основных сосудистых стволов, формируется ложностенотический вариант торакодиафрагмального сердца. «Синдром стеноза» выхода из желудочков сопровождается увеличением напряжения миокардиальных структур в меридиональном и циркулярном направлениях, ростом систолического напряжения миокардиальной стенки с увеличением длительности подготовительного периода к изгнанию, увеличением давления в легочной артерии.
У пациентов с килевидной деформацией грудной клетки II и III степени выявляется увеличение устьев аорты и легочной артерии, связанное со снижением упругости сосудов и зависящее от степени тяжести деформации. Изменения геометрии сердца характеризуются компенсаторным увеличением размеров левого желудочка в диастолу либо в систолу, в результате чего полость приобретает шаровидную форму. Сходные процессы наблюдаются со стороны правых отделов сердца и устья легочной артерии. Формируется псевдодилятационный вариант торакодиафрагмального сердца.
В группе пациентов с дифференцированной ДСТ (синдромами Марфана, Элерса–Данлоса, Стиклера, несовершенного остеогенеза), а также у пациентов с недифференцированной ДСТ, имеющих сочетание выраженных деформаций грудной клетки и позвоночника, морфометрические изменения правого и левого желудочков сердца совпадают: уменьшается длинная ось и площади полостей желудочков, особенно в конце диастолы, отражая снижение сократительной способности миокарда; снижаются конечно- и среднедиастолические объемы. Наблюдается компенсаторное снижение общего периферического сосудистого сопротивления, зависящее от степени снижения сократимости миокарда, выраженности деформаций грудной клетки и позвоночника. Неуклонный рост легочного сосудистого сопротивления приводит в данном случае к формированию торакодиафрагмального легочного сердца.
Метаболическая кардиомиопатия: кардиалгии, аритмии сердца, нарушения процессов реполяризации (I степень: увеличение амплитуды Т V2-V3, синдром Т V2 > Т V3; II степень: инверсия Т, смещение ST V2-V3 вниз на 0,5–1,0 мм; III степень: инверсия Т, косовосходящее смещение ST до 2,0 мм).
Развитие метаболической кардиомиопатии определяется влиянием кардиальных факторов (клапанный синдром, варианты торакодиафрагмального сердца) и экстракардиальных условий (торакодиафрагмальный синдром, синдром вегетативной дисфункции, сосудистый синдром, дефицит микро- и макроэлементов). Кардиомиопатия при ДСТ не имеет специфических субъективных симптомов и клинических проявлений, вместе с тем потенциально определяет повышенный риск внезапной смерти в молодом возрасте с преобладающей ролью в танатогенезе аритмического синдрома.
Аритмический синдром: желудочковая экстрасистолия различных градаций; многофокусная, мономорфная, реже полиморфная, монофокусная предсердная экстрасистолия; пароксизмальные тахиаритмии; миграция водителя ритма; атриовентрикулярные и внутрижелудочковые блокады; аномалии проведения импульса по дополнительным путям; синдром предвозбуждения желудочков; синдром удлинения интервала Q-T.
Частота выявления аритмического синдрома — около 64%. Источником нарушения ритма сердца может быть очаг нарушенного метаболизма в миокарде. При нарушении структуры и функции соединительной ткани всегда присутствует подобный субстрат биохимического генеза. Причиной нарушений сердечного ритма при ДСТ может служить клапанный синдром. Возникновение аритмий при этом может быть обусловлено сильным натяжением митральных створок, содержащих мышечные волокна, способные к диастолической деполяризации с формированием биоэлектрической нестабильности миокарда [29]. Кроме того, появлению аритмий может способствовать резкий сброс крови в левый желудочек с пролонгированной диастолической деполяризацией. Изменения геометрии камер сердца также могут иметь значение в возникновении аритмий при формировании диспластического сердца, особенно торакодиафрагмального варианта легочного сердца. Кроме кардиальных причин происхождения аритмий при ДСТ существуют и экстракардиальные, обусловленные нарушением функционального состояния симпатического и блуждающего нервов, механического раздражения сердечной сорочки деформированным костяком грудной клетки. Одним из аритмогенных факторов может быть дефицит магния, выявляемый у пациентов с ДСТ. В предшествующих исследованиях российских и зарубежных авторов получены убедительные данные о причинной взаимосвязи между желудочковыми и предсердными аритмиями и внутриклеточным содержанием магния [19, 22, 25, 26]. Предполагают, что гипомагниемия может способствовать развитию гипокалиемии. При этом увеличивается мембранный потенциал покоя, нарушаются процессы деполяризации и реполяризации, снижается возбудимость клетки. Замедляется проводимость электрического импульса, что способствует развитию аритмий. С другой стороны, внутриклеточный дефицит магния повышает активность синусового узла, снижает абсолютную и удлиняет относительную рефрактерность [19, 22, 26].
Бронхолегочный синдром: трахеобронхиальная дискинезия, трахеобронхомаляция, трахеобронхомегалия, вентиляционные нарушения (обструктивные, рестриктивные, смешанные нарушения), спонтанный пневмоторакс.
Бронхолегочные нарушения при ДСТ современные авторы описывают как генетически обусловленные нарушения архитектоники легочной ткани в виде деструкции межальвеолярных перегородок и недоразвития эластических и мышечных волокон в мелких бронхах и бронхиолах, ведущие к повышенной растяжимости и сниженной эластичности легочной ткани [12, 15, 23]. Следует отметить, что согласно классификации болезней органов дыхания у детей, принятой на Совещании педиатров-пульмонологов РФ (Москва, 1995), такие «частные» случаи ДСТ органов дыхания, как трахеобронхомегалия, трахеобронхомаляция, бронхоэктатическая эмфизема, а также синдром Вильямса–Кемпбелла, на сегодняшний день трактуются как пороки развития трахеи, бронхов, легких [18].
Изменение функциональных параметров дыхательной системы при ДСТ зависит от наличия и степени деформации грудной клетки, позвоночника и чаще характеризуется рестриктивным типом вентиляционных нарушений со снижением общей емкости легких (ОЕЛ) [18, 23]. Остаточный объем легких (ООЛ) у многих пациентов с ДСТ не меняется или слегка повышается без изменения соотношения объема форсированного выдоха в первую секунду (ОФВ1) и форсированной жизненной емкости легких (ФЖЕЛ) [23]. У некоторых пациентов выявляются обструктивные нарушения, феномен гиперреактивности бронхов, что пока не нашло однозначного объяснения [2, 10, 23]. Пациенты с ДСТ представляют собой группу с высоким риском возникновения ассоциированной патологии, в частности, туберкулеза легких [32].
Синдром иммунологических нарушений: синдром иммунодефицита, аутоиммунный синдром, аллергический синдром.
Функциональное состояние иммунной системы при ДСТ характеризуется как активацией иммунных механизмов, обеспечивающих поддержание гомеостаза, так и их недостаточностью, ведущей к нарушению способности адекватно освобождать организм от чужеродных частиц и, следовательно, к развитию рецидивирующих инфекционно-воспалительных заболеваний бронхолегочной системы. Иммунологические нарушения у части пациентов с ДСТ включают повышение в крови уровня иммуноглобулина Е [4]. В целом, литературные данные о нарушениях в иммунной системе при различных клинических вариантах ДСТ носят неоднозначный, нередко противоречивый характер, что требует дальнейшего их изучения. До сих пор остаются практически неизученными механизмы формирования иммунных нарушений при ДСТ. Наличие иммунных нарушений, сопутствующее бронхолегочному и висцеральному синдромам ДСТ, повышает риск возникновения ассоциированной патологии соответствующих органов и систем.
Висцеральный синдром: нефроптоз и дистопии почек, птозы органов желудочно-кишечного тракта, органов малого таза, дискинезии органов желудочно-кишечного тракта, дуоденогастральные и гастроэзофагеальные рефлюксы, несостоятельность сфинктеров, дивертикулы пищевода, грыжи пищеводного отверстия диафрагмы; птозы половых органов у женщин.
Синдром патологии органа зрения: миопия, астигматизм, гиперметропия, косоглазие, нистагм, отслойка сетчатки, вывих и подвывих хрусталика.
Нарушения аккомодации проявляется в различные периоды жизни, у большинства обследованных — в школьные годы (8–15 лет) и прогрессирует до 20–25 лет.
Геморрагические гематомезенхимальные дисплазии: гемоглобинопатии, синдром Рандю–Ослера–Вебера, рецидивирующие геморрагические (наследственная дисфункция тромбоцитов, синдром Виллебранда, комбинированные варианты) и тромботические (гиперагрегация тромбоцитов, первичный антифосфолипидный синдром, гипергомоцистеинемия, резистентность фактора Vа к активированному протеину С) синдромы [20].
Синдром патологии стопы: косолапость, плоскостопие (продольное, поперечное), полая стопа.
Синдром патологии стопы является одним из самым ранних проявлений несостоятельности соединительнотканных структур. Наиболее часто встречается поперечно-распластанная стопа (поперечное плоскостопие), в части случаев сочетающаяся с отклонением 1 пальца наружу (hallus valgus) и продольное плоскостопие с пронацией стопы (плосковальгусная стопа). Наличие синдрома патологии стопы еще больше уменьшает возможность физического развития пациентов с ДСТ, формирует определенный стереотип жизни, усугубляет психосоциальные проблемы.
Синдром гипермобильности суставов: нестабильность суставов, вывихи и подвывихи суставов.
Синдром гипермобильности суставов в большинстве случаев определяется уже в раннем детском возрасте. Максимальная гипермобильность суставов наблюдается в возрасте 13–14 лет, к 25–30 годам распространенность снижается в 3–5 раз. Частота встречаемости гипермобильности суставов достоверно выше среди пациентов с выраженной ДСТ.
Вертеброгенный синдром: ювенильный остеохондроз позвоночника, нестабильность, межпозвонковые грыжи, вертебробазиллярная недостаточность; спондилолистез.
Развиваясь параллельно развитию торакодиафрагмального синдрома и синдрома гипермобильности, вертеброгенный синдром существенно усугубляет их последствия.
Косметический синдром: диспластикозависимые дисморфии челюстно-лицевой области (аномалии прикуса, готическое небо, выраженные асимметрии лица); О- и Х-образные деформации конечностей; изменения кожных покровов (тонкая просвечивающаяся и легко ранимая кожа, повышенная растяжимость кожи, шов в виде «папиросной бумаги»).
Косметический синдром ДСТ значительно усугубляется наличием малых аномалий развития, выявляемых у абсолютного большинства пациентов с ДСТ. При этом подавляющее большинство пациентов имеет 1–5 микроаномалий (гипертелоризм, гипотелоризм, «мятые» ушные раковины, большие торчащие уши, низкий рост волос на лбу и шее, кривошея, диастема, неправильный рост зубов и др.).
Нарушения психической сферы: невротические расстройства, депрессии, тревожность, ипохондрия, обсессивно-фобические расстройства, нервная анорексия.
Известно, что пациенты с ДСТ формируют группу повышенного психологического риска, характеризующуюся сниженной субъективной оценкой собственных возможностей, уровнем претензий, эмоциональной устойчивости и работоспособности, повышенным уровнем тревожности, ранимостью, депрессивностью, конформизмом [3, 9]. Наличие диспластикозависимых косметических изменений в сочетании с астенией формируют психологические особенности этих больных: сниженное настроение, потеря ощущения удовольствия и интереса к деятельности, эмоциональная лабильность, пессимистическая оценка будущего, нередко с идеями самобичевания и суицидальными мыслями [23]. Закономерным следствием психологического дистресса является ограничение социальной активности, ухудшение качества жизни и значительное снижение социальной адаптации [12, 3, 23], наиболее актуальные в подростковом и молодом возрасте.
Поскольку фенотипические проявления ДСТ чрезвычайно многообразны и практически не поддаются какой-либо унификации, а их клиническое и прогностическое значение определяется не только степенью выраженности того или иного клинического признака, но и характером «комбинаций» диспластикозависимых изменений, с нашей точки зрения, наиболее оптимально использовать термины «недифференцированная дисплазия соединительной ткани», определяющий вариант ДСТ с клиническими проявлениями, не укладывающимися в структуру наследственных синдромов, и «дифференцированная дисплазия соединительной ткани, или синдромная форма ДСТ». Практически все клинические проявления ДСТ имеют свое место в Международном классификаторе болезней (МКБ 10). Таким образом, у практического врача есть возможность определить шифр ведущего на момент обращения проявления (синдрома) ДСТ.При этом в случае недифференцированной формы ДСТ при формулировке диагноза следует указывать все имеющиеся у пациента синдромы ДСТ, формируя таким образом «портрет» пациента, понятный любому врачу последующего контакта.
Варианты формулировки диагноза.
1. Основное заболевание. Синдром Вольфа–Паркинсона–Вайта (синдром WPW) (I 45.6), ассоциированный с ДСТ. Пароксизмальная мерцательная аритмия.
Фоновое заболевание. ДСТ:
Осложнения: хроническая сердечная недостаточность (ХСН) IIА, ФК II.
2. Основное заболевание. Пролапс митрального клапана II степени с регургитацией (I 34.1), ассоциированный с малой аномалией развития сердца — аномально расположенной хордой левого желудочка.
Фоновое заболевание. ДСТ:
Осложнения основного: ХСН, ФК II, дыхательная недостаточность (ДН 0).
3. Основное заболевание. Хронический гнойно-обструктивный бронхит (J 44.0), ассоциированный с диспластикозависимой трахеобронхомаляцией, обострение.
Фоновое заболевание. ДСТ:
Осложнения: эмфизема легких, пневмосклероз, адгезивный двухсторонний плеврит, ДН II ст., ХСН IIА, ФК IV.
Вопросы тактики ведения пациентов с ДСТ также являются открытыми. Единых общепризнанных подходов к лечению пациентов с ДСТ на сегодняшний день не существует. Учитывая, что в настоящее время медицине недоступна генная терапия, врачу необходимо использовать любые способы, которые помогут остановить прогредиентность течения заболевания. Наиболее приемлем синдромальный подход к выбору терапевтических вмешательств: коррекция синдрома вегетативных нарушений, аритмического, сосудистого, астенического и др. синдромов.
Ведущим компонентом терапии должны быть немедикаментозные воздействия, направленные на улучшения гемодинамики (лечебная физкультура, дозированные нагрузки, аэробный режим). Однако нередко существенным фактором, ограничивающим достижения целевого уровня физических нагрузок у пациентов с ДСТ, оказывается плохая субъективная переносимость тренировок (обилие астенических, вегетативных жалоб, эпизоды гипотонии), что снижает приверженность пациентов к этому виду реабилитационных мероприятий. Так, по нашим наблюдениям до 63% пациентов имеют низкую толерантность к физической нагрузке по данным велоэргометрии, большинство из этих пациентов отказываются от продолжения курса лечебной физкультуры (ЛФК). В связи с этим представляется перспективным применение в комплексе с ЛФК вегетотропных средств, препаратов метаболического действия. Целесообразным является назначение препаратов магния. Многогранность метаболических эффектов магния, его способность повышать энергетический потенциал миокардиоцитов, участие магния в регуляции гликолиза, синтезе белков, жирных кислот и липидов, вазодилятационные свойства магния широко отражены в многочисленных экспериментальных и клинических исследованиях [6, 7, 22, 26, 30, 31]. В ряде работ, проведенных к настоящему времени, показана принципиальная возможность устранения характерной кардиальной симптоматики и ультразвуковых изменений у больных с ДСТ в результате лечения препаратами магния [7, 22, 25, 26].
Нами проводилось изучение эффективности поэтапного лечения пациентов, имеющих признаки ДСТ: на первом этапе больным проводилась терапия препаратом «Магнерот», на втором к медикаментозному лечению добавляли комплекс лечебной физкультуры. В исследование были включены 120 пациентов с недифференцированной формой ДСТ, имеющих низкую толерантность к физической нагрузке (по данным велоэргометрии) в возрасте от 18 до 42 лет (средний возраст 30,30 ± 2,12 года), мужчин — 66, женщин — 54. Торакодиафрагмальный синдром проявлялся воронкообразной деформацией грудной клетки различной степени (46 человек), килевидной деформацией грудной клетки (49 пациентов), астенической формой грудной клетки (7 пациентов), комбинированными изменениями позвоночного столба (85,8%). Клапанный синдром был представлен: пролапсом митрального клапана (I степени — 80,0%; II степени — 20,0%) с регургитацией (91,7%) или без таковой. У 8 человек было выявлено расширение корня аорты. В качестве группы контроля были обследованы 30 практически здоровых добровольцев, соответствующих по полу и возрасту.
По данным ЭКГ у всех пациентов с ДСТ выявлялись изменения конечной части желудочкового комплекса: I степень нарушения процессов реполяризации выявлялась у 59 пациентов; II степень — у 48 пациентов, III степень определялась реже — в 10,8 % случаев (13 человек). Анализ вариабельности сердечного ритма пациентов с ДСТ по сравнению с группой контроля продемонстрировал статистически значимо более высокие значения среднесуточных показателей — SDNN, SDNNi, RMSSD. При сопоставлении показателей вариабельности сердечного ритма с тяжестью вегетативной дисфункции у пациентов с ДСТ была выявлена обратная зависимость — чем выраженнее вегетативная дисфункция, тем ниже показатели вариабельности сердечного ритма.
На первом этапе комплексной терапии назначался Магнерот по следующей схеме: 2 таблетки 3 раза в день первые 7 дней, затем по 1 таблетке 3 раза в день в течение 4 недель.
В результате проведенного лечения была отмечена отчетливая положительная динамика частоты кардиальных, астенических и разнообразных вегетативных жалоб, предъявляемых пациентами. Позитивная динамика ЭКГ-изменений проявилась в снижении частоты встречаемости нарушений процессов реполяризации I степени (р Полезная информация – Статьи – Дисплазия соединительной ткани: основные клинические синдромы, формулировка диагноза, лечение