Длинный желудок что это
Разница между SADI-Sleeve и DS
В чем разница между SADI-Sleeve и другими разновидностями билиопанкреатического шунтирования?
Билиопанкреатическое шунтирование Biliopancreatic Diversion (BPD) это одно из самых мощных хирургических вмешательств в современной бариатрической хирургии. Оно приводит к наиболее выраженному снижению избыточной массы тела и коррекции сопутствующих ожирению заболеваний, таких как сахарный диабет, гипертоническая болезнь и т.д.
Билиопанкреатическое шунтирование или Biliopancreatic Diversion (BPD) имеет несколько разновидностей. Самый ранний вариант операции был предложен Scopinaro, затем появился Duodenal Switch (DC), а затем наиболее безопасный современный вариант- Single Anastomosis Duodeno-Ileal bypass with Sleeve Gastrectomy (SADI-Sleev), по-русски — одноанастомозное дуадено-подвдошное шунтирование с продольной резекцией желудка.
Какова анатомия различных модификаций билиопанкреатического шунтирования и в чем преимущества SADI-SLEEVE над DS и БПШ?
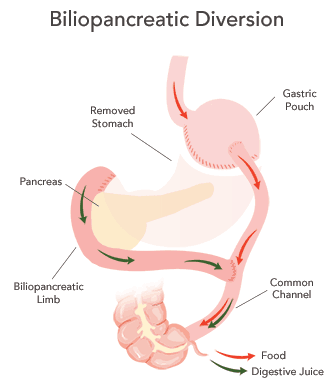
Билиопанкреатическое шунтирование в модификации Scopinaro наиболее часто называется собственно БПШ, Biliopancreatic Diversion (BPD). При этой операции выполняется формирование небольшого желудка, также как и при гастрошунтировании Gastric Bypass, но сформированный минижелудок получается несколько большего, по сравнению с Gastric Bypass, размера. Но зато формируется более длинный шунт тонкой кишки — выключается ее большая часть.
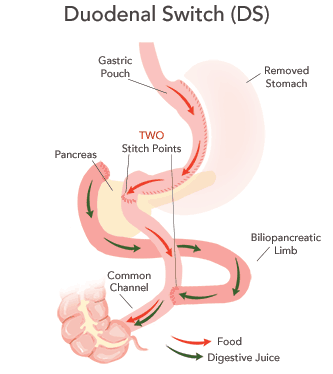
При формировании желудка используется поперечный шов. После этого дистальная (удаленная) часть тонкой кишки, которая называется подвздошная кишка, подшивается к желудку для отведения пищевых масс. Отключенная часть тонкой кишки вшивается в подвздошную ниже анастомоза (соединения) с желудком, по ней к пищевым массам поступает желчь и сок поджелудочной железы. В этой зоне тонкой кишки производится глюкогоноподобный пептид 1-го типа (ГПП-1). Именно ранняя выработка ГПП-1 способствует сведению к минимуму явлений сахарного диабета II типа, вплоть до полной ремиссии. Но при данном типе операции пища поступает из желудка в кишку бесконтрольно и смешивается с пищеварительными соками только в самом конце тонкой кишки. В связи с этими особенностями этот вариант БПШ имеет значительное количество осложнений, таких, как демпинг-синдром, мальабсорбция (недостаточность усвоения питательных элементов), диарея (учащение стула) и др. Это обусловлено совсем коротким участком тонкой кишки, участвующем в пищеварении и отсутствием функции пилоруса — выпускного клапана желудка. Именно пилорус контролирует дробное поступление пищи из желудка в тонкую кишку, но только по достижении необходимой степени переваривания пищи желудочным соком.
Позднее — в конце 90-х годов ученые узнали, что именно в той части желудка, которая удаляется при продольной резекции желудка, производится основное количество грелина — гормона, повышающего аппетит и способствующего развитию ожирения и сахарного диабета 2 типа. Второе принципиальное отличие DS от БПШ это то, что подвздошная кишка подшивается к урезанному желудку сразу после пилоруса. Благодаря этому сохраняется дробное поступление пищи в кишку и не возникает явлений демпинг-синдрома, присущих классическому БПШ и гастрошунтированию во всех модификациях (Gastric Bypass и Mini-Gastric Bypass). Третье отличие — общая петля подвздошной кишки, участвующая в пищеварении, формируется значительно больше, чем при классическом БПШ, что сводит к минимуму явления мальабсорбции (снижению всасывания питательных веществ). Явления учащенного стула также сводятся к минимуму. Таким образом, за счет использования SLEEVE, уменьшается порция пищи, за счет сохранения пилоруса сходят на нет явления демпинга, а за счет более длинной общей кишки, участвующей в пищеварении уменьшаются явления мальабсорбции. В итоге сводятся к минимуму почти все отрицательные явления билиопанкреотического шунтирования, но сохраняются все преимущества — максимальное снижение избыточной массы тела и снижение проявлений сахарного диабета 2 типа и других осложнений ожирения.
С самого начала использования этой операции хирурги имеют возможность, в случае необходимости, разбивать ее на два этапа — сначала выполнить продольную резекцию желудка (SLEEVE Gastrectomy), а затем, через несколько месяцев, вторым этапом выполнить шунтирование. Некоторые пациенты оставались вполне довольны результатом уже после первого этапа — рукавной гастропластики и не нуждались во втором этапе. Так появилась продольная резекция желудка, как самостоятельная бариатрическая операция. Остальным же выполняется шунтирование уже на сниженном весе, что намного безопасней.
SADI-SLEEVE (Single Anastomosis Duodeno-Ileal bypass with Sleeve Gastrectomy)
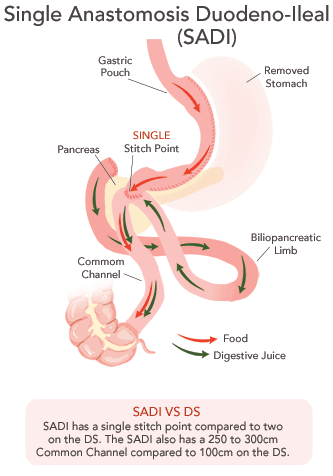
Самый последний шаг в совершенствовании билиопанкреатического шунтирования связан с развитием лапароскопических технологий. Дальнейшее развитие пошло по еще большему снижению риска процедуры для пациента. Все дело в том, что каждый новый анастомоз (место, где сшиваются кишка с желудком либо другой кишкой) потенциально несет риск развития несостоятельности — протечки места сшивания. В связи с этим снижение количества анастомозов значительно повышает безопасность оперативного вмешательства. Так появилось однооанастомзное дуаденально-подвздошное шунтирование с рукавной гастропластикой- самое безопасное и эффективное из современных бариатрических операций.
Операция очень похожа на Duodenal Switch (DS), но, в отличии от нее и от гастрошунтирования (Gastryc Bypass), имеет только один анастомоз. Желудок после рукавной резекции с сохранением пиларуса сразу вшивается в бок подвздошной кишки. Этот факт выгодно отличает вмешательство от всех двуханастомозных вмешательств (БПШ, DS, Gastric Bypass). А от другого одноанастомозного вмешательства мини-гастрошунтирования (mini-Gastryc Bypass) SADI-S отличается сохранением пилорического жома (пилоруса). К тому же важную роль играет удаление грелин-выделяющей зоны желудка.
В результате мы получаем следующие приемущества SADI-SLEEVE :
Восстановление после SADI-S
Снижение избыточной массы тела после SADI-S и DS, по сообщениям большинства исследователей, имеет наиболее высокие показатели по сравнению с бандажированием, изолированной гастропластикой, минигастропластикой, гастрошунтированием и т. д. Так же, по данным большинства крупных исследований, SADI-S и DS показывает наилучшие показатели в коррекции явлений сахарного диабета II типа. Так, исследование Buchwald, опубликованное в 2004 году показало, что после DS явления сахарного диабета II типа снижаются либо полностью уходят в 98% случаев. Снижение уровня холестерина и гипертонической болезни также находятся на самом высоком уровне из всех имеющихся вмешательств в бариатрии.
Между тем, нарушение всасывания жиров, вызванные операцией могут привести к послаблению стула (в среднем до 3-х раз в день). Нарушение всасывания железа, витаминов В12, кальция, железа, витаминов А, D, Е, К в результате могут способствовать развитию легких форм анемии в 10% случаев. Для снижения до минимума подобных явлений всем пациентам после SADI-S, DS, также как и после любых других бариатрических вмешательств рекомендован прием поливитаминов и минералов в таблетированных формах.
SADI-SLEEVE является наиболее мощной операцией по устранению явлений ожирения и сахарного диабета II типа. Выполнение шунтирования на фоне продольной резекции желудка (SLEEVE Gastrectomy) позволяет сочетать наиболее выраженные преимущества современной бариатрии с безопасностью вмешательства. Операция проводится лапароскопически, может быть выполнена либо одномоментно, либо в два этапа. Преимущество двухэтапного подхода в снижении риска процедур и в том, что многие пациенты оказываются удовлетворены первым этапом, и в итоге не нуждаются в шунтирующем компоненте. Однако, в случае необходимости, одноанастомозное дуадено-подвздошное шунтирование является безопасной процедурой — как второй этап операции SADI-S либо самостоятельное ревизионное вмешательство.
Острое расширение желудка (K31.0)
Версия: Справочник заболеваний MedElement
Общая информация
Краткое описание
Период протекания
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
Классификация
2. Вторичное острое расширение желудка:
— после различных хирургических вмешательств на органах брюшной и грудной полостей, позвоночнике, спинном мозге, молочной железе, конечностях;
— после травм, инфекционных заболеваний, интоксикаций;
— при наличии опухолей или рубцов в антральном отделе желудка, вызывающих его стенозирование.
Этиология и патогенез
Возможные причины острого расширения желудка:
— брюшная или тазовая операция;
— травма головы, позвоночника и живота;
— переедание;
— голод;
— сильные раздражения мочевых или желчных путей;
— гнойный панкреатит;
— механические препятствия в привратнике (артерио-мезентериальная непроходимость, рубцующаяся язва, опухоль);
— динамическая непроходимость кишечника;
— сосудистые кризы Паля;
— психические заболевания;
— некоторые инфекционные заболевания;
— роды;
— длительное и обильное употребление алкоголя.
Выявить причину острого расширения желудка возможно не всегда.
В настоящее время данная патология объясняется параличом нервно-мышечного аппарата стенки желудка, что обуславливает прогрессирующее растяжение желудка за счет скопления жидкого содержимого и газов. Такой подход подтверждается экспериментально, когда острое расширение желудка вызывают, воздействуя или на блуждающий нерв, или на интрамуральный нервный аппарат желудка.
У больных с данным заболеванием растянутый до предела атоничный желудок занимает почти всю брюшную полость и оттесняет вниз кишечные петли. Возникает натяжение брыжейки тонкой кишки вместе с проходящей в области ее корня верхней брыжеечной артерией. Двенадцатиперстная кишка (ДПК) пережимается между верхней брыжеечной артерией и аортой. В результате, к острому расширению желудка присоединяется так называемая «артериомезентериальная кишечная непроходимость»: содержимое ДПК (включая желчь и панкреатический сок) поступает только в желудок, еще больше растягивая его. Желудок, увеличенный из-за потери мышечного тонуса, занимает всю полость живота и переполнен собственным секретом, который не всасывается и не эвакуируется. Эвакуации секрета препятствует также уменьшение проходимости ДПК в месте пересечения ее мезентериальной артерией. У больных развиваются хлоропения, алкалоз, обезвоживание тканей.
Заболевания желудочно-кишечного тракта
Симптомы расстройства желудочно-кишечного тракта (ЖКТ) знакомы многим: тяжесть после еды, дискомфорт в животе, диарея, тошнота и проблемы со стулом.
Болезни ЖКТ могут привести к крайне неприятным последствиям, таким, как общее обезвоживание организма, влияющее на работу головного мозга, интоксикация всего организма или злокачественные новообразования пищеварительной системы. И, конечно, любое хроническое заболевание без должного лечения грозит болезнями других органов, ведь человеческий организм – сложная природная система, в которой все элементы связаны между собой.
Причины заболеваний желудочно-кишечного тракта
Причины заболеваний ЖКТ разнообразны. Все болезни органов пищеварения можно условно разделить на две группы: инфекционные и неинфекционные.
Возможны следующие причины инфекционных заболеваний ЖКТ 2 :
В отличие от инфекционных болезней ЖКТ, которые, как правило, начинаются остро и имеют выраженные признаки, неинфекционная группа характеризуется сглаженными симптомами (за исключением острой хирургической патологии).
Болезни могут быть хроническими, протекать с обострениями и ремиссиями. К развитию неинфекционных заболеваний ЖКТ могут привести: 2
Симптомы заболеваний желудочно-кишечного тракта
Признаки заболеваний ЖКТ зависят от вида заболевания и причины его возникновения. Одним из основных симптомов, который ярче всего сигнализирует о наличии болезней ЖКТ, является болевой синдром.
Место локализации боли может свидетельствовать о следующих проблемах 2 :
Большинство болезней ЖКТ не ограничивается только болью в животе. Человека также могут беспокоить 2 :
Диагностика заболеваний желудочно-кишечного тракта
Точная диагностика – основа будущего эффективного лечения болезней ЖКТ. Не зная точную причину неприятных симптомов, нельзя подобрать правильную программу лечения. Вовремя проведенная диагностика может предотвратить развитие серьезных заболеваний и осложнений.
Диагностика болезней ЖКТ может включать 2 :
Лечение заболеваний желудочно-кишечного тракта
Тактика лечения заболеваний ЖКТ определяется индивидуально и зависит от общего состояния человека, характера болезни и стадии развития. Чаще всего заболевания желудочно-кишечного тракта лечат консервативным способом, то есть без хирургического вмешательства.
В зависимости от природы заболевания – инфекционное или неинфекционное поражение – могут применяться следующие группы препаратов 2 :
Важным элементом лечения заболеваний ЖКТ является диета. При нарушениях в работе органов пищеварения очень важно придерживаться принципов здорового образа жизни (ЗОЖ).
Питание должно быть дробным, до 5-6 раз в день с небольшими перерывами. Необходимо полностью отказаться от ресторанов быстрого питания, жирной, жареной и острой пищи, газированных напитков – словом, всего, что может раздражать слизистые пищеварительных органов. Пища должны быть максимально щадящей. Основу рациона при болезнях ЖКТ должны составлять следующие блюда: 2
Следует свести к минимуму продукты, содержащие грубую клетчатку и провоцирующие излишнее газообразование: бобовые, капусту, редис, кукурузу. Исключены также консервы, соусы, специи и приправы.
Профилактика заболеваний желудочно-кишечного тракта
Предотвратить развитие заболеваний ЖКТ не так уж и сложно. Достаточно придерживаться простых принципов здорового образа жизни. Вот несколько правил, на которые стоит ориентироваться в профилактике заболеваний ЖКТ: 2
Препарат Креон® при заболеваниях желудочно-кишечного тракта
Таблетированные препараты представляют собой цельную форму, ее нельзя делить, поскольку это может нарушить защитную оболочку, и действующее вещество попросту погибнет в желудке.
Подробнее о препарате Креон ® 25 000 можно узнать здесь.
Клиническое наблюдение пациентки с гастропарезом и дисплазией соединительной ткани
Пациентка К., 25 лет обратилась с жалобами на чувство тяжести в эпигастрии после еды, раннее насыщение, отрыжку, которые беспокоили пациентку несколько раз в неделю, горечь во рту, тошноту, сердцебиения, аппетит сохранен, стул без патологических примесей.
Пациентка К., 25 лет обратилась с жалобами на чувство тяжести в эпигастрии после еды, раннее насыщение, отрыжку, которые беспокоили пациентку несколько раз в неделю, горечь во рту, тошноту, сердцебиения, аппетит сохранен, стул без патологических примесей.
Из анамнеза: считает себя больной около года. Из анамнеза жизни установлено, что около года назад была сильная психотравмирующая ситуация (смерть близкого человека). С этого момента отмечает эпизоды немотивированной тревоги, страхов. Не обследовалась.
При осмотре состояние удовлетворительное. Астеническое телосложение. Килевидная деформация грудной клетки. Сколиоз грудного отдела позвоночника. Долихостеномелия. Арахнодактилия. Трофологическая недостаточность 2-й степени (рост 176 см, масса тела 54 кг, ИМТ — 17,11 кг/м кв., толщина кожно-жировой складки — 6 мм, окружность мышц плеча — 14 см). Над легкими выслушивается везикулярное дыхание, хрипов нет. Границы сердца в пределах нормы. Тоны сердца несколько приглушены, ритмичные. Частота сердечных сокращений (ЧСС) 98 в минуту. Живот мягкий, при пальпации умеренно болезненный в мезогастральной области. Пальпируется спазмированная сигмовидная кишка, умеренно болезненная. Печень не увеличена. Край при пальпации мягкий, безболезненный. Симптомы Керра, Ортнера отрицательные.
При обследовании патологии в общем анализе крови, мочи не выявлено. Функциональные пробы печени без патологических изменений. Амилаза крови, мочи в норме. Копрограмма — без патологических изменений.
Исследование состояния вегетативной нервной системы: оценка ритмограммы и типа регуляции синусового ритма. Ритмограмма вариабельности сердечного ритма отражает преобладание симпатического влияния на модуляцию сердечного ритма. При проведении ортостатической пробы — реактивность парасимпатического отдела вегетативной нервной системы сниженная.
Фиброгастродуоденоскопия. Пищевод свободно проходим, просвет его и размеры обычные. Складки продольные. Слизистая бледно-розового цвета. Кардия ZET-линия дифференцируется. Желудок в форме длинного атоничного опущенного к гипогастрию крючка с избыточным количеством «грязного» цвета жидкости с примесью застойной желчи. Медленно расправляется воздухом. Стенки эластичные. Складки средние по высоте, с бледным рельефом, перистальтика едва определяется. Слизистая во всех отделах желудка гиперемирована. Пилорус не смыкается, зияет. Постоянный рефлюкс желчи. Уреазный тест на Helicobacter pylori — отрицательный. Двенадцатиперстная кишка: луковица полигональной формы, не смыкается. Просвет кишки овальной формы, широкий. Складки циркулярные, сглажены, обложены слизью и желчью. Слизистая в проксимальной части двенадцатиперстной кишки гиперемирована, в остальных отделах — бледно-розового цвета. Заключение: «Гастростаз. Гастроптоз. Дуоденогастральный рефлюкс».
Рентгенологическое исследование пищевода, желудка, двенадцатиперстной кишки. Акт глотания не затруднен. Пищевод свободно проходим, контуры ровные, четкие, стенки эластичные. Кардия проходима. Газовый пузырь желудка расположен у гребней подвздошной кости. Желудок в форме крючка, натощак содержит избыточное количество жидкости. Рельеф желудка представлен утолщенными, извитыми в средней трети тела желудка складками. При тугом заполнении перистальтика по обеим кривизнам сегментирующая. Эвакуация контрастной взвеси замедлена. Луковица двенадцатиперстной кишки овальной формы, контуры ее ровные, четкие. Отмечаются дуоденогастральные и дуоденобульбарные рефлюксы. Постбульбарные отделы двенадцатиперстной кишки не изменены. В горизонтальном положении с поворотом на левый бок отмечается рефлюкс бариевой взвеси в пищевод.
При ультразвуковом исследовании пищевода, желудка, двенадцатиперстной кишки натощак определяется неоднородное содержимое желудка с гиперэхогенными включениями. После наполнения желудка жидкостью в объеме 500 мл перистальтика почти отсутствует (единичные поверхностные перистальтические волны за весь период обследования). Визуализируется заброс содержимого из двенадцатиперстной кишки в желудок и регургитация по двенадцатиперстной кишке.
При ультразвуковом исследовании органов брюшной полости обнаружен с перегибами в теле желчный пузырь, в полости застойное содержимое, признаки нефроптоза 2-й степени справа.
Допплерография сосудов: воротная вена — диаметр 10 мм, объемная скорость кровотока 1695 мл/мин, через 30 минут после еды 2412 мл/мин. Верхняя брыжеечная вена — диаметр 6 мм, объемная скорость кровотока 674 мм/мин, после еды 824 мл/мин. Селезеночная артерия — диаметр 5,4 мм, систолическая скорость кровотока 93 см/с, диастолическая скорость кровотока 33 см/с, индекс резистентности 0,65, объемная скорость кровотока 792 мл/мин, после еды соответственно: систолическая — 114 см/с, диастолическая — 41 см/с, индекс резистентности — 0,64, объемная скорость кровотока 984 мл/мин. Общая печеночная артерия — диаметр 4,5 мм, систолическая скорость кровотока — 97 см/с, диастолическая скорость — 34 см/с, индекс резистентности — 0,65, объемная скорость кровотока 608 мл/мин, после еды соответственно: систолическая — 120 см/с, диастолическая — 41 см/с, индекс резистентности — 0,65, объемная скорость кровотока — 752 мл/мин. Верхняя брыжеечная артерия — диаметр 6 мм, систолическая скорость — 163 см/с, диастолическая — 18, индекс резистентности — 0,89, объемная скорость кровотока 954 мл/мин, после еды соответственно: систолическая скорость 233 см/с, диастолическая — 40 см/с, индекс резистентности — 0,83, объемная скорость кровотока — 1592 мл/мин. Заключение: после пищевой пробы не зарегистрировано снижения индекса резистентности в общей печеночной артерии, незначительное снижение (-0,01) в селезеночной артерии.
Ирригоскопия. Сигмовидная кишка удлинена, извита. Поперечно-ободочная провисает в гипогастральную область. Заключение: долихосигма, трансверзоптоз 2-й степени.
Пациентке выставлен диагноз: «Гастропарез, дуоденостаз средней степени тяжести, ассоциированный с дисплазией соединительной ткани. Дисфункция желчного пузыря по гипокинетическому типу. Тревожно-депрессивный синдром. Синдром вегетативной дисфункции: симпатикотония».
Пациентке назначена терапия, включающая как медикаментозные, так и немедикаментозные методы.
На фоне проведенной терапии отмечена положительная динамика: нормализовалась моторика желудка, психический статус пациентки, купировались проявления вегетативной дисфункции.
Комментарии. Гастропарез — нарушение моторики желудка, характеризующееся замедленным его опорожнением в отсутствии причин механической обструкции. Распространенность гастропареза в популяции около 4% [5]. Среди основных причин указываются: сахарный диабет, оперативные вмешательства, сопровождающиеся ваготомией [5]. Возможно развитие гастропареза на фоне болезни Паркинсона, гипотиреоза, коллагенозов (системной склеродермии), хронической почечной недостаточности, циррозов печени, кишечной псевдообструкции, следует исключить гастропарез как следствие медикаментозной терапии. На долю идиопатического гастропареза приходится около 36% случаев, диагноз ставят чаще женщинам молодого возраста [5].
В настоящее время доказано, что в основе развития гастропареза лежат расстройства двигательной функции желудка [3]. В норме моторная функция желудка определяется сложными механизмами и различается в разных отделах этого органа. Проксимальные отделы и дно желудка обладают тонической активностью, благодаря которой в желудке поддерживается постоянное давление. Дистальному отделу желудка свойственна перистальтическая активность (3 волны в 1 мин), ответственная за смешивание, измельчение и транспорт пищи через привратник в двенадцатиперстную кишку (ДПК). Привратник периодически закрывается и открывается, и перистальтическая желудочная волна способствует продвижению желудочного содержимого в луковицу ДПК благодаря градиенту давления. В норме давление в желудке выше, чем в ДПК. Желудочная перистальтическая волна запускает перистальтику ДПК (14–15 волн в 1 мин).
Эта так называемая антродуоденальная координация играет важную роль в опорожнении желудка. Моторные нарушения желудка могут проявляться в виде нарушений ритма перистальтики желудка (по типу тахигастрии, брадигастрии, смешанной дисритмии) или в виде ослабления моторики антрального отдела желудка с последующим расширением и гастропарезом, а также нарушений антродуоденальной координации (Римские критерии, III Консенсус, 2006 г.). По данным литературы замедление эвакуации из желудка и ослабление моторики антрального отдела нередко ассоциируется с нарушениями моторики двенадцатиперстной кишки: изменениями нормальной периодичности появления в двенадцатиперстной кишке межпищеварительного моторного комплекса с отсутствием III фазы или даже ее ретроградным распространением, появлением нерегулярных эпизодов тонических и фазовых сокращений. Указанные моторно-тонические расстройства лежат в основе появления симптомов диспепсии. Клинические проявления гастростаза: тошнота, рвота, вздутие живота, ранее насыщение, абдоминальная боль, похудание или увеличение массы тела.
Различают три степени тяжести гастростаза: легкая (симптомы легко купируются, трофологический статус поддерживается соблюдением обычной диеты или незначительными ограничениями; средняя (симптомы контролируются, трофологический статус поддерживается модификацией диеты и образа жизни, госпитализация требуется редко); тяжелая (рефрактерные симптомы, невозможность поддержания трофологического статуса при пероральном питании, частые госпитализации) [5, 6].
В механизме моторных расстройств пищеварительного тракта ведущая роль принадлежит следующим нарушениям [2–4]. Первое — изменения на уровне миоцита (нарушение чувствительности и структуры рецепторного аппарата или биоэлектрических свойств самой мышечной клетки), являющиеся морфологической основой органической патологии ЖКТ. Вторая причина моторных расстройств пищеварительного тракта — нарушения нервной регуляции, дисбаланс вегетативной нервной системы, нейромедиаторов, нейропептидов и гастроинтестинальных гормонов. Доказана роль в развитии гастропареза гормонов мотилина, грелина, гипергликемии. Причинами нарушений гастродуоденальной моторики (гастропареза) может быть развитие автономной нейропатии (при сахарном диабете), а также дисфункция вегетативной нервной системы (преимущественно ее симпатического отдела) на фоне нарушений психической сферы.
Именно психопатологические синдромы с нарушением вегетативной регуляции органов пищеварения, как правило, лежат в основе развития гастропареза у молодых женщин [5, 6]. Внешние психогенные факторы выполняют роль триггера. Симпатический и парасимпатический отделы нервной системы широко представлены в коре головного мозга и регулируются высшими центрами нервной деятельности. В зависимости от исходного вегетативного тонуса роль «первой скрипки» отдается одному из этих отделов. Симпатическая нервная система контролирует реакцию организма на воздействие физического и эмоционального стресса. При длительном воздействии внешнего агрессивного фактора симпатическая нервная система постоянно находится на определенном уровне активности и запускает процессы, связанные с расходом энергии. Если уровень активности симпатической нервной системы длительно остается высоким, ответная реакция парасимпатической нервной системы (реакция релаксации) не включается. Хроническая активизация симпатической нервной системы может стать причиной возникновения так называемой аллостатической нагрузки с последующим срывом регуляторных систем.
При дисплазии соединительной ткани синдром вегетативной дисфункции наблюдается по данным различных исследователей в 45–89% случаев [1]. Нарушения вегетативной регуляции при дисплазии соединительной ткани носят системный характер и проявляются метаболическими, секреторными, гемодинамическими и моторными расстройствами [1]. Среди пациентов с дисплазией соединительной ткани имеются лица как с преобладанием тонуса парасимпатического, так и с преобладанием тонуса симпатического отдела вегетативной нервной системы, однако преобладают пациенты с симпатикотонией [1]. Нарушения вегетативной регуляции при дисплазии соединительной ткани, как правило, протекают ассоциированно с психопатологическими расстройствами (неврастенией, тревожно-фобическими расстройствами).
Выраженность клинической симптоматики напрямую коррелирует с количеством фенотипических признаков «слабости» соединительной ткани со стороны других систем органов, выраженностью морфологических изменений соединительной ткани. При наличии этих расстройств увеличивается частота выявления и тяжесть синдрома вегетативной дистонии, а также частота обнаружения гиперсимпатикотонии. По мнению многих авторов, именно психопатологические расстройства у этих лиц являются первичными, а симптомы вегетативной дистонии — вторичные, возникающие в ответ на внешние психотравмирующие факторы.
Лечение. Важное значение имеют диетические рекомендации: пища должна усиливать гастродуоденальную моторику или, по крайней мере, не тормозить ее. Рекомендуется ограничение в рационе жиров, пищевых волокон, исключение углеводсодержащих напитков. Рекомендуется прием жидкости во время еды, после еды — ходить 1–2 часа, если указанные меры неэффективны, рекомендуется прием жидкой пищи.
Противорвотные средства: фенотиазины, 5-НТ 3-антагонисты (ондансетрон, гранисетрон), антигистаминные, трициклические антидепрессанты, канабиноиды, бензодиазепины, антагонисты нейрокининовых рецепторов, глюкокортикостероиды, имбирь, акупунктура.
Лечение вегетативной дисфункции чрезвычайно сложно, но важным элементом комплексной терапии у пациентов с гастропарезом являются:
Водные процедуры. Рекомендуются: плавание, циркулярный душ, сауна, лечебные ванны.
Физиотерапевтическое лечение (при назначении электропроцедур следует исключить противопоказания со стороны сердечно-сосудистой системы): импульсная магнитотерапия, диадинамические токи, синусоидальные модулированные токи.
Массаж по зонам позвоночника и шейно-воротниковой области.
Традиционно для стимуляции перистальтики желудка используются препараты, непосредственно или опосредованно усиливающие действие парасимпатической нервной системы: агонисты парасимпатических и дофаминовых рецепторов, агонисты 5-HT 4 и антагонисты 5-HT 3 рецепторов, препараты, взаимодействующие с k- и d-опиатными рецепторами [7–14]. Рецепторный аппарат мышечных клеток различных отделов пищеварительного тракта неоднороден, одни рецепторы равномерно распределены в ЖКТ от пищевода до ануса — серотониновые и опиатные, другие расположены локально, например, дофаминовые, которые сосредоточены в нижней части пищевода, желудке и проксимальных отделах двенадцатиперстной кишки [7, 8]. В силу указанных особенностей при лечении гастропареза используются лекарственные препараты, взаимодействующие с различными рецепторами и оказывающими стимулирующее действие на моторику желудка.
К препаратам с доказанным прокинетическим действием на верхний этаж ЖКТ относят метоклопрамид, домперидон и итоприд. Метоклопрамид по химической структуре близок к нейролептикам. Давно известно, что нейролептики уменьшают тошноту и рвоту, блокируя центральные дофаминовые (D2) рецепторы [10, 12, 14]. Механизм действия метоклопрамида основывается не только на блокаде центральных и периферических дофаминергических рецепторов, но и является стимулятором высвобождения ацетилхолина из постганглионарных нервных окончаний, обладает свойствами агониста 5-НТ 4 и антагониста 5-НТ 3 рецепторов. Препарат снижает двигательную активность пищевода, повышает тонус нижнего пищеводного сфинктера, улучшает эвакуацию из желудка за счет возрастания тонуса тела желудка и повышения фазовой активности антрального отдела желудка. Одновременно происходит расслабление верхних отделов тонкой кишки, предотвращается дуоденогастральный рефлекс и ускоряется транзит по тонкой кишке. Биодоступность препарата 30%. Выраженные побочные эффекты метоклопрамида ограничивают его широкое применение. Метоклопрамид проникает через гематоэнцефалический барьер и вызывает сонливость, заторможенность, галакторею, гиперпролактинемию, гинекомастию.
В качестве прокинетического средства может использоваться эритромицин [11, 14]. Препарат вызывает высокоамплитудные пропульсивные сокращения желудка, которые буквально сметают плотное содержимое, включая неперевариваемые вещества из желудка (подобный эффект наблюдается также у азитромицина). Эритромицин также стимулирует сократимость дна желудка или, по крайней мере, ингибирует аккомодационное растяжение проксимальной части желудка после приема пищи [7–9]. Наличие побочных эффектов эритромицина, включающих гастроинтестинальную токсичность, ототоксичность, псевдомембранозный колит и возникновение резистентных бактериальных штаммов, ограничивает его широкое применение. Разработка аналогов эритромицина, не обладающих антибиотическим эффектом, которая проводится в настоящее время, является многообещающей для лечения в будущем.
Домперидон — антагонисты допаминовых рецепторов обладают, аналогично метоклопрамиду и некоторым нейролептикам, прокинетическими эффектами. В отличие от метоклопрамида не проникает через гематоэнцефалический барьер и редко сопровождается экстрапирамидными побочными эффектами, свойственными метоклопрамиду. Препарат увеличивает продолжительность антральных и дуоденальных сокращений, ускоряет опорожнение желудка — выход твердых фракций у больных, у которых этот процесс был замедлен, повышает давление нижнего отдела пищевода, предотвращая гастроэзофагеальные рефлюксы. Биодоступность препарата 30%.
Прокинетиком с комбинированным механизмом действия является препарат итоприд. Препарат усиливает пропульсивную моторику желудка и ускоряет его опорожнение, оказывает противорвотный эффект, который реализуется благодаря взаимодействию с D2 хеморецепторами триггерной зоны. Итоприд является одновременно антагонистом дофаминовых рецепторов и блокатором ацетилхолинэстеразы. Препарат активирует освобождение ацетилхолина и препятствует его деградации. Биодоступность препарата составляет 60%. Препарат обладает минимальной способностью проникать через гематоэнцефалический барьер в центральную нервную систему, включая головной и спинной мозг. Терапия прокинетиками показана в стандартной дозе (10 мг) 3 раза в день на протяжении 2–3 месяцев.
Одним из новых перспективных прокинетиков является тримебутин (Тримедат). Его влияние на моторику ЖКТ, а также обезболивающее и противовоспалительное действие обусловлены неспецифическим действием этого препарата на все классы периферических опиатных рецепторов — µ, κ и δ. Тримедат оказывает стимулирующее действие при гипокинетических состояниях гладкой мускулатуры ЖКТ и спазмолитическое — при гиперкинетических. В экспериментальных и клинических исследованиях показано модулирующее влияние тримебутина на моторную функцию ЖКТ, которое проявляется в его нормализующих эффектах как при гипо-, так и при гиперкинетических нарушениях моторики на всех уровнях ЖКТ. Тримедат действует на всем протяжении ЖКТ, способствует опорожнению желудка и усилению перистальтики кишечника.
Тримебутин восстанавливает нормальную физиологическую активность мускулатуры кишечника при различных заболеваниях ЖКТ, связанных с нарушениями моторики. Установлено, что тримебутин может оказывать выраженное обезболивающее действие, способен устранять симптомы тяжести, вздутия, болей в животе, восстанавливать моторику кишечника как в случае диареи, так и при запорах. После приема внутрь Тримедат быстро всасывается из ЖКТ, максимальная концентрация в плазме крови достигается через 1–2 часа. Тримебутин не проникает через гематоэнцефалический барьер. Модулирующее влияние тримебутина на моторику ЖКТ и его обезболивающий эффект позволяют использовать препарат Тримедат при различных функциональных нарушениях ЖКТ как при терапевтической, так и при хирургической патологии. Препарат взрослым и детям с 12 лет назначается по 100–200 мг 3 раза в сутки, детям 3–5 лет — 25 мг 3 раза в день, 5–12 лет — 50 мг 3 раза в день, продолжительность лечения — до 3 месяцев.
УДХК представляет собой третичную желчную кислоту, особенностью строения которой является то, что гидроксильная группа атома С 7 находится в положении бета, которая определяет гидрофильность УДХК и отсутствие у нее токсических свойств. В желчи человека УДХК содержится в следовых количествах 0,5–1%. Однако при приеме per os происходит вытеснение пула токсичных гидрофобных желчных кислот в результате конкурентного захвата рецепторами в подвздошной кишке и стимуляция экзоцитоза в гепатоцитах путем активации Са-зависимой протеинкиназы А, что ведет к снижению концентрации гидрофобных желчных кислот в желчи, обусловливая холеретический эффект. Обоснованным является применение препаратов УДХК при замедлении моторики и кишечника. При наличии дуоденогастральных рефлюксов показана терапия препаратами УДХК (Урсосан, Урсофальк) в дозе 250 мг на ночь в течение 3 месяцев.
Заключение: в представленном клиническом наблюдении развитие гастростаза у нашей пациентки, по-видимому, связано с психической травмой, фоном послужило наличие дисплазии соединительной ткани с синдром вегетативной дисфункции (симпатикотония).
Синдром вегетативной дистонии проявлялся психовегетативными симптомами с эпизодами панических атак (вегетативных кризов) и висцеральной периферической полиневропатией с нарушениями сердечного ритма (тахикардией), похуданием, нарушением моторики желудка и двенадцатиперстной кишки. Исходный высокий тонус симпатического отдела вегетативной нервной системы был зарегистрирован по результатам кардиоинтервалографии при регистрации вариабельности сердечного ритма. Ультразвуковые допплеровские методы на основе регистрации индекса резистентности подтвердили нарушения вегетативной регуляции пищевапрительного тракта.
Несомненную роль в развитии гастропареза сыграло наличие у пациентки дисплазии соединительной ткани. Синдром вегетативной дистонии с высоким исходным тонусом симпатической нервной системы и гастроптоз, обусловленный дисплазией соединительной ткани, по-видимому, способствовали манифестации заболевания, являясь «благоприятным» фоном для нарушений моторики желудка и двенадцатиперстной кишки.
Комплексная терапия, направленная на восстановление моторики желудка, двенадцатиперстной кишки, вегетативного тонуса, в комплексе с психотерапевтическими методами лечения позволили купировать проявления вегетативной дистонии, нормализовать моторику желудка и двенадцатиперстной кишки.
Литература