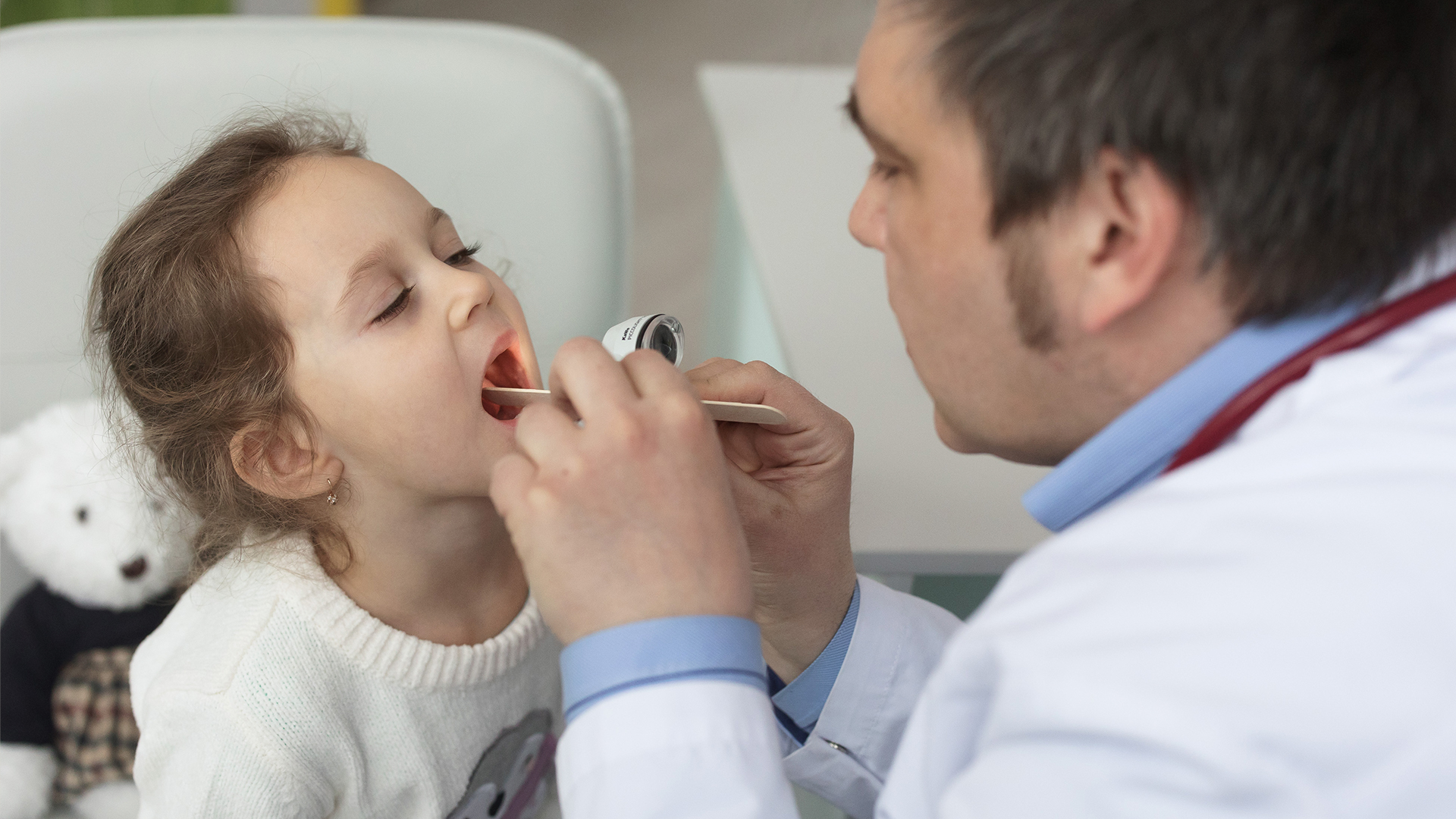
Для чего дают антибиотики новорожденному
Когда можно давать антибиотики детям
Естественно предположить, что подходы к антибактериальной терапии отдельных инфекций дыхательных путей должны различаться.
Принципы назначения антибиотиков
Антибактериальные препараты следует применять только при инфекциях, вызываемых бактериями. В стационаре при тяжелых и угрожающих жизни инфекционных заболеваниях (например, менингите — воспалении оболочек мозга, пневмонии — воспалении легких и др.) ответственность за правильность выбора лекарства целиком лежит на враче, который основывается на данных наблюдения за пациентом (клинической картине) и на результатах специальных исследований.
При легких инфекциях, протекающих в «домашних» (амбулаторных) условиях, ситуация принципиально иная. Врач осматривает ребенка и назначает лекарства, причем иногда это сопровождается объяснениями и ответами на вопросы, иногда — нет. Нередко родители сами просят врача назначить антибиотик. В таких ситуациях педиатру иногда психологически легче выписать рецепт, чем подвергать риску свою репутацию и тратить время на объяснение нецелесообразности такого назначения.
Грамотный подход к назначению лекарств
В любом случае врач должен следовать двум основным принципам антибактериальной терапии:
Надежных внешних признаков или простых и дешевых лабораторных методов, позволяющих различать вирусную и бактериальную природу инфекций дыхательных путей, к сожалению, нет. В то же время известно, что острый ринит (насморк) и острый бронхит (воспаление слизистой оболочки бронхов) практически всегда вызываются вирусами, а ангина (воспаление небных миндалин и глотки), острый отит (воспаление уха) и синусит (воспаление слизистой оболочки околоносовых пазух) в значительной части случаев — бактериями.
Естественно предположить, что подходы к антибактериальной терапии отдельных острых инфекций верхних дыхательных путей должны несколько различаться.
Насморк и бронхит
При остром рините (насморке) и бронхите антибактериальные препараты не показаны. На практике все происходит по-другому: один-два дня повышенной температуры и кашля у ребенка родители, как правило, не дают малышу антибактериальные препараты. Но затем они начинают опасаться, что бронхит осложнится пневмонией, и решают использовать антибиотики. Здесь стоит отметить, что такое осложнение возможно, однако оно практически не зависит от предшествовавшего приема антибактериальных препаратов. Основными признаками развития пневмонии служит ухудшение состояния (дальнейшее повышение температуры тела, усиление кашля, появление одышки). В такой ситуации надо немедленно вызвать врача, который решит, надо ли корректировать лечение.

Если же состояние не ухудшается, но и существенно не улучшается, то очевидной причины для назначения антибактериальных препаратов нет. Тем не менее, именно в этот период некоторые родители не выдерживают и начинают давать препараты детям «на всякий случай».
Особо следует отметить, что очень популярный критерий назначения антибактериальных препаратов при вирусных инфекциях — сохранение повышенной температуры в течение 3-х дней — ровным счетом ничем не обоснован. Естественная длительность лихорадочного периода при вирусных инфекциях дыхательных путей у детей значительно варьирует, возможны колебания от 3 до 7 дней, а иногда и больше. Более длительное сохранение так называемой субфебрильной температуры (37,0-37,5^(0)С) вовсе не обязательно связано с развитием бактериальных осложнений, а может быть следствием совершенно других причин. В таких ситуациях применение антибиотиков обречено на провал.
Типичным признаком вирусной инфекции является сохраняющийся кашель на фоне улучшения общего состояния и нормализации температуры тела. Необходимо помнить, что антибактериальные препараты не являются противокашлевыми средствами. У родителей в этой ситуации есть широкие возможности по применению народных противокашлевых средств. Кашель является естественным защитным механизмом, и исчезает последним из всех симптомов заболевания. Однако если у ребенка интенсивный кашель сохраняется 3-4 и более недель, надо искать его причину.
При остром отите тактика антибактериальной терапии иная, поскольку вероятность бактериальной природы этого заболевания достигает 40-60%. Учитывая это, до недавнего времени антибактериальные препараты назначались всем заболевшим.

Как показывает практика, для острого отита характерны интенсивные боли в первые 24-48 ч, затем у большинства детей состояние значительно улучшается и заболевание проходит самостоятельно. Спустя 48 часов симптомы сохраняются лишь у трети маленьких пациентов. Существуют интересные расчеты, показывающие, что если антибактериальные препараты назначать всем детям с острым отитом, то некоторую помощь (сокращение лихорадочного периода и длительности болей) они могут оказать только тем пациентам, у которых не должно было произойти самостоятельного быстрого выздоровления. Таким может быть лишь 1 ребенок из 20.
Что же будет с остальными 19-ю детьми? При приеме современных препаратов группы пенициллинов, таких, как амоксициллин или аугментин, ничего особо страшного не произойдет. У 2-3 детей может развиться понос или появятся кожные высыпания, которые быстро исчезнут после отмены препаратов, но выздоровление не ускорится. Как и в случае с бронхитом, назначение антибактериальных препаратов при отите не предотвращает развития гнойных осложнений. Осложненные формы отита с одинаковой частотой развиваются как у детей, получавших, так и у не получавших антибактериальные препараты.
Современный подход к лечению отита
К настоящему времени выработана новая тактика назначения антибактериальных препаратов при остром отите. Антибактериальные препараты целесообразно назначать всем детям в возрасте до 6 месяцев даже при сомнительном диагнозе острого отита (выяснить, что у маленького ребенка болит именно ухо, не так просто).
В возрасте от 6 месяцев до 2-х лет при сомнительном диагнозе (или легком течении) острого среднего отита назначение антибиотиков можно отложить, ограничившись наблюдением за ребенком — так называемая выжидательная тактика. Естественно, во время наблюдения детям необходимо давать обезболивающие препараты и, по необходимости, жаропонижающие. Если в течение 24-48 ч его состояние не улучшится, то необходимо начать антибактериальную терапию.
Конечно, в этом случае к родителям предъявляются повышенные требования. Прежде всего, необходимо обсудить с врачом, когда давать антибиотики, и уточнить, на какие признаки заболевания следует обращать внимание. Главное, уметь объективно оценить динамику боли, ее усиление или уменьшение, и вовремя заметить появление новых признаков болезни — кашля, сыпи и др. У родителей должна быть возможность связаться с врачом по телефону, а также иметься в наличии выписанный рецепт на антибиотик.
У детей старше 2 лет выжидание и наблюдение в течение 48 часов является самой предпочтительной тактикой, за исключением случаев тяжелого течения (температура выше 39^(0)С, интенсивные боли) болезни.
Воспаление легких
При диагнозе пневмония или серьезных подозрениях на эту патологию тактика антибактериальной терапии отличается от двух предыдущих случаев.
Для отдельных возрастных групп детей характерны некоторые особенности преобладающих возбудителей болезни. Так, в возрасте до 5-6 лет, по данным некоторых исследователей, до 50% случаев пневмонии могут вызываться вирусами. В более старшем возрасте вероятность вирусной природы пневмонии существенно снижается и возрастает роль бактерий (пневмококков) в развитии воспаления легких. Тем не менее, во всех возрастных группах частым возбудителем данного заболевания является пневмококк, который обуславливает тяжелое течение заболевания. Именно поэтому пневмония является безусловным показанием для назначения антибактериальной терапии.
Антибиотики детям не игрушка
Неконтролируемое и повсеместное применение антибиотиков на всяческий кашель или сопли, оказывается, может привести к неожиданным последствиям.
На вопросы об антибиотиках отвечает педиатр, главный врач детской клиники «Основа Дети» Данил Сергеевич Симановский.
Диагноза простуда не существует. Под простудой обычно подразумевают наличие соплей, кашля, красного горла или болей в горле — то, что врачи называют катаральные явления. И все эти явления могут вызываться вирусными инфекциями, а могут бактериальными. В зависимости от этиологии инфекции (от того, что вызвало эту инфекцию), антибиотики используются или нет.
Даже если сопли, кашель и красное горло достаточно сильные и приносят дискомфорт, но инфекция вызвана вирусом, то антибиотики не назначаются по причине их бесполезности, потому что вирусы не чувствительны к антибиотикам. Антибиотики были придуманы и используются только против бактерий. Поэтому, если ребенок болеет долго и тяжело, и у вас возникают сомнения: а обычная ли это простуда, необходимо обратиться к врачу. Врач осмотрит ребенка, определит этиологию инфекции, иногда для этого нужны дополнительные исследования: анализы крови, мазки. Только после этого назначит антибиотики при необходимости.
По цвету соплей определить этиологию инфекции невозможно. И все-все знают, что зеленые сопли — это страшно, а белые сопли — нет. Это не так, потому что слизь, которая выделяется в носоглотке, может приобретать цвет в зависимости от дополнительных свойств бактерий. Чаще всего зеленый цвет сопли приобретает от зеленящего стафилококка, который является нормальной флорой носоглотки. Помните, цвет соплей самостоятельной ценности не имеет.
Микрофлора толстой кишки очень мобильна, поэтому человеку без заболеваний ЖКТ, который получает лечение антибактериальным препаратом по правильным показаниям, назначение пробиотиков, эубиотиков не является обязательной необходимостью. Но врач всегда смотрит на ребенка, дополнительные риски, возраст и так далее. Как правило, при приеме антибиотиков мы наблюдаем не дисбактериоз, а диарею, которая является побочным действием антибиотиков и проходит, как только мы заканчиваем эту терапию. Например, самый распространенный в амбулаторной практике пенициллиновый антибиотик — амоксициллин, который чаще всего используется при лечении отитов, бронхитов, тонзиллитов. В его состав входит клавулановая кислота, у которой естественное побочное действие — диарея, т. е. жидкий стул. Если возникло такое побочное явление от антибактериального препарата, достаточно принимать энтеросорбент, только не одновременно с антибиотиками. Все на усмотрение доктора.
Конечно, может, и мы очень этого боимся. Поэтому научное и врачебное сообщества борются с полипрагмазией — назначением слишком большого количества лекарств, неадекватного по отношению к заболеванию. Также очень важно бороться с самостоятельным назначением антибиотиков родителями. Поэтому не надо ориентироваться ни на цвет, ни на запах соплей, ни на что-то еще. Надо ориентироваться на рекомендации врача. Если рекомендации вам показались необоснованными, нужно обращаться за вторым мнением. freepik.com
Полирезистентность — это не устойчивость самого организма ребенка к антибиотику, а резистентность микроорганизмов, которые содержатся в организме. На слизистой одномоментно присутствует колоссальное количество вирусов и бактерий, и это нормально. Некоторые из них патогенные, некоторые условно патогенные, некоторые сапрофиты, т. е. нормальная флора. Например, большое количество кожных проблем возникает от регулярного использования антибактериальных средств. Не только потому, что они сушат кожу, а потому, что нарушают нормальный биоценоз кожного покрова. То же самое происходит, когда постоянно используется антибактериальная зубная паста или антибактериальные гели для интимной гигиены. Наше бытовое поведение уже повышает вероятность, что микроорганизмы, которые живут на слизистых и на коже, выработают резистентность к этим антибактериальным средствам. И когда нам понадобится вылечить какую-то инфекцию, может возникнуть ситуация, что выбранный препарат не сработает. В этом случае придется выбирать другие антибиотики с более широким спектром действия, чтобы все-таки победить эту инфекцию. Именно с этим связана необходимость назначать правильную дозу. Не давать антибиотик на всякий случай пару дней. Потому что, когда доза антибиотика слишком маленькая, происходит выработка резистентности: враждебные микроорганизмы не побеждены до конца: часть погибает, но выжившие бактерии этому антибиотик уже будут устойчивы. Длительность антибактериальной терапии важный фактор. Если она не соблюдена, повышается вероятность формирования резистентности к антибиотикам.
Вопрос о другом: эффективность антибактериальной терапии оценивается по итогам 48-72 часов от начала перорального приёма антибиотика. Считать эти часы нужно с момента первого приёма. Это не означает, что через 2-3 дня наступает выздоровление, но должно быть улучшение как самочувствия, так и симптомов заболевания, которые оценивает врач при осмотре. Есть болезни, которые с точки зрения родителей, неадекватно долго лечатся, например, ангина. Курс лечения антибиотиками — 10 дней. Ребенку уже на четвертый день становится хорошо, у него нет никаких жалоб, а врач настаивает на продолжении приема «вредного ужасного антибиотика, который все убивает». Это необходимо для того, чтобы бактерии не выработали устойчивость, а погибли от антибиотиков. Когда на прием приходят дети, которым родители самостоятельно назначили на обычную ОРВИ антибиотик, врачи выбирают минимальный курс приема лекарства. Если мы отменим их на второй-третий день, мы рискуем спровоцировать резистентность оставшихся микроорганизмов. И в следующий раз нам придется использовать антибиотик тяжелее, шире и вреднее для ребенка.
Если дети болеют одной инфекцией, то скорее всего им поможет один и тот же антибиотик. Но, как минимум, надо правильно определить дозировку этого антибиотика, возможно, вашему ребенку нужна индивидуально подобранная дозировка. И у нас, врачей, есть возможность отойти немножко от дозировок, которые написаны в аннотации лекарственных средств. Потому что у врача, в отличие от мамы, есть еще регламент в виде клинических рекомендаций по лечению. Дозировка антибиотика будет разной и для лечений разных заболеваний, поэтому даже несмотря на то, что у вас несколько детей болели друг за другом стереотипно, вам все равно придется проконсультироваться врачом.
Зачем ждать этого, когда можно сразу принять антибиотики? Во-первых, абсолютно научно доказано, что прием антибиотиков на фоне вирусной инфекции не снижает вероятность развития осложнений. Если с первого дня вирусной инфекции вы начинаете давать ребенку антибиотик, то вероятность, что эта вирусная инфекция будет протекать с осложнениями, не уменьшается. Во-вторых, нет такой закономерности, что вы начинаете болеть вирусом и продолжаете болеть бактерией. Более густые зеленые сопли, которые появляются на 4-6 день течения ОРВИ не означают, что произошло какое-то гипотетическое присоединение бактериальной инфекции. Нет, это означает, что сопли дольше находятся в носоглотке и приобретают цвет превалирующей там микрофлоры.
Особенности антибактериальной терапии у недоношенных новорожденных
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
Научный центр здоровья детей РАМН, Москва
И нфекционно-воспалительные заболевания – наиболее частая патология у детей периода новорожденности, что объясняется своеобразием защитных механизмов на данном этапе онтогенеза. Наиболее выражена недостаточность гуморального и клеточного иммунитета, незрелость барьерных функций кожи и слизистых у детей, родившихся преждевременно. В структуре диагнозов в отделениях второго этапа выхаживания недоношеных детей удельный вес гнойно-воспалительных заболеваний приближается к 80%, при этом большинство заболеваний составляют так называемые малые инфекции – гнойничковые сыпи, омфалит, дакриоцистит, отит; у 1% детей выявляются серьезные воспалительные заболевания (флегмона и пузырчатка новорожденных, остеомиелит, менингоэнцефалит, пневмония, сепсис).
В последние годы проблемы инфекционной патологии у незрелых детей приобрели особую актуальность в связи с изменением особенностей как макро-, так и микроорганизмов, что отразилось на течении инфекционного процесса. Утяжелилось течение фоновых состояний, создающих благоприятную почву для манифестации и прогрессирования инфекции – это перинатальные поражения мозга, врожденные пороки развития, пневмопатии; причем достижения современной реаниматологии и интенсивной терапии позволяют обеспечить выживание даже детей с крайне малой массой тела, перенесших тяжелую асфиксию. В свою очередь реанимационные мероприятия, прежде всего длительная ИВЛ и катетеризация магистральных сосудов, создают условия для микробной агрессии. Одним из важных факторов, способствующих бактериальной контаминации и утяжелению течения бактериальных инфекций, является наличие смешанной вирусно-бактериальной внутриутробной инфекции. Внутриутробные паразитарные и вирусные инфекции (так называемый TORCH-синдром) в 13–45% случаев являются основной причиной смертности в периоде новорожденности. Перенесенная внутриутробно специфическая инфекция резко нарушает защитные механизмы ребенка, что способствует присоединению и бурному течению интранатальных и постнатальных бактериальных инфекций.
Современная этиология возбудителей
В этиологической структуре возбудителей бактериальных инфекций у недоношенных детей 10–15 лет назад отмечалось увеличение удельного веса грамотрицательной флоры (клебсиела, протей, псевдомонас). Однако в последующие годы вновь среди этиологических агентов локальных гнойно-воспалительных поражений первое место занимает грамположительная флора (стафилококки, стрептококки). Для недоношенных детей характерны сочетание микроорганизмов, выделяемых из различных очагов (например, из гнойного очага высеваются золотистый и эпидермальный стафилококки, из кала – кишечная палочка и стафилококки), а также смена ведущих возбудителей в процессе лечения (первоначальные агенты воспаления подавляются, их место занимают другие бактерии, часто в сочетании с грибами).
Среди населения циркулируют преимущественно чувствительные к антибиотикам штаммы возбудителей (В.К.Таточенко), а в стационарах дети обсеменяются преимущественно устойчивыми штаммами (внутрибольничная флора), так как условно-патогенные и сапрофитные микроорганизмы многократно пассируются на ослабленных незрелых новорожденных и происходит их селекция под воздействием терапии (Г.В.Яцык, И.В.Маркова). Кроме того, устойчивые штаммы (клебсиеллы, стрептококк В) передаются новорожденным от больных матерей.
Специфика фармакокинетики антибиотиков
У новорожденных детей фармакокинетика любого препарата существенно отличается от таковой у детей более старшего возраста; в наибольшей мере это относится к незрелым (недоношенным) новорожденным. Крайне важной представляется незрелость выделительной функции почек и ферментных систем печени – эти особенности в первую очередь характерны для глубоконедоношенных детей с массой тела менее 1500 г. Помимо этого, незрелость других органов и систем (желудочно-кишечного тракта, нервной системы, органов дыхания), а также общая лабильность метаболизма накладывают на фармакокинетику антибиотиков у недоношенных детей индивидуальные особенности предопределяя высокий риск нежелательных побочных эффектов антибактериальной терапии. Общая особенность фармакокинетики любых препаратов у недоношенных детей – это ее замедление, что способствует кумуляции лекарств и влияет на выбор дозы (уменьшение ее на 1/3–1/4), путей и кратности введения препаратов. В то же время повышенная проницаемость естественных барьеров (кожи и слизистых) способствует всасыванию многих медикаментов. В настоящее время проводятся исследования суточных ритмов фармакодинамики различных препаратов, но в отношении антибиотиков у недоношенных детей таких исследований практически нет.
Показания и выбор антибиотика
Безусловным показанием для назначения антибиотикотерапии недоношенному новорожденному является наличие у него любого инфекционно-воспалительного процесса, включая так называемые малые инфекции, например, нераспространенные гнойничковые поражения кожи, гнойные конъюнктивиты, отиты (в том числе катаральный отит). Лишь в редких случаях легкого течения неосложненной ОРВИ (ринофарингит) антибиотик не назначается – и то только у детей с относительно благополучным фоном (незначительная степень недоношенности, отстутствие анамнестических указаний на внутриутробную инфекцию, нетяжелая перинатальная энцефалопатия).
Безусловным показанием для назначения антибиотикотерапии недоношенному новорожденному является наличие у него любого инфекционно-воспалительного процесса, включая так называемые малые инфекции, например, нераспространенные гнойничковые поражения кожи, гнойные конъюнктивиты, отиты (в том числе катаральный отит). Лишь в редких случаях легкого течения неосложненной ОРВИ (ринофарингит) антибиотик не назначается – и то только у детей с относительно благополучным фоном (незначительная степень недоношенности, отстутствие анамнестических указаний на внутриутробную инфекцию, нетяжелая перинатальная энцефалопатия).
Спорный вопрос о так называемом профилактическом применении антибиотиков у маловесных недоношенных из группы риска по реализации внутриутробной и интранатальной инфекции (больная мать, длительный безводный период и т.п.), как правило, решается в пользу назначения антибиотика, так же как и в случаях так называемых неинфекционных пневмопатий. К условно “профилактическим” можно отнести также назначение антибиотика для “прикрытия” гормональной кортикостероидной терапии и некоторых вмешательств (катетеризации, переливания крови и т.п.).
Выбор антибиотика для недоношенного ребенка – ответственный момент, во многом определяющий эффективность лечения. При выборе препарата следует учитывать следующие факторы:
• вид возбудителя (в начале лечения часто лишь предполагаемый) и его штамм;
• чувствительность возбудителя (также в начале лечения – предполагаемую, через 2–3 дня после получения результатов бактериологических анализов в терапию могут быть внесены коррективы). В последние годы высказывается мнение о том, что параметры чувствительности микробов in vitro не всегда совпадают с таковыми in vivo и нет необходимости строго следовать им при назначении препаратов;
• локализация и степень тяжести инфекционного процесса (при нетяжелых локальных поражениях возможно пероральное применение препарата; при тяжелых, как правило, – сочетание пероральных и парентеральных средств);
• сопутствующие состояния и премобидный фон (предпочтение парентеральных препаратов при тяжелом дисбактериозе или внутривенного введения у крайне маловесных детей с неразвитой мышечной тканью).
Все антибиотики можно условно разделить на 2 группы – препараты первого выбора назначают, когда нет оснований думать о лекарственной устойчивости флоры (полусинтетические пенициллины, аминогликозиды I поколения, цефалоспорины I поколения); препараты второго выбора направлены на преодоление устойчивых штаммов (аминогликозиды и цефалоспорины III–IV поколения, современные макролиды). Существуют и препараты третьего выбора (или препараты резерва), применяемые при крайне тяжелых формах заболеваний с полирезистентной флорой (карбапенемы).
У недоношенных детей в основном сразу используются препараты второго выбора: применение антибиотиков первого ряда у них неэффективно и лишь способствует отсрочке манифестных проявлений инфекционного процесса, маскирует клинические симптомы. У детей периода новорожденности даже по жизненным показаниям не должны использоваться препараты, обладающие высокой токсичностью (фторхинолоны).
Схема 1. Допустимые сочетания антибиотиков у недоношенных детей при одновременном применении (Г.В. Яцык)
Особенности дозировки антибиотиков
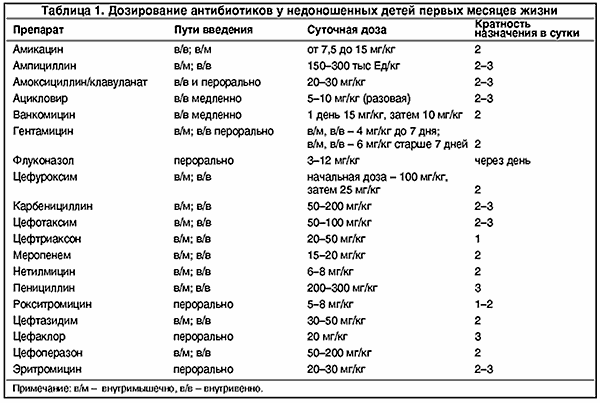
Дозировки используемых в неонатологии антибиотиков для недоношенных детей и кратность их введения представлены в табл. 1 (Г.В. Яцык, 1998 г.) Общий принцип подбора дозы для новорожденного ребенка – большее по сравнению со старшими детьми количество препарата на 1 кг массы тела – сохраняется и у недоношенных детей. Это обусловлено большим процентным содержанием воды в организме новорожденного и большей относительной поверхностью тела.
Дозировки используемых в неонатологии антибиотиков для недоношенных детей и кратность их введения представлены в табл. 1 (Г.В. Яцык, 1998 г.) Общий принцип подбора дозы для новорожденного ребенка – – сохраняется и у недоношенных детей. Это обусловлено большим процентным содержанием воды в организме новорожденного и большей относительной поверхностью тела.
Комбинированная антибактериальная терапия у недоношенных детей должна проводиться с большой осторожностью; одновременное сочетание 2 (очень редко – 3) антибиотиков применяется лишь у детей с тяжелыми гнойно-воспалительными процессами (прежде всего при сепсисе), вызванными смешанной флорой. Допустимые сочетания антибиотиков представлены в табл. 2 и на схеме 1 (данные Н.В. Белобородовой).
Пути и кратность введения антибиотиков недоношенному ребенку
В связи с высокой проницаемостью и ранимостью слизистой желудочно-кишечного тракта у незрелых новорожденных, а также опасностью развития дисбиоза и язвенно-некротического энтероколита пероральные антибиотики использовались ограниченно. К тому же большинство инфекционных заболеваний у недоношенных детей по тяжести состояния требует более мощной терапии. В последние годы появились достаточно действенные антибактериальные и противогрибковые препараты для перорального применения (макролиды, амоксициллин/клавуланат и др.) Кроме того, установлено крайне негативное воздействие болевых раздражений на грудных детей, что делает необходимым ограничение внутримышечных и внутривенных инъекций.
У новорожденных (особенно недоношенных) детей период полувыведения препаратов увеличен вследствие незрелости почек и печени. Поэтому кратность введения большинства препаратов не превышает у них 2 раз в течение суток (за исключением пенициллинов); особенно популярными в неонатологии остаются препараты пролонгированного действия (рокситромицин, цефтриаксон), допускающие однократное применение. Некоторые исследователи (Н.В. Белобородова, О.Б. Ладодо) большинство парентеральных препаратов (в том числе аминогликозиды, цефалоспорины) предлагают вводить однократно – внутривенно или внутримышечно.
Продолжительность антибактериальной терапии и последовательность применяемых антибиотиков у недоношенного ребенка определяются индивидуально, они зависят от эффективности первичного курса антибактериальной терапии, которая оценивается по традиционным клиническим и лабораторным параметрам. Как правило, недоношенным детям со среднетяжелыми инфекционными процессами (омфалит, пневмония, отит и т.д.) проводят два последовательных курса антибиотика (второй курс с учетом чувствительности микрофлоры), каждый по 7–10 дней. При тяжелых заболеваниях (менингит, остеомиелит, сепсис) обычно используют не менее 3–4 курсов антибиотиков (или 2–3 курса; при первом – сочетание антибиотиков, обычно аминогликозида и цефалоспорина III–IV поколения).
Побочные явления и их профилактика
Наиболее распространенные у недоношенных новорожденных нежелательные побочные эффекты антибактериальной терапии обусловлены подавлением симбионтной микрофлоры и, как следствие, колонизацией организма условно-патогенными сапрофитами. В связи с этим даже после короткого курса антибактериальной терапии у недоношенных детей возможно развитие дисбиозов – кандидоза кожи и слизистых, кишечного дисбактериоза. Реже у недоношенных отмечаются токсические (по типу идиосинкразии) и аллергические реакции на антибиотики.
Профилактика осложнений антибактериальной терапии начинается уже с ее правильного подбора, тщательного индивидуального контроля. Одновременно с назначением антибиотиков ребенку необходимо назначать противогрибковые средства (леворин, флуконазол, амфотерицин В) и средства, восстанавливающие микрофлору кишечника (бифидум-бактерин и др.); причем использование последних продолжается не менее недели после окончания курса антибиотиков.
С целью снижения нагрузки антибиотиками на незрелый организм недоношенного ребенка в последние годы делаются попытки сочетания антибактериальной терапии со средствами, усиливающими неспецифическую защиту: иммуноглобулинами, лазеротерапией (использование низкоинтенсивного лазерного излучения на магистральные сосуды с целью иммуностимуляции), метаболитной коррекцией.