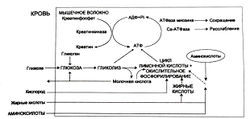
Для чего используется атф при сокращении мышц
АТФ мышц
Дано определение АТФ, описана история открытия АТФ, содержание АТФ в мышечных волокнах, приведена структура АТФ, описаны реакции гидролиза и ресинтеза АТФ в мышечных волокнах
АТФ мышц
Что такое АТФ?
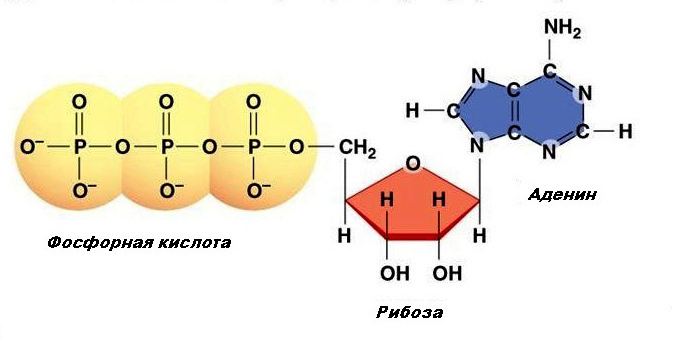
АТФ (аденозинтрифосфат, аденозинтрифосфорная кислота) – основное макроэргическое соединение организма[1]. Состоит из аденина (азотистого основания), рибозы (углевод) и трех последовательно расположенных фосфатных остатков, причем второй и третий фосфатные остатки присоединяются макроэргической связью. Структура АТФ выглядит следующим образом (рис.1).
Рис. 1. Структура АТФ
История открытия АТФ
АТФ был открыт(а) в 1929 году немецким биохимиком Карлом Ломаном (Karl Lohmann) и, независимо Сайрусом Фиске (Cyrus Fiske) и Йеллапрагада Субба Рао (Yellapragada Subba Rao) из Гарвардской медицинской школы. Однако структура АТФ была установлена только спустя несколько лет. Владимир Александрович Энгельгардт в 1935 году показал, что для сокращения мышц необходимо присутствие АТФ. В 1939 году В. А. Энгельгардт совместно со своей женой М. Н. Любимовой предъявили доказательства, что миозин проявляет ферментную активность при этом расщепляется АТФ и высвобождается энергия. Фриц Альберт Липманн (Fritz Albert Lipmann) в 1941 году показал, что АТФ является основным переносчиком энергии в клетке. Ему принадлежит фраза «богатые энергией фосфатные связи». В 1948 году Александр Тодд (Alexander Todd) (Великобритания) синтезировал АТФ. В 1997 году Пол Д. Бойер (Paul D. Boyer) и Джон Э. Уокер (John E. Walker) получили Нобелевскую премию по химии за разъяснение ферментативного механизма, лежащего в основе синтеза АТФ.
Содержание АТФ в мышечных волокнах
Количество АТФ в тканях организма человека относительно невелико, поскольку он (она) в тканях не запасается. В мышечных волокнах содержится 5 ммоль на кг сырой ткани или 25 ммоль на кг сухой мышечной ткани.
Гидролиз АТФ
Непосредственным источником энергии при мышечной деятельности является АТФ, который (ая) находится в саркоплазме мышечных волокон. Освобождение энергии происходит в результате реакции гидролиза АТФ.
Гидролиз АТФ – реакция, протекающая в мышечных волокнах, при которой АТФ, взаимодействуя с водой распадается на АДФ и фосфорную кислоту (Н3РО4). При этом выделяется энергия. Гидролиз АТФ ускоряется ферментом АТФ-азой. Этот фермент находится на каждой миозиновой головке толстого филамента.
Реакция гидролиза АТФ имеет следующий вид:
В результате гидролиза 1 моль АТФ выделяется энергия, равная 42-50 кДж (10-12 ккал). Скорость протекания реакции гидролиза повышают ионы кальция. Следует отметить, что АДФ (аденозиндифосфат) в мышечных волокнах выполняет роль универсального акцептора (приёмника) высокоэнергетического фосфата и используется для образования АТФ.
Фосфорная кислота (Н3РО4) в саркоплазме мышечных волокон достаточно быстро диссоциирует на ионы водорода и остаток фосфорной кислоты. В настоящее время доказано, что именно реакция гидролиза АТФ приводит к ацидозу, то есть закислению мышцы, а не гликолиз АТФ, в результате которого образуется молочная кислота (или более точно — лактат).
Фермент АТФ-аза
Фермент АТФ-аза расположен на миозиновых головках, что играет существенную роль в сокращении мышечных волокон. Активность фермента АТФ-азы лежит в основе классификации мышечных волокон на медленные (I тип), промежуточные (IIA тип) и быстрые (IIB тип).
Химическая энергия, выделяемая в результате гидролиза в мышечных волокнах, расходуется на: сокращение мышечных волокон (взаимодействие белков актина и миозина) и на их расслабление (работу кальциевого и натрий-калиевого насосов). При взаимодействии с актином одна молекула миозина за одну секунду гидролизует 10 молекул АТФ.
Запасы АТФ в мышечных волокнах невелики и могут обеспечить выполнение интенсивной работы в течение 1-2 с. Дальнейшая мышечная деятельность осуществляется благодаря быстрому восстановлению (ресинтезу) АТФ, поэтому при сокращении мышечных волокон в них одновременно протекают два процесса: гидролиз АТФ, дающий необходимую энергию и ресинтез АТФ, восполняющий запасы АТФ в мышечных волокнах.
Ресинтез АТФ
Ресинтез АТФ – синтез АТФ в мышечных волокнах из различных энергетических субстратов во время физической работы. Его формула выглядит следующим образом:
Ресинтез АТФ может осуществляться двумя путями:
Если в саркоплазме мышечных волокон недостаточно АТФ, то затрудняется процесс их расслабления. Возникают судороги.
Литература
[1] Макроэргические соединения – химические соединения, содержащие связи, при гидролизе которых происходит освобождение значительного количества энергии.
Роль АТФ в механизмах мышечного сокращения
В процессе взаимодействия миозиновых и актиновых нитей в присутствии Са²⁺ важную роль играет богатое энергией соединение — АТФ. Впервые В. А. Энгельгард и М. Н. Любимова в 1939 г. нашли, что мышечный белок — миозин — обладает свойствами фермента аденозинтрифосфатазы (АТФ-аза). Эти авторы также обнаружили, что под влиянием АТФ изменяются и механические свойства миозина — резко увеличивается растяжимость его нитей. В последующие годы был открыт белок актин и показано, что он активирует АТФ-азную активность миозина.
В настоящее время взаимодействие АТФ с сократительными белками и ионами Са²⁺ представляют следующим образом. В покоящейся мышце, т. е. в условиях, когда концентрация ионов Са²⁺ в миоплазме очень низкая, взаимодействию миозиновых и актиновых нитей препятствуют молекулы белка тропонина, расположенные на актиновых нитях.
Тропонин обладает очень высоким сродством к ионам Са²⁺. Как только концентрация Са²⁺ в миофибриллах повышается, тропонин связывает Са²⁺ и изменяет свое расположение на актиновой нити таким образом, что делает возможным ее взаимодействие с миозиновой нитью. Формирующиеся при этом поперечные мостики перемещают актиновую нить лишь на 1 % ее длины. Чтобы обеспечить дальнейшее продвижение нити и соответственно сокращение волокна, необходимо, чтобы эти мостики разъединились и прикрепились к новым участкам актиновой нити. Такое разъединение мостиков осуществляется при расщеплении молекул АТФ АТФ-азой миозина. Таким образом, взаимодействие миозина и актина, возможное при связывании Са²⁺ тропонином, активирует АТФ-азу миозина, последняя расщепляет АТФ, а это приводит к разъединению миозина и актина. В присутствии Са²⁺ и АТФ в миоплазме этот процесс многократно повторяется: мостики повторно образуются и расходятся, в результате чего актиновые нити «скользят» и мышечное волокно укорачивается.
Подсчитано, что при изотоническом сокращении скелетной мышцы лягушки поперечные мостики должны совершить за 0,1 с 50 таких движений, чтобы длина каждого саркомера волокна укоротилась на 50 %. При каждом движении мостиков происходит расщепление молекул АТФ.
Итак, энергия АТФ используется во время деятельности скелетной мышцы для трех основных процессов:
Нарушение ресинтеза АТФ ядами, подавляющими гликолитические и окислительные процессы, ведет к полному исчезновению АТФ и креатинфосфата, вследствие чего кальциевый насос перестает работать. Концентрация Са²⁺ в области миофибрилл значительно возрастает и мышца приходит в состояние длительного необратимого укорочения.
Ресинтез АТФ в мышечных волокнах
Дано определение ресинтеза АТФ. Описаны основные пути ресинтеза АТФ в мышечных волокнах: креатинфосфатный, гликолитический, миокиназный и тканевое дыхание. Описаны количественные критерии путей ресинтеза АТФ, соотношение между различными путями ресинтеза АТФ при мышечной работе, а также между путями ресинтеза АТФ и зонами относительной мощности.
Ресинтез АТФ в мышечных волокнах
Определение
Ресинтез АТФ – синтез АТФ из различных энергетических субстратов во время физической работы в мышечных волокнах.
Формула ресинтеза АТФ выглядит следующим образом:
Пути ресинтеза АТФ
Ресинтез АТФ может осуществляться двумя путями:
Аэробный путь (тканевое дыхание, аэробное или окислительное фосфорилирование) – основной способ образования АТФ в мышечных волокнах. Он протекает в митохондриях мышечных волокон. В результате тканевого дыхания выделяется 39 молекул АТФ. Окисляемое вещество распадается до углекислого газа и воды.
Анаэробный ресинтез АТФ
Анаэробные пути ресинтеза АТФ являются дополнительными способами образования АТФ в мышечных волокнах в тех случаях, когда основной путь получения АТФ – тканевое дыхание не может обеспечить мышечную деятельность необходимым количество кислорода. Эти механизмы ресинтеза АТФ активно функционируют в начале выполнения физических упражнений, когда тканевое дыхание не полностью «развернулось», а также при физических нагрузках высокой мощности.
Анаэробный ресинтез АТФ в мышечных волокнах возможен посредством нескольких механизмов:
Количественные критерии путей ресинтеза АТФ
Существуют количественные критерии путей ресинтеза АТФ. К ним можно отнести: максимальную мощность, время развертывания, время сохранения или поддержания максимальной мощности, метаболическую ёмкость (табл. 1).
Таблица 1. Количественные критерии основных путей ресинтеза АТФ (С.С. Михайлов, 2009)
| Пути ресинтеза АТФ | Критерии | |||
| Максимальная мощность, кал/мин кг | Время развертывания | Время сохранения максимальной мощности | Метаболическая ёмкость | |
| Креатинфосфатный | 900-1100 | 1-2 с | 8-10 с | |
| Гликолитический | 750-850 | 20-30 с | 2-3 мин. | При анаэробном окислении гликогена образуются 3 молекулы АТФ в расчете на одну молекулу глюкозы |
| Аэробный | 350-450 | 3-4 мин. | Десятки минут | При аэробном окислении гликогена образуются 39 молекул АТФ в расчете на одну молекулу глюкозы (самый экономичный) |
Соотношение между различными путями ресинтеза АТФ
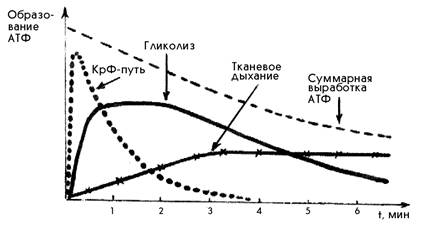
При любой мышечной работе функционируют все три основных механизма ресинтеза АТФ, но включаются они последовательно. В первые секунды ресинтез АТФ осуществляется за счет креатинфосфатной реакции, затем включается гликолиз. По мере продолжения работы на смену гликолизу приходит тканевое дыхание (рис.1). Эта смена механизмов ресинтеза АТФ приводит к уменьшению суммарной выработки АТФ.
Рис.1. Включение путей ресинтеза АТФ при выполнении физической работы (С.С. Михайлов, 2009)
Пути ресинтеза АТФ и зоны относительной мощности
В.С. Фарфель приводит следующее соотношение мощности работы и основной системы энергообеспечения (табл.2)
Таблица 2. Зоны мощности работы и основная система энергообеспечения (В.С. Фарфель)
Энергетические процессы в мышце
Содержание
Энергетические процессы в мышце [ править | править код ]
Естественно, что для совершения мышечного движения требуется энергия. В организме человека существуют разные источники энергии, которые последовательно включаются один за другим. Рассмотрим каждый из них.
АТФ [ править | править код ]
Универсальным источником энергии в живом организме является молекула АТФ, которая образуется в цитратном цикле Кребса. Под действием фермента АТФазы молекула АТФ гидролизуется, отсоединяя фосфатную группу в виде ортофосфорной кислоты (Н3РО4), и превращается в АДФ, при этом высвобождается энергия.
Головка миозинового мостика при контакте с актином обладает АТФазной активностью и соответственно возможностью расщеплять АТФ и получать энергию, необходимую для движения.

Креатинфосфат [ править | править код ]
Запас молекул АТФ в мышце ограничен, поэтому расход энергии при работе мышцы требует постоянного его восполнения, это происходит за счет креатинфосфата. Креатинфосфат обладает способностью отсоединять фосфатную группу и превращаться в креатин, присоединяя фосфатную группу к АДФ, которая превращается в АТФ.
АДФ + креатинфосфат = АТФ + креатин.
Эта реакция получила название – реакции Ломана. Именно поэтому креатин имеет большое значение в бодибилдинге.
Надо заметить, что креатин эффективен только при выполнении анаэробных (силовых) упражнений, так как креатинфосфата достаточно примерно на 2 минуты интенсивной работы, затем подключаются другие источники энергии. Соответственно, в лёгкой атлетике приём креатина как добавки для увеличения атлетических показателей малоэффективен.
Запасы креатинфосфата в волокне не велики, поэтому он используется в качестве источника энергии только на начальном этапе работы мышцы, до момента активизации других более мощных источников – анаэробного и затем аэробного гликолиза. По окончании работы мышцы реакция Ломана идет в обратном направлении, и запасы креатинфосфата в течение нескольких минут восстанавливаются.
Энергетический метаболизм скелетных мышц [ править | править код ]
Алактатные механизмы [ править | править код ]
КФ обеспечивает запас энергии фосфата для ресинтеза АТФ из АДФ при наступлении сократительной деятельности (рис. 3):
КФ + АДФ Креатинкиназа К + АТФ (1)
В состоянии покоя мышечные волокна наращивают концентрацию КФ до пяти раз больше, чем АТФ. В начале сокращения, когда концентрация АТФ начинает падать, а АДФ повышаться вследствие ускорения разложения АТФ, массовая активность способствует образованию АТФ из КФ.
Хотя образование АТФ из КФ происходит быстро, требуя одной единственной ферментативной реакции (1), количество АТФ, которое может быть получено в результате этого процесса, ограничено начальной концентрацией КФ. Мышечные волокна также содержат миокиназу, которая катализирует образование одной молекулы АТФ и одной молекулы АМФ из двух молекул АДФ. АТФ и КФ, вместе взятые, могут обеспечить максимальную силу в течение 8—10 с. Таким образом, энергия, полученная от фосфагенной системы, используется для коротких всплесков максимальной мышечной активности, необходимых в легкой и тяжелой атлетике (забег на 100 м, толкание ядра или поднятие тяжестей).
Гликолиз [ править | править код ]
Хотя метаболизм по гликолитическому пути производит лишь небольшое количество АТФ из каждой усвоенной единицы глюкозы, он может обеспечить быстрый синтез большого количества АТФ при наличии достаточного количества ферментов и субстрата. Этот процесс может также происходить в отсутствие кислорода:
Глюкоза анаэробный быстрый гликолиз 2 АТФ + 2 лактата (2)
Глюкоза для гликолиза поступает либо из крови, либо из запасов гликогена. Когда исходным материалом выступает гликоген, из одной единицы потребленной глюкозы в результате фосфоролитического гликогенолиза образуется три молекулы АТФ. По мере того, как мышечная активность становится интенсивнее, для анаэробного расщепления гликогена мышц требуется все больше и больше АТФ, и, соответственно, увеличивается производство молочной кислоты. Анаэробный гликолиз может обеспечить энергию на 1,3-1,6 мин максимальной мышечной активности.
Образование молочной кислоты понижает уровень pH в мышечных волокнах. Это препятствует действию ферментов и вызывает боль, если удаление молочной кислоты происходит слишком медленно по сравнению с ее образованием.
Окислительное фосфорилирование [ править | править код ]
При умеренном уровне физической нагрузки, например, при беге на 5000 м или марафоне, большая часть АТФ, используемого для сокращения мышц, образуется путем окислительного фосфорилирования. Окислительное фосфорилирование позволяет высвободить из глюкозы гораздо больше энергии по сравнению с отдельно взятым анаэробным гликолизом:
Жиры катаболизируются только с помощью окислительных механизмов, при этом выделяется много энергии. Аминокислоты тоже могут быть метаболизированы подобным образом. Три метаболических пути образования АТФ для сокращения и расслабления мышц показаны на рис. 3.
В течение первых 5
10 мин умеренной физической нагрузки главным потребляемым «топливом» является собственный гликоген мышц. В течение следующих 30 мин доминирующими становятся переносимые кровью вещества; глюкоза крови и жирные кислоты вносят примерно одинаковый вклад в потребление мышцами кислорода. По истечении этого периода все более важную роль приобретают жирные кислоты. Важно подчеркнуть взаимодействие между анаэробными и аэробными механизмами в образовании АТФ во время физической нагрузки. Вклад анаэробного образования АТФ больше при краткосрочной нагрузке высокой интенсивности, в то время как при более продолжительных нагрузках низкой интенсивности преобладает аэробный метаболизм.
Восстановление и кислородная задолженность [ править | править код ]
После того как физическая нагрузка закончилась, поглощение кислорода все еще остается выше нормы (табл.). С недавнего времени для обозначения кислородной задолженности используется также термин «избыточное потребление кислорода после физической нагрузки». Сначала его уровень очень высок, пока тело восстанавливает запасы КФ и АТФ, возвращая тканям запасенный кислород, а затем в течение еще одного часа потребление идет на более низком уровне, пока удаляется молочная кислота. Поэтому ранние и последние фазы кислородной задолженности называют соответственно алактатной и лактатной кислородной задолженностью. Повышение температуры тела также говорит о более высокой скорости метаболизма и росте потребления кислорода.
Чем продолжительнее и интенсивнее физическая нагрузка, тем больше времени занимает восстановление. Например, на восстановление после полного истощения гликогена мышц зачастую требуется несколько дней, а не секунд, минут или часов, необходимых для восстановления запасов КФ и АТФ и удаления молочной кислоты. Физическая нагрузка большой интенсивности, вероятно, приводит к микротравмам мышечных волокон, и их восстановление занимает некоторое время.
Компоненты кислородной задолженности. После длительной, тяжелой физической нагрузки дыхание остается выше нормы для удовлетворения повышенной потребности в кислороде
Восстановление запасов кислорода в тканях(около 1 л)
Восстановление уровней креатинфосфата и других богатых энергией фосфатов (около 1-1,5 л)
Удаление молочной кислоты путем глюконеогенеза и другими путями (до 12 л)
Стимуляция метаболизма вследствие повышения уровня адреналина (около 1 л)
Дополнительное потребление кислорода в дыхательных мышцах и сердце (около 0,5 л)
Общее усиление метаболизма вследствие более высокой температуры тела*
Биохимия метаболического ацидоза, вызванного физическими упражнениями
В обзоре представлены четкие доказательства того, что основной причиной ацидоза скелетных мышц является гидролиз АТФ, а не гликолиз, вызывающий производство молочной кислоты (лактата). Замедление производства лактата, возникающее при гликолизе вызывает ацидоз мышечных волокон.
Робергс Р., Фарзенах Г., Паркер Д.
Биохимия метаболического ацидоза, вызванного физическими упражнениями
Robergs, Robert A., Farzenah Ghiasvand, and Daryl Parker. Biochemistry of exercise-induced metabolic acidosis. Am J Physiol Regul Integr Comp Physiol. 287: R502–R516, 2004; 10.1152/ajpregu.00114.2004
Аннотация
Развитие ацидоза во время интенсивных упражнений традиционно объясняется повышенным производством молочной кислоты, вызывая высвобождение протона и образование кислой соли лактата натрия. На основании этого объяснения, если уровень продукции лактата достаточно высок, буферная способность клеток может быть превышена, что приводит к снижению клеточного pH. Эти биохимические события получили название лактоацидоз.
Лактоацидоз во время физических упражнений был классическим объяснением биохимии ацидоза более 80 лет. Эта вера привела к интерпретации того, что производство лактата вызывает ацидоз и, в свою очередь, что увеличенное производство лактата – одна из нескольких причин мышечного утомления во время интенсивных тренировок.
В этом обзоре показано, что нет биохимических доказательств того, что производство лактата вызывает ацидоз.
Причиной ацидоза является замедление производства лактата. Точно также существует множество исследований, показывающих, что ацидоз вызывается реакциями, отличными от производства лактата. Каждый раз, когда АТФ распадается на АДФ и неорганический фосфат высвобождается протон водорода. Когда потребность в АТФ при сокращении мышц основывается на митохондриальном дыхании (тканевом дыхании), в мышечных волокнах протоны водорода не накапливаются, так как протоны используются митохондриями для окислительного фосфорилирования и для поддержания протонного градиента в межмембранном пространстве. Накопление протонов возникает только тогда, когда интенсивность упражнения увеличивается за пределами устойчивого состояния, что в большей степени возникает при ресинтезе АТФ на основе гликолиза и фосфагенной системы. АТФ, который поступает из этих немитохондриальных источников и в конечном итоге используется как топливо для сокращения питания мышц. увеличивает выброс протонов и вызывает ацидоз при интенсивных упражнениях.
В этом случае усиливается производство лактата, чтобы предотвратить накопление пирувата и поставить НАД+, необходимого для второй фазы гликолиза. Таким образом повышенное производство лактата совпадает с клеточным ацидозом и остается хорошим косвенным маркером условий клеточного метаболизма, вызывающих метаболический ацидоз. Если мышцы не производят лактат, ацидоз возникает чаще и мышечное утомление наступает быстрее, при этом выполнение упражнений будет серьезно ухудшено.
Ключевые слова
Abstract
The development of acidosis during intense exercise has traditionally been explained by the increased production of lactic acid, causing the release of a proton and the formation of the acid salt sodium lactate. On the basis of this explanation, if the rate of lactate production is high enough, the cellular proton buffering capacity can be exceeded, resulting in a decrease in cellular pH. These biochemical events have been termed lactic acidosis.
The lactic acidosis of exercise has been a classic explanation of the biochemistry of acidosis for more than 80 years. This belief has led to the interpretation that lactate production causes acidosis and, in turn, that increased lactate production is one of the several causes of muscle fatigue during intense exercise.
This review presents clear evidence that there is no biochemical support for lactate production causing acidosis. Lactate production retards, not causes, acidosis.
Similarly, there is a wealth of research evidence to show that acidosis is caused by reactions other than lactate production. Every time ATP is broken down to ADP and Pi, a proton is released. When the ATP demand of muscle contraction is met by mitochondrial respiration, there is no proton accumulation in the cell, as protons are used by the mitochondria for oxidative phosphorylation and to maintain the proton gradient in the intermembranous space. It is only when the exercise intensity increases beyond steady state that there is a need for greater reliance on ATP regeneration from glycolysis and the phosphagen system.
The ATP that is supplied from these nonmitochondrial sources and is eventually used to fuel muscle contraction increases proton release and causes the acidosis of intense exercise. Lactate production increases under these cellular conditions to prevent pyruvate accumulation and supply the NAD_ needed for phase 2 of glycolysis. Thus increased lactate production coincides with cellular acidosis and remains a good indirect marker for cell metabolic conditions that induce metabolic acidosis. If muscle did not produce lactate, acidosis and muscle fatigue would occur more quickly and exercise performance would be severely impaired.
Keywords
metabolism; skeletal muscle; lactate; acid-base; lactic acidosis