Для чего используется натрий
Натрий (Na, Natrium)
История натрия
Натрий в чистом виде получил в 1807 году Хемфри Дэви – английский химик, который незадолго до натрия открыл калий. Дэви проводил процесс электролиза одного из соединений натрия – гидроксида, расплавив который и получил натрий. Соединениями натрия человечество пользовалось со времён глубокой древности, содой природного происхождения пользовались ещё в Древнем Египте (calorizator). Называли элемент содий (sodium), иногда именно это название можно встретить даже сейчас. Привычное название натрий (от латинского natrium – сода) было предложено шведом Йенсом Берцелиусом.
Общая характеристика натрия
Натрий является элементом I группы III третьего периода периодической системы химических элементов Д.И. Менделеева, имеет атомный номер 11 и атомную массу 22,99. Принятое обозначение – Na (от латинского natrium).
Нахождение в природе
Соединения натрия содержатся в земной коре, морской воде, в виде примеси, имеющей свойство окрашивать каменную соль в синий цвет из-за действия радиации.
Физические и химические свойства
Натрий является мягким пластичным щелочным металлом, имеет серебристо-белый цвет и блеск на свежем срезе (натрий вполне возможно разрезать ножом). При применении давления превращается в прозрачное вещество красного цвета, при обычной температуре кристаллизуется. При взаимодействии с воздухом быстро окисляется, поэтому хранить натрий необходимо под слоем керосина.
Суточная потребность в натрии
Натрий – важный для организма человека микроэлемент, суточная потребность в нём для взрослых составляет 550 мг, для детей и подростков – 500-1300 мг. В период беременности норма натрия в сутки составляет 500 мг, а в некоторых случаях (обильное потоотделение, обезвоживание, приём мочегонных препаратов) должна быть увеличена.
Продукты питания богатые натрием
Натрий содержится практически во всех морепродуктах (раках, крабах, осьминогах, кальмарах, мидиях, морской капусте), рыбе (анчоусах, сардинах, камбале, корюшке и т.д.), куриных яйцах, крупах (гречневой, рисе, перловой, овсяной, пшённой), бобовых (горохе, фасоли), овощах (томатах, сельдерее, моркови, капусте, свёкле), молочных продуктах и мясных субпродуктах.
Полезные свойства натрия и его влияние на организм
Полезными для организма свойствами натрия являются:
Усвояемость натрия
Натрий содержится практически во всех продуктах, хотя большую его часть (около 80%) организм получает из поваренной соли. Усвоение в основном происходит в желудке и тонком кишечнике. Витамин D улучшает усвоение натрия, однако, чрезмерно соленая пища и пища богатая белками препятствуют нормальному всасыванию.
Взаимодействие с другими
Повышенное потребление натрия вызывает накопление жидкости в организме, отеки, повышает кровяное давление. Большой прием натрия (соли) приведет к истощению запасов калия, кальция и магния.
Применение натрия в жизни
Применение металлического натрия – химическая и металлургическая промышленность, где он выступает в роли сильнейшего восстановителя. Хлоридом натрия (поваренной солью) пользуются все без исключения жители нашей планеты, это самое известное вкусовое средство и древнейший консервант.
Признаки нехватки натрия
Нехватка натрия обычно случается при чрезмерном потоотделении – в жарком климате или при физических нагрузках. Недостаток натрия в организме характеризуется ухудшением памяти и потерей аппетита, головокружением, быстрой утомляемостью, обезвоживанием, мышечной слабостью, а иногда – судорогами, кожными высыпаниями, желудочными спазмами, тошнотой, рвотой.
Признаки избытка натрия
Излишнее количество натрия в организме даёт о себе знать постоянной жаждой, отёками и аллергическими реакциями.
Натрий. Свойства натрия. Применение натрия
В начале 19-го века натрий звали содием. Такое имя элементу дал Гемфри Дэви, сумевший выделить металл из щелочи. Химик слегка увлажнил ее и подверг электролизу. Изменить название открытого Гемфри элемента предложил Вильгельм Гильберт.
Это автор знаменитых «Анналов физики». Ученый стал именовать содий натронием. Дело продолжил Йенс Берцелиус. Химик из Швеции ввел сокращение натрий. О свойствах и роли этого металла в жизни людей – наш следующий материал.
Химические и физические свойства натрия
Это делает натрий мощным восстановителем. Элемент легко отдает электрон внешнего уровня, повышая свою степень окисления. Атом приходит к завершенной оболочке предыдущего уровня.
Восстановительная активность – причина отсутствия чистого металла в природе. Найти можно лишь соединения. Так, натрия хлорид – это поваренная соль. Карбонат натрия – пищевая сода. Так что, металл не зря был изначально назван содием.
Если же, напротив, нужно усилить агрессию натрия, к нему приплюсовывают кислород. Итог – пероксид, мощный окислитель. В его атмосфере большинство веществ воспламеняются.
Непрост и «характер» гидроксида натрия. Его именуют едким. Соединение разъедает ткани, кожу, бумагу и прочую органику и материи, сделанные на ее основе. Правда, на воздухе гидроксид натрия захватывает углекислый газ и обезвреживается, превращаясь в карбонат.
Когда Гемфри Дэви удалось выделить чистый натрий, мир узнал, каков он внешне. Металл серебристо-белый. Тонкие срезы отливают фиолетовым. Формула натрия делает его мягким и податливым.
Режется обычным ножом и блестит на поверхности скольжения лезвия. У элемента невысокая температура плавления – 97 градусов. Закипает же натрий при 883-ех по шкале Цельсия.
Чистый металл хорошо проводит ток и тепло, не отличается высокой плотностью. Ее показатель у 11-го элемента меньше единицы. Это не умоляет весомости натрия в биологических процессах.
Металл есть и в растениях, и в животных тканях. Так, в организме человека раствор натрия – часть плазмы крови, пищеварительных соков и лимфы.
Осмотической давление, к примеру, поддерживается именно за счет 11-го элемента. Применение ему нашла не только природа, но и человек. Масса натрия идет, к примеру, на промышленные цели. Какие? Об этом расскажем в следующей главе.
Применение натрия
В природе элемент представлен лишь 1-им стабильным изотопом. Его массовое число 23. В искусственных условиях создано еще 15 изотопов. Они не стабильны, большинство разрушается за пару минут. Исключение: — 22-ой и 24-ый Na.
Период полураспада этих изотопов значителен. Первый сохраняется 2,5 года, активно излучает позитроны, чем и служит науке. Период полураспада второго – 15 часов. Достаточно, чтобы послужить медицине и помочь больным лейкемией.
В сфере ядерной энергетики натрий стал теплоносителем. Пригодился «разбег» между температурой плавления и кипения элемента. Интервал в 800 градусов Цельсия позволяет, к примеру, заполнять щелочным металлом контуры энергоносителей атомных подлодок. Натрий принимает тепло из реактора, не закипая при этом.
Держать температуру в разумных рамках удается за счет циркуляции жидкого металла между реактором и парогенератором. В последнем происходит охлаждение натрия, испаряется вода. Вот и получается вращать турбину энергией пара высокого давления.
Чистый элемент пригождается и в металлургии. Какую роль в ней выполняет натрий? Инструкция применения такова: металл упрочняет сплавы на основе свинца. В качестве лигатуры достаточно около 1,5% 11-го элемента. Натрий добавляют и к сплавам других металлов. Добиваются уже не прочности, а тугоплавкости смесей.
Параллельно, белый порошок без запаха участвует в изготовлении бумаги и текстиля. Здесь ставку делают на раствор натрия хлорида. Средство способно осветлять, как писчие листы, так и ткани. В народе реагент называют хлоркой.
Натрия тетраборат стал лекарством при кандидозе и прочих вагинальных инфекциях. Сульфацип натрия – препарат, помогающий при конъюнктивите и других воспалительных процесса в глаза. Противоядием при отравлениях солями и вообще интоксикации организма становится тиосульфат натрия.
Пищевая сода известна в народе, как средство от изжоги. Гидрокарбонат натрия – щелочь, нейтрализующая желудочную кислоту. Применяют 11-ый элемент и при запорах. Выручает сульфат натрия.
Кроме непосредственно медицинской сферы, элемент ценят и в косметологии. Натрий кислота – не что иное, как гиалуронка. Она поддерживает молодость кожи. Инъекции водятся, как правило в носогубные складки, морщины. Кислота заполняет их. В молодости гиалуронат вырабатывается организмом, но с возрастом процесс замедляется. Приходится вводить препарат из вне.
На фото продукты, содержащие натрий
Тем не менее, выделить золото из комплексного расплава уже проще, чем из твердых масс. На финальной стадии «подключают» цинк и … драгоценный металл добыт.
Добыча натрия
К соли примешивают фторид натрия и хлорид калия. Они снижают температуру размягчения сырья с 800-от до 500-от градусов Цельсия. Это сокращает потери натрия в виде испарений. Метод выгоден вдвойне, ведь одновременно с 11-ым элементом добывают и чистый хлор.
Цена натрия
Стоимость элемента зависит от того, приобретается раствор гидроксида натрия, чистый металл, его сульфат или другое соединение. Ценник зависит и от того, покупается оно, к примеру, в составе какого-то препарата, или отдельно. Сфер использования натрия масса, производителей сотни и тысячи.
У каждого свои запросы. Какие-то вещества добываются легко практически в готовом виде, та же соль. Она и стоит около 10-20 рублей за килограмм. Другие соединения натрия нужно синтезировать, что увеличивает их стоимость.
Так, или иначе, человечество готово платить за пользу, приносимую ему 11-ым элементом. Его добыча ведется активно и, судя по всему, не собирается затихать.
Натрий (Na) – роль в организме, применение, суточная потребность, источники
Натрий (Natrium, Na) – химический элемент, выполняющий важную роль макроэлемента в организме человека, который участвует в создании условий и поддержания передачи нервных импульсов между клетками всех тканей. Особенно важен для умения мышечных тканей сокращаться.
Основными функциями натрия также являются – регулирование кислотно-щелочного баланса и поддержание нормального уровня водного баланса, обеспечение транспорта между мембранами клеток и поддержка осмотической концентрации крови. Является активатором ряда ферментов (энзимов).
История – краткая справка
Свое название натрий получил от древнегреческого слова «νίτρον», которое в свою очередь произошло от среднеегипетского слова «nṯr», что в переводе означало – «сода» или «едкий натр».
Название «natrium» и его сокращение «Na» предложил использовать основатель общества врачей в Швеции – академик Йенс Якобс Берцелиус (1779—1848) для обозначения природных ископаемых, в состав которых входила сода. Однако, в ряде других стран и языков (Великобритания, Франция и др.) используется другой термин – «sodium» (содий). Этот момент важен, т.к. некоторые фармацевтические компании как раз используют в названии своих препаратов не «natrium», а «sodium».
Общие данные
Расположение в периодической таблице Д.И. Менделеева: в старой версии — III период, III ряд, I группа, в новой версии таблицы – 1 группа, 3 период.
Физико-химические свойства. Натрий представляет собой щелочный мягкий металл серебристо-белого цвета, иногда с фиолетовым оттенком, который легко можно отрезать ножом. На срезе получается серебристый блеск. Под воздействием высокого давления приобретает красный цвет. При контакте с кислородом достаточно быстро окисляется, превращаясь в оксид натрия (Na2O).
При контакте с водой происходит бурная реакция с выделением водорода, который в свою очередь может легко воспламенится. Также взрывоопасен при контакте с алкилгалогенидами, с которыми может даже самовоспламенятся.
Хорошо растворяется в жидкообразном аммиаке, образовывая в конечном итоге раствор синего цвета.
Обладает высоким коэффициентом электропроводности и теплопроводности.
Несмотря на огромную долю среди других элементов Земной коры – 6 место, в свободном виде Na не найти. Чаще всего он встречается в составе каменной соли (NaCl), содалите, полевом шпате и многих других минералов.
В целом кларк натрия в земной коре составляет 25 кг/т. В морской воде в составе соединений Na составляет 10,5 г на 1 л.
Биологическая роль натрия в организме
Большая часть натрия находится в межклеточной жидкости, что связано с тем, что в мембране клетки интегрирован натрий-калиевый насос, выполняющий роль откачивания ионов Na из цитоплазмы клетки в межклеточную жидкость. Разница содержания натрия в клетке и за ее пределами составляет 15 раз!
Натрий выполняет множество важных и полезных функций, среди которых:
Применение натрия в других сферах человеческой жизни
Суточная потребность
Рекомендуемые суточные дозы натрия в зависимости от пола и возраста 1 :
| Дети | до 1 года | 200-350 мг |
| от 1 до 3 лет | 500 мг | |
| от 3 до 7 лет | 700 мг | |
| от 7 до 11 лет | 1000 мг | |
| Юноши и девушки | от 11 до 14 лет | 1100 мг |
| от 14 до 18 лет | 1300 мг | |
| Взрослые | от 18 лет и старше | 1300 мг |
В перерасчете на поваренную соль – в ¾ ч. ложке соли содержится 1725 мг натрия.
Согласно данным «Американской Ассоциации сердечных заболеваний» взрослый человек ежедневно нуждается в 500-1500 мг Na.
Суточная доза натрия повышается при:
Суточную дозу соли понижают при: ожирении, артериальной гипертензии, аллергиях, ревматизме, переломах, заболеваниях различных органов (печени, поджелудочной железы, почек), применении гормональных препаратов.
Нехватка натрия — симптомы
Дефицит натрия в организме может вызвать ряд осложнений со здоровьем, среди которых:
Причины нехватки натрия
Длительную нехватку Na вызвать достаточно сложно, поэтому это редкое явление. Однако, спровоцировать кратковременный дефицит натрия могут:
Применение натрия
Применение натрия с лечебной целью целесообразно в следующих случаях:
Необходимо отметить, что область применения натрия в медицине зависит от конкретного состава того или иного препарата. Поэтому, выбор и применения Na в медицине делает врач, исходя из потребностей организма.
Избыток натрия
Избыток натрия в организме также, как и нехватка может вызвать ряд осложнений со здоровьем, среди которых:
Повышенное употребление поваренной соли каждый день в течение длительного времени способно вызвать развитие воспалительный процесс в почках и органах желудочно-кишечного тракта, что нередко приводит к некрозу тканей данных органов.
Также установлено, что прием 8,2 г Na на 1 кг массы человека в сутки способно вызвать его летальный исход.
Максимальное количество поваренной соли, с которым почки могут справится составляет – от 20 до 30 г в сутки.
Источники натрия
В каких продуктах содержится натрий больше всего?
Конечно же, больше всего натрия в поваренной соли – в 100 г соли содержится 38758 мг, или 38,8 г Na.
Растительные и животные источники (мг на 100 г): треска соленая (5670), соевый соус (5666), Сельдь тихоокеанская среднесоленая (5380), горбуша соленая (5343), килька (4917), лещ вяленый (4566), скумбрия соленая (4450), кета соленая (4053), оливки консервированные (2250), икра горбуши зернистая (2245), сервелат (2226), икра минтая пробойная (2206), икра осетровая паюсная (2022), икра белужья зернистая (1630), икра осетровая зернистая (1620), сыр рокфор (1300), брынза коровья или овечья (1200), огурец соленый (1111), сыр голландский (1100), тунец в масле консервированный (961), капуста белокочанная квашеная (930), курага (170), помидоры (40), гречка и овес (33), смородина черная (32), абрикосы (30), картофель (28), пшено (28), крыжовник (23,6), морковь (21), малина (19), лук репчатый (18), сливы (18), земляника (18), арбуз (16), свекла (16), тыква (14), груши (14), капуста белокочанная (13), мандарины (12), лимон (12), кабачки (10), какао (7).
Химические источники (Na): «Натрия сульфат», «Натрия хлорид», витаминные комплексы («Витрум», «Компливит») и другие.
Взаимодействие натрия с другими веществами
Видео
Источники:
1. Методические рекомендации о нормах физиологических потребностей в энергии и пищевых веществах для различных групп населения России от 18.12.2008 г. №2.3.1.2432-08.
Важность натрия в жизни человека

Особые химические свойства натрия:
— высокая химическая активность (на воздухе щелочной металл легко окисляется);
— активное взаимодействие со многими неметаллами;
— при переизбытке кислорода образуется пероксид натрия;
— бурное взаимодействие с водой;
— растворяемость почти во всех кислотах.
В естественной среде натрий можно встретить только в виде химического соединения.
Соединения натрия известны человечеству с давних времён. Ранее этот элемент именовался содием. Название «натрий» пришло из среднеегипетского языка, где оно означало «едкий натр», «сода» – природная сода, которая встречается в натронных озёрах Египта. Данный природный элемент древние египтяне использовали очень активно: при бальзамировании, изготовлении разных видов красок, отбеливании холста, при варке пищи. Как химическое вещество натрий впервые был открыт английским химиком Хемфридом Дэви, который смог получить его путем использования особого лабораторного оборудования с применением электрического тока.
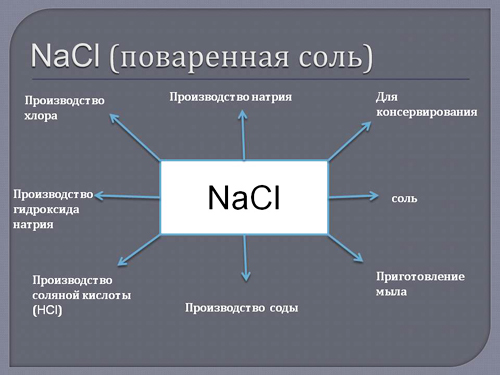
Основным поставщиком натрия можно назвать поваренную соль, сфера применения которой очень обширна:
— производство хлора; 
— натрия;
— соды;
— консервирования и соления пищевых продуктов;
— в кулинарии в качестве пищевого продукта, а именно соли (очищенная и неочищенная, йодированная, морская и т.д.);
— приготовление мыла;
— производство соляной кислоты.
В лабораторных условиях все вышеуказанные процессы проводят исключительно с использованием лабораторной посуды из стекла или фарфора, резинотехнических изделий и фильтровальной бумаги.
Роль натрия в жизнедеятельности организма
Содержание натрия в организме достаточно велико. Суточная потребность здорового человека составляет от 4 до 7г, что равняется приблизительно 10-15г поваренной соли. Натрий является настолько важным элементом, что он присутствует почти во всех органах, биологических жидкостях и тканях человеческого организма и выполняет особую роль во внутриклеточных и межклеточных обменных процессах. Основная часть натрия находится во внеклеточных жидкостях – примерно 50 %, в костях – около 40 % и до 10 % – внутри клеток.

— в возникновении и передаче нервного импульса;
— в работе механизма кратковременной памяти;
— в поддержании нормального состояния мышечной и сердечно-сосудистой системы;
— в выделении секреции соляной кислоты в желудке;
— в транспорте сахаров, аминокислот, различных анионов.
Основные признаки избытка натрия в организме – утомление, перевозбуждение, различного рода неврозы, дисфункция надпочечников, образование камней в почках, отеки.
Условия хранения и меры предосторожности
В лабораториях или аптеках натрий в небольших количествах (до 1 кг ) хранят в герметичных стеклянных банках под слоем керосина таким образом, чтобы последний покрывал весь металл. Несмотря на то, что натрий безвреден, не стоит забывать, что это химический реактив, и при работе с ним следует соблюдать некоторые меры предосторожности. Работы проводить в перчатках нитриловых или перчатках смотровых. С целью исключения взаимодействия данного реактива с другими химическими веществами использовать специальную лабораторную посуду из стекла. Хранить натрий дома, как и производить с ним опыты и эксперименты в домашних условиях, не рекомендуется.
Соединения натрия и их применение
Магазин химических реактивов Москва розница и оптом предлагает большой выбор соединений натрия широкого спектра применения:
— хлористый натрий – при обезвоживании организма; для промывки ран, глаз и слизистой оболочки носа; повышения осмотического давления крови;
— натрий лактат – в косметологии, в пищевой промышленности в качестве пищевой добавки E325;
— натрий глюконат – в качестве усилителя вкуса;
— натрий бромистый – в медицине как средство с седативным действием; в фотоделе – при производстве фотопленок и проявителей;
— натрий гидроокись (самая распространённая щёлочь) в химической и целлюлозно-бумажной промышленности, в нефтепереработке.
Где лучше купить соединения натрия
«Прайм Кемикалс Групп» – один из лидеров по продаже лабораторного оборудования и приборов, лабораторного стекла, химических реактивов, резинотехнических изделий в Москве и МО. Весь товар соответствует стандартам ГОСТ.
“Prime Chemicals Group” – это удачное решение «лабораторного вопроса»!