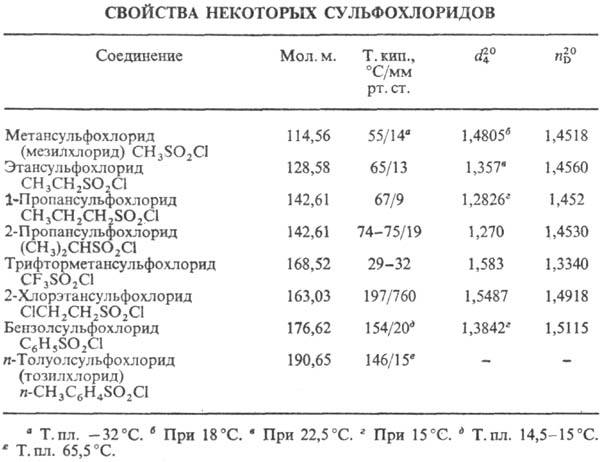
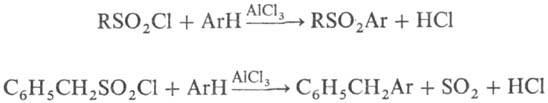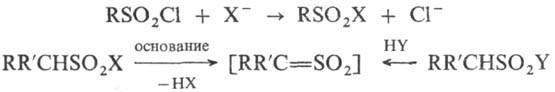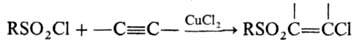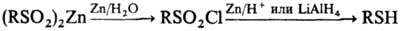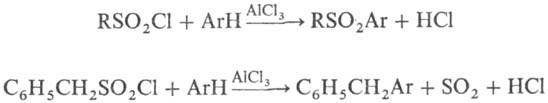Для чего используют сульфохлориды
СУЛЬФОХЛОРИДЫ
С. называют, добавляя к назв. соединения-основы окончание «сульфохлорид», напр. бензолсульфохлорид.
Атом S в С. имеет тетраэдрич. конфигурацию; связи SЧО почти двойные, напр. длины связей для C 6 H 5 SO 2 C1 0,1417 нм (SЧО), 0,176 нм (СЧS), 0,2047 нм (SЧC1), углы CSC1 100,4°, CSO 110°, OSO 122,5°. Группа SO 2 C1 обладает отрицательными индукционным и мезомерным эффектами.
При нагревании выше температуры кипения С., особенно ароматические, разлагаются с выделением SO 2 ; в воде и в к-тах довольно устойчивы, в присут. оснований легко гидролизуются до сульфокислот. Р-ция С. с нуклеоф. реагентами приводит к продуктам замещения атома С1, в присут. третичных аминов промежуточно генерируются сульфены, напр.:
В промышленности С. получают взаимод. алифатич. углеводородов с SO 2 C1 2 или смесью SO 2 и С1 2 в газовой или жидкой фазе под действием света либо в присутствии инициаторов радикальных р-ций; ароматические С.-обработкой соответствующих углеводородов хлорсульфоно-вой кислотой.
Применяют C. в произ-ве моющих ср-в, ионообменных смол, эластомеров, лек. ср-в, красителей, инсектицидов и гербицидов; в качестве полупродуктов в синтезе эфиров сульфокислот; как мягкие алкилирующие агенты в орг. синтезе.
С. раздражают слизистые оболочки глаз и верхних дыхательных путей, при попадании на кожу или при нахождении в атмосфере, содержащей пары или аэрозоли С., вызывают дерматиты. Лакриматоры (особенно ненасыщенные С.). Вдыхание паров может привести к отеку легких. С увеличением мол. массы раздражающее действие С. ослабевает,
См. также Бензолсульфохлориды, Метансульфохлорид, То-луолсульфохлориды.
Лит.: Джильберт Э. Е., Сульфирование органических соединений, пер. с англ., М., 1969; Общая органическая химия, пер. с англ., т. 5, М., 1983. с. 519-22; Houben-Weyl, Methoden der organischen Chemie, Bd 9, Stuttg., 1955; «Methodicum Chimicura», v. 7, pt B, Stuttg., 1977. Я. И. Крылов.
СУЛЬФОХЛОРИДЫ
С ульфохлориды называют, добавляя к назв. соединения-основы окончание «сульфохлорид», напр. бензолсульфохлорид.
Атом S в сульфохлоридах имеет тетраэдрич. конфигурацию; связи S—О почти двойные, напр. длины связей для C 6 H 5 SO 2 Cl 0,1417 нм (S—О), 0,176 нм (С—S), 0,2047 нм (S—Cl), углы CSCl 100,4°, CSO 110°, OSO 122,5°. Группа SO 2 Cl обладает отрицательными индукционным и мезомерным эффектами.
При нагревании выше температуры кипения сульфохлориды, особенно ароматические, разлагаются с выделением SO 2 ; в воде и в к-тах довольно устойчивы, в присут. оснований легко гидролизуются до сульфокислот. Р-ция сульфохлоридов с нуклеоф. реагентами приводит к продуктам замещения атома С1, в присут. третичных аминов промежуточно генерируются сульфены, напр.:
В промышленности сульфохлориды получают взаимод. алифатич. углеводородов с SO 2 Cl 2 или смесью SO 2 и Сl 2 в газовой или жидкой фазе под действием света либо в присутствии инициаторов радикальных р-ций; ароматические сульфохлориды-обработкой соответствующих углеводородов хлорсульфоно-вой кислотой.
Применяют сульфохлориды в произ-ве моющих ср-в, ионообменных смол, эластомеров, лек. ср-в, красителей, инсектицидов и гербицидов; в качестве полупродуктов в синтезе эфиров сульфокислот; как мягкие алкилирующие агенты в орг. синтезе.
С ульфохлориды раздражают слизистые оболочки глаз и верхних дыхательных путей, при попадании на кожу или при нахождении в атмосфере, содержащей пары или аэрозоли, сульфохлориды вызывают дерматиты. Лакриматоры (особенно ненасыщенные сульфохлориды). Вдыхание паров может привести к отеку легких. С увеличением мол. массы раздражающее действие сульфохлоридов ослабевает,
Лит.: Джильберт Э. Е., Сульфирование органических соединений, пер. с англ., М., 1969; Общая органическая химия, пер. с англ., т. 5, М., 1983. с. 519-22; Houben-Weyl, Methoden der organischen Chemie, Bd 9, Stuttg., 1955; «Methodicum Chimicura», v. 7, pt B, Stuttg., 1977. Я. И. Крылов.
Методы получения органических сульфокислот и сульфохлоридов в химической технологии БАВ
3. Методы получения органических сульфокислот и сульфохлоридов в химической технологии БАВ
3.1. Общие сведения о процессе. Значение сульфопроизводных в синтезе БАВ
Исходными продуктами при сульфировании служат, главным образом, ароматические и гетероароматические соединения и их производные, а в ряде случаев и сами лекарственные вещества. Реже используются вещества алифатического и алициклического ряда. Среди них наибольшее значение в синтезе сульфо-БАВ имеют полисахариды и стероиды.
Алканы сульфируют крайне редко, так как реакция сопровождается окислением и приводит к образованию сложной смеси продуктов. Однако карбоновые кислоты, N, N-дизамещенные аминокислоты, альдегиды и кетоны можно сульфировать непосредственно в a-положение.
Алкены сульфируются легко, но в результате реакции образуются, в основном, сульфаты, а не сульфонаты (при сульфировании H2SO4) или смесь сульфокислот и сульфонов (при сульфировании SO3).
В качестве сульфирующих агентов применяются концентрированная серная кислота, олеум, хлорсульфоновая кислота, серный ангидрид и его комплексные соединения.
Сульфогруппа может вводиться в молекулу соединения как с целью придания ему новых свойств, так и с целью дальнейшей замены сульфогруппы на гидроксил, аминогруппу и т. п.
Целевым продуктом сульфирования являются сульфоновые кислоты (сульфокислоты).
Сульфокислоты, как правило, являются твердыми гигроскопичными кристаллическими веществами, хорошо растворимыми в воде и обладающими ярко выраженным кислотным характером. Ароматические сульфокислоты по силе близки к минеральным. В разбавленных водных растворах они практически полностью диссоциированы. Тепловой эффект нейтрализации ароматических сульфокислот 58,1 кДж/г×экв.
Выделение сульфокислот обычно встречает трудности, так как они хорошо растворимы в сульфомассе. Поэтому сульфокислоты чаще всего выделяют в виде солей, из которых свободные сульфокислоты могут быть получены с помощью ионообменных смол. Бариевые и кальциевые соли сульфокислот в противоположность щелочноземельным сульфатам, как правило, растворимы в воде, что позволяет на стадии выделения продуктов реакции отделять избыточную серную кислоту в виде нерастворимых сульфатов.
Растворимость в воде аминосульфокислот, имеющих структуру цвиттер-ионов, обычно незначительна. При подкислении водных растворов натриевых солей аренсульфокислот хлоридом водорода во многих случаях осаждается хлорид натрия, а свободная кислота может быть выделена концентрированием раствора.
Соли сульфокислот, образованные органическими катионами, например, S-бензилтиуроний-ионом
имеют четкие температуры плавления, что используют для идентификации кислот, которые четких температур плавления, как правило, не имеют.
Число синтетических сульфокислот очень велико, и они широко используются в практике.
Из природных сульфокислот следует, прежде всего, отметить аминосульфокислоты: таурин и цистеиновую кислоту, которые играют большую роль в процессе всасывания жиров в организме млекопитающих.
С другой стороны, были специально синтезированы вещества, регулирующие свертываемость крови. Так, например, препарат тромбовар (децилат) является эффективным средством для лечения варикозного расширения вен. Многие поверхностно-активные вещества, содержащие сульфогруппу, обладают сильным антимикробным действием. Ряд сульфо-ПАВ способны усиливать действие антибиотиков и сульфамидных препаратов. Среди сульфо-ПАВ имеются прекрасные солюбилизаторы, что перспективно с точки зрения создания инъекционных форм нерастворимых в воде препаратов.
Широким спектром биологической активности обладают сульфированные полисахариды. В частности, декстрансульфат активирует ряд ферментов, обладает иммунорегулирующими свойствами и т. д.
Сульфокислоты являются промежуточными веществами в синтезе ряда химико-фармацевтических препаратов (диазолин, амидопирин и др.). В ряде случаев сульфогруппа входит в состав лекарственного препарата, придавая ему большую растворимость в воде. Последнее обусловливает снижение токсичности, придает препарату несколько иную биологическую активность, а также создает предпосылки для создания инъекционных лекарственных форм.
3.2. Сульфирование ароматических соединений серной кислотой и олеумом
Сульфирование ароматических соединений является реакцией электрофильного замещения и в среде концентрированной серной кислоты обычно протекает по схеме:
Существенным отличием этой реакции от других реакций электрофильного замещения является ее обратимость. (Следует отметить, что в отсутствие воды обратимость практически не проявляется, так как константы скорости обратных реакций на 5-6 порядков ниже констант скоростей реакций, ведущих к образованию целевых продуктов).
Тем не менее, обратимость реакции свидетельствует о том, что переходное состояние имеет несколько иную структуру, чем в реакции нитрования, которая необратима.
В связи с рассмотрением вопроса о механизме сульфирования необходимо обсудить строение и основные свойства как серной кислоты, так и олеума.
Безводная серная кислота при комнатной температуре представляет собой в сильной мере ассоциированное соединение с длинными образованными за счет водородных связей, цепевидными молекулами:
При повышении температуры эти цепочки разрушаются.
Жидкая 100%-ая серная кислота (tпл = 10,4°С) является ионизирующим растворителем, однако, ее собственная ионизация незначительна и, в первом приближении, соответствует уравнению:
Безводная серная кислота кипит с разложением до образования азеотропной смеси состава 98,3% H2SO4 и 1,7% Н2О (tкип = 338,8°С). Серная кислота смешивается с Н2О и SO3 в любых соотношениях. В водных растворах она полностью диссоциирована:
При растворении SO3 в концентрированной серной кислоте образуется целая серия полимерных кислот:
и полагали, что сульфирующими агентами являются поляризованные молекулы SO3 и S2O6, а также катионы НSO3Å и Н3SO4Å:
с сотрудниками впервые применил для исследования механизма и кинетики сульфирования помимо традиционных химических и физико-химических методов математическое моделирование процесса на ЭВМ. Проведенные исследования подтвердили правильность точки зрения К. Ингольда о том, что основным сульфирующим реагентом является поляризованная молекула SO3. Механизм сульфирования НSO3Å следует, по-видимому, рассматривать как кислотно-катализируемое сульфирование SO3.
Предложенные математические модели оказались адекватными эксперименту и позволили не только найти значения кинетических параметров сульфирования ряда соединений, но проводить полное параметрическое исследование процессов и их оптимизацию применительно к различным аппаратурным схемам.
Для промышленного сульфирования серной кислотой чаще всего используют 92-93%-ную серную кислоту (купоросное масло) и 98-100%-ную серную кислоту (моногидрат).
При сульфировании малоактивных субстратов используют олеум (обычно 20-25%-ный или 60-65%-ный).
Сульфирование начинается обычно как гетерогенный процесс. Спустя непродолжительное время после начала реакции масса гомогенизируется, и основное время процесс протекает как гомогенный.
Реакция десульфирования протекает при повышенных температурах при наличии в реакционной массе воды и катализируется кислотами.
Концентрация серной кислоты оказывает решающее влияние на ход процесса сульфирования. По мере прохождения сульфирования концентрация серной кислоты вследствие разбавления ее реакционной водой падает:
С уменьшением концентрации серной кислоты скорость сульфирования резко снижается вследствие кислотной диссоциации в соответствии с уравнением:
и резким уменьшением концентрации сульфирующих реагентов (SO3, HSO3Å). Между тем, концентрация сульфирующих частиц даже в 100%-ной H2SO4 невысока и составляет доли процента. Предельную или критическую концентрацию серной кислоты (выраженную в % SO3), при которой она еще способна сульфировать соединение, называют «p-сульфирования» (pс). Для устранения неопределенности за величину pс принимают концентрацию серной кислоты, при которой скорость образования продукта составляет менее 1% за час. Практически в конце сульфирования концентрация оставшейся серной кислоты должна быть выше pс, так как в противном случае скорость сульфирования будет слишком мала. Минимальное количество серной кислоты или олеума, требующееся для моносульфирования 1 кмоль соединения, может быть вычислено по формуле:
Из формулы видно, что чем выше концентрация исходной кислоты, тем меньше ее понадобится для проведения процесса. Однако следует иметь в виду, что повышение концентрации сульфирующего агента может привести к нежелательным побочным эффектам (образование полисульфокислот, сульфонов, окисление реакционной массы и т. д.).
От выбора концентрации сульфирующего агента зависит также место вхождения сульфогруппы в ароматическое ядро. Например, для получения a-нафталинсульфокислоты, рационально применять более концентрированную кислоту, чтобы предотвратить ее десульфирование. При получении b-нафталинсульфокислоты следует брать серную кислоту несколько меньшей концентрации, чтобы способствовать гидролизу побочного a-изомера (b-изомер в этих условиях не десульфируется).
Большое влияние на ход процесса сульфирования оказывает температура. Энергия активации реакции сульфирования серной кислотой колеблется в довольно широких пределах в зависимости от химической природы субстрата и места вхождения сульфогруппы. Для бензола и его гомологов это обычно 30-50 кДж/моль, что обусловливает увеличение скорости реакции в 1,5-2 раза с ростом температуры на каждые 10°С.
образование которого объясняют электрофильной атакой ArSO2Å исходного субстрата. При сульфировании хлорбензола моногидратом при 80-100°С образуется практически только п-хлорбензолсульфокислота.
Поскольку процесс сульфирования описывается рядом параллельных и последовательных реакций, максимальный выход целевого продукта может быть достигнут не только при определенной температуре, соотношении реагентов, концентрации серной кислоты, но и при определенной продолжительности ведения процесса.
Одним из основных недостатков сульфирования серной кислотой является необходимость использования избытка сульфирующего агента, что, в свою очередь, приводит к необходимости затраты больших количеств нейтрализующих средств на стадии выделения продукта, технологическому усложнению этой стадии и образованию большого количества отходов производства. В значительной мере устранить эти недостатки можно либо оптимизацией процесса, либо удалением образующейся воды из реакционной массы. Последнее можно осуществить азеотропной отгонкой воды с парами сульфируемого вещества. Этот метод, называемый «сульфированием в парах» можно применять при сульфировании летучих ароматических углеводородов, образующих с водой азеотропные смеси (бензол, толуол, ксилолы). Подобный метод можно рекомендовать и для сульфирования высококипящих углеводородов, если вводить в реакционную массу инертный азеотропный агент специально для удаления образующейся во время реакции воды (хлороформ, лигроин и др.).
При сульфировании бензола «в парах» расход серной кислоты снижается в 1,8 раза по сравнению с жидкофазным сульфированием. Однако скорость сульфирования значительно снижается вследствие уменьшения концентрации H2SO4 в реакционной массе.
Другим выходом является использование в качестве сульфирующего агента серного ангидрида, так как в этом случае вода не образуется:
Серный ангидрид является очень энергичным сульфирующим агентом, пригодным для сульфирования малоактивных соединений. Недостатком этого сульфирующего агента является возможность протекания побочных реакций (окисление, образование сульфонов и др.). Кроме того, сульфирование серным ангидридом, особенно в отсутствие жидкого разбавителя, технологически сложно. По мере образования сульфокислоты реакционная масса загустевает, затрудняется отвод тепла, создаются местные перегревы, резко ухудшается контакт серного ангидрида с субстратом. Если повышение температуры нежелательно или не приводит к снижению вязкости реакционной массы, процесс рекомендуется проводить в две стадии. Сначала сульфируют парами серного ангидрида до загустевания реакционной массы (обычно до глубины превращения 70-80%), а затем завершают реакцию действием олеума. Это позволяет снизить расход сульфирующих агентов (в пересчете на SO3) почти вдвое по сравнению с сульфированием олеумом в одну стадию.
При сульфировании малоактивных субстратов используют олеум (обычно 20-25%-ный или 60-65%-ный). Типичным примером такого процесса является получение натриевой соли N-диметилметаниловой кислоты в производстве прозерина:
Прозерин является синтетическим антихолинэстеразным веществом. По химическому строению его можно рассматривать как упрощенный аналог природного алкалоида физостигмина. Прозерин применяют при миастениях, двигательных нарушениях после травм мозга, после перенесенного менингита, полиомиелита, энцефалита и т. п. N-диметилметаниловая кислота является ключевым веществом в синтезе прозерина:
Сульфирование ведут 30%-ным олеумом. Естественно, что при этом диметиламиногруппа протонируется и превращается в сильный электроноакцепторный мета-ориентирующий заместитель. По окончании сульфирования массу нейтрализуют гашеной известью, а затем переводят кальциевую соль в натриевую действием соды.
Олеум и серную кислоту нестандартных концентраций готовят путем смешения стандартного сырья в необходимых пропорциях. При этом необходимо учитывать тепловой эффект процесса смешения. Процесс приготовления кислоты нужной концентрации следует вести так, чтобы температура в массе не превышала 50-60°С, так как при более высокой температуре усиливается коррозия, а при смешении олеума происходит также испарение серного ангидрида.
В рассмотренном выше примере удалось получить целевой продукт прямым сульфированием ароматического амина, поскольку было необходимо ввести сульфогруппу в мета-положение к аминогруппе. Ввести таким образом сульфогруппу в орто- или пара-положение к аминогруппе прямым сульфированием невозможно, так как протонированная аминогруппа будет мешать электрофильной атаке по о— и п-положениям ароматического кольца. В этом случае необходимо предварительно защитить аминогруппу (например, ацилировать), затем провести сульфирование и, после этого, снять защиту аминогруппы.
Другим способом получения о— и п-аминосульфокислот ароматического ряда является «сульфирование запеканием». Метод заключается в том, что сначала при обработке амина разбавленной серной кислотой получают соль амина, которую выделяют и при нагревании до 160-190°С («запекании») перегруппировывают в о— или п-аминосульфокислоту. Раньше перегруппировку сульфата амина проводили при нагревании в специальных печах (запекали). В настоящее время этот процесс проводят в среде полихлоридов бензола:
Первоначально при нагревании сульфата амина с полихлоридами бензола отгоняют азеотропную смесь воды с полихлорбензолами. Пары конденсируют, воду отделяют в отстойнике, а полихлорбензолы возвращают в реактор. Процесс ведут при температуре 180°С при кипении полихлорбензолов. По окончании процесса полихлорбензолы отгоняют, оставшуюся реакционную массу обрабатывают раствором NaOH и отгоняют острым паром остатки полихлоридов и оставшийся ароматический амин. Таким образом получают сульфаниловую кислоту (1), нафтионовую кислоту (2), 4-амино-2,5-дихлорбензол-1-сульфокислоту (3), 4-диметиламинобензол-1-сульфокислоту (4).
3.3. Основные способы выделения сульфокислот
В большинстве случаев сульфокислоты выделяются в виде солей. В качестве нейтрализующих агентов применяют соду, мел, известь, сульфит натрия и щелочь. В редких случаях используют высаливание хлоридом или сульфатом натрия. Однако последний метод никогда не дает хорошего выхода продукта.
При нейтрализации сульфомассы содой или сульфитом натрия происходят следующие реакции:
Образующиеся в результате нейтрализации сульфомассы натриевые соли сульфокислот могут находиться либо в растворе, либо в осадке. Это зависит от концентрации раствора и соотношения растворимости сульфата натрия и арилсульфоната натрия.
Нейтрализация сульфитом выгодна в тех производствах, где комбинируются процессы сульфирования с процессами щелочного плавления сульфонатов. В этом случае используемый для нейтрализации сульфомассы сульфит является отходом процесса щелочного плавления сульфоната, а образующийся при нейтрализации диоксид серы может быть использован для нейтрализации щелочного плава..
Нейтрализация карбонатом натрия безопаснее, требует более простого аппаратурного оформления, но дороже по сырьевым затратам. Следует также учесть стоимость процессов упарки водных растворов солей и сложность утилизации отходов производства.
Мел и известь являются относительно дешевым сырьем. Нейтрализация протекает в соответствии с уравнениями:
Основное отличие заключается в том, что при нейтрализации сульфомассы известью не образуется углекислый газ, что существенно облегчает ведение процесса на данной стадии. С другой стороны, мел является более дешевым сырьем, и при нейтрализации мелом сульфат кальция образуется в более легко фильтрующейся форме. Наиболее легко фильтрующаяся форма соответствует дигидрату СаSO4×2Н2О (гипс). Для образования гипса необходимо поддержание слабокислой среды и температуры 60-65°С.
С целью уменьшения потерь продукта промывные воды, получающиеся при промывке осадков, используют для приготовления меловой суспензии.
Большие трудности вызывает утилизация отходов производства, так как для использования СаSO4, Na2SO4, Na2SO3 нужна их предварительная очистка.
3.4.Сульфирование триоксидом серы и его растворами в инертных растворителях
Стандартные методы сульфирования часто оказываются непригодными для введения сульфогруппы в молекулу лекарственного вещества. Это связано либо с химической лабильностью субстрата и его деструкцией под действием серной кислоты (фуран, тиофен, пиррол, индол и т. п.; углеводы, стероиды, и т. д. и т. п.), либо с сильной дезактивацией субстрата в кислой среде (амины, азолы, пиридины, пиримидины и т. п.).
Серный ангидрид (триоксид серы) является очень энергичным сульфирующим агентом, пригодным для сульфирования малоактивных соединений.
Молекула SO3 существует в виде мономерной, тримерной и полимерной форм:
С большей частью электронодонорных растворителей (эфиры, амины, алкилфосфаты и др.) триоксид серы образует комплексы с переносом заряда (КПЗ), которые также являются сульфирующими агентами (см. 3.5.).
Активность серного ангидрида зависит от полярности среды, которая влияет на поляризацию молекулы триоксида серы и величину +d заряда на атоме серы:
Полярность среды влияет также и на механизм реакции. В полярных средах (например, жидком SO2, 1-фтор-2-хлорэтане) механизм сульфирования принципиально не отличается от рассмотренного выше. В неполярных инертных средах (1,2-дихлорэтан, тетрахлорэтан, метиленхлорид) сульфирование проходит по пиросульфатному механизму,
Серный ангидрид может поступать на предприятие в жидком стабилизированном виде в баллонах под давлением либо получаться непосредственно на предприятии обжигом пирита и последующим каталитическим окислением SO2 в SO3. Последний способ практикуется на производствах большой мощности, например, на заводах по синтезу поверхностно-активных веществ (ПАВ) сульфированием (сульфатированием) первичных спиртов, олефинов, алкилбензолов и т. п.
При отсутствии стабилизированного серного ангидрида и малом тоннаже продукции, что имеет место в химико-фармацевтических производствах, триоксид серы получают десорбцией его из высокопроцентного олеума при нагревании. Остающаяся после десорбции серного ангидрида 100%-ная серная кислота может быть использована в других производствах.
Перспективным является использование растворов серного ангидрида в сернистом ангидриде. Сульфирование ведут в жидком сернистом ангидриде при температуре его кипения (-10°С). Отвод тепла осуществляется за счет испарения растворителя. Ароматические соединения, как правило, хорошо растворяются в диоксиде серы, а потому реакция протекает в гомогенной среде. Избыток серного ангидрида составляет обычно не более 5%.
Сульфирование аминов неводными растворами серного ангидрида является наиболее перспективным методом введения сульфогруппы в молекулу ряда биологически активных аминов, используемых при синтезе лекарственных субстанций, так как процесс в этом случае может быть проведен без деструкции субстрата вследствие высокой температуры и кислотности среды.
3.5.Сульфирование комплексными соединениями триоксида серы
В связи с этим серный ангидрид легко вступает в различные химические взаимодействия, в том числе в реакции сульфирования и комплексообразования. Химическая активность серного ангидрида в качестве акцептора в реакциях комплексообразования и сульфирования объясняется атакой кислого атома (S) богатых электронами (основных) систем.
В тех случаях, когда отрицательный заряд локализован на одном из атомов (например, p-электроны гетероатома), присоединение происходит быстро и со значительным выделением тепла. Если отрицательный заряд делокализован, основная реакция сопровождается протеканием различных побочных процессов.
С органическими основаниями серный ангидрид реагирует как кислота Льюиса, образуя стабильные аддукты:
Оказалось, что тепловой эффект присоединения второй молекулы триоксида серы (171,3 кДж/моль) лишь немного меньше теплоты присоединения первой молекулы (175,4 кДж/моль), что свидетельствует в пользу структуры
которая предполагалась рядом авторов. Тепловой эффект присоединения третьей молекулы SO3 составляет лишь 11,7 кДж/моль.
Наиболее устойчивыми и наименее реакционноспособными являются комплексные соединения, в которых донором электронов выступает атом азота (пиридин и третичные амины).
Комплексы серного ангидрида характеризуются специфичной устойчивостью и реакционной способностью, которые зависят от основности и строения комплексообразователей, а также от свойств среды и ряда других факторов. На практике их в основном используют в качестве сульфирующих агентов для ацидофобных субстратов.
Комплексы NAlk3.SO3 в неводных растворах практически недиссоциированы. Поэтому для успешного проведения реакции во многих случаях требуется дополнительное введение веществ, способствующих поляризации комплекса и активации субстрата.
3.6.Сульфирование хлорсульфоновой кислотой
Важное место среди сульфирующих агентов занимает хлорсульфоновая кислота. Применение этого реагента позволяет получать в зависимости от условий проведения процесса либо сульфокислоты, либо их хлорангидриды (сульфохлориды).
Доказано, что хлорсульфоновая кислота является полухлорангидридом серной кислоты и соответствует формуле:
хотя ранее некоторые исследователи рассматривали ее как комплексное соединение триоксида серы и хлорида водорода SO3.HCl. Температура плавления хлорсульфоновой кислоты (-80)°С, температура кипения 155°С (с разл.). Хлорсульфоновая кислота является более сильной кислотой, чем серная. Следует считать, что при сульфировании хлорсульфоновой кислотой имеет место взаимодействие субстрата не только с серным ангидридом
но и с катионом HSO3Å
Последнее можно рассматривать как кислотно-катализируемое сульфирование SO3.
Хлорсульфоновая кислота бурно реагирует с водой, образуя H2SO4 и HCl. Тепловой эффект такого взаимодействия велик, так как складывается из теплового эффекта трех экзотермических реакций: образования H2SO4 и HCl и взаимодействия последних с водой. В связи с этим хлорсульфоновая кислота является опасным реагентом: она вызывает ожоги кожи и тяжелые поражения дыхательных путей.
Для образования сульфокислот следует использовать эквимольное по отношению к субстрату количество хлорсульфоновой кислоты, так как при использовании избытка HSO3Cl образуются хлорангидриды сульфоновых кислот (сульфохлориды):
Такой метод проведения процесса неудобен технологически вследствие образования вязкой реакционной массы и выделения газообразного HCl. Поэтому реакцию предпочитают проводить в среде инертного растворителя (метиленхлорид, дихлорэтан, хлороформ, тетрахлорэтан и т. п.).
Сульфирование хлорсульфоновой кислотой является хорошим методом введения сульфогруппы в молекулу арена, так как не связано с использованием избытка реагента и, как правило, приводит к получению продукта с высоким выходом при высокой селективности процесса. Однако, вследствие опасности работы с хлорсульфоновой кислотой, этот метод редко используется в промышленных синтезах.
3.8. Получение хлорангидридов сульфоновых кислот
3.8.1. Общие сведения о реакции
Реакция сульфохлорирования, т. е. введения группы SO2Cl в молекулу органического соединения, используется как для получения сульфохлоридов RSO2Cl, так и сульфокислот последующим гидролизом сульфохлоридов. Последний способ является одним из основных при получении алкилсульфокислот.
Значение реакции сульфохлорирования в синтезе лекарственных веществ обусловлено тем, что сульфохлориды являются важными промежуточными продуктами в синтезе сульфаниламидных препаратов.
Как уже указывалось (с. ), при взаимодействии эквимолекулярного количества хлорсульфоновой кислоты с ароматическими углеводородами образуются сульфокислоты:
Сульфохлорирование ароматических соединений хлорсульфоновой кислотой проходит лишь при значительном избытке последней (4-6 кратным). Действие на ароматические соединения избытком хлорсульфоновой кислоты при температуре не выше 100°С является основным методом получения ароматических сульфохлоридов, которые используются для получения амидов, анилидов, эфиров сульфокислот, а также ароматических сульфиновых кислот и др. соединений:
Известны и другие способы получения сульфохлоридов..
Прямое сульфохлорирование возможно благодаря образованию катиона SO2Cl+ при диссоциации хлорсульфоновой кислоты по уравнению:
В качестве побочных продуктов при сульфохлорировании помимо сульфокислот могут образовываться сульфоны:
Процесс сульфохлорирования можно вести как непрерывным, так и периодическим способом. Периодический метод применяется значительно чаще. Аппараты для проведения сульфохлорирования практически не отличаются от сульфураторов. Следует, однако, иметь в виду, что выделение хлорида водорода в процессе сульфохлорирования создает повышенную опасность коррозии оборудования, поэтому применение эмалированных аппаратов предпочтительно. Кроме того, использование змеевиков в таких аппаратах опасно, так как при их разъедании и попадании воды в сульфомассу возможен выброс последней вследствие бурной реакции хлорсульфоновой кислоты с водой:
Выделяющийся в процессе реакции хлорид водорода улавливают водой в поглотительной системе.
Сульфохлориды, как правило, не растворяются или плохо растворяются в холодной воде, поэтому их выделяют при выливании сульфомассы на лед или воду, охлаждаемую льдом или рассолом. Перегрев может привести к гидролизу сульфохлорида:
Наибольшее промышленное значение имеет процесс сульфохлорирования фенилуретилана:
Реакцию проводят при температуре 42-45°С и избытке хлорсульфоновой кислоты в 5,3-5,5 раза. Выход сульфохлорида при этом составляет 82-83%.
Вторым по значимости является производство п-ацетанилидсульфохлорида:
п-Толуолсульфохлорид получается при производстве сахарина и используется в синтезе лекарственного препарата этамид.