Для чего назначают лучевую терапию после операции
Лучевая терапия при лечении рака: виды лечения, последствия.
Показания к лечению
Лучевая терапия при лечении рака: виды лечения, последствия.
Известно, что основными методами лечения различных злокачественных новообразований являются хирургический, лекарственный, лучевой и их сочетание. При этом операция и облучение считаются методами локального воздействия на опухоль, а лекарственная терапия (химиотерапия, таргетная терапия, гормонотерапия, иммунотерапия) – системным. Ассоциация онкологов во всем мире проводит различные многоцентровые исследования, призванные ответить на вопрос: «Какому методу или их сочетанию следует отдать предпочтение в различных клинических ситуациях?» В целом, все эти исследования преследуют одну цель – увеличить продолжительность жизни больных с онкопатологией и улучшить ее качество.
Пациент должен быть проинформирован лечащим врачом о различных способах лечения, включая альтернативное воздействие. Например, больным ранним раком легкого с тяжелой сопутствующей патологией и абсолютными противопоказаниями к операции, вместо хирургического лечения можно предложить облучение новообразования (стереотаксическая лучевая терапия), так называемое, лечение рака без операции. Или, например, при определенных показаниях у больных раком печени, предстательной железы. Активно и успешно используется стереотаксическая лучевая терапия вместо операции при опухолях головного мозга, тем самым значительно снижая риск послеоперационных осложнений и ускоряя реабилитацию пациентов после лечения. В центре «ОнкоСтоп» решение о проведении лучевой терапии (ЛТ), как самостоятельного варианта, так и в составе комплексного лечения, принимается консилиумом специалистов.
Радиотерапия (radiotherapy) планируется с учетом ниже перечисленных факторов. Во-первых, это основной диагноз, т.е. локализация злокачественной опухоли и степень ее распространения в окружающие ткани и отдаленные органы. Во-вторых, это степень злокачественности, наличие лимфоваскулярной инвазии и других прогностических и предиктивных факторов, которые определяются при морфологическом, иммуногистохимическом и молекулярно-генетическом исследованиях. В-третьих, это наличие предшествующего лечения и его эффективность. И в четвертых, это, безусловно, общее состояние пациента, возраст, наличие и степень коррекции сопутствующей патологии и ожидаемая продолжительность жизни больного.
Действие лучевой терапии основано на ионизирующем облучении определенной зоны потоком частиц, которые способны повреждать генетический аппарат (ДНК) клетки. Особенно это выражено у активно делящихся клеток, так как они наиболее восприимчивы к повреждающим факторам. Происходит нарушение функций и жизнедеятельности раковых клеток, что в свою очередь останавливает их развитие, рост и деление. Таким образом, в результате радиотерапии злокачественная опухоль уменьшается в размерах вплоть до полного исчезновения. К сожалению, здоровые клетки, которые располагаются по периферии новообразования, также могут входить в зону облучения в разном объеме (в зависимости от вида используемой радиотерапии), что впоследствии отражается на степени их повреждения и развития побочных эффектов. После лечения или в перерывах между сеансами облучения здоровые клетки способны восстанавливать свои радиационные повреждения, в отличие от опухолевых. 
Виды лучевой терапии
Существуют несколько классификаций лучевой терапии. В зависимости от того, когда назначается радиотерапия, она подразделяется на: неоадъювантную (до операции), адъювантную (после операции) и интраоперационную. Целями неоадъювантного облучения являются уменьшение размеров опухоли, достижение операбельного состояния, снижение риска метастазирования по сосудам кровеносной и лимфатической системы в лимфатические узлы и отдаленные органы (например, при раке молочной железы, раке прямой кишки). Адъювантное облучение направлено на минимизацию риска возникновения местных рецидивов опухоли (например, при раке молочной железы, злокачественной опухоли головного мозга, кости). В каждом конкретном случае целесообразность назначения радиотерапии определяется индивидуально.
При выборе способа доставки дозы излучения радиотерапевт оценивает в первую очередь локализацию опухоли, ее размер, близость сосудов, нервов, критических органов. В связи с этим существуют 3 способа подведения дозы:
Рассмотрим каждый из этих видов радиотерапии более подробно.
1. ДИСТАНЦИОННАЯ ЛУЧЕВАЯ ТЕРАПИЯ
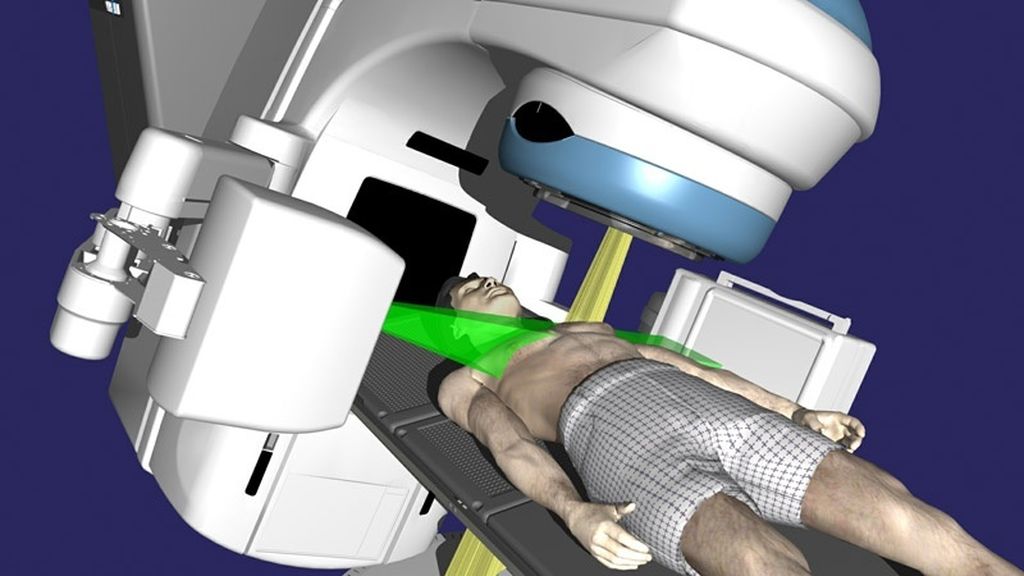
При дистанционной лучевой терапии на опухоль через кожу направляется один или несколько пучков ионизирующего излучения (генерируются линейным ускорителем), которые захватывают саму опухоль и рядом расположенные ткани, уничтожая клетки внутри основного опухолевого объема и клетки, рассеянные вблизи него. Облучение линейным ускорителем обычно проводится 5 раз в неделю, с понедельника по пятницу, на протяжении нескольких недель.
* Аппарат для проведения дистанционного лучевого лечения: линейный ускоритель Varian TrueBeam
Далее рассмотрим отдельные виды дистанционной лучевой терапии.
ТРЕХМЕРНАЯ КОНФОРМНАЯ ЛУЧЕВАЯ ТЕРАПИЯ (3D-CRT)
Как известно, организм каждого пациента уникален и опухоли также неодинаковы по форме, размеру и локализации. При трехмерной конформной лучевой терапии возможно учитывать все эти факторы. В результате использования этой методики наведение пучка становится точнее, а прилежащие к опухоли здоровые ткани получают меньше радиации и быстрее восстанавливаются.
ЛУЧЕВАЯ ТЕРАПИЯ С МОДУЛЯЦИЕЙ ИНТЕНСИВНОСТИ ПУЧКА
Лучевая терапия с модуляцией интенсивности пучка (IMRT) – это особый вид трехмерной конформной лучевой терапии, при котором можно еще больше снизить лучевую нагрузку на здоровые ткани рядом с опухолью при условии точной адаптации пучка излучения к форме новообразования. Облучение на линейном ускорителе с использованием IMRT позволяет разбить каждый пучок на множество отдельных сегментов, при этом интенсивность излучения в пределах каждого сегмента регулируется индивидуально.
ЛУЧЕВАЯ ТЕРАПИЯ ПОД КОНТРОЛЕМ ВИЗУАЛИЗАЦИИ
Лечение лучевой терапией под визуальным контролем (IGRT) – это тоже конформное облучение опухоли, при котором для наведения пучка ежедневно используются методы визуализации (например, компьютерная томография, ультразвуковое или рентгенологическое исследование), проводимые непосредственно в каньоне (специальное помещение, в котором происходит лечение) перед каждой процедурой. В связи с тем, что между сеансами облучения линейным ускорителем опухоль может смещаться (например, в зависимости от степени наполнения полого органа или в связи с дыхательными движениями), IGRT позволяет более точно «прицеливаться» в опухоль, сберегая окружающие здоровые ткани. В некоторых случаях врачи имплантируют в опухоль или близлежащие ткани маленький маркер, чтобы лучше визуализировать мишень облучения.
СТЕРЕОТАКСИЧЕСКАЯ ЛУЧЕВАЯ ТЕРАПИЯ
Стереотаксическая лучевая терапия – особый метод лечения, позволяющий подводить высокую дозу ионизирующего излучения с субмиллиметровой точностью, в отличие от классической лучевой терапии (вышеописанные методики). Это позволяет эффективно и безопасно облучать опухоли, различные по локализации и размерам (даже самые маленькие очаги), и сохранять от повреждающего действия радиации окружающие здоровые ткани. Кроме того, стереотаксическая лучевая терапия может использоваться для повторного облучения. Эффект от терапии оценивается через 2-3 месяца после ее завершения. Все это время доктор активно наблюдает за состоянием здоровья пациента.
Интересный факт: стереотаксическая лучевая терапия впервые была разработана для однократного облучения опухолей головного мозга, что называется стереотаксической радиохирургией (SRS). Кроме онкопатологий, радиохирургию можно применять в лечении доброкачественных опухолей (например, менингиома, невринома слухового нерва) и определенных неопухолевых неврологических состояний (например, невралгия тройничного нерва, не поддающаяся консервативным методам лечения). Эта методика облучения большинству людей известна под названием «Гамма Нож», «КиберНож».
* Установка для стереотаксической радиохирургии патологий головного мозга: Гамма-нож (Gamma Knife)
Лечение опухолей вне черепа (экстракраниальных локализаций) называется стереотаксической лучевой терапией тела (SBRT), обычно реализуется за несколько сеансов, используется при раке легкого, печени, поджелудочной железы, предстательной железы, почки, опухолях спинного мозга, скелета. В целом, применение стереотаксической лучевой терапии в лечении различных онкопатологий открывает новые возможности.
* Аппарат для проведения стереотаксической лучевой терапии новообразований любых локализаций: КиберНож (Accuray CiberKnife)
Лечение с помощью стереотаксической лучевой терапии на современном роботизированном аппарате «КиберНож» доступно в центре лучевой терапии «Онкостоп».
ПРОТОННАЯ ЛУЧЕВАЯ ТЕРАПИЯ.
Протонная терапия является особым видом дистанционной лучевой терапии, при которой используются протоны. Физические свойства пучка протонов позволяют радиотерапевту более эффективно снижать дозу радиации в близко расположенных к опухоли нормальных тканях. Имеет узкий спектр применения (например, при опухолях головного мозга у детей).
* Аппарат для проведения протонной лучевой терапии: Varian ProBeam
НЕЙТРОННАЯ ЛУЧЕВАЯ ТЕРАПИЯ.
Нейтронное облучение также является особым видом дистанционной лучевой терапии, при которой используется нейтронное излучение. В клинической практике широко не используется.
2. КОНТАКТНАЯ ЛУЧЕВАЯ ТЕРАПИЯ (БРАХИТЕРАПИЯ)
Контактная ЛТ подразумевает временное или постоянное размещение радиоактивных источников внутри опухоли или в непосредственной близости от нее. Существует две основные формы брахитерапии – внутриполостная и внутритканевая. При внутриполостной лучевой терапии радиоактивные источники размещаются в пространстве рядом с опухолью, например, в канале шейки матки, влагалище или трахее. При внутритканевом лечении (например, рака предстательной железы) радиоактивные источники устанавливаются непосредственно в ткани (в предстательную железу). Ещё один вариант брахитерапии – это аппликационная форма, когда источники размещаются на поверхности кожи в специальные индивидуально адаптированные аппликаторы (например, для лечения рака кожи). Брахитерапия может быть назначена как изолированно, так и в комбинации с наружным облучением.
В зависимости от методики контактной ЛТ, ионизирующее излучение может подводиться с высокой мощностью дозы (high dose rate, HDR) или низкой (low dose rate, LDR). При высокодозной брахитерапии источник излучения размещается в опухоль временно посредством (тонкой) трубки – катетера. Установка катетера – это хирургическая манипуляция, требующая анестезии. Курс лечения обычно реализуется за большое количество сеансов (фракций), в режиме 1-2 раза в день или 1-2 раза в неделю. При низкодозной брахитерапии радиоактивные источники могут устанавливаться в опухоль временно или постоянно, что также требует хирургического пособия, анестезии и кратковременного пребывания в стационаре. Пациенты, которым установлены постоянные источники, в первое время после облучения ограничены в своей повседневной жизни, однако со временем восстанавливаются и возвращаются к прежнему ритму.
“Зерно” с радиоактивным материалом, вживляемых в опухоль при брахитерапии
СИСТЕМНАЯ ЛУЧЕВАЯ ТЕРАПИЯ
В некоторых клинических случаях пациентам назначается системная лучевая терапия, при которой радиоактивные препараты вводятся в кровоток и затем распределяются по всему организму. Их можно вводить через рот (радиоактивные таблетки) или через вену (внутривенное введение). Например, капсулами радиоактивного йода (I-131) лечатся некоторые виды рака щитовидной железы. Внутривенное введения радиоактивных препаратов эффективно при лечении боли, обусловленной наличием костных метастазов, например, при раке молочной железы.
Различают несколько этапов ЛТ: подготовительный (предлучевой), лучевой и восстановительный (постлучевой). Рассмотрим более подробно каждый этап терапии.
Подготовительная стадия начинается с первичной консультации радиотерапевта, который определяет целесообразность проведения лучевой терапии и выбирает методику. Следующим шагом является разметка опухоли, расчет дозы радиоактивного облучения и его планирование, в котором участвует радиотерапевт, медицинский физик и рентгенолаборант. При планировании лучевой терапии определяются область облучения, разовая и суммарная дозы радиации, максимум ионизирующего излучения, который приходится на опухолевую ткань и окружающие ее структуры, оценивается риск побочных эффектов. При необходимости выполняется маркирование опухоли (т.е. в нее имплантируются специальные маркеры), помогающее в дальнейшем отслеживать ее при дыхании. В некоторых случаях разметка границ облучения осуществляется специальным маркером, который нельзя стирать с кожи до завершения лечения. Если разметка стерлась в результате неосторожного обращения или после гигиенических процедур, то ее следует обновить под контролем лечащего врача. Перед лечением необходимо защищать кожу от прямого попадания солнечных лучей, не использовать косметику, раздражающие вещества, антисептики (йод). При кожных заболеваниях, аллергических проявлениях целесообразна их коррекция. При планировании облучения опухолей головы и шеи необходимо вылечить больные зубы и заболевания полости рта (например, стоматит).
Непосредственно сам процесс облучения сложный, и проводится согласно индивидуальному плану лечения. Он состоит из фракций (сеансов) ЛТ. Длительность и расписание фракций облучения индивидуальна в каждом случае, и зависит только от плана, который был составлен специалистами. Например, при стереотаксической радиохирургии лечение составляет одну фракцию, а при дистанционной лучевой терапии курс длится от одной до нескольких недель и осуществляется в течение недели пять дней подряд. Затем следует два дня перерыва для восстановления кожных покровов после проведенного облучения. В некоторых случаях, суточную дозу радиотерапевт разделяет на 2 сеанса (утром и вечером). Облучение проходит безболезненно в специальном помещении – каньоне. Перед лечением проводится подробный инструктаж техники безопасности. Во время терапии пациент должен находится в каньоне в неподвижном состоянии, дышать ровно и спокойно, с больным поддерживается двусторонняя связь посредством громкоговорителя. Оборудование во время сеанса лечения может создавать специфический шум, что является нормальным и не должно пугать пациента.
*Каньон Центра лучевой терапии проекта «ОнкоСтоп»
На протяжении всего курса лечения необходимо придерживаться следующих рекомендаций.
Особенности лучевой терапии опухолей различных локализаций
При раке молочной железы лучевая терапия используется после органосохраняющего хирургического вмешательства или после мастэктомии по показаниям (наличие метастатических регионарных лимфатических узлов, опухолевые клетки в краях операционного материала и др.). Используемая дистанционная радиотерапия в этих случаях имеет цель элиминировать (уничтожить), возможно оставшиеся в ране опухолевые клетки, тем самым снижая риск локального рецидива. При местно-распространенном раке молочной железы облучение может быть назначено и до хирургического лечения с целью достижения операбельного состояния. Во время лечения женщин могут беспокоить такие жалобы, как утомляемость, отечность и изменение цвета кожи молочной железы (так называемое «бронзирование»). Однако, эти симптомы обычно исчезают сразу или в течение 6 месяцев после завершения лучевой терапии.
При лечении рака прямой кишки активно используют лучевую терапию до операции, поскольку она позволяет уменьшить объем операции и снизить риск метастазирования опухоли в дальнейшем (во время хирургического вмешательства и после него). Сочетание облучения и химиотерапии приводит к увеличению эффективности терапии этой категории пациентов.
При раке женских половых органов применяется как дистанционное облучение органов малого таза, так и брахитерапия. Если при I стадии рака шейки матки лучевая терапия может назначаться по определенным показаниям, то при II, III, IVA стадиях облучение совместно с химиотерапией является стандартом лечения этой когорты больных.
Восстановительный (постлучевой) период
Постлучевой период начинается сразу после окончания облучения. В большинстве случаев пациенты активно не предъявляют жалобы и чувствуют себя относительно удовлетворительно. Однако некоторых больных могут беспокоить побочные эффекты, которые различаются по степени своей выраженности в каждом конкретном случае. При появлении нежелательных реакций необходимо сразу обратиться к врачу.
Восстановительный период (реабилитация) заключается в соблюдении щадящего режима дня и полноценного питания. Важное значение имеет эмоциональный настрой больного, помощь и доброжелательное отношение к нему близких людей, правильное соблюдение предписанных рекомендаций (контрольное обследование).
Усталость при облучении обусловлена повышенным уровнем энергозатрат и сопровождается различными метаболическими изменениями. Поэтому, если пациент активно работает, то ему лучше перейти на легкий труд или уйти в отпуск для восстановления сил и здоровья.
После завершения курса лучевой терапии необходимо регулярно посещать врача для контроля за состоянием здоровья и оценки эффективности лечения. Динамическое наблюдение осуществляется онкологом в районной поликлинике, онкодиспансере, частной клинике по желанию больного. В случае ухудшения состояния здоровья, развития болевого синдрома, появлении каких-либо новых жалоб, связанных, например, с нарушением функции желудочно-кишечного тракта, мочеполовой системы, сердечно-сосудистых и дыхательных нарушений, повышением температуры тела, следует обращаться к врачу, не дожидаясь очередного запланированного визита.
Особую роль играет правильный уход за кожей, которая легко поддается повреждающему действию радиации (особенно при дистанционной лучевой терапии). Необходимо часто пользоваться питательным жирным кремом, даже в отсутствии признаков воспаления и ожога кожного покрова. В период облучения и после него нельзя посещать бани или ванны, пользоваться жесткими мочалками, скрабами. Лучше принимать душ и использовать мягкие питательные и увлажняющие косметические средства.
Многие считают, что пациенты, перенесшие лучевую терапию, могут сами излучать радиацию, поэтому им целесообразно минимизировать общение с окружающими людьми, особенно с беременными женщинами и детьми. Однако, это заблуждение. Облученные больные не представляют опасности для окружающих. Не стоит отказываться по этой причине и от интимных отношений. При изменении состояния слизистых оболочек половых путей и возникновении неприятных ощущений следует рассказать об этом врачу, он подскажет, как с этим бороться.
Некоторые больные испытывают стресс, в связи с чем необходимо правильно организовать свой досуг: кино, театр, музеи, выставки, концерты, встреча с друзьями, прогулки на свежем воздухе и различные общественные мероприятия на ваш выбор.
Лучевые повреждения кожи, такие как покраснение (со временем оно проходит, иногда оставляя после себя пигментацию), сухость, зуд, жжение, шелушение в зоне облучения. При правильном уходе кожные покровы восстанавливаются в течение 1-2 месяцев после лучевой терапии. В ряде случаев при выраженном лучевом повреждении развиваются ожоги разной степени выраженности, которые впоследствии могут инфицироваться.
Инфекционные осложнения, риск их возникновения повышается при сахарном диабете, наличии сопутствующей патологии кожи, при высокой дозе радиации, светлом типе кожи.
Чтобы избежать подобных осложнений, необходимо строго соблюдать предписанные рекомендации лечащего врача и правильно осуществлять уход за кожей.
Лучевые повреждения слизистой оболочки облучаемой области. Например, при облучении опухолей головы и шеи возможно повреждение слизистой полости рта, носа, гортани. В связи с этим, пациентам необходимо соблюдать некоторые правила:
При лучевом лечении опухолей прямой кишки может появиться склонность к запорам, примесь крови в кале, боль в области ануса и животе, поэтому важно соблюдать диету (исключить «закрепляющие» продукты).
При облучении органов малого таза больные могут предъявлять жалобы на расстройство мочеиспускания (болезненность, жжение, затруднение мочеиспускания).
Осложнения со стороны дыхательной системы: кашель, затрудненное дыхание, болезненность и отек кожи грудной стенки. Может наблюдаться при лучевой терапии опухолей грудной клетки, легкого, молочной железы.
О любом ухудшении самочувствия, появлении вышеперечисленных изменений, необходимо проинформировать об этом лечащего врача, который назначит соответствующее сопроводительное лечение согласно выявленным нарушениям.
В целом, лучевая терапия в большинстве случаев переносится пациентами хорошо, и после нее больные быстро восстанавливаются. Облучение является важным этапом в комплексном лечении злокачественных новообразований, позволяя с еще большей эффективностью воздействовать на опухоль, что в свою очередь приводит к увеличению продолжительности жизни больных и повышению ее качества.
Специалисты центра лучевой терапии проекта «ОнкоСтоп» успешно владеют всеми видами дистанционной лучевой терапии, включая стереотаксическую, и бережно заботятся о здоровье своих пациентов.
Что такое лучевая терапия? Словарь радиотерапевта
Елена Ивановна Тюряева, онколог и радиотерапевт НМИЦ онкологии им. Н.Н. Петрова, рассказала о возможностях современной лучевой терапии и ее значении в борьбе с онкологическими заболеваниями.
Когда появилась лучевая терапия?
В 1896 году в Вене доктор Фройнд впервые в мире применил рентгеновское излучение не для диагностики заболевания, а для лечения поверхностно расположенного доброкачественного образования. Несколькими годами позднее супруги Пьер и Мария Кюри открыли радиоактивный радий, который стал использоваться для контактной радионуклидной терапии.
За 125 лет лучевая терапия, проделав огромный путь совершенствования, получила широкое применение и вышла на качественно новый уровень. По мнению экспертного сообщества, в настоящее время не менее 60-70 % всех онкологических пациентов нуждается в лучевой терапии.
Что такое лучевая терапия?
Лучевая терапия – это процесс использования ионизирующего излучения для лечения различных заболеваний, прежде всего, онкологических. Это один из самых высокотехнологичных методов терапии, объединяющий инженерно-технические разработки, физико-математические модели и достижения информационных технологий. Лучевая терапия требует специалистов-радиотерапевтов знаний в области биологии, анатомии, радиобиологии, лучевой диагностики и общей онкологии.
Цели лучевой терапии
Задача лучевой терапии – достижение максимально возможного воздействия на опухоль и зоны ее клинического и субклинического распространения с высокой степенью точности и минимальными последствиями для окружающих тканей и органов. Цель лучевой терапии – разрушение опухолевой массы, в идеале приводящее к ее ликвидации или уменьшению размеров и метастатического потенциала, замедлению роста, что способствует продлению жизни и улучшению ее качества.
Лучевая терапия может использоваться на разных этапах лечения:
Предоперационная лучевая терапия
Задача предоперационной лучевой терапии — максимальное уменьшение объема опухоли, предотвращение попадания опухолевых клеток в лимфатическую или кровеносную систему, снижение риска развития отдаленных метастазов. При большинстве типов опухолей наиболее часто используется тандем лучевой и химиотерапии. Такое комбинированное воздействие позволяет в дальнейшем выполнить радикальное вмешательство с полным удалением новообразование. В ряде случаев предоперационная лучевая/химиолучевая терапия может приводить к полному регрессу опухоли, таким образом оказываясь самостоятельным методом лечения. Достижение полного клинического регресса, доказанное рентгенологическими методами (КТ, МРТ, ПЭТ-КТ) и подкрепленное данными биопсии, увеличивает возможность отсрочки или отказа от операции. Так, для опухолей прямой кишки, с полным клиническим ответом на химиолучевую терапию, получила признание концепция «waitandsee», т.е. «жди и наблюдай», закрепленная в международных и национальных стандартах лечения.
Интраоперационная лучевая терапия
Интраоперационная лучевая терапия – это облучение ложа опухоли сразу же после удаления ее хирургическим путем, непосредственно в операционном поле. Это действенный метод снижения риска развития местного рецидива. Интраоперационная лучевая терапия используется при опухолях молочной железы, при саркомах мягких тканей и даже при новообразованиях ЖКТ. Этот метод очень эффективен, но не лишен недостатков. Во-первых, для ее проведения необходимы специальные мобильные и компактные лучевые установки, которые могут располагаться в операционной. Во-вторых, однократная доза облучения может оказаться недостаточной, а объем интраоперационно облучаемых тканей достаточно ограничен. Интраоперационная лучевая терапия не позволяет воздействовать на пути лимфоотока. Трудно обеспечить точность дозиметрического планирования. Лучевая процедура увеличивает время пребывания пациента под наркозом и общую продолжительность вмешательства. Поэтому чаще интраоперационная лучевая терапия является составной частью сочетанного облучения, этапом комплексного лечения.
Послеоперационная лучевая терапия
Послеоперационная лучевая терапия – это воздействие на зону удаленной опухоли и пути лимфооттока для того, чтобы предотвратить возможность распространения отдельных опухолевых клеток в ходе хирургического вмешательства, т.е. снижения рисков развития местных и отдаленных метастазов. Послеоперационная лучевая терапия бывает необходима и после обширных операций, и после малоинвазивных вмешательств. В настоящее время наиболее часто применяется в лечении рака молочной железы, сарком мягких тканей, опухолей головы и шеи.
Самостоятельная или дефинитивная лучевая терапия
Самостоятельная лучевая/химиолучевая терапия показана в тех случаях, когда ее эффективность сравнима с радикальным оперативным лечением, т.е. при раннем раке, или, напротив, когда радикальное вмешательство невозможно – при наличии общих противопоказаний или из-за распространенности опухоли. В настоящее время рассматривается в качестве альтернативного метода лечения ранних опухолей голосового отдела гортани, ряда новообразований кожи. Наибольшее применение нашла в лечении рака предстательной железы. В сочетании с химиотерапией успешно используется при ранних опухолях пищевода, анального канала. Химиолучевое лечение является ведущим методом лечения рака шейки матки.
Наконец, лучевая терапия применяется для устранения симптомов опухолевого заболевания, таких, как боль, нарушение глотания и др. (симптоматическая лучевая терапия) или сдерживания опухолевого процесса (паллиативная лучевая терапия).
Технология лучевой терапии
Последовательность лечебных мероприятий для каждого больного принимается на онкологическом консилиуме в составе хирурга-онколога, химиотерапевта и радиотерапевта. Определив показания к лучевому лечению, врач-радиотерапевт формулирует общий план лечения: продолжительность курса, режим фракционирования дозы (доза за один сеанс облучения), суммарную дозу облучения, необходимость одновременного химиолучевого лечения, применения радиомодификаторов. Проведению сеансов облучения предшествуетэтап предлучевой подготовки.
Предлучевая подготовка включает:
Компьютерная топометрия
Создание индивидуальной дозиметрической карты облучения начинается с компьютерной топометрии, которую проводит врач-рентгенолог совместно с радиотерапевтом. На компьютерном томографе-симуляторе, с теми же фиксирующими приспособления и в том же положении, в котором будет проводиться лечение, сканируется область анатомического расположения опухоли (грудная клетка, брюшная полость, головной мозг и т.д.). Оцениваются структурные и анатомические особенности — локализация опухоли, протяженность объема, взаимоотношение со смежными органами, плотность внутренних тканей. Во время этой процедуры на кожу больного выносятся графические ориентиры –метки для центрации пучков излучения, которые в дальнейшем позволят ускорить навигацию в процессе проведения сеансов лечения. Последовательность компьютерных сканов передается на планирующую станцию для создания индивидуального плана облучения.
Контуринг мишени и смежных органов
Дальше наступает этап обработки полученных изображений. Сканы импортируются в планирующую систему, где врач-радиотерапевт с помощью врача-рентгенолога производит выделение очертаний (оконтуривание) опухолевой мишени, всех смежных органов в каждом полученном скане. На основании совокупности объемных изображений в дальнейшем производится расчет дозных нагрузок в ходе лечения на опухоль и соседние органы с учетом их толерантности к облучению.
Дозиметрическое планирование
После завершения оконтуривания, оценки расположения опухоли и смежных органов, наступает этап дозиметрического планированиякурса лучевого лечения, который выполняется медицинскими физиками.Дозиметрическое планирование – это подбор количества и условий формирования пучков излучения, их пространственного размещения для того, чтобы подвести к опухоли максимально возможную терапевтическую дозу с минимальными последствиями для соседних органов. Современные медицинские ускорители, обладающие многолепестковыми коллиматорами, позволяют формировать поля сложной конфигурации, максимально точно соответствующие объему и форме облучаемой мишени, производя т.н. конформное облучение. Исходя из поставленных задач, оптимальный охват мишени может быть спланирован с использованием 3D многопольного облучения с объемно-модулируемой интенсивностью (IMRT) или дуговой модулируемой интенсивностью пучка излучения (VMAT).
На изображении представлен пример 3D многопольного излучения. Видно, что для облучения опухоли используется 3 пучка.
Средства иммобилизации пациента
Для того, чтобы осуществлять точную подачу ионизирующего излучения к облучаемой мишени, необходимо четко воспроизводить то положение, в котором шел процессе подготовки к лучевому лечению, т.е. компьютерная топометрия и дозиметрическое планирование. Это обеспечивается разнообразными средствами для укладки, иммобилизации пациента. Они могут быть в виде разных штатных дек с подголовниками, креплениями, валикамии подставками для рук, ног, таза. Есть и индивидуальные средства. Например, вакуумные матрасы и термопластические маски, фиксирующие индивидуальные формы тела пациента в положении облучения. Эти приспособления позволяют избегать смещения облучаемой зоны из-за непроизвольных движений пациента.
Виды лучевой терапии
Дистанционная лучевая терапия
При дистанционном облучении источник ионизирующего излучения находится на расстоянии — вне тела пациента и вне опухолевой мишени. В зависимости от типа излучающего аппарата дистанционная лучевая терапия включает в себя рентгенотерапию, телегамматерапию, электронную и протонную терапию. Наиболее распространенным вариантом дистанционной лучевой терапии в настоящее время является облучение высокоэнергетическими фотонами и пучками электронов на медицинских ускорителях электронов. Современные модели ускорителей с помощью компьютерного управления параметрами и геометрией пучка излучения обеспечивают максимальное соответствие формы очага-мишени и распределения в нем дозы облучения. Возможность формирования пучков тормозного (фотонного) и корпускулярного (электронного) излучения с различной мощностью — от 6 МэВ до 18-20 МэВ — позволяет облучать как поверхностные, так и расположенные глубоко в тканях тела объекты.
Особое внимание в настоящее время приковано к протонной терапии. Первый в России клинический центр протонной терапии был построен в Санкт-Петербурге. Преимущество метода состоит в особенности тяжелых заряженных частиц (протонов). Протоны максимально высвобождают энергию торможения в конце пути своего пробега, причем спад дозы от 90% до 20% происходит на дистанции 2-5 мм. Такая возможность концентрации дозы в конце пробега частицы позволяет не только наилучшим образом сконцентрировать дозу, но и минимизировать лучевую нагрузку на ткани по ходу пучка и за патологическим очагом. Протонная терапия актуальна в онкоофтальмологии, радионейрохирургии, и особенно для пациентов детского возраста. В настоящее время сфера применения протонной терапии расширяется, однако пока использование метода существенно ограничивается его высокой стоимостью.
Современной технологией дистанционного облучения является стереотаксическая лучевая терапия – метод высокопрецизионного крупнофракционного облучения опухолей размером не более 5 см. В отличие от радиохирургии, разработанной для лечения опухолей головного мозга, использующей однократное облучение, общее число фракций при стереотаксическом облучении варьирует от 1 до 5-6. Разовая очаговая доза составляет от 8 Гр до 20 Гр, суммарная эквивалентная поглощенная доза от 50 Гр до 150 Гр, что существенно выше, чем при классическом варианте фракционирования лучевой терапии. Гамма-нож — один из видов лучевых установок для стереотаксического облучения новообразований головного мозга. Ускорители с микролепестковыми коллиматорами позволяют производить стереотаксическое облучение любых очагов (головной мозг, предстательная железа, легкое, кости, печень, поджелудочная железа, лимфоузлы, мягкие ткани). При стереотаксическом облучении обязательно учитываются смещения очага, возникающие при дыхании. Для этого запись КТ-изображений при КТ-симуляции производится с синхронизацией дыхательного цикла (4D лучевая терапия).
Контактная лучевая терапия
При контактной лучевой терапии или брахитерапии, источник излучения вводится внутрь пораженного органа. Преимущества такого вида терапии – это короткий курс, высокая точность и низкая нагрузка на смежные органы, что очень важно для дальнейшего качества жизни пациентов. Для брахитерапии используются различные радиоактивные источники – изотопы кобальта (Co⁶⁰), иридия (Ir¹⁹²), цезия (Cs¹³⁶).
Контактная лучевая терапия имеет разновидности: аппликационная, внутриполостная, внутритканевая и радионуклиднаялучевая терапия.
Аппликационная лучевая терапия
При аппликационной лучевой терапии источник располагается на поверхности облучаемого наружного объекта (кожа).
Внутриполостная лучевая терапия
При внутриполостной лучевой терапии источник подводят напрямую к опухоли в полости органа. Наиболее часто применяется при раке прямой кишки, анального канала, пищевода, при внутрибронхиальных образованиях. Внутриполостная или внутрипросветная брахитерапия чаще используется как этап сочетанной лучевой терапии, до или после дистанционного облучения. Однако нередко брахитерапия как самостоятельный метод достаточна после малоинвазивных операций при ранних стадиях рака. При паллиативном лечении рака пищевода брахитерапия — эффективный способ устранения дисфагии (расстройства акта глотания).
Внутритканевая лучевая терапия
При внутритканевой лучевой терапии источник вводят в ткани самой опухоли. Внутритканевая брахитерапия наиболее распространена при опухолях предстательной железы, широко используется при облучении молочной железы, при опухолях головы и шеи и при новообразованиях в печени.
Радионуклидная лучевая терапия
Перспективы лучевой терапии
Основными векторами дальнейшего развития лучевой терапии являются усовершенствование методик визуально ориентированного подведения дозы, влияние на радиочувствительность опухолевых клеток с помощью радиомодификаторов, применений комбинаций лучевого лечения с новыми химио- и иммунотерапевтическими агентами.
Беседовала
Анастасия Башкова
практикант отдела по связям с общественностью НМИЦ онкологии им. Н. Н. Петрова
Санкт-Петербургский государственный университет
Высшая школа журналистики и массовых коммуникаций