Для чего нужен железистый эпителий
Эпителиальные ткани
Анатомия
Гистология
Отлично зная анатомию и гистологию, вы легко сможете отличить патологическое состояние органа от здорового, будете понимать механизмы развития многих болезней. Приглашаю вас совершить увлекательное путешествие по человеческому организму, в путь! 🙂
Группы тканей
Все ткани делятся на четыре морфофункциональные группы:
Эти группы (кроме нервной ткани) подразделяют на те или иные виды тканей.
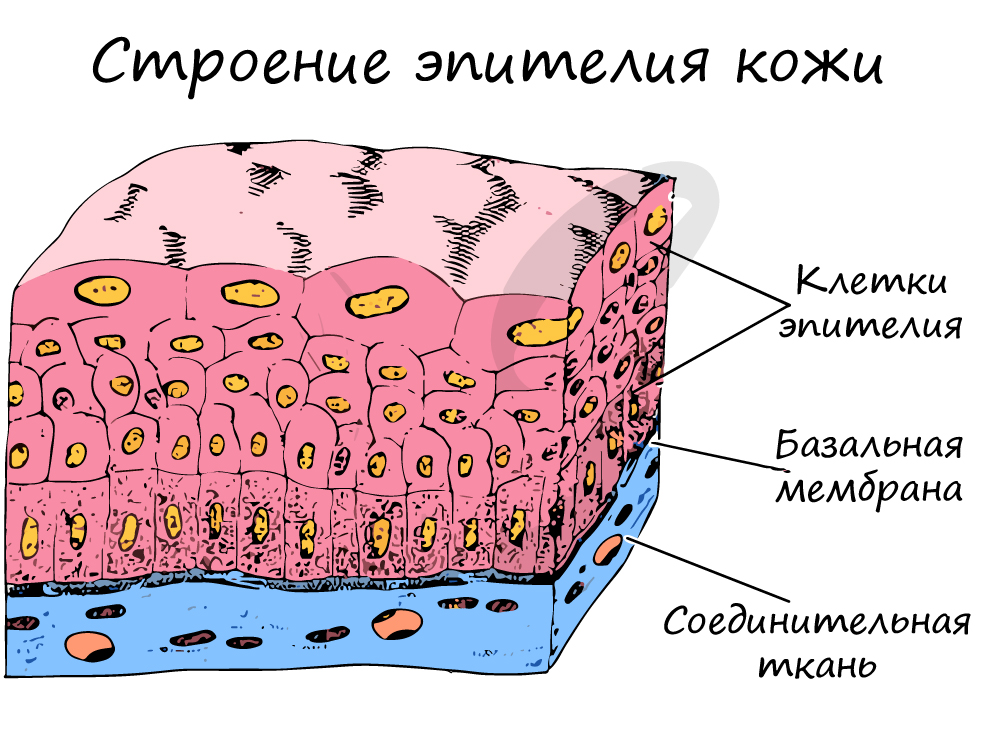
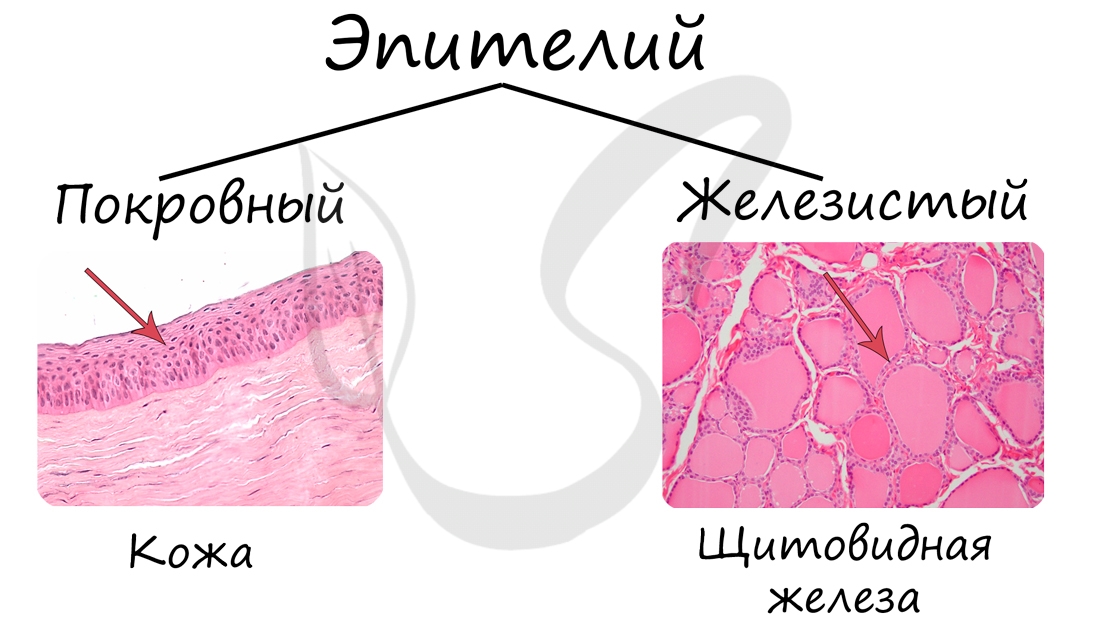
Эпителиальные ткани (эпителии)
Классификация
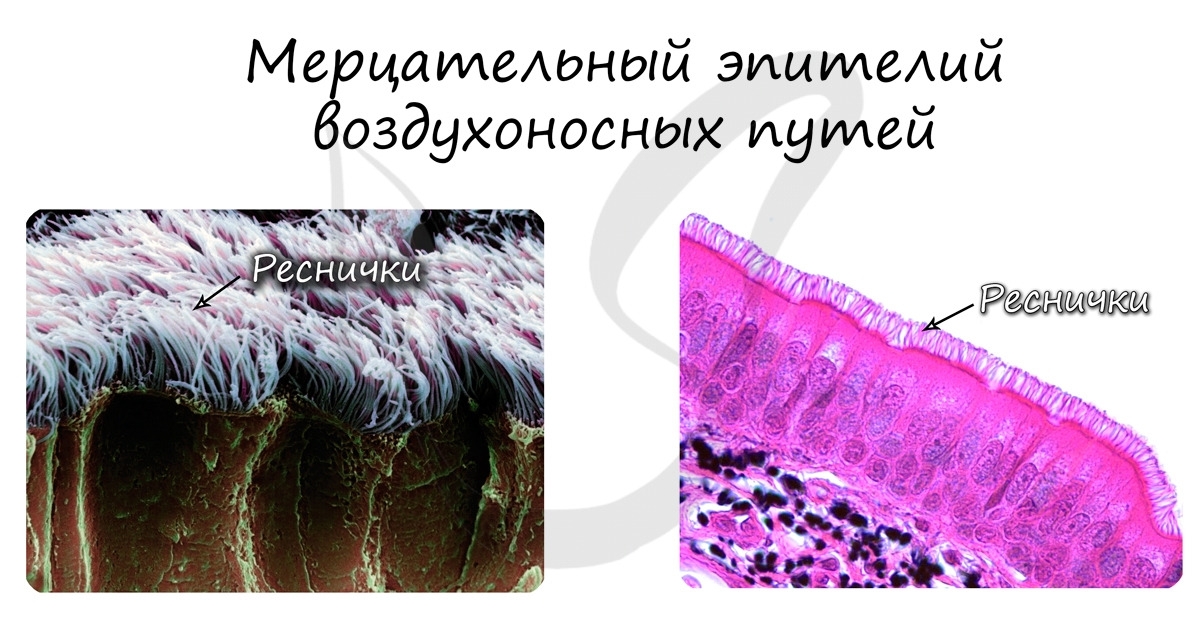
Мерцательный (реснитчатый) эпителий выстилает воздухоносные пути. На поверхности клеток данного эпителия расположены реснички, движения которых создают ток жидкости, направленный наружу, в сторону ноздрей.
Известен факт, что с течением длительного времени у курильщиков эти реснички отмирают, образуются участки «лысой слизистой», что затрудняет отток пылевых частиц, слизи из легких. В результате развиваются воспалительные заболевания бронхов, возникает кашель курильщика, практически неизлечимый, так как реснички не восстанавливаются.
Функции эпителиев
Эпителии отделяют внутреннюю среду от внешней, создают барьер, защищают организм от проникновения в него инфекционных агентов: бактерий, вирусов, простейших.
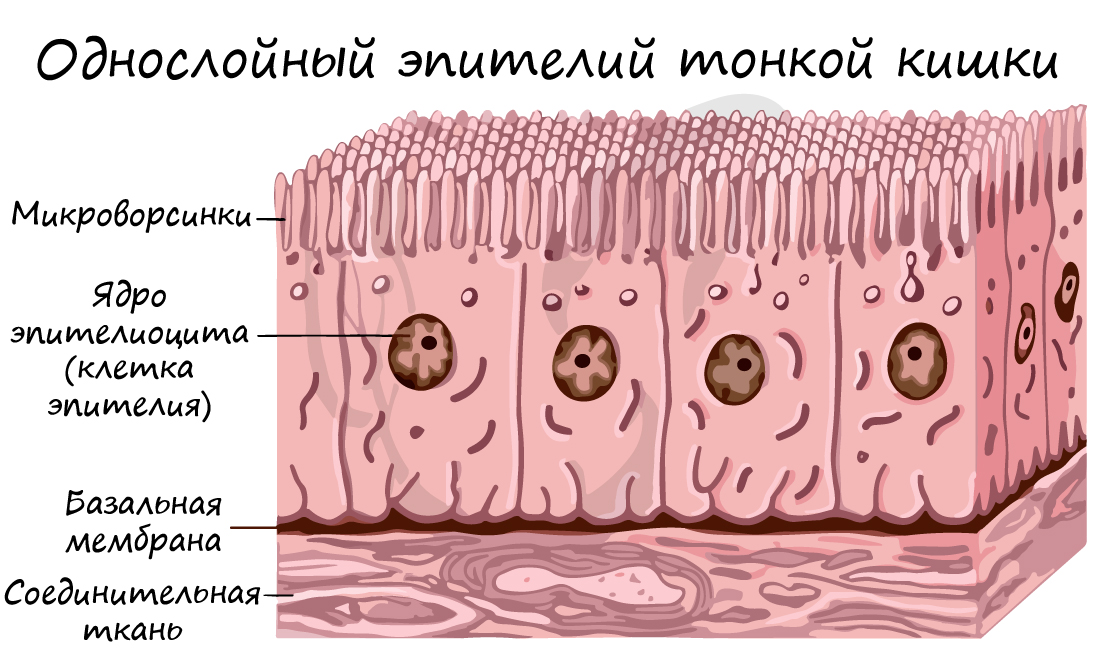
Через эпителий тонкой кишки всасываются необходимые организму питательные вещества. В то же время через эпителий из организма удаляются продукты обмена веществ.
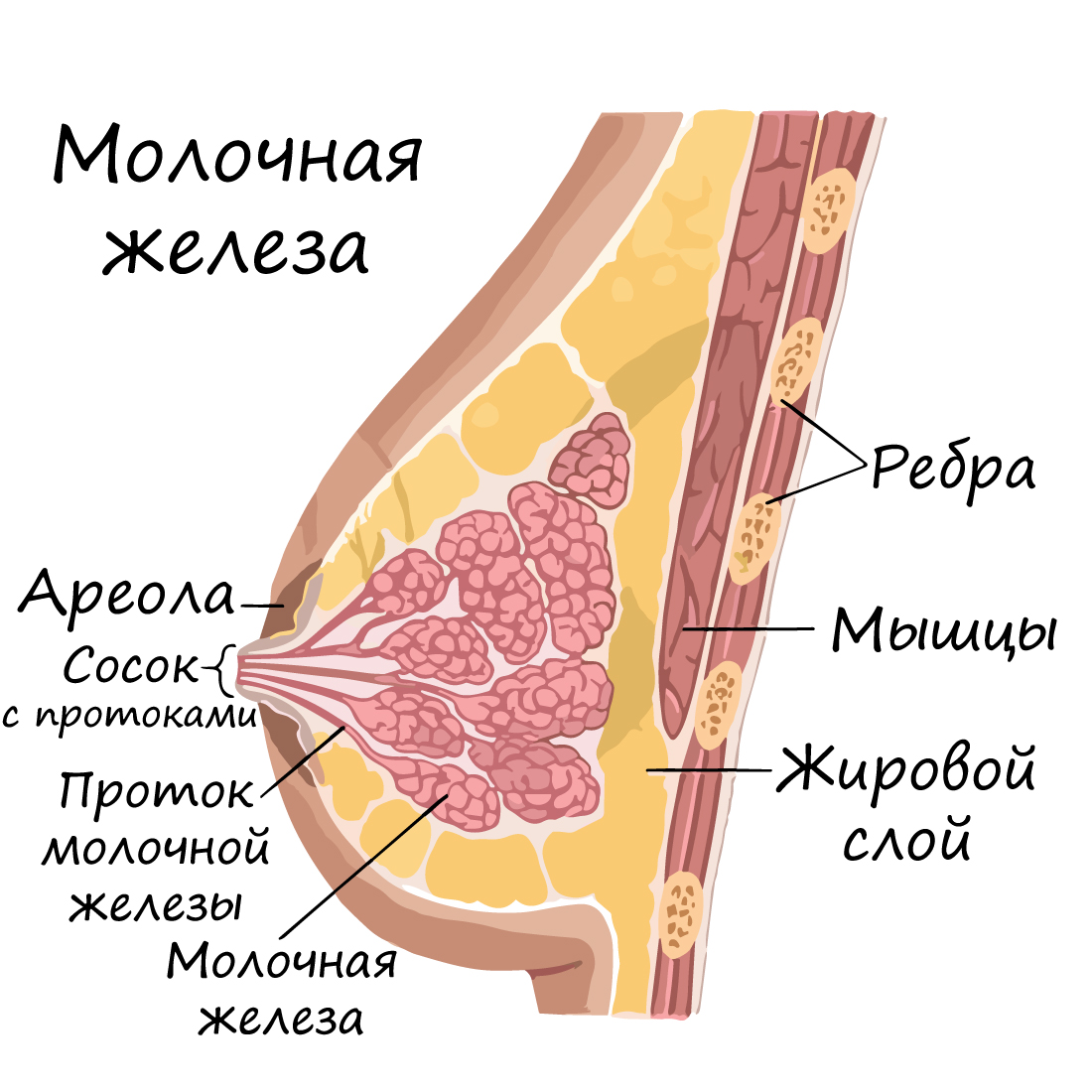
Эта функция принадлежит железистому эпителию, который располагается в железах внутренней и внешней секреции. Железы могут секретировать гормоны, ферменты.
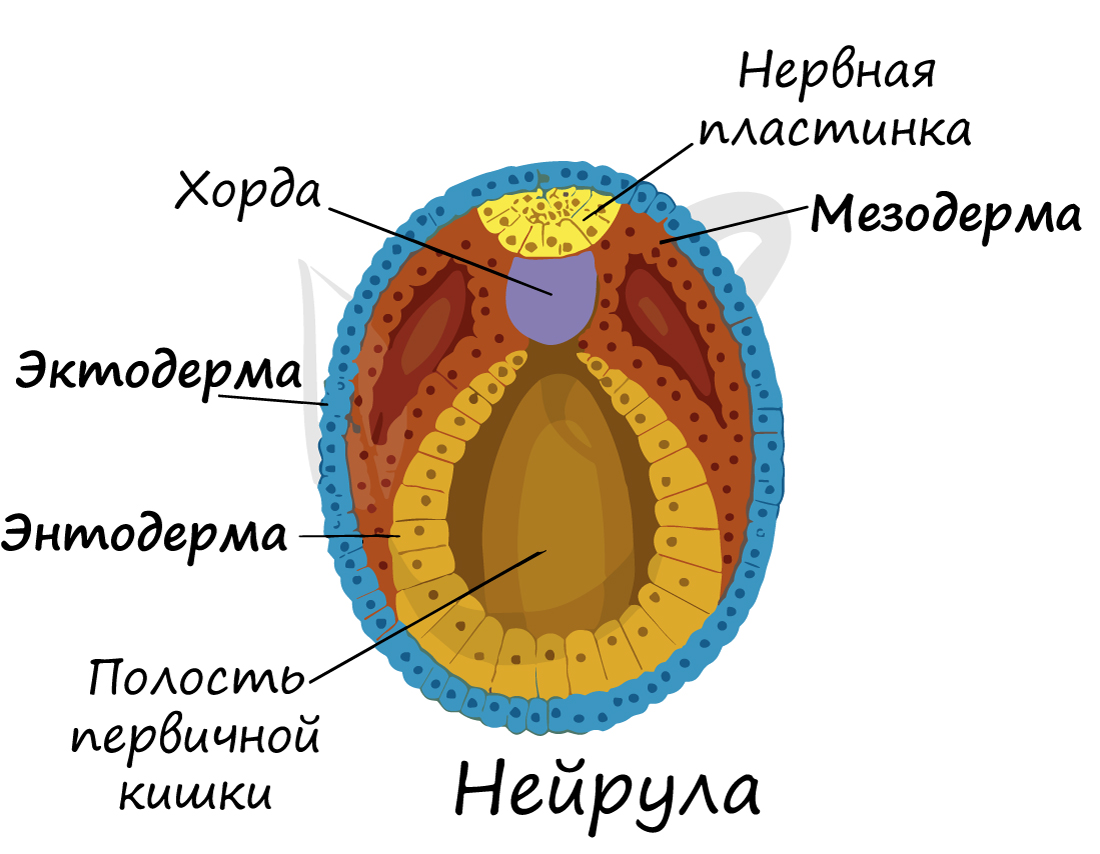
Происхождение эпителия
© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Опасная дисплазия железистого эпителия шейки матки лечится только методом ФДТ
Дисплазия железистого эпителия шейки матки
Д.м.н., профессор Сеченовского университета, онколог, хирург, онкогинеколог, гинеколог-иммунолог, эксперт по лечению дисплазии, предраковых и опухолевых заболеваний шейки матки.
Если говорить совсем коротко, то железистая дисплазия – это предраковое заболевание шейки матки. Из-за особенности своего расположения оно практически не поддается лечению классическими хирургическими методами. Фотодинамическая терапия в этом случае – пожалуй, единственный эффективный способ лечения, который защищает от рецидивов и раковой трансформации.
А теперь обо всем по порядку.
Чтобы лучше понять, что такое железистая дисплазия шейки матки, мы немного погрузимся в теорию и изучим строение шейки матки.
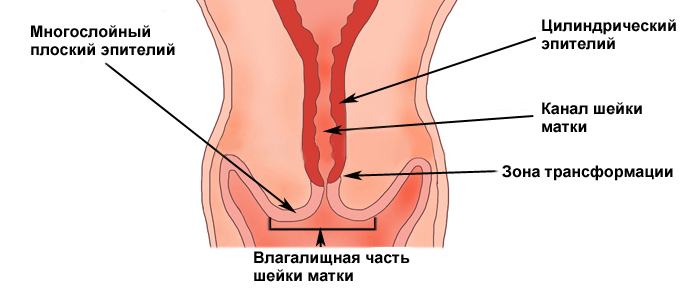
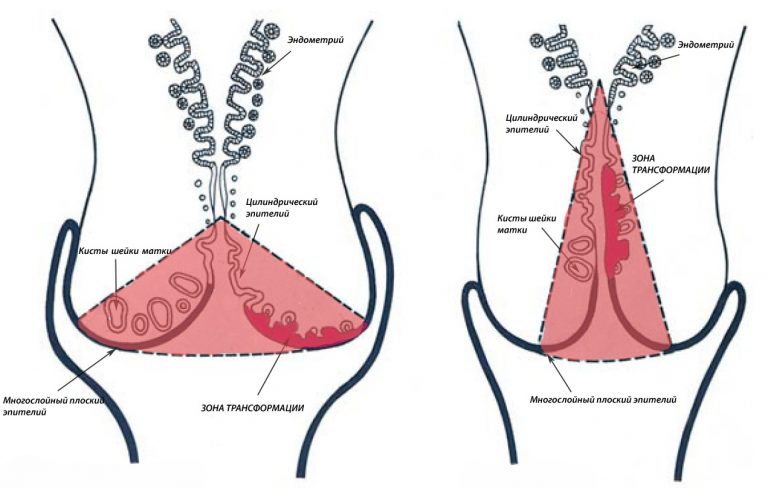
Строение шейки матки: эктоцервикс, эндоцервикс. зона трансформации.
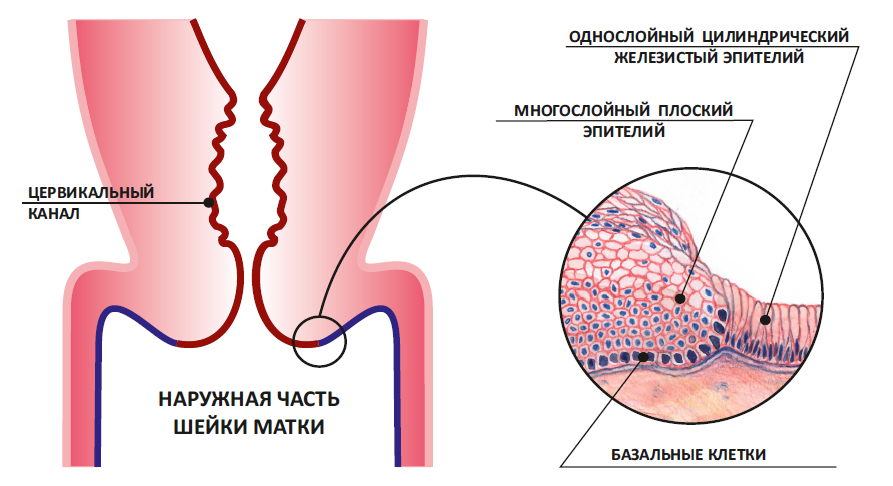
Участок шейки матки, который погружен во влагалище (синий прямоугольник) называется эктоцервиксом. Он покрыт многослойным плоским эпителием.
Участок шейки матки от наружного зева по направлению к матке называется цервикальным каналом шейки матки (оранжевый прямоугольник). Он покрыт эндоцервиксом, или железистым (цилиндрическим) эпителием.
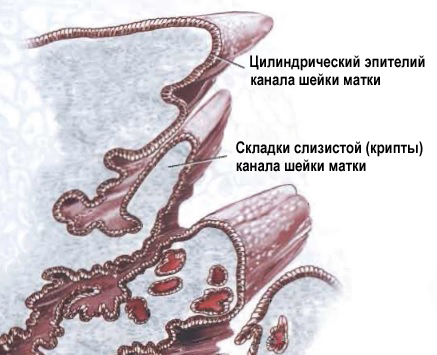
Цервикальный канал не ровный, а складчатый. На медицинском языке эти складки называются криптами. Железы цилиндрического эпителия секретирует слизь, которая составляет основной объём нормальных выделений.
Так выглядят крипты шейки матки. Всю поверхность крипты выстилает цилиндрический эпителий.
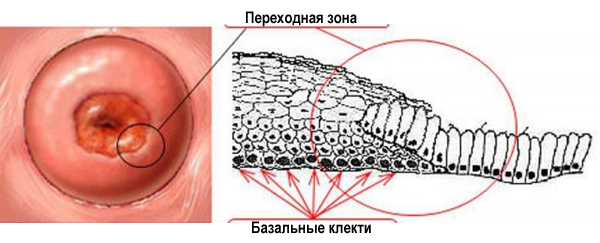
Зона, в которой многослойный плоский эпителий переходит в железистый эпителий называется переходной зоной, или зоной трансформации. Обычно дисплазия начинает свое развитие в зоне трансформации – в ней идет непрерывное клеточное деление, и вирусу папилломы легче всего проникнуть сквозь слабую защиту незрелых клеток в необходимые для его выживания базальные клетки.
Переходная зона или зона трансформации.
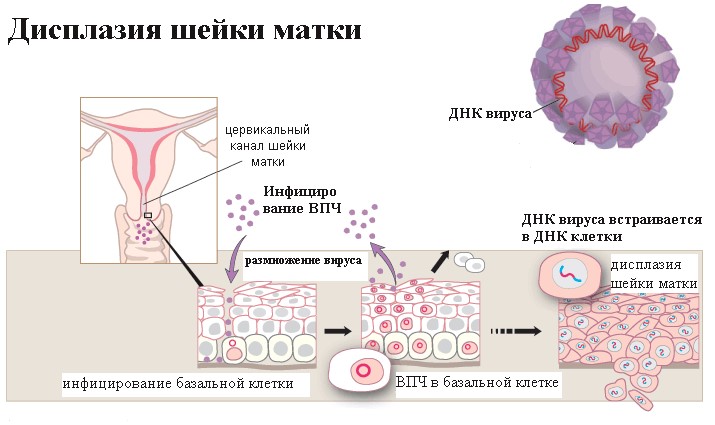
Дисплазия представляет собой скопление измененных вирусом клеток. Такие клетки называются атипическими, а само заболевание чаще всего относится к предраковым.
Что такое «дисплазия метаплазированного эпителия»?
Мы уже выяснили: зона, в которой сходится плоский и цилиндрический эпителий, называется зоной трансформации. Втрое ее название – переходная зона.
Но это только на схеме она представляет собой ровную линию. На самом деле, в этой зоне один эпителий заходит на другой, как морские волны на песчаный берег. Молодой плоский эпителий перекрывает молодой цилиндрический. Такой незрелый плоский эпителий и называется метаплазированным.
Незрелый метаплазированный эпителий.
Само словосочетание «метаплазированный эпителий» вызывает много вопросов. Не скрывается ли за этой формулировкой рак? – Нет, не скрывается.
Хуже, если в вашей цитологии ничего про метаплазированный эпителий не написано. Это значит, что он отсутствует в мазке, и анализ взят неправильно (помните, я писал о том, что правильная цитология начинается в кабинете врача, а не в лаборатории?).
А теперь давайте обратим внимание на то, что написано в заключении. Если в заключении написано «на фоне метаплазии очаги дисплазии», перед нами дисплазия переходного эпителия. Так как в зоне трансформации идет непрерывный процесс интенсивного деления клеток, незрелые клетки менее защищены от заражения, и вирусу папилломы (причина дисплазии) как раз в области метаплазированного эпителия легче проникнуть в глубокий базальный слой и встроиться в ДНК клетки.
Именно поэтому шейку матку так тщательно осматривают и берут с нее анализ на цитологию – дисплазия обычно начинается в переходной зоне.
А теперь поговорим о том, что означает диагноз «интраэпителиальная дисплазия железистого эпителия шейки матки».
Что такое дисплазия цервикального канала и чем она опасна
«Интраэпителиальная дисплазия железистого эпителия шейки матки» – это так называемый «цитологический» или «гистологический» диагноз. Такое заключение пишет специалист в лаборатории после изучения вашего цитологического мазка или биопсии.
Он видит в микроскоп, что в клетках железистого эпителия происходит предраковая трансформация клеток.
Формулируя таким образом свое заключение, врач-морфолог подчеркивает, что процесс происходит не в зоне трансформации, а В ЦЕРВИКАЛЬНОМ КАНАЛЕ ШЕЙКИ МАТКИ.
Поэтому заболевание еще называют «цервикальная дисплазия», или «дисплазия канала».
Такой диагноз говорит о том, что при лечении его классическими методами вероятность рецидива заболевания приближается к 80%.
Классический метод лечения дисплазии называется конизацией шейки матки. Это операция, в ходе которой хирург удаляет кусочек эктоцервикса и эндоцервикса в форме конуса. Задача хирурга – удалить участок вместе с дисплазией.
Низкая (слева) и высокая (справа) конизация шейки матки.
Но такой способ лечения для диагноза «дисплазии цилиндрического эпителия» изначально порочен.
Дело в том, что при работе с цервикальным каналом хирург действует фактически вслепую. Он не видит зоны поражения, не может оценить ее размера, глубины и по факту удаляет ткани «на ощупь». Практика показывает, что после такого лечения частота рецидива дисплазии приближается к 80%.
Фактически, когда врач-морфолог в заключении описывает наличие проблемы в области железистого эпителия, он таким образом подчеркивает сложный характер расположения дисплазии и бесперспективность хирургической тактики лечения.
Этим недостатки хирургического метода не ограничиваются.
Во-первых, радикальность и как следствие, эффективность конизации – всегда сомнительна. Объясню почему. Крипты эндоцервикса достигают глубины 5 мм. У всех разная физиология, и хирург никак не может проверить, убрал ли он достаточно цилиндрического эпителия.
У нерожавших женщин глубокое удаление тканей чревато развитием осложнений, которые могут препятствовать зачатию, вынашиванию и родам (на эту тему читайте мою статью «Беременность после конизации шейки матки»). Хирурги знают об этом, и стараются проводить операцию максимально щадящим образом.
Определение границ изменённого дисплазией эпителия носит всегда субъективный характер. А при проведении конизации глубина конуса определяется хирургом «на глазок», здесь доказательная медицина не подсказывает хирургу как действовать. Глубина обычно определяется длиной электрода – «паруса», а не тяжестью диспластического процесса.
Недостаточно радикальная конизация, как следствие, вызывает закономерный рецидив.
Во-вторых, любое лечебное воздействие само по себе является для вируса провоцирующим фактором.
После лечения вирус начинает вести себя более агрессивно и приводит к быстрому рецидиву, который развивается по негативному сценарию: дисплазия 2 степени переходит в 3, а дисплазия 3 степени и рака ин ситу могут трансформироваться в инвазивный рак шейки матки.
В-третьих, хирургия делает вирус резистентным (устойчивым) К ЛЮБОМУ лечению, даже к фотодинамической терапии. Увы, и я, и коллеги часто наблюдаем это в своей практике.
При таком развитии событий рано или поздно возникнет необходимость в удалении матки. Именно поэтому при диагнозе «дисплазия эндоцервикса» я настоятельно не рекомендую делать конизацию, так как она не устраняет причину болезни.
Как избежать рецидива?
Избежать рецидива можно единственным способом – устранить измененные клетки вместе с причиной заболевания – вирусом папилломы человека.
К сожалению, механическое удаление в процессе конизации атипических клеток не приводит к выздоровлению. ВПЧ остается в цервикальном канале. В теории, вместе с очагами дисплазии удаляются и все зараженные ВПЧ клетки. Но на практике так не происходит.
Единственный метод, который позволяет убрать из цервикального канала ВПЧ и атипичные клетки, – это правильно и в полном объеме выполненная фотодинамическая терапия с соблюдением протокола проведения.
Цервикальная дисплазия шейки матки хорошо лечится методом фотодинамической терапии
Я не буду рассказывать о самой: фотодинамической терапии – об этом очень хорошо рассказывает это видео:
Фундаментальные исследования доказали, что лазерный свет глубоко проникает в ткани и запускает фотохимические реакции на глубине минимум 7 мм. Крипты (складки) цервикального канала имеют максимальную глубину 5 мм, поэтому даже самые глубоко залегающие атипические клетки попадают под лечебное воздействие.
При соблюдении протокола проведения ФДТ в ходе фотохимических реакций образуются активные токсичные формы кислорода, которые увеличивают реальную глубину лечебного воздействия до 1,5 см! Соответственно, фотодинамическое воздействие в полной мере оказывает необходимый лечебный эффект, и даже с запасом.
Положительный терапевтический результат процедуры достигается только при неукоснительном соблюдении протокола ФДТ, который включает в себя обязательное облучение и зоны эктоцервикса, и цервикального канала специальным цилиндрическим диффузором.
Этот диффузор вводится в полость цервикального канала на всю его глубину, и по периметру облучает все поле железистого эпителия.
Только такой подход позволяет полностью уничтожить патологические клетки и содержащийся в них вирус папилломы человека (ВПЧ) на всех участках шейки матки и говорить о качественно выполненном лечении.
При такой адекватно проведённой ФДТ ВПЧ уничтожаются в 93% случаев.
Хочу отметить, что до сих пор даже очень уважаемые мои коллеги допускают ошибки в обучении специалистов-гинекологов и не показывают им необходимость облучения цервикального канала при лечении дисплазии шейки матки.
В этом случае ФДТ не оказывает нужного лечебного воздействия. Воздействие осуществляется только в области эктоцервикса, а вся полость цервикального канала шейки матки остается не задействованной в лечении. Такой «урезанный» протокол ФДТ зачастую приводит к тем же печальным последствиям, что и конизация.
Я горжусь, что могу менять медицинскую практику вокруг себя в лучшую сторону. Так, методическое пособие для врачей ГНЦ лазерной медицины МЗ РФ «Фотодинамическая терапия фоновых и предраковых заболеваний шейки матки» от 2004 года не включало в себя важный этап обработки цервикального канала.
После моего выступления на конференции StatusPraesens «Перинатальная медицина: от прегравидарной подготовки к здоровому материнству и детству», 18–20 февраля 2016 года, отель «Санкт-Петербург», методические рекомендации подверглись пересмотру и теперь включают в себя обработку цервикального при лечении дисплазии канала шейки матки как обязательный этап.
Многие теперь стали использовать диффузор для облучения цервикального канала. Однако даже после этой революции многие используют его, не понимая, какая интенсивность света выходит из этого диффузора. А это важный параметр, от которого зависит эффективность проведённой фотодинамической терапии.
Многие также используют диффузоры многократно, хотя уже после одного облучения мощность инструмента падает, и необходимое лечебное воздействие не достигается. Но никто об этом не задумывается!
Прием ведет Афанасьев Максим Станиславович, акушер-гинеколог, онкогинеколог, онколог, иммунолог, доктор медицинских наук, профессор и член ученого совета Первого МГМУ им. И.М. Сеченова МЗ РФ, эксперт по лечению дисплазии шейки матки.
После лечения я поддерживаю обратную связь со всеми пациентками и решаю все возникающие вопросы. Гепатит и положительный ВИЧ статус не является противопоказаниями для лечения методом ФДТ.
Для чего нужен железистый эпителий
Опухолевые клетки отличаются от нормальных нарушениями прочной сопряженности между процессами роста и дифференцировки [9]. Увеличение темпа воспроизводства озлокачествленных клеток обеспечивается не столько через укорочение митотического цикла, сколько за счет возрастания количества тех элементов, которые вместо достижения терминальной степени дифференцировки остаются во фракции роста [6, 11, 13]. В качестве еще одного механизма немалую роль играет «карикатурная» сигнальная связь, то есть нарушенная интеграция между малигнизированными клетками, проходящими через этапы дифференцировки, и микроокружением [2, 4]. Достигнут значительный прогресс в области изучения морфофункциональных особенностей слизистой оболочки желудка при предраке и раке, отчасти связанный с развитием высокочувствительных способов выявления в гистологических срезах отдельных тканевых и клеточных компонентов [1, 3]. Однако многие аспекты структурно-метаболической перестройки слизистой оболочки желудка при ее малигнизации остаются предметом дискуссий, и поиск изменений, предшествующих возникновению опухоли, по-прежнему актуален [5, 10].
Материал и методы исследования
Срезы окрашивали гематоксилином и эозином в комбинации с реакцией Перлса, по ван Гизону с окраской эластических волокон резорцин-фуксином Вейгерта, ставили ШИК-реакцию. Полутонкие срезы окрашивали реактивом Шиффа и азуром II. Исследования проводили в универсальном микроскопе Leica DM 4000B (Германия). Ультратонкие срезы, контрастированные уранилацетатом и цитратом свинца, исследовали в электронном микроскопе JEM 1010 при ускоряющем напряжении 80 кВт.
Результаты исследования и их обсуждение
Светооптическое исследование первичных опухолей пациентов 1-й группы выявило превалирование зрелых форм аденокарцином, характеризующихся формированием папиллярных и тубулярных железистых структур, умеренно выраженной тканевой и клеточной атипией, появлением патологических митозов, в разной степени выраженными фиброзными изменениями стромы. В низкодифференцированной аденокарциноме среди обширных скоплений опухолевых клеток или фиброзных полей с трудом обнаруживались мелкие железы, степень анаплазии опухолевых клеток возрастала. Перстневидно-клеточный рак отличался диффузным распределением клеток типичной перстневидной формы и, как правило, отсутствием десмопластической реакции стромы.
Особый интерес представляло изучение состояния слизистой оболочки желудка в отдаленных от опухоли участках. При кишечном типе рака светооптическое исследование фрагментов пилорического отдела желудка во всех наблюдениях выявило наличие распространенной неполной кишечной метаплазии. Обращала на себя внимание атрофия слизистой оболочки, иногда выраженная, с заметным истончением собственной пластинки, дистрофическими изменениями покровно-ямочного эпителия и уменьшением количества желез [7]. Диспластические изменения эпителия от слабой до тяжелой степени (увеличение ядерно-цитоплазматического соотношения, снижение секреции мукоида, псевдомногорядность, повышение митотической активности) обнаружены в большинстве исследованных фрагментов. Характерна многофокусность диспластических изменений, нарастающих по направлению к опухолевому очагу.
В фундальном отделе желудка очаговая кишечная метаплазия эпителиоцитов отмечена у 25% пациентов. Диспластические изменения энтеролизованного и интактного эпителия выявлены в половине наблюдений. Мононуклеарная инфильтрация отличалась слабой интенсивностью и поверхностной локализацией. В целом, патологические изменения в фундальном отделе желудка носили менее выраженный характер по сравнению с пилорическим отделом.
При изучении регионарных лимфатических узлов обращали внимание на наличие, размер и множественность метастазов. У пациентов с аденокарциномами метастазы в лимфатических узлах обнаружили у 37% больных.
Таким образом, светооптическое исследование первичных опухолей желудка пациентов 1-й группы выявило преобладание зрелых форм аденокарцином, характеризующихся формированием капиллярных и тубулярных железистых структур, умеренно выраженной тканевой и клеточной атипией. В большинстве случаев зрелых аденокарцином опухолевый очаг хорошо отграничен от окружающих тканей стенки желудка. Перстневидно-клеточный рак отличался диффузным распределением изолированных округлой формы клеток, содержащих в цитоплазме большое количество слизи. Опухоль характеризовалась инфильтративным ростом и была плохо отграничена от окружающих тканей [8, 12].
Новообразования у пациентов 2-й группы состояли из полиморфных либо мономорфных по составу анапластических клеток, располагающихся в виде тяжей, комплексов, или изолированно друг от друга. Клеточные ядра различались по основным светооптическим характеристикам: форме, размерам, окраске. Наиболее часто в клетках недифференцированного рака желудка встречались крупные гиперхромные угловатой формы ядра, а также небольшие светлые пузырьковые ядра. Цитоплазма была, как правило, скудная и плохо различима. Анализ частоты и выраженности патологических изменений нетрансформированной слизистой оболочки обнаружил их сходство с перифокальными процессами при диффузном типе карцином в первой группе наблюдений, что свидетельствует об определенном гистогенетическом единстве этих вариантов рака желудка. Ведущим патологическим изменением являлась дисплазия генеративных зон желудочного эпителия на фоне атрофически-склеротических процессов. Метастазы в регионарных лимфатических узлах обнаружены у 38% пациентов, что соответствует аналогичному показателю в первой группе.
Таким образом, светооптическое исследование опухолей желудка пациентов 2-й группы выявило наличие недифференцированного рака с солидным или скиррозным характером роста. Опухолевый очаг был плохо отграничен от окружающих тканей стенки желудка, отличался инфильтративным ростом и латеральным распространением опухоли по подслизистому слою.
Смешанные формы (3-я группа) сочетали в одном опухолевом очаге участки аденокарцином с различной степенью дифференцировки (часто с перстневидными клетками) либо разные патогистологические варианты рака желудка. Морфологическая картина отражала направление «дедифференцировки» клеточных популяций от центра к периферии опухоли. Практически во всех исследованных случаях карцинома распространялась в глубь желудочной стенки, инвазируя подслизистый, мышечный, иногда серозный слои, в ряде наблюдений комплексы раковых клеток выявлялись в большом сальнике или брыжейке поперечной ободочной кишки.
В слизистой оболочке вне опухолевого очага у 60% пациентов имелась кишечная метаплазия, ограниченная пилорическим отделом желудка; с такой же частотой встречались атрофия, склероз и густая полиморфно-клеточная инфильтрация. Наличие метастазов в регионарных лимфатических узлах выявлено у 60% оперированных больных этой группы, что значительно превышало данные первых двух анализируемых групп.
Таким образом, светооптический анализ перифокальных процессов в слизистой оболочке при различных патогистологических формах рака желудка показал, что при высоко- и умереннодифференцированных аденокарциномах наиболее типичными изменениями являются распространенная неполная кишечная метаплазия и ассоциированная с этими участками дисплазия на фоне диффузной атрофии эпителия. При низкодифференцированной и перстневидно-клеточной аденокарциномах, а также при недифференцированном раке желудка на первый план выходят атрофические изменения слизистой оболочки и дисплазия генеративных зон эпителия [14].
Электронно-микроскопический анализ аденокарциномы желудка выявил множественные патологические изменения ультраструктуры малигнизированных клеток: большие, неправильной формы ядра с изрезанными контурами и неравномерным распределением крупноглыбчатого гетерохроматина в кариоплазме, увеличенным количеством ядрышек, иногда атипичными митозами.
При перстневидно-клеточном раке желудка преобладали опухолевые клетки с переполненной секреторными гранулами цитоплазмой и эксцентрически расположенным ядром аномальной формы. Слизистая оболочка желудка вне опухолевого очага отличалась мозаичностью ультраструктурной картины. В очагах кишечной метаплазии, кроме типичных покровно-ямочных эпителиоцитов, обнаружены также каемчатые и бокаловидные клетки, цитоплазма которых была переполнена крупными электронно-прозрачными глобулами слизи, а уплощенные ядра оттеснены к базальному полюсу клеток. На апикальной поверхности каемчатых эпителиоцитов выявлялись высокие, нерегулярно расположенные микроворсинки. В цитоплазматическом матриксе большое число митохондрий и развитая гранулярная цитоплазматическая сеть. Отражением атрофических процессов в слизистой оболочке желудка было наличие большого числа эпителиоцитов, почти лишенных микроворсинок, имеющих электронно-плотную цитоплазму с едва различимыми органеллами. В дистрофически измененных клетках покровно-ямочного эпителия наблюдалось уменьшение количества секреторных мукоидных гранул, среди которых преобладали незрелые, с плотным содержимым и неровными контурами. Диспластические изменения эпителиоцитов выражались в увеличении размеров ядер, появлении крупных ядрышек, значительном снижении содержания внутриклеточного муцина.
При недифференцированном раке желудка преобладали атипичные клетки с гладкими, лишенными микроворсинок контурами. Клеточные ядра отличались большими размерами, с глубокими инвагинациями в нуклеолемме, придающими ядру причудливую двухлопастную или трехлопастную форму. Изучение желудка при недифференцированном раке на отдалении от первичной опухоли показало высокую степень развития атрофически-склеротических процессов слизистой оболочки и наличие диспластических изменений эпителия, ассоциированных с генеративными зонами (желудочные ямки, верхние отделы шеек желез). Неполная кишечная метаплазия носила очаговый характер и была ограничена, как правило, пилорическим отделом желудка. Анализ частоты и выраженности патологических изменений нетрансформированной слизистой оболочки при недифференцированном раке выявил их сходство с перифокальными процессами при диффузном типе карцином в первой группе наблюдений, что свидетельствует об определенном гистогенетическом единстве этих вариантов рака желудка.
Ультраструктурный анализ карцином желудка со смешанным типом строения подтвердил полиморфизм тканей и клеточную атипию, обнаруженные при светооптическом исследовании. В участках опухоли обнаружили злокачественные клетки с признаками секреции слизи в виде различных по размеру гранул, содержащих муцин. При снижении уровня дифференцировки по направлению к периферии опухоли наблюдалось прогрессирующее изменение ядерно-цитоплазматического соотношения в сторону увеличения размеров ядер. В слизистой оболочке желудка на отдалении от опухолевого очага в ряде случаев отсутствовали патологические изменения покровно-ямочного эпителия. По мере приближения к опухолевому очагу нарастала выраженность и гетерогенность изменений эпителиальных структур слизистой оболочки желудка. Анализ перифокальных процессов в окружающей слизистой оболочке желудка выявил меньшую распространенность и частоту предраковых изменений (дисплазии, неполные кишечные метаплазии и атрофии эпителия), чем в других исследованных группах пациентов. В целом, это свидетельствует о более высоких темпах опухолевой прогрессии смешанных форм карцином желудка.
Проведен комплексный морфологический анализ, включающий световую и электронную микроскопию опухолевых очагов, нетрансформированной слизистой оболочки, и регионарных лимфатических узлов при раке желудка. По результатам микроскопического исследования слизистой оболочки желудка на отдалении от опухолевого очага у пациентов с высоко- и умереннодифференцированными карциномами желудка установлено, что наиболее типичными изменениями являются распространенная неполная кишечная метаплазия и ассоциированная с этими участками дисплазия. В прилежащих к опухоли участках слизистой оболочки нередко обнаруживалась неравномерная гиперплазия эпителия. При низкодифференцированной и перстневидно-клеточной карциномах, а также при недифференцированном раке желудка на первый план выходит дисплазия генеративных зон эпителия; неполная кишечная метаплазия носит очаговый характер.