Для чего применяется хлор
Для чего применяется хлор
Еще в 2014 году Россия присоединилась к Минаматской конвенции ООН по ртути (The Minamata Convention on Mercury), которая предусматривает поэтапный отказ от использования ртути во всем мире – как в промышленности, так и в быту. Это касается хлорно-щелочного производства. Как говорилось выше, хлор получают в процессе электролиза. Есть три вида технологий. Самый эффективный и экологичный метод получения хлора и каустика – мембранный, он был разработан в 1975 году специалистами японской компании Asahi Kasei Chemicals Corporation. На сегодняшний день мембранный электролиз – доминирующая технология в Европе. По данным Ассоциации «РусХлор», в Европе по ней работают уже 83% мощностей.
В России в основном применяют диафрагменный (около 58% мощностей), три предприятия – «Башкирская содовая компания», «Каустик», «ГалоПолимер Кирово-Чепецк» (примерно 26% мощностей) – до сих пор используют амальгамный (ртутный) электролиз, который был распространен повсеместно в прошлом столетии. Во многом это связано с тем, что при использовании в качестве катода ртуть получают чистую каустическую соду, не содержащую хлоридов. Кроме того, переход на мембранный электролиз процесс технологически сложный и дорогостоящий.
На сегодня мембранная технология в стране внедрена пока только на АО «Саянскхимпласт». Электролизеры по лицензии японской компании были запущены в эксплуатацию в Саянске еще в 2006 году. В том же году на предприятии был остановлен ртутный электролиз, использовавшийся 27 лет. Важно отметить, что объемы выпуска продукции, в том числе ПВХ, были сохранены, а с годами увеличены. О начале перевода имеющейся на предприятии в Кирово-Чепецке ртутной технологии производства хлора и каустика на мембранную заявляла компания «ГалоПолимер».
Переход на безопасную технологию – одно из актуальных направлений развития отечественного хлорного производства.
Хлор (Cl, Chlorine)
История хлора
В 1774 году Карл Шееле, химик из Швеции, впервые получил хлор, но считалось, что это не отдельный элемент, а разновидность соляной кислоты (calorizator). Элементарный хлор был получен в начале XIX века Г. Дэви, который разложил поваренную соль на хлор и натрий путём электролиза.
Общая характеристика хлора
Хлор (от греческого χλωρός – зелёный) является элементом XVII группы периодической таблицы химических элементов Д.И. Менделеева, имеет атомный номер 17 и атомную массу 35,452. Принятое обозначение Cl ( от латинского Chlorum).
Нахождение в природе
Хлор является самым распространённым в земной коре галогеном, чаще всего в виде двух изотопов. В силу химической активности встречается лишь в виде соединений многих минералов.
Физические и химические свойства
Хлор является ядовитым жёлто-зелёным газом, имеет резкий неприятный запах и сладковатый вкус. Именно хлор после его открытия предложили называть галогеном, в одноимённую группу он входит как один из самых химически активных неметаллов.
Суточная потребность в хлоре
В норме взрослый здоровый человек должен получать в сутки 4-6 г хлора, потребность в нём возрастает при активных физических нагрузках или жаркой погоде (при повышенном потоотделении). Обычно суточную норму организм получает из продуктов питания при сбалансированном рационе.
Продукты питания богатые хлором
Основным поставщиком хлора в организм является поваренная соль – особенно, если она не подвергается термической обработке, поэтому лучше солить уже готовые блюда. Также хлор содержат яйца, морепродукты, мясо, горох, фасоль и чечевица, гречка и рис, оливки.
Взаимодействие с другими
Кислотно-щелочной и водный баланс организма регулируется калием, натрием и хлором.
Признаки нехватки хлора
Нехватка хлора вызвана процессами, приводящими к обезвоживанию организма – сильное потоотделение в жару или при физических нагрузках, рвота, диарея и некоторые заболевания моче-выделительной системы. Признаками недостатка хлора являются вялость и сонливость, слабость в мышцах, явная сухость во рту, потеря вкусовых ощущений, отсутствие аппетита.
Признаки избытка хлора
Признаками избытка хлора в организме являются: повышение кровяного давления, сухой кашель, боль в голове и в груди, резь в глазах, слезотечение, расстройства деятельности желудочно-кишечного тракта. Как правило, переизбыток хлора может быть вызван употреблением обычной воды из-под крана, которая проходит процесс дезинфекции хлором и случается у работников тех отраслей промышленности, которые напрямую связаны с использованием хлора.
Полезные свойства хлора и его влияние на организм
Хлор в организме человека:
Применение хлора в жизни
Основное применение хлора – химическая промышленность, где с его помощью изготавливают поливинилхлорид, пенопласт, материалы для упаковки, также боевые отравляющие вещества и удобрения для растений. Обеззараживание питьевой воды хлором – практически единственный доступный способ очистки воды.
Хлор элемент. Свойства хлора. Применение хлора
19 граммов на литр. Таково содержание хлора в морской воде. Норма для водопроводной – не более 1,5 грамма на литр. Для обеззараживания этого достаточно. Почему такая разница? Причина в соли, растворенной в океанах.
По химическому составу она является хлоридом натрия. В одном литре морской воды на него приходятся 35 граммов.
Не удивительно, что 19 из них – хлор. В мире его, как видно, немало. Велика и роль. Кто-то элемент боится, а кто-то понимает, что без него никак. Чтобы утвердиться в принятой позиции, или поменять ее, ознакомимся с фактами.
Свойства хлора
Хлор – элемент газообразный. Цвет у него желто-зеленый. Название 17-го элемента с греческого так и переводиться. Однако, ткани и бумагу вещество отбеливает. Правда, для этого нужна хлорноватистая кислота – итог взаимодействия хлора с водой.
В 18-ом веке, когда 17-е вещество только открыли, говорили «хлорная вода», не зная о том, что имеют дело с кислотой.
В начале 19-го века ей начали ополаскивать свои руки медики. Такая практика была введена, к примеру, в одном из госпиталей Вены. Врачи, конечно, не хотели отбелить руки. Хлорная вода служила обеззараживающим средством.
Способность 17-го элемента убивать болезнетворные бактерии заметили в конце 18-го столетия.
Раствор хлора – одно из примерно 200-от его соединений. В чистом виде элемент не встречается. Причина – высокая химическая активность. Вещество обязательно вступает во взаимодействие с «соседями». Однако, чистый хлор, все же, получен.
Первый удачный опыт проведен в 1774-ом году Карлом Шеелем. Это шведский химик. Он соединил соляную кислоту с пиролюзитом оксида марганца.
Понадобились предосторожности в работе с газом, ведь он токсичен. Если хлор попадает в легкие, то вызывает удушье и ожоги. Поэтому, в дыхательной системе, точнее в ее кровотоках, находят лишь соединения хлора. Общее содержание 17-го вещества в организме человека – 0,25% от массы.
Интересно! Хлор – хим. элемент, обнаруженный в большем количестве в телах профессиональных пловцов. Они, как говорится, не вылезают из бассейнов. Вода в них хлорирована и, видимо, ионы вещества просачиваются в кровоток.
Жидкий хлор – часть соляной кислоты, находящейся в желудке человека. 17-ый элемент в реагенте играет не только обеззараживающую роль, но и расщепляет пищу.
Получается, хлор, опасный в газообразном состоянии, приносит пользу в виде соединений, к примеру, той же поваренной соли.
Как видно, роль хлора весьма относительна. Он может быть благом, а может и ядом. В последнем амплуа элемент использовали немецкие войска.
Применение хлора
Хлор – химический элемент, используемый для производства соляной кислоты, не только в желудке.
Соляную кислоту с помощью 17-го вещества получают и вне организма. Соединение пригождается при дублении и окрашивании кож, на производстве активированного угля, синтетических красителей и органических полупродуктов.
Без хлора не обойтись и в гальванопластике. В составе соляной кислоты элемент нужен при изготовлении различных клеев и гидролизного спирта.
Обеззараживающая характеристика элемента пригождается теперь не в госпиталях, а в обработке водопроводной воды.
Ее хлорирование применяется больше века. Появилась альтернатива – озонирование. Хлор воду обеззараживает, но может негативно влиять на организм. Ресурсоснабжающие организации волнует еще и то, что 17-е вещество разъедает трубы.
Следовательно, сети чаще требуют ремонта и замены. Это убытки. Однако, пока, озонирование – лишь перспектива, а не реалии сегодняшнего дня.
Метод затратнее хлорирования, а результаты обработки воды не столь впечатляющие. В металлургии активный хлор участвует в процессах получения ниобия, титана, тантала. Это редкие и ценные металлы, так что у 17-го элемента важная роль. Уважают вещество и аграрии. Они закупают хлорорганические соединения.
С их помощью борются с сорняками. Чтобы отравление хлором «не заработали» и культурные растения, они должны быть двудольными. Реагент пагубно действует лишь на однодольные побеги. Содержат хлор и инсектициды. Эти соединения направлены уже на вредителей-насекомых.
Инсектициды убивают их избирательно, оставляя нетронутыми растения и полезные микроорганизмы. Потребность человеческого организма – 800 миллиграммов в сутки. Получают их не только из соли.
Продукты содержащие хлор
Помогут морская рыба, а так же, яйца, стручковый горох, гречка и рис. Рыбу заменяют устрицами и морскими огурцами.
Ионы хлора из них поддерживают осмотическое равновесие систем организма и регулируют водно-соляной обмен. Орган, в котором сосредоточенна основная масса 17-го элемента – кожа. Хлор в ней должен постоянно обновляться, поскольку выводится с потом и мочой.
В них переходит почти столько же вещества, сколько потребляется. Поэтому, хлор должен присутствовать в рационе всегда.
Добыча хлора
Методы 18-го века в 21-ом не актуальны. Вместо использованного когда-то Карлом Шееле оксида марганца и соляной кислоты применяют обычные соль и воду. Натрий хлор растворяют и подвергают действию электрического тока.
Не нужно ни специального оборудования, ни тары, ни повышенных температур. Современный метод прост и дешев. Сколько хлора произвести диктует спрос. Так, в 1970-е миру требовались 20 000 000 тонн в год.
Тогда, в производстве основных неорганических продуктов 17-ый элемент занял 5-е место. Позиция осталась прежней, но объем потребления вырос. На 2015-ый год — около 28 000 000 тонн. Это и хлор для бассейна, и хлористый винил, и пестициды, и растворители, и хлор в таблетках.
Последние растворяют в воде и используют, как моющее и обеззараживающее средство.
Половину хлора производят в Соединенных Штатах. Это обосновано потребностью в 17-ом веществе самой Америки.
В год внутренняя промышленность потребляет около 12 000 000 тонн реагента. Весома роль на рынке и у Великобритании. Производят, в основном, соединения 17-го элемента, к примеру, кислоты хлора.
Если говорить не об искусственном получении хлора и его производстве, а о добычи в природе, то она сводится к выработке каменной соли. Получается, месторождения 17-го вещества разрабатывали еще 3000-4000 лет назад. Тогда, добывать соль начали на землях современной Ливии.
Общее количество хлора в земных недрах – всего 0,017%. Получается, при активной добыче есть возможность истощения ресурсов. Так что, в далекой перспективе стоимость 17-го элемента может возрасти. А какова она на данный момент?
Цена хлора
Хлор купить в чистом виде можно канистрами. Как правило, это 30-литровая тара. В нее вмещаются 34 килограмма хлора. Это указывает на тяжесть вещества, даже в газообразном состоянии. Цена канистры со сжиженным хлором 1500-1800 рублей.
Остальная продукция основана на соединениях 17-го элемента, поэтому, стоимость, порой, непредсказуема. Ценник зависит от производителя, разрекламированности товара, его транспортировки, затрат на синтез, или добычу основы.
Так, белизну можно купить и за 13, и за 45 рублей. На отбеливающие порошки, собственно, столь же весомый разброс цен. Речь и о стиральных, и о чистящих составах. Средство для плиты, к примеру, предлагают и за 20, и за 80 рублей. Причем, объем одинаков. Обычно, это 500 граммов.
Интересно! Многие хлорсодержащие средства можно использовать в качестве изоляторов.
Сжиженный элемент №17 проводит электрический ток в миллиард раз хуже дистиллированной воды. Можно поаплодировать сему факту. Но, услышать авиации придется с запозданием. Дело в том, что звук тоже «вязнет» в хлоре, распространяясь в полтора раза медленнее, чем в атмосферном воздухе.
(молярная масса)
(первый электрон)
(жид. при −35 °C) 1,557 г/см 3 ;
(тв. при −105 °C) 1,9 г/см³
Простое вещество хлор при нормальных условиях — ядовитый газ желтовато-зелёного цвета, тяжелее воздуха, с резким запахом и сладковатым, «металлическим» вкусом. Молекула хлора двухатомная (формула Cl2).
Содержание
История открытия хлора
Соединение с водородом — газообразный хлороводород — был впервые получен Джозефом Пристли в 1772 г. Хлор был получен в 1774 г. шведским химиком Карлом Вильгельмом Шееле, описавшим его выделение при взаимодействии пиролюзита с соляной кислотой в своём трактате о пиролюзите:
Шееле отметил запах хлора, схожий с запахом царской водки, его способность взаимодействовать с золотом и киноварью, а также его отбеливающие свойства. Однако Шееле, в соответствии с господствовавшей в химии того времени теорией флогистона, предположил, что хлор представляет собой дефлогистированную муриевую (соляную) кислоту. Бертолле и Лавуазье в рамках кислородной теории кислот обосновали, что новое вещество должно быть оксидом гипотетического элемента мурия. Однако попытки его выделения оставались безуспешными вплоть до работ Г. Дэви, которому электролизом удалось разложить поваренную соль на натрий и хлор, доказав элементарную природу последнего.
В 1811 г. Дэви предложил для нового элемента название «хлорин» (chlorine). Спустя год Ж. Гей-Люссак «сократил» название до хлора (chlore). В том же 1811 г. немецкий физик Иоганн Швейгер предложил для хлора название «галоген» (дословно солерод), однако впоследствии этот термин закрепился за всей 17-й (VIIA) группой элементов, в которую входит и хлор.
В 1826 году атомная масса хлора была с высокой точностью определена шведским химиком Йёнсом Якобом Берцелиусом (отличается от современных данных не более, чем на 0,1 %).
Распространение в природе
В природе встречаются два изотопа хлора 35 Cl и 37 Cl. В земной коре хлор самый распространённый галоген. Хлор очень активен — он непосредственно соединяется почти со всеми элементами периодической системы. Поэтому в природе он встречается только в виде соединений в составе минералов: галита NaCl, сильвина KCl, сильвинита KCl·NaCl, бишофита MgCl2·6H2O., карналлита KCl·MgCl2·6H2O., каинита KCl·MgSO4·3H2O. Самые большие запасы хлора содержатся в составе солей вод морей и океанов (содержание в морской воде 19 г/л). На долю хлора приходится 0,025 % от общего числа атомов земной коры; кларковое число хлора — 0,017 %. Человеческий организм содержит 0,25 % ионов хлора по массе. В организме человека и животных хлор содержится в основном в межклеточных жидкостях (в том числе в крови) и играет важную роль в регуляции осмотических процессов, а также в процессах, связанных с работой нервных клеток.
Изотопный состав
В природе встречаются 2 стабильных изотопа хлора: с массовым числом 35 и 37. Доли их содержания соответственно равны 75,78 % и 24,22 %. Свойства стабильных и некоторых радиоактивных изотопов хлора перечислены в таблице:
| Изотоп | Относительная масса, а. е. м. | Период полураспада | Тип распада | Ядерный спин |
|---|---|---|---|---|
| 35 Cl | 34,968852721 | Стабилен | — | 3/2 |
| 36 Cl | 35,9683069 | 301 тыс. лет | β-распад в 36 Ar | 0 |
| 37 Cl | 36,96590262 | Стабилен | — | 3/2 |
| 38 Cl | 37,9680106 | 37,2 минуты | β-распад в 38 Ar | 2 |
| 39 Cl | 38,968009 | 55,6 минуты | β-распад в 39 Ar | 3/2 |
| 40 Cl | 39,97042 | 1,38 минуты | β-распад в 40 Ar | 2 |
| 41 Cl | 40,9707 | 34 c | β-распад в 41 Ar | |
| 42 Cl | 41,9732 | 46,8 c | β-распад в 42 Ar | |
| 43 Cl | 42,9742 | 3,3 c | β-распад в 43 Ar |
Физические и химические свойства
При нормальных условиях хлор — жёлто-зелёный газ с удушающим запахом. Некоторые его физические свойства представлены в таблице.
| Свойство | Значение |
|---|---|
| Цвет (газ) | Жёлто-зелёный |
| Температура кипения | −34 °C |
| Температура плавления | −100 °C |
| Температура разложения (диссоциации на атомы) | |
| Плотность (газ, н.у.) | 3,214 г/л |
| Сродство к электрону атома | 3,65 эВ |
| Первая энергия ионизации | 12,97 эВ |
| Теплоёмкость (298 К, газ) | 34,94 Дж/(моль·K) |
| Критическая температура | 144 °C |
| Критическое давление | 76 атм |
| Стандартная энтальпия образования (298 К, газ) | 0 кДж/моль |
| Стандартная энтропия образования (298 К, газ) | 222,9 Дж/(моль·K) |
| Энтальпия плавления | 6,406 кДж/моль |
| Энтальпия кипения | 20,41 кДж/моль |
| Энергия гомолитического разрыва связи Х—Х | 243 кДж/моль |
| Энергия гетеролитического разрыва связи Х—Х | 1150 кДж/моль |
| Энергия ионизации | 1255 кДж/моль |
| Энергия сродства к электрону | 349 кДж/моль |
| Атомный радиус | 0,073 нм |
| Электроотрицательность по Полингу | 3,20 |
| Электроотрицательность по Оллреду — Рохову | 2,83 |
| Устойчивые степени окисления | −1, 0, +1, +3, (+4), +5, (+6), +7 |
Газообразный хлор относительно легко сжижается. Начиная с давления в 0,8 МПа (8 атмосфер), хлор будет жидким уже при комнатной температуре. При охлаждении до температуры в −34 °C хлор тоже становится жидким при нормальном атмосферном давлении. Жидкий хлор — жёлто-зелёная жидкость, обладающая очень высоким коррозионным действием (за счёт высокой концентрации молекул). Повышая давление, можно добиться существования жидкого хлора вплоть до температуры в +144 °C (критической температуры) при критическом давлении в 7,6 МПа.
Растворимость
| Растворитель | Растворимость г/100 г |
|---|---|
| Бензол | Растворим |
| Вода (0 °C) | 1,48 |
| Вода (20 °C) | 0,96 |
| Вода (25 °C) | 0,65 |
| Вода (40 °C) | 0,46 |
| Вода (60 °C) | 0,38 |
| Вода (80 °C) | 0,22 |
| Тетрахлорметан (0 °C) | 31,4 |
| Тетрахлорметан (19 °C) | 17,61 |
| Тетрахлорметан (40 °C) | 11 |
| Хлороформ | Хорошо растворим |
| TiCl4, SiCl4, SnCl4 | Растворим |
Степень диссоциации молекулы хлора Cl2 → 2Cl при 1000 К равна 2,07⋅10 −4 %, а при 2500 К — 0,909 %.
Порог восприятия запаха в воздухе равен 2—3 мг/м³.
По электропроводности жидкий хлор занимает место среди самых сильных изоляторов: он проводит ток почти в миллиард раз хуже, чем дистиллированная вода, и в 10 22 раз хуже серебра. Скорость звука в газообразном хлоре примерно в полтора раза меньше, чем в воздухе.
Химические свойства
Строение электронной оболочки
| Валентность | Возможные степени окисления | Электронное состояние валентного уровня | Пример соединений |
|---|---|---|---|
| I | +1, −1, 0 | 3s 2 3p 5 | NaCl, NaClO, Cl2 |
| III | +3 | 3s 2 3p 4 3d 1 | NaClO2 |
| V | +5 | 3s 2 3p 3 3d 2 | KClO3 |
| VII | +7 | 3s 1 3p 3 3d 3 | KClO4 |
Также известны соединения хлора, в которых атом хлора формально проявляет валентности IV и VI, например, ClO2 и Cl2O6. Однако оксид хлора(IV) является радикалом, то есть у него есть один неспаренный электрон, а оксид хлора(VI) содержит два атома хлора, имеющих степени окисления +5 и +7.
Взаимодействие с металлами
Хлор непосредственно реагирует почти со всеми металлами (с некоторыми только в присутствии влаги или при нагревании):
Взаимодействие с неметаллами
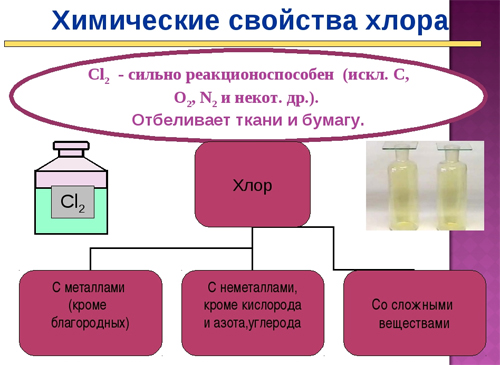
C неметаллами (кроме углерода, азота, фтора, кислорода и инертных газов) образует соответствующие хлориды.
На свету или при нагревании активно реагирует (иногда со взрывом) с водородом по радикально-цепному механизму. Смеси хлора с водородом, содержащие от 5,8 до 88,3 % водорода, взрываются при облучении с образованием хлороводорода. Смесь хлора с водородом в небольших концентрациях горит бесцветным или жёлто-зелёным пламенем. Максимальная температура водородно-хлорного пламени 2200 °C.
С кислородом хлор образует оксиды (см. статью Оксиды хлора), в которых он проявляет степень окисления от +1 до +7: Cl2O, ClO2, Cl2O5, Cl2O7. Они имеют резкий запах, термически и фотохимически нестабильны, склонны к взрывному распаду. Напрямую хлор с кислородом не реагирует. При реакции с фтором образуется не хлорид, а фториды:
Известны фторид хлора(I), фторид хлора(III) и фторид хлора(V) (ClF, ClF3 и ClF5), Могут быть синтезированы из элементов, степень окисления хлора меняется в зависимости от условий синтеза. Все они представляют собой при комнатной температуре бесцветные ядовитые тяжёлые газы с сильным раздражающим запахом. Сильные окислители, реагируют с водой и стеклом. Используются как фторирующие агенты.
Другие свойства
Хлор вытесняет бром и йод из их соединений с водородом и металлами:
При реакции с монооксидом углерода образуется фосген:
При растворении в воде или щелочах, хлор диспропорционирует, образуя хлорноватистую (а при нагревании хлорноватую) и соляную кислоты, либо их соли:
Cl2 + H2O ⇄ HCl + HClO Cl2 + 2NaOH → NaCl + NaClO + H2O 3 Cl2 + 6NaOH → 5NaCl + NaClO3 + 3H2O (при нагревании)
Хлорированием сухого гидроксида кальция получают хлорную известь:
Действием хлора на аммиак можно получить трихлорид азота:
Окислительные свойства хлора
Хлор — очень сильный окислитель:
Раствор хлора в воде используется для отбеливания тканей и бумаги.
Реакции с органическими веществами
С насыщенными соединениями:
CH3-CH3 + Cl2 → C2H5Cl + HCl CH4 + Cl2 → CH3Cl + HCl (получение хлороформа, реакция идет многоступенчато с образованием тетрахлорметана CCl4)
Присоединяется к ненасыщенным соединениям по кратным связям:
Ароматические соединения замещают атом водорода на хлор в присутствии катализаторов (например, AlCl3 или FeCl3):
Способы получения
Химические методы
Химические методы получения хлора малоэффективны и затратны. На сегодняшний день имеют в основном историческое значение.
Метод Шееле
Первоначально промышленный способ получения хлора основывался на методе Шееле, то есть реакции пиролюзита с соляной кислотой:
Метод Дикона
В 1867 году Диконом был разработан метод получения хлора каталитическим окислением хлороводорода кислородом воздуха. Процесс Дикона в настоящее время используется при рекуперации хлора из хлороводорода, являющегося побочным продуктом при промышленном хлорировании органических соединений.
Современные лабораторные методы
Ввиду доступности хлора в лабораторной практике обычно используется сжиженный хлор в баллонах. Хлор можно получить действием кислоты на гипохлорит натрия:
При этом также выделяется кислород. Если использовать соляную кислоту, то реакция выглядит по-другому:
NaOCl + 2HCl = NaCl + Cl2 ↑ + H2O
Для получения хлора в небольших количествах обычно используются процессы, основанные на окислении хлороводорода сильными окислителями (например, оксидом марганца (IV), перманганатом калия, хлоритом кальция, хроматом калия, дихроматом калия, диоксидом свинца, бертолетовой солью и т. п.), обычно используется диоксид марганца или перманганат калия:
При невозможности использования баллонов и химических методов получения хлора могут быть использованы электрохимические — при помощи небольших электролизеров с обычным или вентильным электродом для получения хлора.
Электрохимические методы
Сегодня хлор в промышленных масштабах получают вместе с гидроксидом натрия и водородом путём электролиза раствора поваренной соли, основные процессы которого можно представить суммарной формулой:
Применяется три варианта электрохимического метода получения хлора. Два из них — электролиз с твердым катодом: диафрагменный и мембранный методы, третий — электролиз с жидким ртутным катодом (ртутный метод производства). Качество хлора, получаемого электрохимическими методами, отличается мало:
| Ртутный метод | Диафрагменный метод | Мембранный метод | |
|---|---|---|---|
| Выход хлора % | 99 | 96 | 98,5 |
| Электроэнергия (кВт·ч) | 3 150 | 3 260 | 2 520 |
| Чистота хлора | 99,2 | 98 | 99,3 |
| Массовая доля O2 в хлоре, % | 0,1 | 1—2 | 0,3 |
Диафрагменный метод
Наиболее простым, из электрохимических методов, в плане организации процесса и конструкционных материалов для электролизера, является диафрагменный метод получения хлора.
Раствор соли в диафрагменном электролизере непрерывно подается в анодное пространство и протекает через, как правило, насаженную на стальную катодную сетку асбестовую диафрагму, в которую иногда добавляют небольшое количество полимерных волокон.
Насасывание диафрагмы производится путём прокачивания через электролизер пульпы из асбестовых волокон, которые, застревая в сетке катода, образуют слой асбеста, играющий роль диафрагмы.
Во многих конструкциях электролизеров катод полностью погружен под слой анолита (электролита из анодного пространства), а выделяющийся на катодной сетке водород отводится из-под катода при помощи газоотводных труб, не проникая через диафрагму в анодное пространство благодаря противотоку.
Анод: 2Cl − − 2e − → Cl2 ↑ — основной процесс 2H2O − 4e − → O2↑ + 4H + 12ClO − + 6H2O − 12e − → 4ClO3 − + 8Cl − + 3O2↑ + 6H + Катод: 2H2O + 2e − → H2↑ + 2OH − — основной процесс ClO − + H2O + 2e − → Cl − + 2OH − ClO3 − + 3H2O + 6e − → Cl − + 6OH −
В качестве анода в диафрагменных электролизерах может использоваться графитовый или угольный электроды. На сегодня их в основном заменили титановые аноды с окисно-рутениево-титановым покрытием (аноды ОРТА) или другие малорасходуемые.
Поваренная соль, сульфат натрия и другие примеси при повышении их концентрации в растворе выше их предела растворимости выпадают в осадок. Раствор едкой щёлочи декантируют от осадка и передают в качестве готового продукта на склад или продолжают стадию упаривания для получения твёрдого продукта, с последующим плавлением, чешуированием или грануляцией.
Обратную, то есть кристаллизовавшуюся в осадок поваренную соль возвращают назад в процесс, приготавливая из неё так называемый обратный рассол. От неё, во избежание накапливания примесей в растворах, перед приготовлением обратного рассола отделяют примеси.
Убыль анолита восполняют добавкой свежего рассола, получаемого подземным выщелачиванием соляных пластов галита, бишофита и других минералов, содержащих хлорид натрия, а также растворением их в специальных ёмкостях на месте производства. Свежий рассол перед смешиванием его с обратным рассолом очищают от механических взвесей и значительной части ионов кальция и магния.
Полученный хлор отделяется от паров воды, компримируется и подаётся либо на производство хлорсодержащих продуктов, либо на сжижение.
Благодаря относительной простоте и дешевизне диафрагменный метод получения хлора до сих пор широко используется в промышленности.
Схема диафрагменного электролизера.
Мембранный метод
Мембранный метод производства хлора наиболее энергоэффективен, однако сложен в организации и эксплуатации.
С точки зрения электрохимических процессов мембранный метод подобен диафрагменному, но анодное и катодное пространства полностью разделены непроницаемой для анионов катионообменной мембраной. Поэтому в мембранном электролизере, в отличие от диафрагменного, не один поток, а два.
В анодное пространство поступает, как и в диафрагменном методе, поток раствора соли. А в катодное — деионизированная вода. Из анодного пространства вытекает поток обеднённого анолита, содержащего также примеси гипохлорит- и хлорат-ионов и выходит хлор, а из катодного — щелока и водород, практически не содержащие примесей и близкие к товарной концентрации, что уменьшает затраты энергии на их упаривание и очистку.
Однако питающий раствор соли (как свежий, так и оборотный) и вода предварительно максимально очищаются от любых примесей. Такая тщательная очистка определяется высокой стоимостью полимерных катионообменных мембран и их уязвимостью к примесям в питающем растворе.
Кроме того, ограниченная геометрическая форма, а также низкая механическая прочность и термическая стойкость ионообменных мембран, во многом определяют сравнительно сложные конструкции установок мембранного электролиза. По той же причине мембранные установки требуют наиболее сложных систем автоматического контроля и управления.
Схема мембранного электролизера.
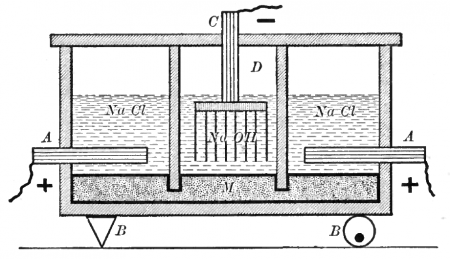
Ртутный метод с жидким катодом
В ряду электрохимических методов получения хлора ртутный метод позволяет получать самый чистый хлор.
Схема ртутного электролизера.
Установка для ртутного электролиза состоит из электролизёра, разлагателя амальгамы и ртутного насоса, объединённых между собой ртутепроводящими коммуникациями.
Катодом электролизёра служит поток ртути, прокачиваемой насосом. Аноды — графитовые, угольные или малоизнашивающиеся (ОРТА, ТДМА или другие). Вместе с ртутью через электролизёр непрерывно течёт поток питающего раствора поваренной соли.
На аноде происходит окисление ионов хлора из электролита, и выделяется хлор:
2Cl − − 2e − → Cl2 ↑ — основной процесс 2H2O − 2e − → O2↑ + 4H + 12ClO − + 6H2O − 12e − → 4ClO3 − + 8Cl − + 3O2↑ + 12H +
Хлор и анолит отводится из электролизёра. Анолит, выходящий из электролизера, донасыщают свежим галитом, извлекают из него примеси, внесённые с ним, а также вымываемые из анодов и конструкционных материалов, и возвращают на электролиз. Перед донасыщением из анолита извлекают растворённый в нём хлор.
Растущие требования к экологической безопасности производств и дороговизна металлической ртути ведут к постепенному вытеснению ртутного метода методами получения хлора с твердым катодом.
Хранение хлора
Производимый хлор хранится в специальных «танках» или закачивается в стальные баллоны высокого давления. Баллоны с жидким хлором под давлением имеют специальную окраску — защитный цвет c зелёной полосой. Следует отметить, что при длительной эксплуатации баллонов с хлором в них накапливается чрезвычайно взрывчатый трихлорид азота, и поэтому время от времени баллоны с хлором должны проходить плановую промывку и очистку от хлорида азота.
Стандарты качества хлора
Согласно ГОСТ 6718-93 «Хлор жидкий. Технические условия» производятся следующие сорта хлора:
| Наименование показателя ГОСТ 6718-93 | Высший сорт | Первый сорт |
|---|---|---|
| Объемная доля хлора, не менее, % | 99,8 | 99,6 |
| Массовая доля воды, не более, % | 0,01 | 0,04 |
| Массовая доля треххлористого азота, не более, % | 0,002 | 0,004 |
| Массовая доля нелетучего остатка, не более, % | 0,015 | 0,10 |
Применение
Хлор применяют во многих отраслях промышленности, науки и бытовых нужд:
Этот старинный способ отбеливания тканей, бумаги, картона.
Многие развитые страны стремятся ограничить использование хлора в быту, в том числе потому, что при сжигании хлорсодержащего мусора образуется значительное количество диоксинов.
Биологическая роль
Хлор относится к важнейшим биогенным элементам и входит в состав всех живых организмов в виде соединений.
У животных и человека ионы хлора участвуют в поддержании осмотического равновесия, хлорид-ион имеет оптимальный радиус для проникновения через мембрану клеток. Именно этим объясняется его совместное участие с ионами натрия и калия в создании постоянного осмотического давления и регуляции водно-солевого обмена. Под воздействием ГАМК (нейромедиатор) ионы хлора оказывают тормозящий эффект на нейроны путём снижения потенциала действия. В желудке ионы хлора создают благоприятную среду для действия протеолитических ферментов желудочного сока. Хлорные каналы представлены во многих типах клеток, митохондриальных мембранах и скелетных мышцах. Эти каналы выполняют важные функции в регуляции объёма жидкости, трансэпителиальном транспорте ионов и стабилизации мембранных потенциалов, участвуют в поддержании рН клеток. Хлор накапливается в висцеральной ткани, коже и скелетных мышцах. Всасывается хлор, в основном, в толстом кишечнике. Всасывание и экскреция хлора тесно связаны с ионами натрия и бикарбонатами, в меньшей степени с минералокортикоидами и активностью Na + /K + — АТФ-азы. В клетках аккумулируется 10-15 % всего хлора, из этого количества от 1/3 до 1/2 — в эритроцитах. Около 85 % хлора находятся во внеклеточном пространстве. Хлор выводится из организма в основном с мочой (90—95 %), калом (4-8 %) и через кожу (до 2 %). Экскреция хлора связана с ионами натрия и калия, и реципрокно (взаимно) с гидрокарбонат-ионами HCO3 − (кислотно-щелочной баланс).
Человек потребляет 5—10 г NaCl в сутки. Минимальная потребность человека в хлоре составляет около 800 мг в сутки. Младенец получает необходимое количество хлора через молоко матери, в котором содержится 11 ммоль/л хлора. NaCl необходим для выработки в желудке соляной кислоты, которая способствует пищеварению и уничтожению болезнетворных бактерий. В настоящее время участие хлора в возникновении отдельных заболеваний у человека изучено недостаточно хорошо, главным образом из-за малого количества исследований. Достаточно сказать, что не разработаны даже рекомендации по норме суточного потребления хлора. Мышечная ткань человека содержит 0,20—0,52 % хлора, костная — 0,09 %; в крови — 2,89 г/л. В организме среднего человека (масса тела 70 кг) 95 г хлора. Ежедневно с пищей человек получает 3—6 г хлора, что с избытком покрывает потребность в этом элементе.
Ионы хлора жизненно необходимы растениям. Хлор участвует в энергетическом обмене у растений, активируя окислительное фосфорилирование. Он необходим для образования кислорода в процессе фотосинтеза изолированными хлоропластами, стимулирует вспомогательные процессы фотосинтеза, прежде всего те из них, которые связаны с аккумулированием энергии. Хлор положительно влияет на поглощение корнями кислорода, соединений калия, кальция, магния. Чрезмерная концентрация ионов хлора в растениях может иметь и отрицательную сторону, например, снижать содержание хлорофилла, уменьшать активность фотосинтеза, задерживать рост и развитие растений.
Но существуют растения, которые в процессе эволюции либо приспособились к засолению почв, либо в борьбе за пространство заняли пустующие солончаки, на которых нет конкуренции. Растения, произрастающие на засоленных почвах, называются галофитами. Они накапливают хлориды в течение вегетационного сезона, а потом избавляются от излишков посредством листопада или выделяют хлориды на поверхность листьев и веток и получают двойную выгоду, притеняя поверхности от солнечного света.
Среди микроорганизмов также известны галофилы — галобактерии, — которые обитают в сильносоленых водах или почвах.
Токсичность
Хлор — токсичный удушающий газ, сильный ирритант, при попадании в лёгкие вызывает ожог лёгочной ткани (в результате образования в них хлорноватистой и соляной кислоты), удушье.
Раздражающее действие на дыхательные пути оказывает при концентрации в воздухе уже от 1 до 6 мг/м³ (что близко к порогу восприятия запаха хлора), при 12 мг/м³ переносится с трудом, концентрации больше 100 мг/м³ опасны для жизни (смерть от остановки дыхания наступает через 5—25 минут, при высоких концентрациях — мгновенно).
Предельно допустимая концентрация хлора в атмосферном воздухе следующие: среднесуточная — 0,03 мг/м³; максимально разовая — 0,1 мг/м³; в рабочих помещениях промышленного предприятия — 1 мг/м³.
При работе с хлором следует пользоваться защитной спецодеждой, противогазом, перчатками. На короткое время защитить органы дыхания от попадания в них хлора можно тряпичной повязкой, смоченной раствором сульфита натрия Na2SO3 или тиосульфата натрия Na2S2O3.
Хлор был одним из первых химических отравляющих веществ, использованных Германией в Первую мировую войну, впервые применен в 1915 году во время битвы при Ипре.