Добавочная долька селезенки что это
Добавочная долька селезенки что это
Институт хирургии им. А.В. Вишневского, Москва
Институт хирургии им. А.В. Вишневского, Москва
Институт хирургии им. А.В. Вишневского Минздрава России, Москва
Институт хирургии им. А.В. Вишневского, Москва
Институт хирургии им. А.В. Вишневского Министерства здравоохранения и социального развития РФ, Москва
Добавочная селезенка в паренхиме поджелудочной железы
Журнал: Хирургия. Журнал им. Н.И. Пирогова. 2018;(8): 68-71
Кригер А. Г., Горин Д. С., Калдаров А. Р., Берелавичус С. В., Ахтанин Е. А. Добавочная селезенка в паренхиме поджелудочной железы. Хирургия. Журнал им. Н.И. Пирогова. 2018;(8):68-71.
Kriger A G, Gorin D S, Kaldarov A R, Berelavichus S V, Akhtanin E A. Intrapancreatic accessory spleen. Khirurgiya. 2018;(8):68-71.
https://doi.org/10.17116/hirurgia2018868
Институт хирургии им. А.В. Вишневского, Москва
Введение. Добавочная селезенка (ДС) — аномалия развития, которая возникает на этапе эмбриогенеза. ДС располагается в связках селезенки и реже — в хвосте поджелудочной железы (ПЖ). ДС в хвосте ПЖ может имитировать нейроэндокринную опухоль или метастаз почечноклеточного рака. Цель — обратить внимание на сложность диагностики ДС, располагающейся в паренхиме ПЖ. Материал и методы. Наблюдали 3 пациентов (2 женщины, 1 мужчина) с ДС в хвосте ПЖ. При обследовании применялись КТ и МРТ. Результаты. Оперировано 2 пациентов. У женщины 43 лет, перенесшей нефрэктомию по поводу почечноклеточного рака, диагностирован метастаз в хвосте ПЖ, у мужчины 61 года — нефункционирующая нейроэндокринная опухоль хвоста ПЖ. В обоих случаях выполнена робот-ассистированная дистальная резекция ПЖ с сохранением селезенки. Послеоперационный период у больных осложнился панкреатическим свищом, не повлиявшим на сроки пребывания в стационаре. Динамическое наблюдение в течение 4 лет проводится за пациенткой 38 лет, у которой по данным КТ и МРТ установлен диагноз ДС хвоста ПЖ. При контрольном обследовании динамики в размере и лучевых характеристиках ДС нет. Заключение. Дифференциальная диагностика ДС, расположенной в паренхиме хвоста ПЖ, является сложной задачей. Сходную рентгенологическую картину имеют нейроэндокринные опухоли, метастазы почечноклеточного рака, солидно-псевдопапиллярная опухоль. При возникновении диагностических затруднений следует склоняться к выполнению миниинвазивного хирургического вмешательства.
Институт хирургии им. А.В. Вишневского, Москва
Институт хирургии им. А.В. Вишневского, Москва
Институт хирургии им. А.В. Вишневского Минздрава России, Москва
Институт хирургии им. А.В. Вишневского, Москва
Институт хирургии им. А.В. Вишневского Министерства здравоохранения и социального развития РФ, Москва
Добавочная селезенка (ДС) ― аномалия развития человека, возникающая на этапе эмбриогенеза. Наиболее часто ДС располагается в связках селезенки, реже ― в хвосте поджелудочной железы (ПЖ) [1―3]. ДС в хвосте ПЖ может имитировать нейроэндокринную опухоль или метастаз почечно-клеточного рака. ДС, как правило, обнаруживают во время операции или планового диспансерного обследования. Дооперационная дифференциальная диагностика ДС, располагающейся в ткани ПЖ, с опухолями этого органа вызывает сложности. Приводим описание 3 пациентов с интрапанкреатической ДС, симулировавшей нейроэндокринную опухоль в 1-м наблюдении, метастаз почечно-клеточного рака ― во 2-м.
Больная Х., 43 лет, была госпитализирована в ФГБУ «Институт хирургии им. А.В. Вишневского» 25.10.17 с диагнозом рак правой почки (T1bN0M0); лапароскопическая правосторонняя нефрэктомия в 2010 г.; прогрессирование заболевания ― метастаз почечно-клеточного рака в хвост П.Ж. На протяжении прошедших лет больная находилась на диспансерном наблюдении в онкологическом диспансере, ей ежегодно выполняли компьютерную томографию (КТ) с контрастированием. При плановой диспансерной КТ в июле 2017 г. выявлена гиперваскулярная опухоль хвоста ПЖ диаметром 18 мм. При сцинтиграфии 21.07.17 патологических изменений не обнаружено. Рентгенологическая картина дифференцировалась между нейроэндокринной опухолью ПЖ и метастазом почечно-клеточного рака.
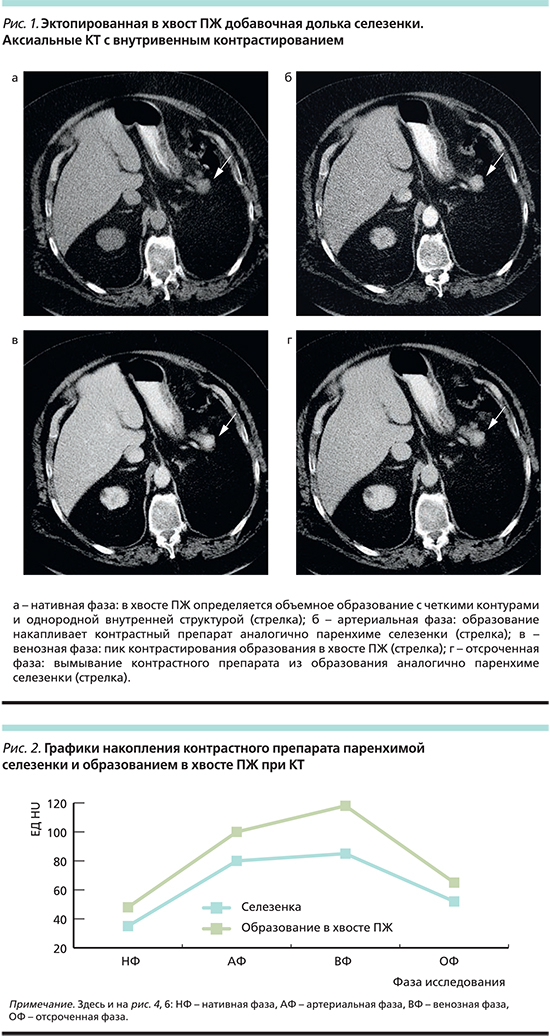
При поступлении в институт состояние удовлетворительное. Жалоб не предъявляла. Физикальное и инструментально-лабораторное обследование не выявило каких-либо отклонений от нормы. При контрольной КТ 10.10.17 в хвосте ПЖ опухоль прежнего размера, накапливающая контрастный препарат (рис. 1, а). 
Больной Н., 61 года, госпитализирован в отделение 13.11.17 с диагнозом нефункционирующая нейроэндокринная опухоль хвоста ПЖ.
При плановом диспансерном обследовании в июле 2017 г., по данным МРТ, в хвосте ПЖ обнаружена гиперконтрастная опухоль диаметром 20 мм. Уровни инсулина, с-пептида в норме. Больному выполнена КТ с внутривенным контрастированием, при котором подтверждено наличие гиперваскулярной опухоли в хвосте ПЖ (рис. 2, а, 
При поступлении в институт состояние удовлетворительное. Жалоб не предъявлял. Сопутствующих заболеваний не выявлено. На основании результатов лучевых методов диагностики (КТ, МРТ) установлен диагноз нефункционирующая нейроэндокринная опухоль хвоста ПЖ ― сT2N0M0. Больной был оперирован 14.11.17 ― выполнена робот-ассистированная дистальная резекция ПЖ с сохранением селезенки. При гистологическом исследовании в толще паренхимы железы выявлена ДС (см. рис. 2, в). Через 6 сут после операции при контрольной КТ обнаружено жидкостное скопление в области культи П.Ж. Произведено дренирование под ультразвуковым контролем, получено 50 мл панкреатогенного содержимого. Проводилась антисекреторная терапия. По дренажу выделялось около 40 мл панкреатогенного отделяемого в сутки. Выписан с дренажом для дальнейшего амбулаторного лечения на 9-й день после операции. Панкреатический свищ закрылся самостоятельно через 29 сут после операции.
Больная М., 38 лет, госпитализирована 27.08.12 с предварительным диагнозом опухоль хвоста ПЖ, которая была выявлена амбулаторно при УЗИ. Больной выполнена КТ с контрастным усилением, при которой в дистальных отделах хвоста ПЖ по задней поверхности определялось образование неоднородной структуры с четкими неровными контурами размерами до 10×18 мм, плотностью до 71 ед. Н и 108 ед. Н, что аналогично ткани селезенки. С целью уточнения диагноза выполнена МРТ, при которой суждение о наличии ДС подтвердилось. Пациентке рекомендовано динамическое наблюдение, выполнение МРТ брюшной полости спустя 6 мес. При контрольном обследовании, по данным МРТ от 16.01.18, имеющееся опухолевидное образование хвоста ПЖ ― без какой-либо динамики.
Обсуждение
ДС ― врожденная аномалия, связанная с нарушением механизмов слияния эмбриональных закладок селезеночной ткани на 5-й неделе эмбриогенеза [4―6]. Структура Д.С. полностью соответствует ткани селезенки. По данным литературы, основанным на материалах аутопсий, ДС может встречаться у 10―20% населения [1, 2]. Наиболее частой локализацией (80%) являются ворота селезенки, в 16% наблюдений ДС наблюдается интрапанкреатическое расположение с локализацией в хвосте ПЖ [1―3].
Как правило, ДС носит бессимптомный характер и является случайной находкой при обследовании по поводу сопутствующих заболеваний. Исключение составляют больные идиопатической тромбоцитопенической пурпурой, имеющие характерную гематологическую симптоматику. При отсутствии клинических проявлений ДС не нуждается не только в хирургическом лечении, но и в динамическом наблюдении, однако основные трудности заключаются в точности диагностики. Учитывая гиперваскулярный характер интрапанкреатической ДС, локализацию в хвосте ПЖ, дифференциально-диагностический ряд должен включать нефункционирующие нейроэндокринные опухоли, солидно-псевдопапиллярную опухоль, а также метастазы почечно-клеточного рака в ПЖ.
Основным методом диагностики является КТ с контрастным усилением, при котором отмечается идентичное контрастирование ДС и основного органа в различные фазы исследования, что тем не менее позволяет лишь заподозрить наличие интрапанкреатической ДС (ИДС) и не дает возможности исключить опухоль П.Ж. Для уточнения диагноза необходимо выполнение МРТ, а в отдельных случаях и тонкоигольной биопсии под контролем УЗИ. При МРТ измеряемые коэффициенты диффузии ДС и основного органа совпадают [5―9].
Дооперационная верификация ИДС позволяет избежать выполнения хирургического вмешательства на ПЖ, сопряженного с высоким риском послеоперационных осложнений. Тем не менее, по данным литературы, в большинстве случаев диагноз ИДС устанавливался на основании послеоперационного морфологического исследования, что в очередной раз подчеркивает отсутствие четких дооперационных диагностических критериев [10―13].
При анализе мировой литературы выявлены 47 случаев упоминания ДС, находящейся в хвосте ПЖ (см. таблицу). 
Заключение
Описанные случаи эктопии ткани селезенки демонстрируют сложность диагностики этой ситуации. Отсутствие клинических проявлений ИДС является причиной того, что ткань селезенки в паренхиме ПЖ обнаруживается лишь при лучевых методах исследования. Сходную рентгенологическую картину имеют нейроэндокринные опухоли, метастазы почечно-клеточного рака, солидно-псевдопапиллярная опухоль небольшого размера. Как показывают наш опыт и данные мировой литературы, провести дифференциальную диагностику среди этих заболеваний чрезвычайно сложно.
Эктопированная ткань селезенки не требует удаления. При возникновении диагностических затруднений и отсутствии возможности исключить опухолевое поражение ПЖ следует решать вопрос в пользу хирургического лечения. Разумный подход к выполнению органосохраняющих и миниинвазивных операций с соблюдением онкологических принципов позволяет свести к минимуму нежелательные последствия вмешательства.
Авторы заявляют об отсутствии конфликта интересов.
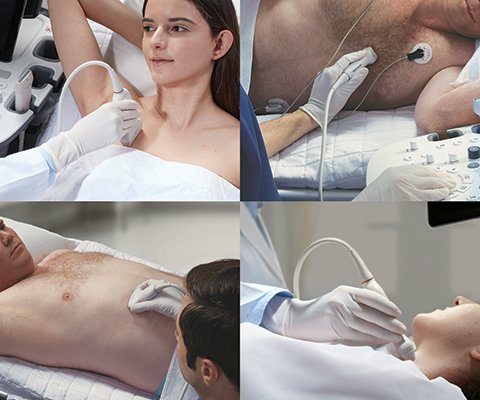
Эхография селезенки у детей и подростков
УЗИ сканер HS60
Профессиональные диагностические инструменты. Оценка эластичности тканей, расширенные возможности 3D/4D/5D сканирования, классификатор BI-RADS, опции для экспертных кардиологических исследований.
Клинико-эхографическая семиотика
Селезенка редко поражается первично, но практически всегда изменяется при гематологических, онкологических, иммунных, сосудистых, инфекционных, системных заболеваниях. Однако обнаружить эти изменения непросто. Ситуацию с выявлением патологии селезенки и возможностью динамического наблюдения радикально изменили ультразвуковые исследования.
Эктопия селезенки может быть как врожденной (наличие дополнительных селезенок или смещение закладки единственной селезенки), так и приобретенной. В последнем случае эктопия может быть при разрыве диафрагмы и смещении селезенки в грудную полость или смещении селезенки в грудную полость при грыже Бохдалека. Описан даже инфаркт селезенки при ее ущемлении в грыжевом отверстии [3].
Селезенка достаточно хорошо фиксирована лиеногастральной и лиеноренальной связками. При отсутствии лиеноренальной связки появляется феномен так называемой подвижной селезенки. Не исключен заворот селезенки (иногда самостоятельно разрешающийся). У детей заворот селезенки чаще всего встречается в возрасте до 1 года, среди взрослых он свойственен женщинам 20-40 лет. Провокаторами могут быть травма, беременность, спленомегалия. Заворот селезенки ведет к нарушению оттока крови, увеличению размеров селезенки, гиперспленизму и ее инфаркту. При допплеровском исследовании кровоток в области ворот селезенки не определяется. Очень редко заворот селезенки приводит к перекруту хвоста поджелудочной железы. Из других аномалий селезенки известна спленогонадная ассоциация. Аномалия только левосторонняя, возникает на 5-6-й неделе внутриутробной жизни. Она обусловлена либо минимальными воспалительными спайками между закладками гонады и селезенки с последующей транслокацией части селезеночной ткани в мошонку, либо тесным контактом закладочных клеток селезенки и половой железы. В большинстве случаев селезенка и яичко в мошонке или селезенка и яичник дискретны и связаны только нежным соединительнотканным жгутиком (дискретный тип спленогонадной ассоциации). При непрерывном типе ассоциации гонада и селезенка связаны селезеночной тканью или фиброзным тяжем с включенными в него дополнительными селезенками. Обычно ортотопно расположенная селезенка не изменена. В редких случаях спленогонадная непрерывная ассоциация сочетается с аномалиями конечностей, челюстей, дополнительными долями легких и печени, атрезией ануса. 50% всех диагностированных случаев спленогонадной ассоциации приходятся на мальчиков до 10 лет. Клинически аномалия проявляется безболезненным увеличением левого яичка без признаков отека мошонки и первоначально трактуется как грыжевое выпячивание. Эхографически обнаруживают дополнительное небольшое (1-2 см в диаметре) образование, расположенное в непосредственной близости от яичка и отличающееся от него по эхотекстуре. Возникают дифференциальнодиагностические сложности при исключении полиорхидии, экстрагонадной опухоли, эпидидимита. Сцинтиграфия с технецием-99m, накапливающимся в селезенке, помогает заподозрить эктопированную селезеночную ткань. Однако окончательный диагноз можно поставить только по результатам операции. Важно, что эхографические находки позволяют избежать орхоэктомии. У девочек аномалия обнаруживается случайно при эхографических исследованиях.
Обилие анатомо-топографических особенностей и сопряженность многих функций в сравнительно небольшом объеме объясняют изменение селезенки в ответ на широкий набор факторов: инфекционных, иммунных, гемодинамических и т. д. Но все они приводят к изменениям размера селезенки и ее плотности.
Термин «спленомегалия» широко применяется для обозначения той или иной степени увеличения селезенки. При спленомегалии различной этиологии в селезенке происходят и разные структурные изменения. Так, при нарушениях оттока крови из селезенки (портальная гипертензия, сдавление v. lienalis) общая длина синусов в результате их новообразования резко увеличивается, а поперечник оказывается меньше, чем в норме. Число клеток стенок синусов уменьшается (на единицу площади стенки синуса, или см²), общее число фагоцитоактивных клеток резко увеличивается. При спленомегалии в ответ на усиленный внутриселезеночный распад эритроцитов увеличиваются расширяются тяжи пульпы с увеличением фагоцитирующих клеток и гиперплазией клеток синусов.
Ультразвуковые исследования являются первыми, а нередко и завершающими при исключении патологии селезенки.
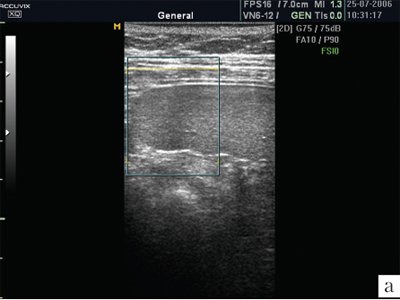
Капсула селезенки чрезвычайно тонкая, поэтому не визуализируется. Но благодаря капсуле изображение края селезенки предстает очень четким, хотя бывает сложно, особенно у полных пациентов, отграничить латеральный край селезенки от брюшной стенки. От капсулы селезенки в паренхиму отходят тончайшие соединительнотканные прослойки, которые намечают деление на дольки, хотя полностью дольчатого строения нет, поэтому орган очень хрупкий, особенно при спленомегалии, когда соотношение паренхимы и соединительной ткани резко изменяется в пользу первой составляющей. В норме эхографическое изображение селезенки гомогенное. Эхогенность селезенки у новорожденных, детей раннего и младшего возраста ниже, чем у взрослых, что объясняется слабым развитием трабекулярной ткани и полностью повторяет возрастную динамику эхоструктуры лимфатических узлов. Эхогенность ворот селезенки выше, чем ее паренхимы. В самой селезенке при использовании датчиков с частотой излучения 3-5 МГц регистрируется большое количество мелких линейных или точечных сигналов. Использование датчиков высокой частоты (13 МГц) позволило доказать, что эти сигналы являются отражением ультразвука от лимфоидных фолликулов (белой пульпы). Коэффициент корреляции с гистологическими находками оказывается очень высоким (r=0,71; p=0,03) [4]. Построение изображения в различных режимах открывает новые перспективы в возможностях оценки структуры селезенки. Ультразвуковое изображение селезенки в режиме МРТ позволяет лучше визуализировать паренхиму, убрать посторонние сигналы (рис. 1).
а) Изображение селезенки при ультразвуковом сканировании в обычном режиме. В паренхиме определяется множество дополнительных эхосигналов.
Добавочная долька селезенки что это
И.А. Антюхова, Б.М. Медведева, А.Б. Лукьянченко
Национальный медицинский исследовательский центр онкологии им. Н.Н. Блохина, Москва, Россия
Введение
Добавочные селезенки встречаются нередко и обычно возникают на 5-й неделе эмбриогенеза в результате нарушения слияния в группах мезодермальных клеток дорсального мезогастрия, приводящего к формированию одного или нескольких отдельно расположенных узелков, не слившихся с основной массой селезенки [1, 2].
Подобные случаи не являются редкостью. По данным 3000 проведенных аутопсий было выявлено 364 добавочные селезенки, из которых 61 обнаружена в хвосте поджелудочной железы – ПЖ [1, 3]. Хотя хвост ПЖ и ворота селезенки являются наиболее распространенными местами эктопии, добавочные селезенки могут обнаруживаться в желудке, тощей кишке и ее брыжейке, а также в яичниках и яичках [1, 3]. Подчеркивается, что корректное распознавание обсуждаемого варианта развития селезенки не всегда бывает успешным [1, 4]. Не проявляя себя клинически, эктопированная в хвост ПЖ ткань селезенки зачастую принимается за опухоль, вследствие чего пациенты могут подвергаться неадекватным хирургическим вмешательствам. Именно поэтому необходимо уметь дифференцировать эктопированную добавочную селезенку (не требующую лечения) с другими сóлидными поражениями ПЖ, подлежащими оперативным вмешательствам.
В данной статье представлен обзор шести клинических наблюдений эктопированной селезенки в хвост ПЖ. Во всех шести случаях, используя комплексный диагностический подход, нам удалось поставить правильный диагноз и избежать неоправданных хирургических вмешательств.
Клинический обзор
С 2016 по 2018 г. мы наблюдали 6 пациентов (4 женщины и 2 мужчины) в возрасте 43–68 лет с эктопированными в хвост ПЖ добавочными дольками селезенки.
Результаты ультразвукового исследования (УЗИ) органов брюшной полости всех шести пациентов свидетельствовали о наличии новообразования в хвосте ПЖ без уточнения его природы, что послужило основой для дальнейших исследований. Четырем из шести пациентов была выполнена магнитно-резонансная томография (МРТ), позволившая однозначно опровергнуть опухолевую природу новообразования. Пятому пациенту с противопоказаниями к проведению МРТ была выполнена компьютерная томография (КТ). Шестому пациенту из-за сложностей трактовки наблюдаемой картины проведено комплексное исследование (КТ и МРТ) с динамическим контролем через 8 месяцев.
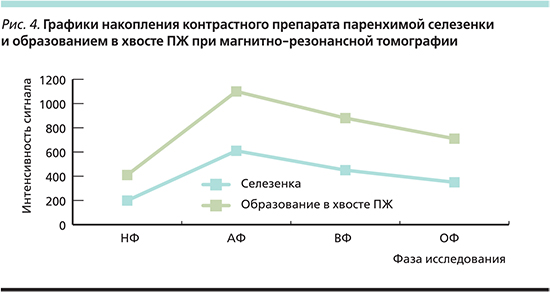
В четырх случаях при МРТ отображение эктопированных селезенок полностью соответствовало отображению основной селезенки и было гипоинтенсивным на Т1-томограммах и ИКД (измеряемый коэффициент диффузии)-картах, повышенной интенсивности на Т2-томограммах и на диффузионно-взвешенных изображениях (ДВИ). При внутривенном контрастировании пик накопления контрастного препарата в них отмечался в ранние фазы исследования (артериальную или венозную). При КТ особенности накопления контрастного препарата в эктопированной дольке были аналогичными таковым в основной селезенке. В 3 из 6 случаев добавочные дольки наблюдались также и в воротах основной селезенки.
Клиническое наблюдение 1
В НМИЦ онкологии им. Н.Н. Блохина обратился мужчина 68 лет, у которого по данным УЗИ при плановом медицинском осмотре по месту жительства выявлено новообразование хвоста ПЖ. Каких-либо жалоб пациент не предъявлял. Уровни маркеров СА (Cancer Antigen)19-9 и РЭА (раково-эмбриональный антиген) были в пределах нормы.
По данным УЗИ в области хвоста ПЖ, определено гипоэхогенное образование с четкими неровными контурами размером около 2,0×2,5 см в поперечнике. С целью уточнения характера выявленного образования пациенту выполнена КТ (от проведения МРТ пациент отказался ввиду клаустрофобии).
При КТ абдоминальной области с внутривенным контрастированием в хвосте ПЖ выявлено округлое объемное образование с четкими контурами и однородной внутренней структурой с КА (коэффициент абсорбции)=+48 HU, которое как при нативном исследовании, так и при внутривенном контрастировании отображалось аналогично ткани основной селезенки (рис. 1 а–г, рис. 2). Именно поэтому данное образование было расценено нами как эктопированная в хвост ПЖ добавочная долька селезенки.
Клиническое наблюдение 2
У пациентки 62 лет с жалобами на умеренно выраженные абдоминальные боли при УЗИ по месту жительства было выявлено новообразование в хвосте ПЖ, расцененное как опухоль. Для уточнения характера изменений и выбора тактики лечения пациентка направлена в НМИЦ онкологии им. Н.Н. Блохина.
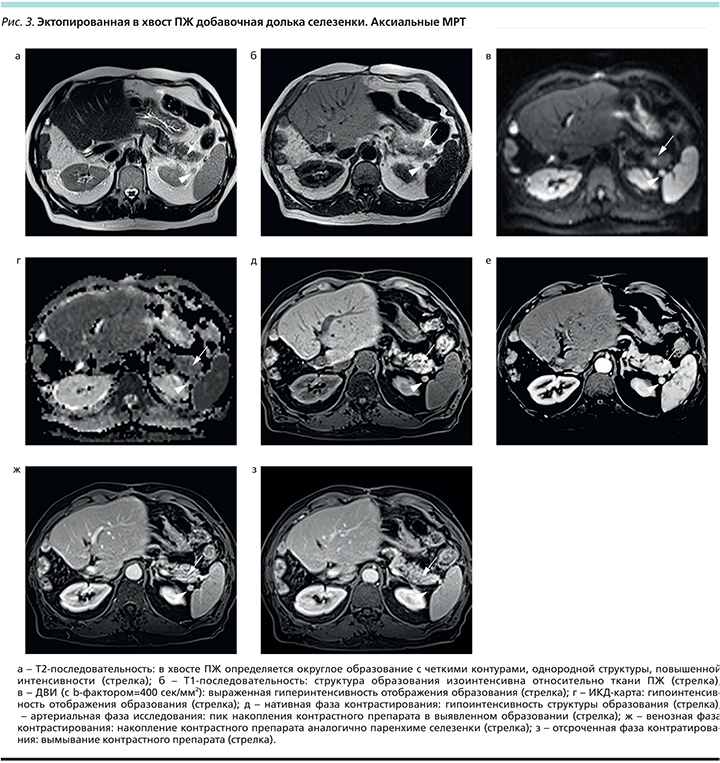
С целью дообследования была выполнена МРТ органов брюшной полости с внутривенным контрастированием: в области хвоста ПЖ обнаружено округлой формы образование (около 1,2 см в диаметре) с четкими контурами и однородной структурой повышенной интенсивности в Т2 (рис. 3а), изоинтенсивное в Т1 (рис. 3б), на ДВИ – гиперинтенсивное при всех значениях b-value (рис. 3в), но гипоинтенсивное на ИКД-картах (рис. 3г). Пик накопления контрастного препарата в данном образовании отмечен в артериальную фазу (рис. 4), при этом кривая контрастирования была аналогичной таковой в ткани основной селезенки (рис. 5д–з). Можно отметить, что у данного пациента была еще одна добавочная долька селезенки (расположенная в области ее ворот), которая имела схожую картину с выявленным образованием в ПЖ (головка стрелки, рис. 3а–з).
Клиническое наблюдение 3
В НМИЦ онкологии им. Н.Н. Блохина поступила женщина 42 лет, у которой, по данным УЗИ, при медицинском осмотре по месту жительства выявлено опухолеподобное образование хвоста ПЖ. При УЗИ органов брюшной полости в НМИЦ данное образование также было расценено как опухоль хвоста ПЖ, однако при обследовании уровни маркеров СА 19-9 РЭА были в пределах нормы.
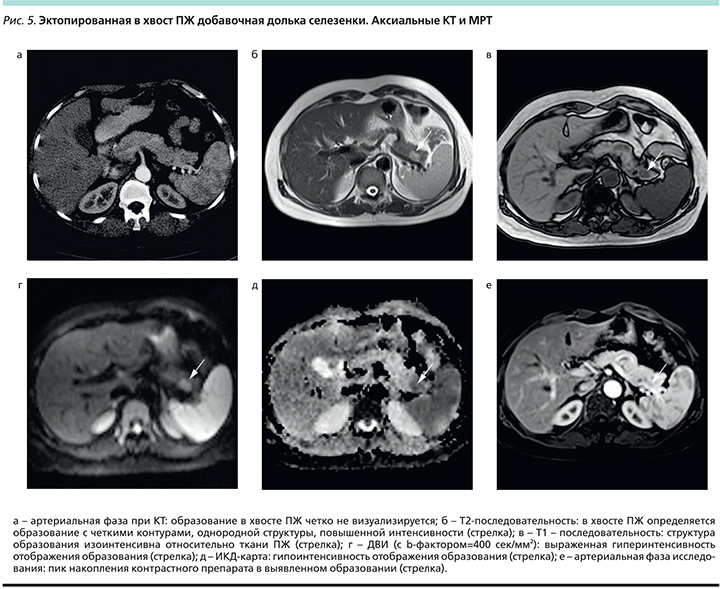
С целью дообследования пациентке выполнены КТ и МРТ органов брюшной полости с внутривенным контрастированием. При КТ с внутривенным контрастированием дополнительных узловых образований в ПЖ четко не определялось (рис. 5а). При МРТ в области хвоста ПЖ было выявлено образование с четкими контурами размером до 1,0×1,7 см повышенной интенсивности в Т2 (рис. 5б), изоинтенсивное – в Т1 (рис. 5в), на ДВИ – гиперинтенсивное при всех значениях b-value (рис. 5г), а также гипоинтенсивное на ИКД-картах (рис. 5д).
Пик накопления контрастного препарата в данном образовании был отмечен в артериальную фазу (рис. 5е, рис. 6), и оно также было расценено как эктопированная добавочная долька в хвост ПЖ. Пацентке было рекомендовано наблюдение в динамике, и спустя 8 месяцев при повторном обследовании МР-картина образования сохранялась прежней, размер его не изменился, что опровергало его опухолевую природу.
Обсуждение
Эктопированные в хвост ПЖ добавочные дольки селезенки встречаются нередко, но их дифференциальная диагностика с опухолевыми поражениями крайне важна во избежание неадекватных хирургических мероприятий. Высокая частота ложноотрицательных результатов пункционной биопсии (20%) и ее возможные осложнения не позволяют использовать в рутинной практике этот метод верификации [1, 5]. Поэтому применение неинвазивных лучевых методов диагностики следует считать более приемлемым.
При УЗИ добавочная долька селезенки выглядит как округлое гипоэхогенное образование с однородной внутренней структурой. При использовании соответствующих методик внутривенного контрастирования и допплеровского режима выявляются характерные особенности ее кровоснабжения (с чувствительностью 90% и специфичностью 60%) [6–8].
Нативная КТ не позволяет отчетливо визуализировать эктопированную дольку селезенки в хвосте ПЖ. Исследование с внутривенным контрастированием позволяет выявлять наличие новообразования, по особенностям своего отображения отличного от паренхимы ПЖ, однако уточнить его характер (природу) бывает затруднительно.
МРТ с внутривенным контрастированием в сочетании с диффузионно-взвешенной МРТ позволяет наиболее точно выявлять полное соответствие особенностей отображения селезенки с ее эктопированной долькой, что служит основанием для установления корректного диагноза и исключения опухолевой природы обнаруженных изменений.
Заключение
Из трех упомянутых методов лучевой диагностики (УЗИ, КТ и МРТ) наиболее результативным в дифференциальной диагностике опухолевых новообразований хвоста ПЖ и эктопированной дольки селезенки следует считать МРТ с внутривенным контрастированием в сочетании с методикой ДВИ. Применение данного метода, на наш взгляд, позволяет ставить корректный диагноз и таким образом избегать неоправданных инвазивных мероприятий и хирургических вмешательств.
Литература
1. George M., Evans T., Lambrianides A.L. Accessory spleen in pancreatic tail. J. Surg. Case Rep. 2012;2012(11):rjs004. Doi: 10.1093/jscr/rjs004.
2. Dodds W.J., Taylor A.J., Erickson S.J., et. al. Radiologic imaging of splenic anomalies. Am. J. Roentgenol. 1990;155:805–10.
3. Halpert B., Gyorkey F. Lesions observed in accessory spleens of 311 patients. Am. J. Clin. Pathol. 1959;32:165–68.