Если не помогает верошпирон что принимать
Торасемид — новая возможность в лечении пациентов с хронической сердечной недостаточностью и артериальной гипертензией
Торасемид — петлевой диуретик пролонгированного действия, характеризуется высокой биодоступностью и благоприятными фармакодинамическими свойствами. Представлены данные о клинической эффективности применения торасемида при лечении пациентов с хронической с
Torsemide — loop diuretic prolonged action, has high bioavailability and favorable pharmacodynamic properties. The article presents data on the clinical efficacy of torasemide in patients with chronic heart failure and hypertension.
Согласно данным эпидемиологических исследований распространенность клинически выраженной хронической сердечной недостаточности (ХСН) в Российской Федерации составляет 4,5% (5,1 млн человек), годовая смертность данной категории пациентов — 12% (612 тыс. больных) [1, 2]. Основными причинами развития ХСН является в 88% случаев наличие артериальной гипертензии (АГ), а в 59% ишемической болезни сердца, комбинация данных заболеваний встречается у каждого второго пациента с ХСН [3]. При этом среди всех больных с сердечно-сосудистыми заболеваниями основной причиной госпитализации в 16,8% в любой стационар служит декомпенсация ХСН [2].
Декомпенсация ХСН проявляется на практике усилением одышки, застоем в легких и при осмотре выраженными отеками нижних конечностей. Основным мероприятием терапии является коррекция водного гомеостаза как важнейшего инструмента гармонизации нейрогуморального дисбаланса. В данной ситуации диуретики — препараты первой линии при лечении острой и хронической сердечной недостаточности [4]. В ежедневной клинической практике каждый врач — кардиолог, терапевт сталкивается с необходимостью назначения препарата из группы диуретиков для лечения пациентов с ХСН, АГ, что требует огромного врачебного искусства, так как нерациональное применение препаратов этой группы является одной из важных причин декомпенсации ХСН [5].
Диуретики — это гетерогенная группа препаратов, увеличивающая объем выделяемой мочи и экскрецию натрия. Различаются по механизму действия, фармакологическим свойствам и соответственно показаниям к назначению. В соответствии с механизмом действия препараты делятся на 4 класса [6]:
В кардиологии активно применяются последние 3 класса диуретиков. Наиболее мощным диуретическим эффектом обладают петлевые диуретики, именно их применение рекомендовано у пациентов с клинически выраженными проявлениями ХСН [4]. Помимо мочегонного действия петлевые диуретики через индукцию синтеза простагландинов способны вызывать дилатацию почечных и периферических сосудов [7]. Ярким представителем данного класса является фуросемид, применяемый с 1959 года до настоящего времени при лечении остро декомпенсированной и терминальной ХСН [8]. Однако его ежедневное применение вызывает дискомфорт у пациентов, который выражается в императивном позыве к мочеиспусканию в течение 1–2 часов после приема, отмечается ортостатическая гипотензия на пике активности препарата, все это способствует снижению приверженности к лечению.
В этой связи появление на отечественном фармакологическом рынке петлевого диуретика пролонгированного действия — оригинального торасемида в 2011 г. позволило не только более качественно и эффективно лечить пациентов с ХСН, но и повысить комплаентность среди пациентов. Торасемид, как и все петлевые диуретики, ингибирует реабсорбцию натрия и хлоридов в восходящей части петли Генле, но в отличие от фуросемида блокирует также эффекты альдостерона, т. е. в меньшей степени усиливает почечную экскрецию калия. Это снижает риск развития гипокалиемии — одной из главных нежелательных лекарственных реакций петлевых и тиазидных диуретиков. Главным преимуществом торасемида является наличие у него камедьсодержащей оболочки, которая замедляет высвобождение действующего вещества, что уменьшает колебания его концентрации в крови и, следовательно, обеспечивает более стойкий и длительный эффект [9]. Фармакокинетические свойства торасемида отличаются от фуросемида, отличия представлены в табл.
Важным преимуществом торасемида является высокая биодоступность, которая составляет более 80% и превосходит таковую у фуросемида (50%). Биоусвояемость торасемида не зависит от приема пищи, в связи с чем, в отличие от фуросемида, появляется возможность применять его в любое время суток. Высокая и предсказуемая биодоступность определяет надежность диуретического действия торасемида при ХСН и позволяет более успешно применять препарат перорально, даже при случаях тяжелой ХСН [10]. Преимуществом торасемида пролонгированной формы является медленное высвобождение действующего вещества, что не приводит к развитию ярко выраженного пика действия и позволяет избежать феномена «повышенной постдиуретической реабсорбции». Это свойство представляется очень важным в аспекте обсуждаемой проблемы безопасности, так как с ним связывается уменьшение риска рикошетной гиперактивации нейрогормональной системы. Кроме того, однократный прием торасемида в сутки повышает приверженность пациентов к лечению согласно данным исследования на 13% в сравнении с терапией фуросемидом [11].
Торасемид метаболизируется цитохромом Р450, чем объясняется отсутствие изменений его фармакокинетических свойств у пациентов с сердечной недостаточностью или хронической болезнью почек. Только 25% дозы выводится с мочой в неизмененном виде (против 60–65% при приеме фуросемида). В связи с этим фармакокинетика торасемида существенно не зависит от функции почек, в то время как период полувыведения фуросемида увеличивается у больных с почечной недостаточностью. Действие торасемида, как и других петлевых диуретиков, начинается быстро. Доза торасемида 10–20 мг эквивалентна 40 мг фуросемида. При увеличении дозы наблюдалось линейное повышение диуреза и натрийуреза [11].
Торасемид является единственным мочегонным средством, эффективность которого подтверждена в крупных многоцентровых исследованиях [12–14]. Так, в одном из самых крупных до настоящего времени исследовании TORIC (TORasemide In Chronic heart failure) было включено 1377 больных с ХСН II–III ФК (NYНА), рандомизированных к приему торасемида (10 мг/сут) или фуросемида (40 мг/сут), а также других диуретиков. В исследовании оценивали эффективность, переносимость терапии, динамику клинической картины, а также смертность и концентрацию калия в сыворотке крови. По результатам данного исследования терапия торасемидом была достоверно эффективней и позволяла улучшить функциональный класс у пациентов с ХСН, и значительно реже на данной терапии отмечалась гипокалиемия (12,9% против 17,9% соответственно; р = 0,013). Также в ходе исследования была выявлена достоверно более низкая общая смертность в группе пациентов, принимавших торасемид (2,2% против 4,5% в группе фуросемида/другие диуретики; p
ГБОУ ВПО ОмГМА МЗ РФ, Омск
Обзор таблеток от повышенного давления нового поколения
Частое повышение показателей артериального давления (АД) – причина развития серьезных заболеваний (инсульт, инфаркт миокарда и пр.). Гипертоническая болезнь в России диагностируется у каждого третьего человека преклонного возраста. Для борьбы с гипертонией многим пациентам приходится принимать препараты на протяжении всей жизни, чтобы исключить осложнения.
Современные фармакологические компании предлагают большой выбор лекарственных средств, эффективных при гипертонии. Если не знаете, как выбрать таблетки от повышенного давления, ознакомьтесь с рейтингом, представленным ниже. В ТОП вошли лучшие медикаменты с учетом эффективности, стоимости и отзывов.
Классификация препаратов от повышенного давления
Причины гипертонии
Когда нужно вызвать врача на дом при повышении давления?
Общепринятые показатели АД – 120/80. Параметры могут незначительно варьировать в зависимости от времени суток, физической активности и возраста человека.
Таблица – Показатели артериального давления и рекомендации
Артериальная гипертония – пожизненный прием препаратов?
Диагноз АГ обычно не ставится после однократного измерения давления, за исключением тех случаев, когда показатели слишком высоки, например, свыше 170-180/105-110 мм рт. ст. Обычно проводят серию измерений в течение определенного периода времени, чтобы полностью исключить случайные колебания и неточности. Необходимо также принимать во внимание и те обстоятельства, во время которых проводятся измерения артериального давления. Как правило, показатели давления увеличиваются под воздействием стресса, после крепкого кофе или выкуренной сигареты.
Интересен факт, что в кабинете врача при измерении давления показатели могут быть выше, чем в состоянии покоя, дома. Этот эффект называется «гипертонией белого халата» и вызван страхом пациента перед заболеванием или перед доктором. Кроме измерения артериального давления врач обычно проверяет изменения со стороны других органов, особенно если показатели давления находятся на уровне высоких цифр.
Если показатели давления у взрослого не превышают 140/90 мм. рт. ст., то повторное измерение обычно проводят не раньше, чем через год. У пациентов, чье давление находится в пределах от 140/90 до 160/100, проводят повторное измерение через небольшой промежуток времени для подтверждения диагноза.
Высокое диастолическое (нижнее) давление, например 110 или 115 мм.рт.ст., свидетельствует о необходимости немедленной терапии.
Артериальная гипертония чаще всего носит первичный характер и является симптомом гипертонической болезни. Реже повышенное артериальное давление вторично и является признаком заболеваний различных органов (почек, сосудов и др.). Каждое из этих заболеваний нуждается в специальном лечении, вот почему любое повышение артериального давления требует консультации врача-кардиолога.
Если же значения артериального давления превышают указанный уровень, то следует обсудить с врачом возможные причины недостаточной эффективности проводимого лечения. Среди них:
Как показывает практика, при доверии пациента к своему лечащему врачу, при грамотном взаимодействии врача и пациента, в большинстве случаев удается контролировать это грозное заболевание.
А что, если Вы уже принимаете 3 или больше препаратов, а давление так и не стабилизировалось на целевом уровне? Подобная форма гипертонии относится к резистентной.
Каков же выход?
Обычно в случае резистентной (рефрактерной) гипертонии врачи продолжают увеличивать дозы принимаемых пациентом препаратов до максимально переносимых или добавляют последовательно четвертый, пятый, иногда и шестой препарат из других групп. Пациенты реагируют на это по-разному. Многие перестают доверять врачу, некоторые отказываются от приема препаратов совсем, потому что не отмечают никакой разницы между давлением на фоне приема горстей препаратов, и без них.
Конечно же, это решение ошибочно в корне. Для того чтобы избежать прогрессирующего поражения органов-мишеней и грозных осложнений в будущем, продолжать прием препаратов необходимо даже в случае, если достичь целевого уровня АД не удается. Но, никто не будет отрицать, использование многокомпонентной комбинации препаратов значительно увеличивает риск развития побочных эффектов и непредсказуемых реакций взаимодействия препаратов между собой.
Что современная медицина может предложить в этом случае? Оказывается, есть выход.
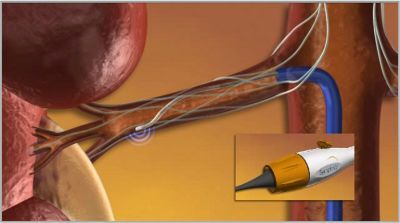
В скором времени в нашей клинике мы будем иметь возможность предложить нехирургический метод коррекции АД путем денервации почечных артерий. Новая процедура, катетерная почечная денервация почечных артерий, помогает контролировать высокое кровяное давление путем деструкции части нервных волокон, расположенных в стенке почечных артерий.
Как нередко бывает, идея денервации не нова, это хорошо забытое старое. Хирургам давно было известно, что иссечение симпатических нервных волокон, ответственных за поддержание артериального давления, приводило к снижению артериального давления. Но процедуру нельзя было применять для лечения АГ, так как она сопровождалась высокой операционной смертностью и такими долгосрочными осложнениями как тяжелая гипотония при переходе в вертикальное положение, вплоть до потерь сознания, нарушений функции кишечника и тазовых органов. Но так бывает потому, что полностью выключается симпатическая стимуляция почек и других органов, что приводит к дисбалансу нервной регуляции. Поскольку симпатические нервные волокна, иннервирующие почку, проходят непосредственно в стенке главной почечной артерии и прилежат к ней, то с помощью катетерной радиочастотной абляции (РЧА) прицельное разрушение волокон в почечных артериях не приведет к нарушению иннервации органов брюшной полости и нижних конечностей. Кроме того, разрушая лишь небольшую часть нервных окончаний в почечных артериях, почки не лишаются нервной регуляции. ПРИЧИНА РЕЗИСТЕНТНОЙ ГИПЕРТОНИИ В ИЗБЫТОЧНОЙ СИМПАТИЧЕСКОЙ АКТИВНОСТИ ПОЧЕК. А катетерная РЧА позволяет устранить эту избыточную активность. ГИПЕРТОНИЯ СТАНОВИТЬСЯ УПРАВЛЯЕМОЙ.
Введение этой процедуры в нашу практику базируется на исследовании, опубликованном в знаменитом журнале Lancet, которое показало безопасность и эффективность методики, позволяющей достигнуть стойкого снижения артериального давления до 30 мм. рт. ст. от исходного уровня.
Для подобного лечения используется радиочастотный катетер фирмы Ардиан, который вводится через прокол в бедренной артерии. Далее катетер проводится под рентгеновским контролем в почечную артерию. Через кончик катетера радиочастотная энергия дозировано подается по окружности в 4-5 точках почечных артерий. Процедура занимает около 40 мин, после чего катетер удаляется. Длительность пребывания пациента в стационаре составляет 24 ч. Условием для проведения процедуры является нормальная функция почек. Но самое поразительное в процедуре то, что со временем лечебный эффект не только не уменьшается, а наоборот, артериальное давление у большинства плавно и стойко нормализуется.
В настоящее время почечную денервацию применяют только у пациентов с резистентной гипертензией. Это должно привести, примерно, к 50-процентному снижению числа осложнений и смертности, связанных с АГ. Это не означает, что препараты больше не нужны. Пациентам все равно, скорее всего, придется принимать лекарства от высокого давления, но количество препаратов для поддержания артериального давления на целевом уровне, значительно снизится.
Каковы побочные эффекты метода РЧА почечных артерий?
На сегодняшний день во всем мире не отмечено никаких серьезных осложнений катетерной почечной денервации. Процедура сопровождалась умеренной болью в животе, которая была купирована внутривенным введением анальгетиков и седативных средств. Только у одного больного отмечено повреждение почечной артерии катетером до РЧА, устраненная имплантацией стента. Наиболее распространенным осложнением у незначительного числа пациентов была болезненность и припухлость в области паха. Ухудшения функции почек не отмечено.
Кому необходимо проводить почечную денервацию?
Даннное вмешательство показано пациентам с резистентной АГ, т.е. при стойком повышении систолическоого (верхнего) артериального давления выше, чем 160 мм рт. ст., несмотря на применение 3 и более антигипертензивных препаратов, включая диуретик. Это особенно показано при плохой переносимости комбинации препаратов или при наличии побочных эффектов. При этом пациенты должны быть предварительно обследованы, у них должны быть надежно исключены возможные вторичные причины артериальной гипертензии (например, заболевания надпочечников). На предварительном этапе обязательно проведение компьютерной томографии почечных артерий для уточнения анатомических особенностей сосудов.
Лекарства от высокого давления для пожилых
Артериальное давление считается одним из главных показателей состояния организма, так как оно отражает работу сердечно-сосудистой, эндокринной и нервной системы, почек, кроветворения. Повышение давления может быть эпизодическим или стойким. Универсальных лекарств от высокого давления у пожилых людей не бывает — препараты должны назначаться врачом, с учетом клинической картины и индивидуальных особенностей пациента.
первичной, когда она высокое давление является ведущим симптомом;
вторичной, когда она сопровождает заболевания почек, эндокринной и нервной системы. В этом случае повышенное давление — один из симптомов.
Гипертония относится к числу хронических заболеваний, которые могут прогрессировать, поэтому требует постоянной терапии. Чтобы поддерживать давление в пределах нормы, нужен хороший препарат. Выбрать его можно только после диагностики, по рекомендациям специалиста.
Причины повышенного давления у пожилых
почек и надпочечников;
стенозе (коарктации) аорты и атеросклерозе.
Факторами риска считаются также употребление большого количества соли, нервные перегрузки, наследственность, вредные привычки.
Пациентам старше 60 лет рекомендуется обращаться к врачу, если есть хотя бы один из следующих симптомов:
головная боль, локализованная в области затылка и сопровождающаяся головокружением;
чувствительность к перемене погоды;
повышенная утомляемость, общая слабость, нарушения памяти;
ощущение удушья, боли в груди;
повторяющиеся приступы тошноты.
Виды препаратов
Лекарства от повышенного давления для пожилых людей можно разделить на:
Антагонисты кальция
Артериальные сосуды сохраняют тонус в норме, благодаря ионам кальция. Средства с их содержанием способствуют расслаблению сосудистых стенок, из-за чего снижается артериальное давление. Из побочных действий отмечается учащенное сердцебиение, периодическое головокружение.
Дилтиазем
Препарат назначается при диагностировании серьезных патологий сердца, вызванных прогрессирующей гипертонией.
наличие артериальной гипертензии;
профилактические меры при загрудинных болях (приступы стенокардии);
предупреждение развития аритмии, представленной наджелудочковыми пароксизмами, экстрасистолией, трепетаниями и мерцаниями предсердий.
Патогенетические подходы к диуретической терапии асцита у больных циррозом печени
Асцит — одно из самых значимых осложнений цирроза печени, которое возникает примерно у 40–50% пациентов за 10-летний период от постановки диагноза. Развитие асцита считают важным неблагоприятным прогностическим признаком прогрессии заболевания
Асцит — одно из самых значимых осложнений цирроза печени, которое возникает примерно у 40–50% пациентов за 10-летний период от постановки диагноза. Развитие асцита считают важным неблагоприятным прогностическим признаком прогрессии заболевания, так как он связан с50% смертностью втечение двух ближайших лет [23, 26].
До настоящего времени механизмы формирования асцита при циррозе печени остаются недостаточно ясными. Каким образом накапливается жидкость в брюшной полости, в чем физиологическая сущность данного процесса, какова его связь с центральной гемодинамикой, состоянием почек и брюшины? Почему именно данный синдром является поворотным в жизни пациентов с циррозом и независимо от этиологии заболевания определяет дальнейшую выживаемость и качество жизни этих больных?
Кроме того, прогрессивный рост фармакологического рынка почти не заметен в гепатологии. Тогда как в других областях медицины, например в кардиологии, ежегодно принимаются согласительные документы по лечению пациентов с сердечной недостаточностью (СН), куда включаются новые мочегонные препараты, оптимизируются схемы и подходы к терапии. Лечение отечно-асцитического синдрома у кардиологического больного четко отработано, тогда как обсуждение принципов курации гепатологического пациента влечет за собой целый ряд споров и разногласий.
Эти и многие другие вопросы уже сегодня требуют своего разрешения, прежде всего для врачей-специалистов, ежедневно участвующих в лечении больных хроническими заболеваниями печени.
Механизмы возникновения асцита у больных циррозом печени
Развитие асцита обусловлено повышенной лимфопродукцией в печени в связи с блокадой оттока из нее венозной крови, однако его возникновение начинается с момента повреждения гепатоцитов, т. е. с этапа гепатита.
Основными механизмами развития отечно-асцитического синдрома являются (рис.):
Остановимся на более детальном рассмотрении данных положений.
Развитие синдрома печеночно-клеточной недостаточности (ПКН) у больных циррозом печени. Характеризуется:
Выброс вазодилятаторов и цитокинов поврежденными гепатоцитами. Нарушение детоксицирующей функции печени, развитие ПКН и порто-кавального шунтирования способствуют проникновению в кровь из поврежденных гепатоцитов вазодилятаторов, таких как глюкагон, оксид азота, простагландин E2α, предсердный натрий-уретический гормон, вазоинтестинальный пептид, простациклин, что приводит к генерализованной вазодилятации и снижению общего периферического сопротивления сосудов (ОПС). При этом в эндотелии сосудов печени, под влиянием эндотоксинов и цитокинов, синтезируются мощные вазоконстрикторы, в частности эндотелин-1, что вызывает спазм сосудов. То есть происходит разобщение местного и общего кровотока, связанное с дисбалансом вазодилятирующих и вазоконстриктивных веществ, что приводит:
Активация САС и РААС. Активированные САС и РААС воздействуют на основные мишени:
Основными факторами поражения ССС при циррозе печени являются шунтирование крови с прямым токсическим воздействием на миокард биологически активных веществ (адреналина, гистамина, серотонина), дисметаболические расстройства, связанные с нарушением печеночных функций, вегетативные нарушения, длительная гиперактивация САС и РААС [7, 35, 38]. Совокупность нарушений обмена биологически активных веществ приводит к развитию так называемой метаболической кардиомиопатии с дилятацией полостей сердца и СН. Данное состояние усугубляется хронической функциональной перегрузкой сердца на фоне гиперкинетического типа кровообращения [2, 4, 6]. То есть при развитии заболевания печени развивается системная реакция, которая реализуется через вовлечение в процесс ССС, формируя аналогичные СН способы компенсации и декомпенсации с возникновением отечно-асцитического синдрома [11, 12, 34].
Основными факторами поражения почек при циррозе печени являются:
Поражение почек развивается вследствие нарушения баланса между системной вазодилятацией и почечной вазоконстрикцией. Несмотря на характерную для цирроза печени системную вазодилятацию, в почках, как и в печени, происходит вазоконстрикция, что приводит к снижению скорости клубочковой фильтрации, уровень ренина в плазме при этом возрастает. Натрий компенсаторно усиленно реабсорбируется в почечных канальцах, что вызывает повышение осмолярности мочи. Происходит накопление жидкости в организме, несмотря на нормальный объем мочи, малосолевую диету и диуретическую терапию. Во внепочечных сосудах преобладает расширение артерий, и в результате снижается ОПС с развитием артериальной гипотензии. Сердечный выброс не изменяется или даже повышен, однако эффективный почечный кровоток уменьшается в результате перераспределения кровотока в селезенку, кожу и другие органы, таким образом происходит шунтирование коркового слоя почек. Наиболее ранним признаком включения почечного механизма при развитии асцита у больных циррозом печени является задержка натрия в организме, что проявляется снижением суточной экскреции натрия с мочой менее 78 ммоль/сут [8, 16].
Задержка натрия почками — это одна из вероятных причин асцита, предшествующая накоплению асцитической жидкости. На ранних этапах она является результатом блокады венозного оттока из печени и первичной вазодилятации.
Формирование ПГ. Развитие мощного дисбаланса вазоактивных веществ, вызывающего спазм синусоидов, а также способствующего активному фиброгенезу в печени, с формированием цирротических узлов, приводят к нарушению венозного русла печени и развитию ПГ.
Обратимость асцита определяется стадией ПГ. Асцит потенциально обратим, если имеется функциональная ПГ, и необратим, если произошли изменения сосудистого русла печени и сформировалась органическая ПГ [1, 11].
Функциональная (синусоидальная) ПГ определяется [19, 23, 38]:
Органическая ПГ формируется на фоне нарушения цитоархитектоники печени, она определяется [23]:
При этом важно отметить, что даже на этапе органической ПГ сохраняется ее функциональный компонент, который можно уменьшить, используя медикаментозную терапию, направленную на коррекцию состояния САС, РААС, реологию крови и другие патогенетические звенья.
Блокада венозного и лимфатического оттока от печени. Повышенное давление в портальной системе приводит к нарушению венозного оттока из печени и непарных органов брюшной полости, что сопровождается переполнением синусоидов, усилением продукции лимфы в печени.
У больных циррозом печени объем суточного лимфооттока через грудной лимфатический проток может увеличиваться до 20 литров. Лимфа из сосудов печени и непарных органов пропотевает в брюшную полость, формирует асцит, устанавливая динамическое равновесие с процессом всасывания ее в кишечные капилляры.
Таким образом, условно можно выделить несколько уровней формирования асцита, тесно взаимосвязанных между собой:
При этом обратимость указанных изменений зависит от стадии ПГ (функциональной или органической).
Классификация асцита
В зависимости от количества асцитической жидкости и эффективности терапии выделяют:
Критериями резистентного (рефрактерного) асцита являются отсутствие снижения или снижение массы тела менее 200 г/сут у больного в течение 7 дней на фоне низкосолевой диеты (5,2 г поваренной соли в сутки) и интенсивной диуретической терапии (спиронолактон по 400 мг/сут и фуросемид по 160 мг/сут), а также уменьшение экскреции натрия с мочой менее 78 ммоль в сутки [16, 25]. О резистентном асците говорят также в тех случаях, когда он не уменьшается или быстро рецидивирует после парацентеза или осложнения диуретической терапии не позволяют назначать диуретики в эффективных дозах. В практике критерии резистентного асцита выявляются менее чем у 10% пациентов с циррозом печени.
Причинами резистентного асцита, как правило, являются:
Многие причины рефрактерности асцита являются потенциально обратимыми, поэтому своевременное их устранение может значительно повысить эффективность проводимой терапии.
Лечение асцита у больных циррозом печени
Следует отметить, что сама по себе задача терапии асцита у больных циррозом печени труднее, чем лечение других форм накопления жидкости в организме, потому что формирование отечно-асцитического синдрома является проявлением значительной декомпенсации заболевания. По результатам контролируемых исследований появление асцита значительно ухудшает качество жизни и увеличивает риск развития фатальных осложнений цирроза печени [27, 39], поэтому его терапия представляет собой одну из важнейших составляющих успешного лечения этих больных. Однако, с учетом того, что в развитии асцита задействованы сложные нейрогормональные механизмы, бездумная дегидратация может вызвать лишь побочные эффекты и «рикошетную» задержку жидкости.
Режим, диета и потребление жидкости больными циррозом печени и асцитом. У пациентов с асцитом, не ограничивающих потребление соли с пищей, суточная экскреция натрия с мочой снижена до 78 ммоль и менее, при этом внепочечные потери натрия могут достигать 10 ммоль/сут.
Употребление больными циррозом печени натрия более 90 ммоль/сут ведет к развитию асцита, так как каждый грамм натрия задерживает до 200 мл жидкости. Поэтому с пищей в течение суток рекомендуется употреблять не более 90 ммоль натрия (5,2 г поваренной соли), в сочетании с ограничением до 1 литра в сутки количества жидкости. При этом важно учитывать, что ограничение жидкости не показано больным с низким содержанием Nа в сыворотке крови (менее 120 ммоль/л) [16].
На сегодняшний день не опубликовано исследований, которые демонстрировали бы положительное или отрицательное влияние ограничения воды на разрешение асцита. Большинство экспертов считают, что у больных с неосложненным асцитом роль ограничения воды отсутствует. Несмотря на это во многих центрах диета с ограничением воды у пациентов с асцитом и гипонатриемией стала стандартом клинической практики. В этом вопросе существует много противоречий, и лучший подход пока не найден. Как правило, гепатологи лечат таких больных со строгим ограничением воды. С точки зрения патогенеза гипонатриемии, такое лечение является алогичным и может ухудшить тяжесть центральной гиповолемии, которая запускает неосмотическую секрецию АДГ. Еще большее повышение концентрации циркулирующего АДГ ведет к дальнейшему снижению почечной функции. Нарушенный клиренс свободной воды имеют 25–60% пациентов с цирротическим асцитом, при этом у них часто развивается спонтанная гипонатриемия.
Погрешности в диете часто служат причиной плохо поддающегося лечению (резистентного, рефрактерного) асцита. При употреблении большого количества соли применение современных мочегонных препаратов даже в высоких дозах окажется неэффективным.
Диета должна быть по существу вегетарианской, так как большинство продуктов с высоким содержанием белка (мясо, яйца и молочные продукты) содержат много натрия, поэтому в связи с этим рацион нужно дополнять белковой пищей с низким содержанием натрия. Рекомендуется употреблять бессолевой хлеб, масло и все блюда готовить без добавления соли. Показаны также продукты, богатые калием и микроэлементами. Энергетическая ценность диеты должна составлять
1500–2000 ккал с содержанием 70 г белка и 90 ммоль натрия в сутки.
Пациенту с асцитом рекомендуется ограничение физической активности, что способствует уменьшению количества метаболитов, образующихся в печени. Также в положении лежа несколько усиливается портальный венозный и почечный кровоток.
Общие подходы к терапии асцита у больных циррозом печени. Стратегические направления терапии асцита включают ограничение соли в пище и медикаментозное выведение избыточной жидкости из организма. Кроме этого, исходя из рассмотренных позиций патогенеза асцита у больных циррозом печени, важно решить терапевтические задачи по коррекции ПГ, ПКН, блокированию периферических вазодилятаторов, подавлению активности САС и РААС, нормализации функции ССС, почек и т. д.
Для безопасного медикаментозного выведения жидкости из организма необходимо соблюдение трех этапов:
Для перевода избыточной жидкости из внеклеточного пространства в сосудистое русло используются:
Наиболее оптимальными бета-блокаторами у пациентов с заболеваниями печени, эффективность которых подтверждена результатами метаанализа, являются неселективные производные группы пропранолола — Анаприлин в индивидуально подобранной дозе — 40–80 мг/сут или карведилол в индивидуальной дозе — 25–50 мг/сут [3, 14, 28, 31].
Среди ИАПФ у больных циррозом печени препаратами выбора является группа лизиноприла в индивидуально подобранной (2,5–20 мг/сут) дозе или препарат с двойным путем выведения спираприл по 6 мг/сут.
В отличие от других представителей этого класса они являются готовой лекарственной формой, а их эффективность подтверждена результатами сравнительных исследований [11, 17].
Из АРА у данной категории пациентов может использоваться эпросартан в индивидуально подобранной дозе — 300–600 мг/сут. В открытых исследованиях продемонстрирована эффективность препаратов данной группы у больных циррозом печени [32, 40].
Для доставки избыточной жидкости к почкам применяют положительные инотропные средства:
Для улучшения почечной фильтрации рекомендованы:
Для блокады реабсорбции первичной мочи в почечных канальцах применяются собственно диуретики (преимущественно петлевые диуретики и антагонисты альдостерона).
Диуретическая терапия больных циррозом печени с асцитом. Принимая во внимание сложный патогенез развития отечно-асцитического синдрома, при его терапии используют диуретики различных фармакологических групп: антагонисты рецепторов альдостерона, калийсберегающие, петлевые, тиазидные диуретики и ингибиторы карбоангидразы. Алгоритм назначения диуретиков больным циррозом печени представлен на схеме 1.
Действие диуретиков при циррозе печени и асците носит многогранный характер и состоит в их влиянии на почечные структуры и внепочечные механизмы регуляции водно-электролитного баланса [9, 10], включая воздействие на уровне:
Основным принципом разгрузочной терапии отечно-асцитического синдрома у больных циррозом печени является получение постепенно развивающегося и стабильного диуретического эффекта, при этом препаратом выбора является спиронолактон [15, 23].
В случаях рефрактерности к терапии антагонистами альдостерона перед назначением других диуретиков, действующих на иных участках нефрона, целесообразно оценить показания для использования дополнительных терапевтических мероприятий, в частности для введения альбумина и кровезамещающих коллоидных растворов.
При выраженном отечно-асцитическом синдроме объем диуретической терапии может быть расширен за счет петлевых или тиазидных диретиков, подавляющих реабсорбцию натрия и воды.
Рекомендуется комбинированное назначение калийвыводящих и калийсберегающих диуретиков, что способствует снижению риска возникновения электролитных нарушений [18, 21, 29].
Дозировку и частоту приема препарата подбирают индивидуально каждому больному. При поступлении пациента в стационар рекомендуется определить суточную экскрецию натрия, что облегчает подбор диуретика и контроль за эффектом лечения [16].
При начальных признаках асцита терапия начинается одним из препаратов группы калийсберегающих диуретиков, обычно спиронолактоном. В случае неэффективности добавляют петлевой диуретик.
Наличие признаков выраженного асцита требует изначального применения комбинированной терапии, при этом спиронолактон назначается в качестве надежного партнера петлевых диуретиков.
У больных циррозом печени с умеренной и выраженной ПГ возможно начало лечения курсами антагонистов альдостерона еще до формирования асцита в минимальных (25–50 мг/сут), не изменяющих диурез, дозировках в качестве нейрогуморального модулятора, однако данная точка зрения является авторской и не подтверждена широкими клиническими испытаниями.
При декомпенсации цирроза печени (в виде развития асцита) применение спиронолактона абсолютно необходимо и можно не бояться его сочетания с ИАПФ или АРА, если параллельно правильно использовать активные диуретики в достижении положительного диуреза. Препарат принимают в высоких дозах (100–300 мг, назначаемых однократно утром или в два приема утром и в обед) на период 1–3 недели до достижения компенсации. После этого доза спиронолактона должна быть уменьшена.
Нужно помнить, что концентрация спиронолактона в плазме крови выходит на плато к третьему дню лечения и после отмены (или уменьшения дозы препарата) его концентрация и действие пропадает (снижается) через трое суток. После достижения компенсации применение высоких доз спироналактона прекращается и рассматривается вопрос о назначении малых доз препарата в качестве дополнительного нейрогормонального модулятора.
Для длительной поддерживающей терапии больных циррозом печени рекомендуется использование малых (25–50 мг) доз спиронолактона дополнительно к ИАПФ и бета-адрено-блокаторам (БАБ), позволяющее более полно блокировать РААС и САС.
В случаях, когда необходима замена спиронолактона, препаратом выбора является амилорид по 10–15 мг/сут.
Оптимальное соотношение спиронолактона и фуросемида 5:2, например 100 мг спиронолактона и 40 мг фуросемида и т. д. Максимальные суточные дозы этих препаратов составляют 400 и 160 мг соответственно.
Фуросемид, в свою очередь, может быть неэффективен при выраженном гиперальдостеронизме, когда натрий, не реабсорбированный в петле Генле, всасывается в дистальном отделе нефрона. Вторая причина — гипокалиемия и алкалоз.
Альтернативными, в случаях неэффективности, фуросемиду петлевыми диуретиками для лечения асцита у больных циррозом печени могут рассматриваться: Урегит (этакриновая кислота) 25–50 мг/сут и буметанид, который не слабее фуросемида и применяется в дозах от 0,5 до 10 мг, что позволяет достичь оптимального диуреза.
Этакриновая кислота и тиазиды, как диуретики длительного действия, менее показаны больным циррозом печени, поскольку они способны усугублять развившиеся электролитные нарушения, и даже после их отмены могут продолжаться потеря калия с мочой и нарастание алкалоза.
Поэтому, в частности, тиазиды применяются преимущественно на этапе поддерживающей терапии и/или невозможности использовать спиронолактон. Принимая во внимания возможные побочные эффекты, тиазидные диуретики у больных циррозом печени назначают курсом не более 7–14 дней с перерывом на 3–4 дня.
Кроме вышеперечисленных, в 2006 году в России был зарегистрирован один из самых эффективных и безопасных петлевых диуретиков — торасемид (Диувер). Его стартовая доза составляет 5–10 мг, а при необходимости она может быть увеличена до 20 мг в сутки. Торасемид обладает не только более выраженным, чем фуросемид, мочегонным эффектом, но и имеет собственную активность в отношении рецепторов к альдостерону, что обеспечивает ему калийсберегающий эффект. Преимуществом является отсутствие нежелательных эффектов антагонистов альдостерона (гиперкалиемия, гирсутизм и другие), препарат обладает высокой биодоступностью (80% против 50% у фуросемида), пролонгированным эффектом (период полувыведения 3–5 часов против 1 часа у фуросемида) и мягким гипотензивным действием. Фармакокинетика торасемида мало зависит от функции почек и состояния кишечника, что обеспечивает низкий риск кумуляции препарата и меньшую, по сравнению с фуросемидом, экскрецию калия, кальция, неорганических фосфатов и магния.
При лечении отечно-асцитического синдрома у больных циррозом печени возможно использовать торасемид как в качестве монотерапии, так и в сочетании с Верошпироном. Терапия торасемидом показана при декомпенсации асцита, а также в целях профилактики его возникновения в дозировках 5–20 мг, не вызывающих гипокалиемии даже при длительном приеме. Рекомендуется использовать ступенчатый подход, начиная с 5 мг/сут, увеличивать дозу на 5 мг каждые 2–3 дня до достижения эффекта. На амбулаторном этапе не рекомендуется превышать суточную дозу 20 мг, так как большее количество препарата требует частого контроля уровня калия.
Для оценки эффективности мочегонной терапии у пациентов с циррозом печени и асцитом был проведен ряд сравнительных исследований торасемида и фуросемида. Так, в двойном слепом перекрестном исследовании были сопоставлены результаты однократного приема фуросемида (80 мг) и торасемида (20 мг) внутрь у 14 больных. Торасемид превосходил фуросемид по диуретической и натрийуретической активности. У 5 пациентов наблюдался слабый ответ на прием фуросемида, при этом торасемид вызвал значительное увеличение натрийуреза и диуреза [30, 33, 36].
Аналогично в двойном слепом рандомизированном исследовании у 28 пациентов с асцитом, получавших спиронолактон (200 мг/сут), были сопоставлены результаты 6-недельной терапии торасемидом (20 мг/сут) и фуросемидом (50 мг/сут). Оба препарата оказывали сопоставимое влияние на массу тела, диурез и экскрецию мочевой кислоты, натрия и хлоридов, однако в группе торасемида экскреция калия, кальция, неорганических фосфатов и магния была ниже [30, 33, 36].
В группе из 46 больных циррозом печени, осложнившимся асцитом (рандомизированное исследование), проводили лечение торасемидом 20 мг/сут или фуросемидом 40 мг/сут в сочетании со спиронолактоном 200 мг/сут. Если не удавалось добиться снижения массы тела на 300 г/сут, дозы диуретиков каждые 3 дня увеличивали до 40, 120 и 400 мг/сут соответственно. Торасемид вызывал более выраженное увеличение диуреза, чем фуросемид, хотя в целом результаты лечения в 2 группах оказались сопоставимыми. Увеличение доз диуретиков потребовалось у 2 больных группы торасемида и у 9 пациентов группы фуросемида [33, 36].
То есть по результатам исследований торасемид может рассматриваться как альтернатива комбинированной терапии Фуросемид + Верошпирон у больных циррозом печени и асцитом.
Ингибиторы карбоангидразы не нашли широкого применения у пациентов с асцитом, так как подавление ими реабсорбции натрия и воды в проксимальном канальце компенсируется усилением ее в дистально расположенных сегментах канальцев.
Препараты этой группы могут использоваться в качестве вспомогательного средства на фоне приема активных мочегонных (петлевых и/или тиазидных). Ингибиторы карбоангидразы блокируют фермент в области проксимальных почечных канальцев, что сопровождается незначительным диурезом (прирост до 10–15%), однако при этом усиливается «загрузка» натрием нижележащих отделов канальцев, что повышает эффективность более сильных диуретиков. При истощении фермента карбоангидразы через 3–4 дня непрерывного применения активность ацетазоламида падает, что требует перерыва в лечении.
Поэтому ацетазоламид (Диакарб) рекомендуется в дозе по 0,25 г трижды в день в течение 3–4 дней с двухнедельным перерывом. Данная терапевтическая тактика способствует подкислению среды, восстанавливает диуретическую активность тиазидных и петлевых диуретиков, при длительном применении которых развивается алкалоз. При сочетании с Эуфиллином мочегонный эффект Диакарба увеличивается.
Для избежания развития рефрактерности и побочного действия диуретиков на пациентов с асцитом важно оценивать эффективность лечения и проводить клинико-лабораторный скрининг с определением показаний для последующей коррекции режима дозирования или отмены препаратов.
Продолжение статьи читайте в следующем номере.
С. Н. Мехтиев, доктор медицинских наук, профессор
Ю. А. Кравчук, кандидат медицинских наук
И. В. Субботина
О. А. Мехтиева *
М. В. Шаповалов
ВМА им. С. М. Кирова, *СПб ГМА им. И. И. Мечникова, Санкт-Петербург
.gif)