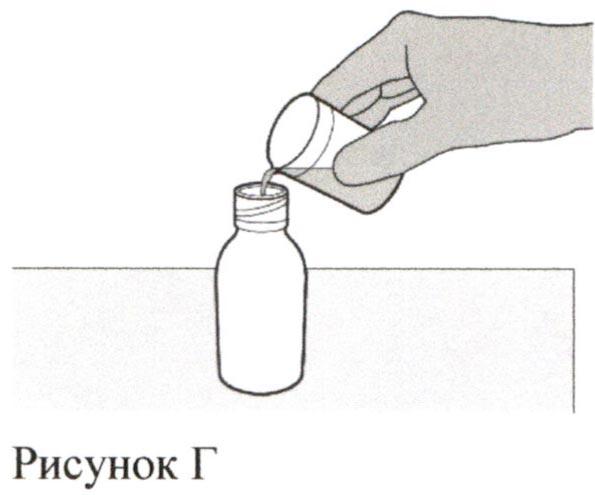
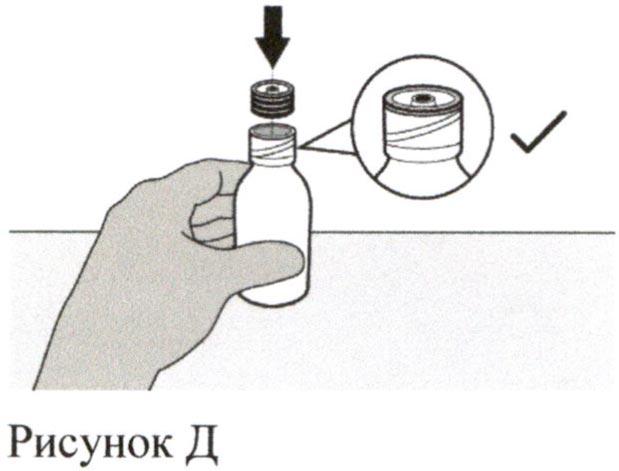
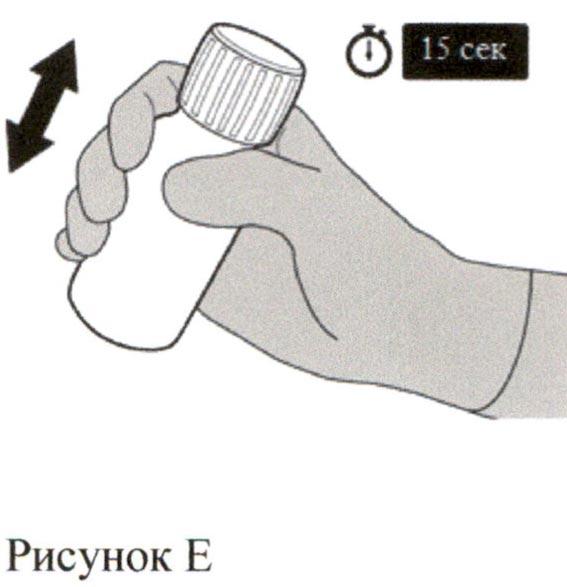
Евродиплом что это за лекарство
Рисдиплам (Эврисди)
Рисдиплам (Эврисди) – препарат для лечения СМА, разработанный компанией Roche в сотрудничестве с PTC Therapeutics и SMA Foundation.
Рисдиплам является модификатором сплайсинга (генетической модификации) гена SMN2, увеличивающим экспрессию полноразмерных функциональных белков.
Рисдиплам применяется перорально, минует гематоэнцефалический барьер (ГЭБ) и системно воздействует на центральную и периферическую нервную систему.
Регистрация Рисдиплама в России
26 ноября 2020 года Рисдиплам был зарегистрирован и одобрен в России для лечения спинальной мышечной атрофии (СМА) у взрослых и детей с двух месяцев. Таким образом, может применяться без ограничения по типу заболевания в соответствии с назначением врача.
Инструкция к препарату Рисдиплам (Эврисиди)
В целях информирования публикуем официальную инструкцию к препарату на русском языке.
Клинические исследования препарата
Предварительные результаты программы исследований Firefish на детях со СМА 1-го типа (возраста до 6 месяцев)
В конце октября 2020 года на 25 Международном Конгрессе World Muscle Society компания Roche представила обновленные данные результатов 1-ой части программы Firefish. Новые данные, полученные за 2 года исследования части 1 у малышей в возрасте 1-7 месяцев с симптоматической спинальной мышечной атрофией (СМА) 1 типа показали, что младенцы, получавшие терапевтическую дозу рисдиплама (17/21), продолжали улучшать и достигать двигательных вех.
Анализ полученных данных показал, что
Ранее, предварительные результаты 1-ой части программы Firefish исследования препарата рисдиплам (RG7916) на детях со СМА 1-го типа были представлены на прошедшей в июне 2018 года ежегодной конференции Cure SMA.
По данным, представленным Джованни Баранелло, педиатром-неврологом Института Неврологии имени Карло Беста (Милан, Италия), препарат Рисдиплам (RG7916) хорошо переносится во всех использованных в ходе исследования дозировках и побочных эффектов, связанных с приемом препарата, не было выявлено.
Около 90% всех детей на 182-й день приема препарата показали улучшение моторной функции как минимум на 4 пункта по шкале CHOP-INTEND (шкала была специально разработана Детской больницей Филадельфии для оценки двигательных навыков у пациентов со СМА 1-го типа) по сравнению с состоянием на момент начала участия в исследовании. Доктор Баранелло показал видеозаписи, на которых дети-участники исследования демонстрировали антигравитационные движения, способности держать голову, переворачиваться или сидеть, что не свойственно младенцам с 1-м типом СМА.
В исследовании Firefish (часть 1) среднее увеличение по CHOP-INTEND составило 5,5 баллов (n=20) на 56-й день, 12,5 баллов (n=11) на 119-й день, 14 баллов (n=11) на 182-й день лечения соответственно.
Пропорция пациентов, чьи результаты выше, чем 4-х бальное увеличение по CHOP-INTEND, составила 75% (n=20) на 56-й день, 94% (n=16) на 119-й день, 91% (n=11) на 182-й день лечения.
Кроме того, рисдиплам хорошо переносится пациентами вне зависимости от выбранной дозировки и на настоящий момент не было обнаружено ни одного побочного эффекта, связанного с приемом препарата и требующего прекратить его прием.
Ни один ребенок в исследовании не потерял способность глотать, никому из них не потребовалась трахеостомия или постоянная вентиляции легких.
Средний возраст пациентов на начало приема препарата составил 6,7 месяца. Самому старшему пациенту в исследовании на настоящий момент 23.8 месяцев (почти 2 года).
Обзор таблеток от повышенного давления нового поколения
Частое повышение показателей артериального давления (АД) – причина развития серьезных заболеваний (инсульт, инфаркт миокарда и пр.). Гипертоническая болезнь в России диагностируется у каждого третьего человека преклонного возраста. Для борьбы с гипертонией многим пациентам приходится принимать препараты на протяжении всей жизни, чтобы исключить осложнения.
Современные фармакологические компании предлагают большой выбор лекарственных средств, эффективных при гипертонии. Если не знаете, как выбрать таблетки от повышенного давления, ознакомьтесь с рейтингом, представленным ниже. В ТОП вошли лучшие медикаменты с учетом эффективности, стоимости и отзывов.
Классификация препаратов от повышенного давления
Причины гипертонии
Когда нужно вызвать врача на дом при повышении давления?
Общепринятые показатели АД – 120/80. Параметры могут незначительно варьировать в зависимости от времени суток, физической активности и возраста человека.
Таблица – Показатели артериального давления и рекомендации
Препараты для восстановления микрофлоры кишечника
Относится к группе пребиотиков. Содержит в себе ЛАКТУЛОЗУ (дисахарид, созданный искусственным путем. В процессе разложения лактулозы снижается кислотность содержимого кишечника, повышается давление в просвете кишки и усиливается ее перистальтика. Поэтому при нарушении микрофлоры с нарушением стула (запором), наблюдается значительное улучшение состояния при приеме Дюфалака. Большинство патогенных бактерий живут в слабощелочной или нейтральной среде. Препарат угнетает рост патогенной микрофлоры, за счёт создания кислой среды в кишечнике, а так как лактулоза служит питательным субстратом для бактерий кишечника, нормализуется состав микрофлоры.
Как принимать: Дюфалак выпускается в виде сиропа со сливовым вкусом. Можно принимать как в разбавленном виде, так и неразбавленном. Всю дозу необходимо сразу проглотить.Пребиотическая доза препарата и длительность приема подбираются индивидуально, учитывая частоту стула у пациента, у взрослых 5–10 мл, у детей 2,5–5 мл 1 раз в сутки.
Бифиформ.
Относится к многокомпонентным пробиотикам. Содержит в себе Бифидобактерии и Энтерококки. А сама капсула препарата является одновременно и защитой от расщепления в желудке и питательным субстратом для данных штаммов бактерий. Важно, что препарат, в отличии от многих других препаратов для восстановления микрофлоры не содержит лактозы. Поэтому он актуален для людей с ее непереносимостью. Препарат не только помогает заселить кишечник полезными бактериями, но и стимулирует развитие местного иммунитета. Как принимать: для восстановления и поддержания микрофлоры рекомендуется принимать по 1 капсуле 2-3 раза в день курсом от 2 до 3 недель. Не зависит от приема пищи, что тоже является дополнительным плюсом при применении.
Флорин Форте.
Поликомпонентный пробиотик, который содержит в себе 2 типа штаммов: Бифидобактерии и Лактобактерии. Это единственный в своем роде поликомпонентный пробиотик, в котором микроколонии бактерий сорбированы по специальной технологии на частицы активированного угля. Данная технология позволяет препарату доставить бактерии в кишечник в неизменном виде, а компоненты угля помогают им прикрепиться к кишечной стенке. Штаммы бактерий не являются генно-модифицированными. Выявлена высокая эффективность препарата при нарушениях стула (диареи). При данном симптоме средство действует наиболее эффективно, по сравнению с другими препаратами-пробиотиками по данным последних исследований. Большим достоинством вещества является его безопасность. Его можно давать детям с первых дней жизни (и даже недоношенным детям), а также беременным и кормящим женщинам. Как принимать:Флорин-Форте представлен в форме порошка. Прием желательно производить во время еды, но строгой зависимости нет. Препарат смешивают с жидкой пищей (в идеале с кисломолочным продуктом) или водой. Новорожденным и детям грудного возраста препарат смешивают с грудным молоком. Дозировка зависит от возраста. Взрослым пациентам назначается по 2 пакета 3 раза в сутки, детям по 1 пакету 2-4 раза в сутки. Препарат содержит лактозу.
Линекс.
Является одним из самых известных в группе поликомпонентным пробиотиком. В составе Линекса целых три непатогенные бактерии — Лактобактерии, Бифидобактерии и Молочный Стрептококк. Особо эффективна эта комбинация при нарушении микрофлоры, связанной с приемом антибиотиков, а Энтерококк позволяет нормализовать микрофлору в верхних отделах кишечника, что можно встретить не у все пробиотических препаратов. По данным исследований, именно при диарее, вследствие приема антибиотиков, Линекс показал хорошие результаты. Также препарат положительно влияет на иммунитет, т.к. участвует в синтезе аскорбиновой кислоты и образует вещества с антибактериальными свойствами, что может помочь при легких формах кишечных инфекций. Большим плюсом Линекса является устойчивость микроорганизмов, входящих в состав препарата к антибиотикам. Именно поэтому препарат можно принимать параллельно с терапией антибактериальными препаратами. Как принимать: его можно принимать детям, пожилым людям, беременным и кормящим женщинам. Дозировка зависит от формы выпуска. Для взрослых более удобен прием в форме капсул (рекомендованная доза — по 2 капсулы 3 раза в день). Для детей существуют саше с порошком или капли, которые можно добавлять в молоко, сок и другие негорячие напитки. Запивать капсулы также не рекомендуется горячими напитками или алкоголем. Если при приеме препарата наблюдается повышение температуры или ухудшение общего состояния требуется дополнительное наблюдение врача.
Пробифор.
Пробиотик, содержащий один штамм бактерий — Бифидобактерии. Также в составе — активированный уголь. Препарат, используемый не только для поддержания и восстановления микрофлоры, но и для лечения кишечных инфекций неизвестной этиологии, диареи и интоксикации. Содержит лактозу, поэтому противопоказан при ее непереносимости. Является достаточно активным препаратом, которые показывает высокую эффективность в лечении кишечных заболеваний. Как принимать: Пробифор принимают внутрь во время приема пищи, при необходимости — независимо от приема пищи. Выпускается в форме капсул и порошка. Капсулы можно принимать только детям от 5 лет и взрослым, порошок всем возрастным группам.
Бифидумбактерин.
Однокомпонентный пробиотик, содержащий штамм Бифидобактерий. Имеет много лекарственных форм (капсулы, суспензия, суппозитории, порошок). У данного препарата очень мягкое воздействие на микрофлору, поэтому четкой схемы приема нет. Можно применять как детям, так и беременным женщинам. Одним из плюсов препарата является его ценовая доступность.
Лактобактерин плюс.
Пробиотик, содержащий один штамм бактерий — Лактобактерии. Помимо нормализации микрофлоры, имеет свойство повышения иммунной защиты организма. При аллергических проявлениях также оказывает высокую эффективность. Форма выпуска: жидкий концентрат. Такая форма более удобна чем порошковая, так как нет необходимости разведения. Рекомендуется сочетать препарат с приемом витаминов, так как это усиливает его действие. Ввиду высокой устойчивости к антибактериальным препаратам, также допускается совместный прием при антибактериальной терапии. Как принимать: важно, что Лактобактерин разрешен для приема детям с первых дней жизни. Принимать его нужно не позднее чем за 30 минут до еды, предварительно встряхнув флакон, запивая небольшим количеством воды. Дозировка зависит от возраста, у детей до 12 лет это 1-3 мл в день, у взрослых – 3-5 мл. Также Лактобактерин назначается для поддержания микрофлоры уже после лечения курсами на 1-1,5 месяца.
Полисорб.
Данный препарат не входит в группу про- и пребиотиков. Но он отлично справляется с подготовкой организма к приему препаратов для восстановления кишечной микрофлоры, особенно после приема курсов антибиотиков. Это мощный энтеросорбент. Он обладает всеми важными качествами данной группы препаратов (не обладает токсическими свойствами, не травмирует слизистые оболочки, хорошо удаляется из кишечника, имеет хорошие связывающие свойства, не вызывает нарушения микрофлоры и имеет удобную лекарственную форму). Основное предназначение данного препарата — выведение токсинов из организма. Он очень эффективен при аллергических проявлениях нарушения микрофлоры. Улучшает состояние кожи. Также связывает избыток холестерина и других вредных жирных кислот, нейтрализуя их. Как принимать: выпускается в виде порошка, который обязательно нужно растворить в ¼-1/2 стакане воды. Доза препарата зависит от массы тела пациента. Полисорб проходит через желудочно-кишечный тракт и выводится в полностью неизменном состоянии.
Все эти препараты направлены на улучшения состояния нормальной микрофлоры кишечника. При постоянном приеме и соблюдении инструкций, пациент начинает отмечать улучшение уже после 5-7 дней приема. При выборе пробиотика или пребиотика, необходимо учитывать индивидуальную непереносимость некоторых компонентов препарата, возраст и степень выраженности нарушения микрофлоры кишечника. Во всех случаях рекомендуется проконсультироваться с лечащим врачом. При правильном выборе и приеме препаратов, а также сбалансированном питании и ведении здорового образа жизни ваш кишечник скажет вам спасибо!
ИМЕЮТСЯ ПРОТИВОПОКАЗАНИЯ, НЕОБХОДИМО ОЗНАКОМИТЬСЯ С ИНСТРУКЦИЕЙ ИЛИ ПРОКОНСУЛЬТИРОВАТЬСЯ СО СПЕЦИАЛИСТОМ.
Статины: плюсы и минусы
«Высокий холестерин» не болит, но именно он может приводить к развитию атеросклероза. Атеросклероз поражает сердечно-сосудистую систему, приводит к образованию атеросклеротических бляшек и нарушениям кровоснабжения. Нередко это заканчивается инфарктами, инсультами.
Сегодня существует немало препаратов из группы статинов. Доказана их эффективность в снижении смертности от сердечно-сосудистых заболеваний, но продолжаются споры об их безопасности. Для достижения и удержания нужных показателей липидного обмена требуется длительный прием препаратов, но многие пациенты не выполняют рекомендации, отчего эффективность лечения резко снижается. Что говорить о пациентах, когда врачи имеют разные мнения на этот счет.
Что такое статины
Статины — это группа гиполипидемических препаратов. Они замедляют работу одного из главных ферментов, участвующих в синтезе холестерина — ГМК-КоА-редуктазы. Это приводит к уменьшению синтеза холестерина в печени.
Снижение синтеза холестерина в гепатоцитах увеличивает количество рецепторов к липопротеидам низкой плотности (ХС ЛПНП) и последующему захвату их из кровотока. Кроме того, возможно, некоторое снижение образования ЛПНП за счет угнетения синтеза в печени их предшественника — липопротеидов очень низкой плотности (ЛПОНП). Так статины способствуют снижению общего ХС, ХС ЛПНП и ХС ЛПОНП в плазме крови. Одновременно препараты этой группы способны уменьшить уровень ТГ и несколько повысить уровень «хорошего холестерина» (липопротеидов высокой плотности). Эффективность снижения уровня холестерина в крови зависит от дозы препарата. Для получения нужного уровня снижения требуются достаточно высокие дозы.
Вклад в пользу статинов вносят и их многочисленные дополнительные свойства:
Статины полезны не только своей способностью снижать холестерин в крови.
Виды статинов
В группе статинов препараты отличаются путями, по которому идет их обмен, силой подавления образования холестерина, лекарственными взаимодействиями. Лекарства отличаются не только названиями, но и действующим веществом:
Показания
Препараты этой группы назначает только врач и он подбирает какое действующее вещество подойдет, его дозировку. Обычно для этого определяют риск сердечно-сосудистых событий по специальной шкале, опроснику, сдаются анализы для определения липидного спектра и биохимических показателей крови. Сегодня статины назначают не только после инфарктов, инсультов как вторичную профилактику. При определенных условиях, высоком риске, врач может использовать статины в первичной профилактике сердечно-сосудистых заболеваний.
Минусы
Но есть и нерешенные вопросы в лечении статинами. Так от 40 до 75% пациентов прекращают прием статинов в течение 1-2 лет после начала лечения. Причинами этого пациенты называют: опасение развития нежелательных эффектов из инструкции к препарату (46%), неверие в то, что лекарство продлевает жизнь (29,4%), прием большого количества других таблеток (27,6%), забывчивость (26,5%), плохой контроль уровня ХС крови на фоне приема лекарства (18,8%), отмену препарата нелечащим врачом (13,5%). При этом реальное развитие нежелательных эффектов на терапии статинами наблюдалось только у 11,7% пациентов, причем их проявления были легкой и умеренной степени выраженности.
Мышечные симптомы
Частота развития симптомов поражения мышц составляет 7-29% по разным данным. К ним относят:
Причины этого изучены недостаточно. По одной версии происходит снижение коэнзима Q10 в мышечной ткани и снижение уровня витамина D. Затрагивается работа митохондрий.
Мышечные симптомы встречаются в 7-29%.
Симптомы, как правило, появляются в обеих руках или ногах. Срок появления около 4-6 недель после начала приема статинов. Иногда при болезнях суставов, связок происходит усиление боли. Возможно, этому способствует мышечная слабость. Необычно, но физически активные люди чаще страдают от мышечных симптомов.Так в одном из исследований указывалось, что спортсмены хуже переносят липидснижающую терапию.
По данным исследований, эти симптомы встречаются редко. Но в сами исследования часто не допускаются пациенты старшего возраста, с нарушениями функции печени и почек, принимающие определенные лекарственные препараты, то есть нельзя сказать, что это обычный пожилой человек с «букетом болезней».
Сахарный диабет и инсулинорезистентность
Установлено, что длительный прием статинов при определенных факторах может способствовать развитию инсулинорезистентности и сахарного диабета. Об этом говорят не только данные исследований, но и национальные рекомендации некоторых стран.
Факторами риска развития СД при приеме липидоснижающих препаратов могут стать:
Воздействие на печень
При приеме статинов для снижения негативного влияния на печень необходимо исключить прием:
Статины могут негативно влиять на поврежденную печень.
Не следует их назначать при активном вирусном гепатите, пока показатели печени не вернутся к норме.
Взаимодействие с лекарствами
Статины обладают множественным эффектом. Это происходит из-за того, что они действуют не изолированно, а затрагивают многие химические реакции в организме. Особенно это важно у пациентов принимающих множество лекарственных препаратов по поводу сердечно-сосудистых заболеваний.
Что делать?
Задумавшись о приеме статинов стоит понимать, что это не «волшебная таблетка». И даже длительная терапия на многие годы для увеличения продолжительности жизни будет эффективной только в комплексном подходе, так как развитие атеросклероза зависит не только от приема препаратов. Схемы терапии меняются, но никто не отменял собственных усилий, которые должен делать человек. Нужно поменять образ жизни, который десятилетиями приводил к накоплению проблем.
Диета. Оптимальной диетой для профилактики ССЗ, связанных с атеросклерозом, признана средиземноморская диета. Рекомендуется высокое содержание овощей, бобовых, цельнозерновых продуктов, фруктов, рыбы и ненасыщенных ЖК (особенно оливкового масла). Возможно умеренное потребление алкоголя (в основном красного вина, преимущественно с пищей). Держать в рационе низкий процент красного мяса, молочных продуктов и насыщенных жиров.
Отказ от курения. Курение одна из причин развития атеросклероза. Риск смерти или развития острого инфаркта миокарда у продолжающих курить, после успешной операции по восстановлению проходимости коронарных сосудов, почти в 2 раза выше, чем у некурящих. Отказ от курения уже в течение первого года снижает риск развития ИБС на 50%, а при отказе от курения в течение 5-15 лет риск развития ОКС и инсульта уравнивается с некурящими.
Курение — одна из причин развития атеросклероза.
Физическая активность. Установлено, что сокращение сидения перед телевизором до 2 ч в день увеличивает продолжительность жизни на 1,4 года. Лучшее начало увеличения физической активности это ходьба, особенно в возрасте от 60 лет. Основной принцип плавное повышение интенсивности и объема в течение нескольких недель.
Так обсудив с врачом все плюсы и возможные риски приема статинов нужно придерживаться выбранного пути многие годы для достижения результата.
Регистрационный номер
Торговое наименование
Международное непатентованное или группировочное наименование
Лекарственная форма
Порошок для приготовления раствора для приема внутрь
Состав
Один флакон (2 г порошка для приготовления раствора для приема внутрь) содержит:
действующее вещество: рисдиплам – 60 мг;
вспомогательные вещества: маннитол – 1344.70 мг, изомальт – 237.25 мг, ароматизатор клубничный (мальтодекстрин кукурузный, крахмал кукурузный восковой модифицированный (Е1450), ароматизирующие компоненты) – 150.00 мг, винная кислота – 120.50 мг, натрия бензоат – 30.00 мг, макрогол/полиэтиленгликоль 6000 – 20.00 мг, сукралоза – 16.00 мг, аскорбиновая кислота – 14.10 мг, динатрия эдетата дигидрат – 7.45 мг.
1 мл приготовленного (восстановленного) раствора содержит 0.75 мг рисдиплама.
Описание
Порошок или порошок с комками от светло-желтого до желтого с сероватым или зеленоватым оттенком или светло-зеленого с желтоватым оттенком цвета (при выпуске). Порошок или порошок с комками, или скомковавшийся порошок от светло-желтого до желтого с сероватым или зеленоватым оттенком или светло-зеленого с желтоватым оттенком цвета (в течение срока годности).
Приготовленный (восстановленный) раствор
Прозрачный раствор от зеленовато-желтого до желтого цвета.
Фармакотерапевтическая группа
Прочие препараты для лечения заболеваний костно-мышечной системы.
Код АТХ
Фармакологические свойства
Фармакодинамика
Рисдиплам представляет собой модификатор сплайсинга предшественника матричной рибонуклеиновой кислоты (пре-мРНК) гена выживаемости двигательных нейронов 2 (SMN2), разработанный для лечения спинальной мышечной атрофии (СМА), причиной которой являются мутации в хромосоме 5q, что приводит к недостаточности белка SMN. Недостаточность функционального белка SMN является патофизиологическим механизмом развития СМА всех типов. Рисдиплам корректирует сплайсинг SMN2, сдвигая баланс с исключения экзона 7 на включение экзона 7 в транскрипте м-РНК. приводя к образованию функционального и стабильного белка SMN. Таким образом, рисдиплам лечит СМА путем увеличения и сохранения уровней функционального белка SMN.
Рисдиплам равномерно распределяется во всем организме, в том числе в центральной нервной системе (ЦНС), проникая через гематоэнцефалический барьер и соответственно приводя к увеличению уровня белка SMN в ЦНС и по всему организму. Концентрации рисдиплама в плазме и белка SMN в крови отражают распределение и фармакодинамические эффекты рисдиплама в тканях, а именно: мышечных тканях и тканях мозга.
Во всех клинических исследованиях применение рисдиплама приводило к устойчивому и длительному увеличению уровня белка SMN. В течение 4 недель после начала лечения медианный уровень белка SMN был более чем в 2 раза выше по сравнению с исходным значением, согласно измерениям в крови. Повышение уровня белка SMN сохранялось на протяжении периода лечения ≤2 лет у пациентов с манифестацией СМА в младенческом возрасте и у пациентов с поздней манифестацией СМА (см. подраздел «Клиническая эффективность»).
Клиническая эффективность
Эффективность препарата Эврисди ® для лечения пациентов с манифестацией СМА в младенческом возрасте и пациентов с поздней манифестацией СМА оценивалось в 2 опорных клинических исследованиях FIREFISH и SUNFISH и подтверждено дополнительными данными, полученными в исследовании JEWELFISH. В целом результаты исследований подтверждают эффективность препарата Эврисди ® у пациентов со СМА.
Манифестация СМА в младенческом возрасте
ВР39056 (FIREFISH) представляет собой открытое исследование по изучению эффективности, безопасности, фармакокинетики и фармакодинамики препарата Эврисди ® у пациентов с симптоматической СМА 1 типа (у всех пациентов было генетически подтверждено заболевание с двумя копиями гена SMN2). Исследование состоит из двух частей. Часть 1 исследования FIREFISH разработана как часть исследования по подбору дозы. В подтверждающей части 2 исследования FIREFISH оценивалась эффективность препарата Эврисди ® в терапевтической дозе, которая была выбрана на основании результатов части 1 исследования (см. раздел «Способ применения и дозы»). Пациенты из части 1 не принимали участия в части 2.
В часть 2 исследования FIREFISH был набран 41 пациент со СМА 1 типа.
Медиана возраста возникновения клинических признаков и симптомов СМА 1 типа составила 1.5 месяцев (1.0-3.0 месяцев), 54% были женского пола, 54% – представители европеоидной расы и 34% – представители азиатской расы.
Медиана возраста на момент набора в исследование составила 5.3 месяцев (2.2-6.9 месяцев), медиана времени между возникновением симптомов и приемом первой дозы составила 3.4 месяцев (1.0-6.0 месяцев).
На исходном уровне средний индекс по результатам теста детской больницы Филадельфии для оценки двигательных функций при нейромышечных заболеваниях у новорожденных (Children’s Hospital of Philadelphia Infant Test of Neuromuscular Disorders, CHOP-INTEND) составил 22 балла (8.0-37.0) и средний индекс по результатам неврологической оценки младенцев по шкале Хаммерсмита, модуль 2 (Module 2 of the Hammersmith Infant Neurological Examination, HINE-2) составил 1.0 (0.0-5.0).
Таблица 1. Резюме ключевых результатов по эффективности на 12 месяце (FIREFISH часть 2).
| Конечные точки по эффективности | Доля пациентов N=41 (90% ДИ) | |||
| Основные критерии двигательной функции и развития | ||||
| BSID-III: способность сидеть без поддержки в течение, как минимум, 5 секунд Значение р на основании критерия функционирования 5% a | 29.3% (17.8%, 43.1%) a | 56.1% (42.1%, 69.4%) a | 90.2% (79.1%, 96.6%) b Значение р на основании критерия функционирования 12% a | 78.0% (64.8%, 88.0%) Выживаемость и выживаемость без событий |
| Выживаемость без событий c Значение р на основании критерия функционирования 42% a | 85.4% (73.4%, 92.2%) a | 92.7% (82.2%, 97.1%) 0.0005 | ||
| Глотание и кормление | ||||
| Способность глотать | 85.4% (73.15%, 93.43%) | |||
| Способность принимать пищу через рот d | 82.9% (70.3%, 91.7%) | |||
| Использование ресурсов здравоохранения | ||||
| Отсутствие госпитализаций e | 48.8% (35.1%, 62.6%) | |||
a Значения р по выживаемости и выживаемости без событий основаны на Z-тестировании; значения р для других конечных точек (BSID-III, CHOP-INTEND, HINE-2) основаны на точном биноминальном тестировании. Доля выживаемости устанавливается с использованием методологии Каплана-Мейера.
b Согласно HINE-2: увеличение на ≥2 балла [или максимальный показатель] для способности брыкаться, ИЛИ увеличение на ≥1 балл по основным критериям двигательной функции: способность держать голову, перекатываться, сидеть, ползать, стоять или ходить И улучшение по большему числу категорий основных критериев двигательной функции по сравнению с ухудшением, что определяется как пациент, ответивший на этот анализ.
c Явлением считается достижение конечной точки по постоянной вентиляции легких (трахеостомия или ≥16 часов неинвазивной вентиляции легких в течение суток или интубация в течение >21 последовательного дня в отсутствие или после разрешения острого обратимого явления). Три пациента достигли конечной точки по постоянной вентиляции легких до 12 месяца. Все 3 пациента достигли увеличения, как минимум, на 4 балла по их индексу CHOP-1NTEND по сравнению с исходным уровнем.
d Включает пациентов, которых кормили исключительно через рот (всего 28 пациентов) и пациентов, которых кормили как через рот, так и с помощью трубки для кормления (всего 6 пациентов) на 12 месяце.
e Госпитализации включают все госпитализации, которые длились, как минимум, 2 дня.
После 12 месяцев терапии препаратом Эврисди ® 29% (12/41) пациентов соответствовали критерию способности сидеть без поддержки (BS1D-III, пункт 22), 93% (38/41) пациентов были живы и 85% (35/41) пациентов были живы и без событий (без постоянной вентиляции), см. рисунок 1. Эти результаты указывают на клинически значимое отличие от естественного течения заболевания у нелеченных пациентов с манифестацией СМА в младенческом возрасте. Нелеченные пациенты с манифестацией СМА в младенческом возрасте никогда не смогут сидеть без поддержки, и ожидается, что только 25% пациентов смогут выжить без постоянной вентиляции легких после достижения возраста в 14 месяцев.
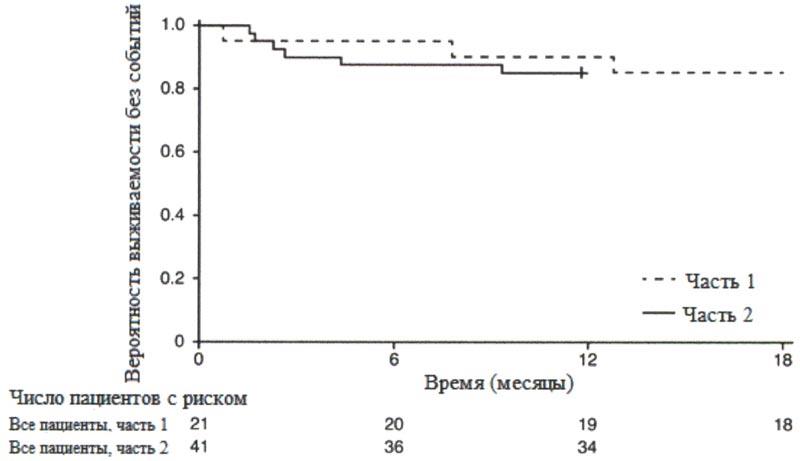
+ цензурировано: один пациент в части 2 был цензурирован, поскольку он рано осуществил визит 12 месяца.
Большинство пациентов достигли ответа по категориям основных критериев двигательной функции HINE-2, включая определенный уровень способности держать голову (76%, 31/41), сидеть (61%, 25/41), перекатываться (56%, 23/41) и стоять (22%, 9/41). Согласно измерениям общего индекса CHOP-INTEND также наблюдались улучшения двигательной функции, см. рисунок 2.
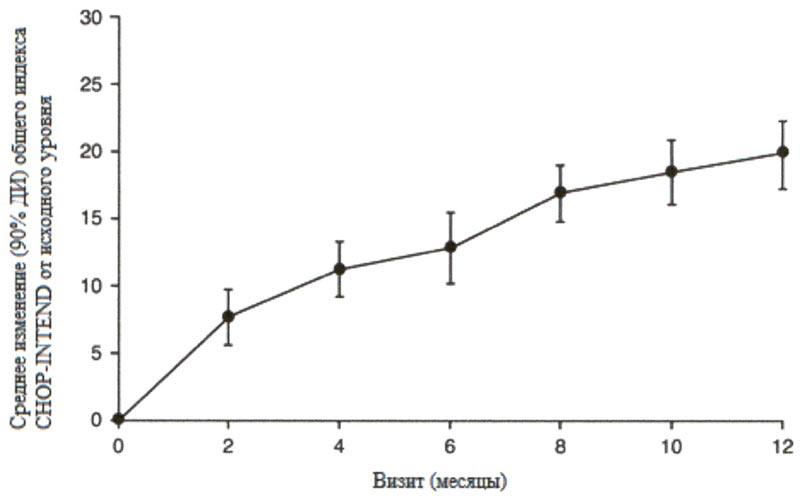
Эффективность препарата Эврисди ® у пациентов со СМА 1 типа также подтверждается результатами из части 1 исследования FIREFISH. Для 21 пациента из части 1 характеристики на исходном уровне согласовывались с таковыми у пациентов с симптомами со СМА 1 типа.
Медиана возраста включения в исследование составила 6.7 месяцев (3.3-6.9 месяцев); медиана времени между возникновением симптомов и приемом первой дозы составила 4.0 месяцев (2.0-5.8 месяцев). Всего 17 пациентов получили терапевтическую дозу (дозу, выбранную для части 2) в течение первых 12 месяцев терапии. После 12 месяцев терапии 41% (7/17) пациентов могли сидеть без поддержки, как минимум, в течение 5 секунд (BSID-III, пункт 22). После 18 месяцев терапии 88% (15/17) пациентов были живы и без событий (без постоянной вентиляции), см. рисунок 1. Данные результаты по выживаемости и развитию двигательной функции согласовывались с результатами исследования FIREFISH часть 2.
Поздняя манифестация СМА
ВР39055 (SUNFISH) представляет собой многоцентровое исследование по изучению эффективности, безопасности, фармакокинетики и фармакодинамики препарата Эврисди ® у пациентов со СМА 2 или 3 типа в возрасте 2-25 лет. Исследование состоит из двух частей. В части 1 осуществлялся подбор дозы. Часть 2 представляла собой рандомизированную, двойную слепую, плацебо-контролируемую, подтверждающую часть исследования. Пациенты из части 1 не принимали участия в части 2.
Первичной конечной точкой было изменение оценочного показателя двигательной функции – 32 (Motor Function Measure-32, MFM32) от исходного уровня на 12 месяце. Индекс MFM32 позволяет оценить обширный спектр двигательных функций у большого диапазона пациентов со СМА. Общий индекс MFM32 выражают в виде процента (0-100) от максимально возможного, причем более высокий показатель обозначают лучшую двигательную функцию. Индекс MFM32 измеряет двигательную функцию, в частности важные ежедневные двигательные способности. Небольшие изменения в двигательной функции могут привести к значительному приобретению или потере ежедневных двигательных способностей.
SUNFISH часть 2 представляет собой рандомизированную, двойную слепую, плацебо-контролируемую часть исследования SUNFISH у 180 не амбулаторных пациентов со СМА 2 типа (71%) или 3 типа (29%). Пациентов рандомизировали в соотношении 2:1 в группу лечения препаратом Эврисди ® в терапевтической дозе (см. раздел «Способ применения и дозы») или в группу плацебо. Рандомизация была стратифицирована по возрастным группам (2-5 лет, 6-11 лет, 12-17 лет и 18-25 лет).
Медиана возраста пациентов на момент начала лечения составляла 9.0 лет (2-25 лет), а медиана времени между возникновением первых симптомов СМА и приемом первой дозы составила 102.6 месяцев (1-275). Из 180 пациентов, включенных в исследование, 51% были женщинами, 67% – представителями европеоидной расы, и 19% – представителями азиатской расы.
На исходном уровне у 67% пациентов выявлен сколиоз (у 32% пациентов – тяжелый сколиоз). Среднее значение индекса MFM32 на исходном уровне составляло 46.1, а индекса по Обновленному модулю оценки функции верхних конечностей (Revised Upper Limb Module, RULM) – 20.1.
В целом, демографические характеристики пациентов на исходном уровне были хорошо сбалансированы между группами Эврисди ® и плацебо, за исключением сколиоза (63.3% пациентов в группе препарата Эврисди ® в сравнении с 73.3% пациентов в группе плацебо).
Таблица 2. Резюме данных по эффективности у пациентов с поздней манифестацией СМА на 12 месяце лечения (SUNFISF1 часть 2).
| Конечная точка | Эврисди ® (N=120) | Плацебо (N=60) |
| Первичная конечная точка | ||
| Изменение общего индекса MFM32 1 на 12 месяце от исходного уровня Среднее значение, рассчитанное по методу НК (95% ДИ) | 1.36 (0.61,2.11) | -0.19 (-1.22, 0.84) |
| Различие по сравнению с плацебо Расчетное значение (95% ДИ) Значение р 2 | 1.55 (0.30, 2.81) 0.0156 | |
| Вторичные конечные точки | ||
| Доля пациентов с изменением общего индекса MFM32 1 на 12 месяце на ≥3 балла от исходного уровня (95% ДИ) | 38.3% (28.9, 47.6) | 23.7% (12.0, 35.4) |
| Отношение шансов для общего ответа (95% ДИ) Значение р 3,4 с коррекцией (без коррекции) | 2.35 (1.01,5.44) 0.0469 (0.0469) | |
| Изменение общего индекса RULM 5 на 12 месяце от исходного уровня Среднее значение, рассчитанное по методу НК (95% ДИ) | 1.61 (1.00, 2.22) | 0.02 (-0.83, 0.87) |
| Различие по сравнению с плацебо Расчетное (95% ДИ) значение р 2,4 с коррекцией (без коррекции) | 1.59(0.55, 2.62) 0.0469 (0.0028) | |
НК = наименьшие квадраты
1 На основании правила по отсутствующим данным для индекса MFM32 6 пациентов были исключены из анализа (Эврисди ® n = 115, контрольная группа плацебо n = 59).
2 Данные анализировали с использованием смешанной модели повторного измерения с общим индексом на исходном уровне, лечением, визитом, возрастной группой, лечением к визиту, а также исходным уровнем к визиту.
3 Данные анализировали с использованием логистической регрессии с общим индексом на исходном уровне, лечением и возрастной группой.
4 Значение р с коррекцией было получено для конечных точек, включенных в иерархическое тестирование, и выделялось на основании всех значений р, полученных для конечных точек в порядке увеличения иерархии до текущей конечной точки. Значение р без коррекции тестировали при уровне значимости 5%.
5 На основании правила отсутствующих данных для индекса RULM из анализа исключили 3 пациентов (Эврисди ® n = 119; контрольная группа плацебо, n = 58).
Эффективность препарата Эврисди ® у пациентов с поздней манифестацией СМА также подтверждается результатами из части 1 (часть исследования SUNFISH по подбору дозы). В часть 1 был включен 51 пациент со СМА 2 типа и 3 типа (включая 7 амбулаторных пациентов) в возрасте 2-25 лет.
После 1 года лечения препаратом в терапевтической дозе (доза, выбранная для части 2) было отмечено клинически значимое улучшение двигательной функции согласно измерениям индекса MFM32. Среднее изменение по сравнению с исходным уровнем составило 2.7 баллов (95% ДИ: 1.5, 3.8). Улучшение индекса MFM32 сохранялось ≤2 лет во время лечения препаратом Эврисди ® (среднее изменение на 2.7 баллов [95% ДИ: 1.2, 4.2]).
Фармакокинетика
Фармакокинетические параметры препарата Эврисди ® были изучены у здоровых взрослых добровольцев и у пациентов со СМА.
После приема препарата Эврисди ® в виде раствора внутрь фармакокинетика рисдиплама была приблизительно линейной между 0.6 и 18 мг. Фармакокинетика рисдиплама наилучшим образом описывалась с помощью популяционной фармакокинетической модели со всасыванием с тремя транзитными камерами, двухкамерным распределением и выведением первого порядка. Было обнаружено, что масса тела и возраст оказывают значимое влияние на фармакокинетику.
При применении рисдиплама в терапевтической дозе 0.2 мг/кг один раз в сутки у пациентов с манифестацией СМА в младенческом возрасте (от 2 до 7 месяцев при наборе в исследование) расчетная экспозиция (средняя площадь под кривой «концентрация-время» (AUC)0-24) составила 1930 нг.ч/мл. В исследовании SUNFISH (часть 2) при применении рисдиплама в терапевтической дозе 0.25 мг/кг один раз в сутки у пациентов с массой тела ® у пациентов со СМА старше 60 лет не проводилось. Пациенты со СМА ≤60 лет принимали участие в исследовании JEWELFISH. Субъекты без СМА ≤69 лет принимали участие в клинических исследованиях по фармакокинетике. Согласно результатам данных исследований коррекции дозы у пациентов ≤69 лет не требуется.
Пациенты с нарушением функции почек
Исследований по изучению фармакокинетики рисдиплама у пациентов с нарушением функции почек не проводилось. Рисдиплам в виде неизменного соединения выводится почками в малой степени (8%).
Пациенты с нарушением функции печени
Нарушение функции печени легкой или средней степени тяжести не оказывало влияния на фармакокинетику рисдиплама. После применения 5 мг рисдиплама средние соотношения для Сmax и AUC составили 0.95 и 0.80 у субъектов с нарушением функции печени легкой степени тяжести (n=8), а также 1.20 и 1.08 у субъектов с нарушением функции печени средней степени тяжести (п=8) по сравнению с соответствующими здоровыми добровольцами (n=10). Безопасность и фармакокинетика у пациентов с нарушением функции печени тяжелой степени тяжести не изучались.
Фармакокинетика рисдиплама у японских субъектов и субъектов европеоидной расы не отличалась.
Показания к применению
Лечение спинальной мышечной атрофии (СМА) у взрослых и детей с 2 месяцев.
Противопоказания
Повышенная чувствительность к рисдипламу или к другим вспомогательным веществам препарата в анамнезе.
Беременность и период грудного вскармливания.
Младенцы младше 2 месяцев.
Применение при беременности и в период грудного вскармливания
Беременность
Применение препарата Эврисди ® при беременности противопоказано.
Данные клинических исследований препарата Эврисди ® у беременных женщин отсутствуют. Была показана эмбриофетальная токсичность и тератогенность рисдиплама у животных. На основании данных, полученных в исследованиях у животных, установлено, что рисдиплам проходит через плацентарный барьер и может оказывать повреждающее действие на плод.
Безопасность применения препарата Эврисди ® во время родов и родоразрешения не установлена.
Период грудного вскармливания
Применение препарата в период грудного вскармливания противопоказано. Неизвестно, выводится ли препарат Эврисди ® с грудным молоком у человека. Исследования у крыс показали, что рисдиплам выводится с грудным молоком.
Фертильность
На основании данных доклинических исследований влияния препарата Эврисди ® на фертильность у женщин не ожидается.
Тестирование на беременность
Перед началом терапии препаратом Эврисди ® следует проверить статус беременности у женщин репродуктивного потенциала. Беременных женщин следует четко проинформировать о потенциальном риске для плода.
Контрацепция
Пациенты (мужчины и женщины) репродуктивного потенциала должны соблюдать следующие требования в отношении контрацепции:
Способ применения и дозы
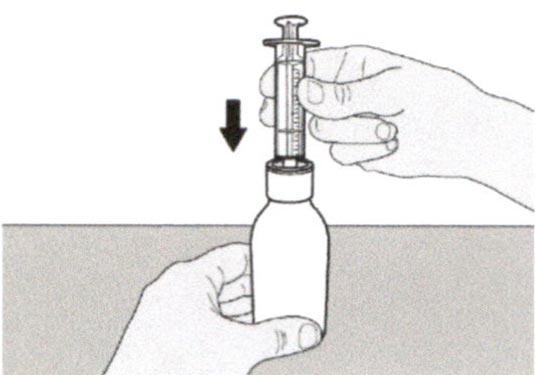
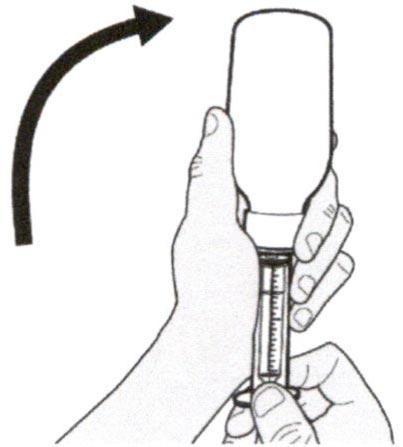
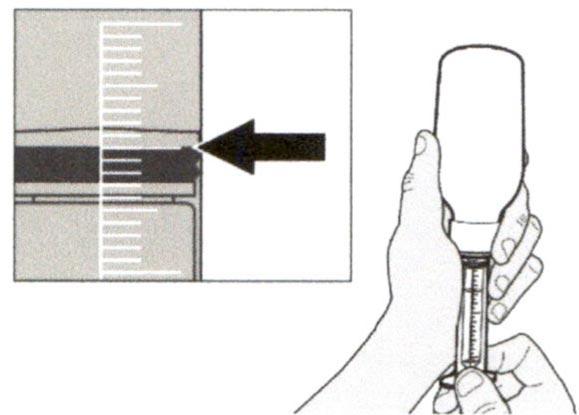
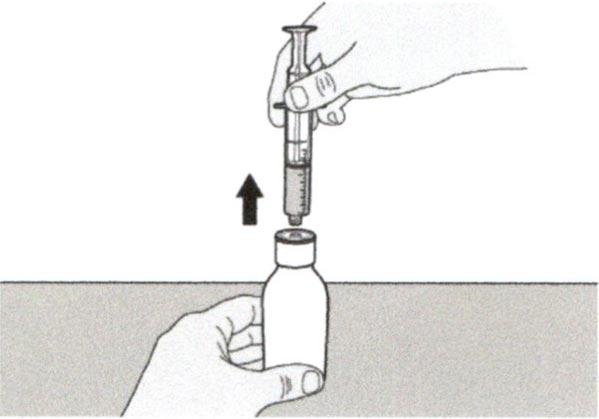
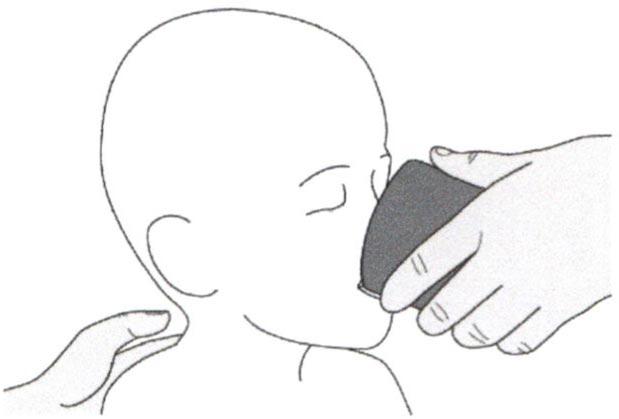
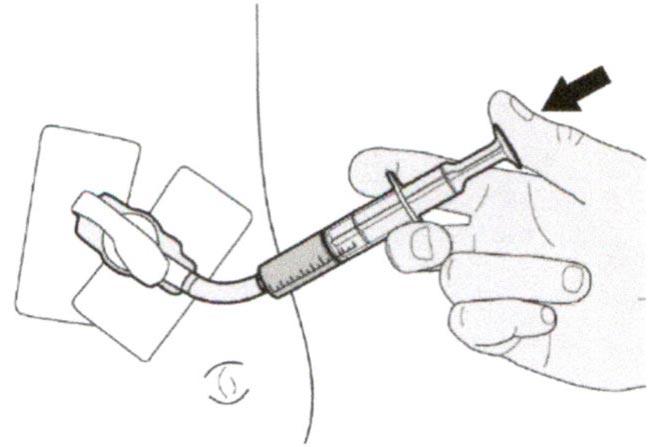
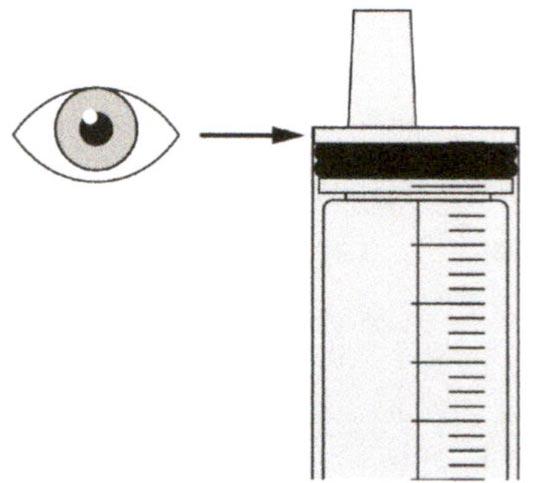
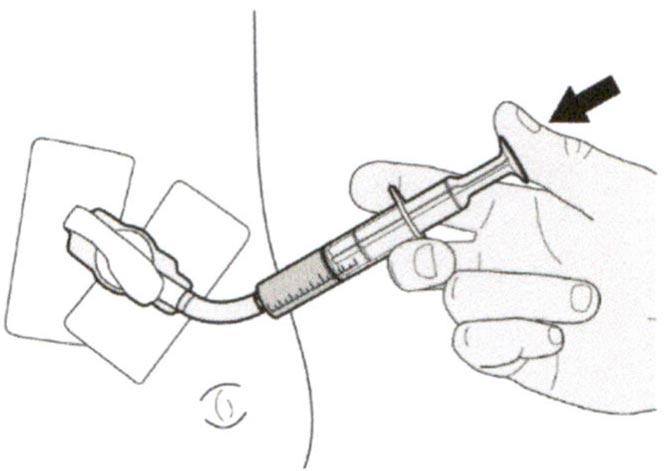
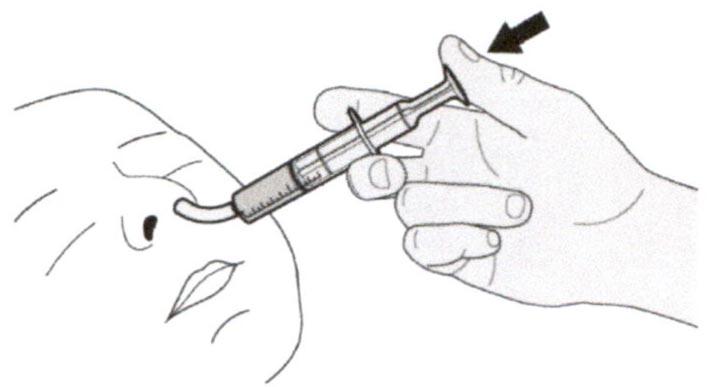
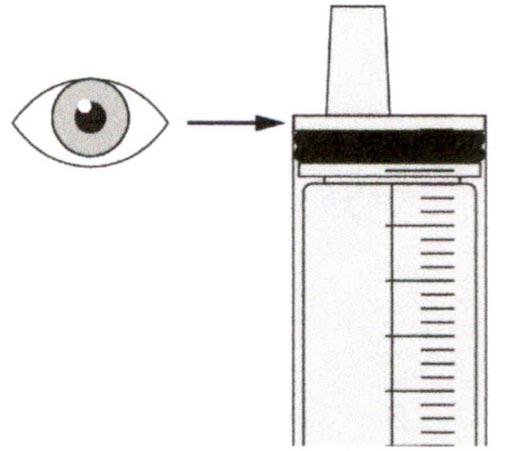
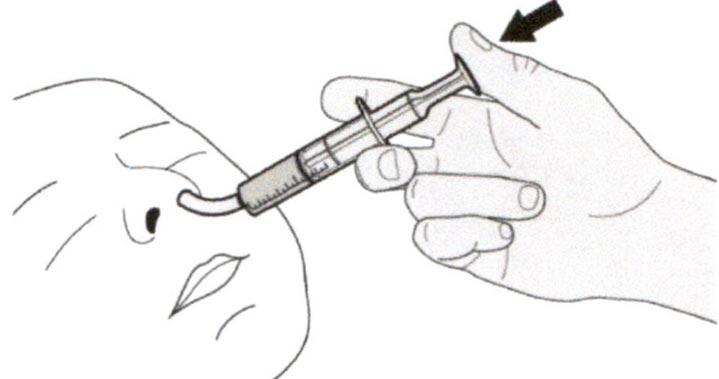
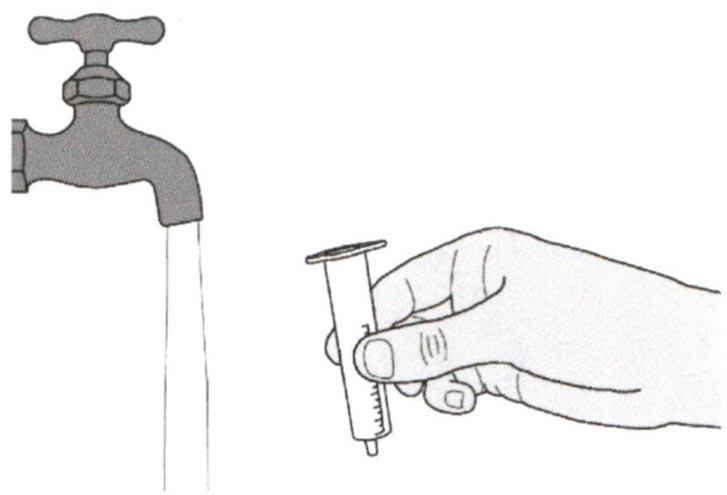
Раствор для приема внутрь должен быть приготовлен медицинским работником перед его выдачей пациенту.
Лечение СМА следует начать как можно раньше после постановки диагноза.
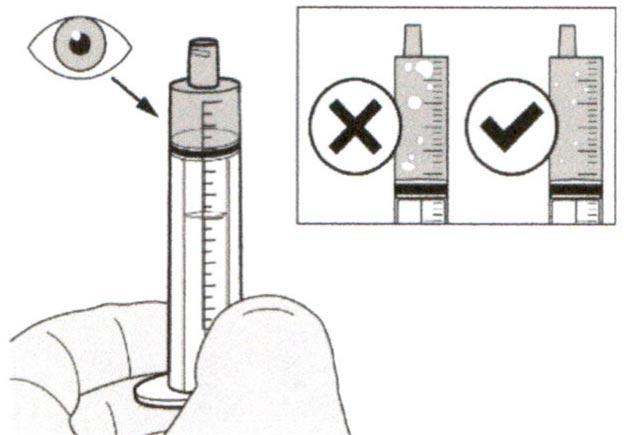
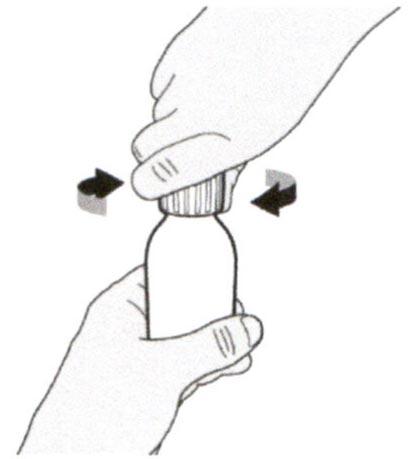
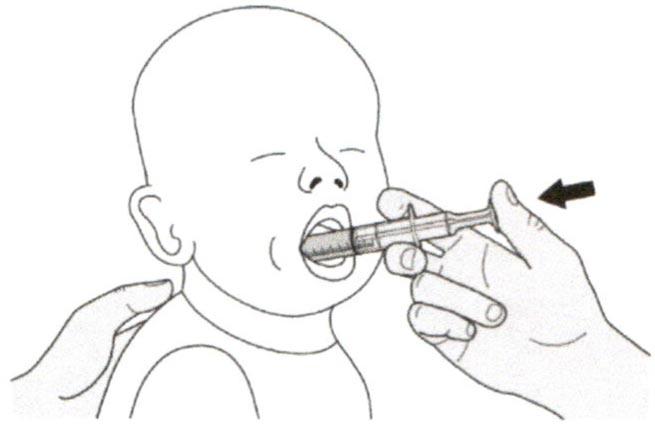
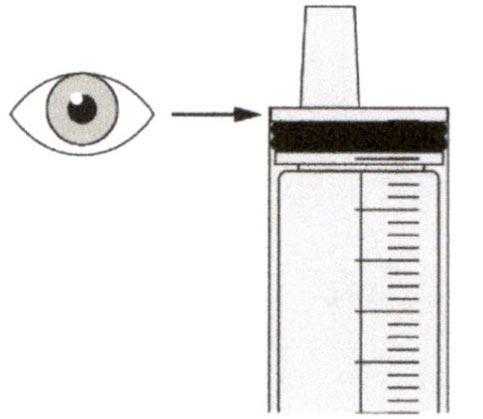
Препарат Эврисди ® принимают внутрь один раз в сутки приблизительно в одно и то же время каждый день с помощью предоставляемого перорального шприца.
Рекомендуемая суточная доза препарата Эврисди ® у пациентов со СМА определяется в зависимости от возраста и массы тела (см. таблицу 3).
Таблица 3. Режим дозирования в зависимости от возраста и массы тела.