Ferri hydroxydi polymaltosati что это
Железа (III) гидроксид полимальтозат
Фармакологическое действие
Препарат железа в виде полимальтозного комплекса гидроксида Fe 3+ (является декстрином железа, в отличие от Fe 3+ гидроксид полиизомальтозата — декстрана железа, не содержит декстранов, обусловливающих большую вероятность развития анафилактических реакций).
Данный макромолекулярный комплекс стабилен, не выделяет железо в виде свободных ионов, сходен по структуре с естественным соединением железа и ферритина. Благодаря такому сходству, Fe 3+ из кишечника поступает в кровь только путём активного всасывания, что объясняет невозможность передозировки (и интоксикации) препаратом в отличие от простых солей железа, всасывание которых происходит по градиенту концентрации. Всосавшееся железо депонируется в связанном с ферритином виде, главным образом в печени. Позже, в костном мозге оно включается в гемоглобин.
Фармакокинетика
Степень абсорбции после перорального приёма зависит от степени дефицита железа (чем больше дефицит, тем выше абсорбция) и от величины дозы препарата (чем выше доза, тем хуже абсорбция). Всасывается преимущественно в двенадцатиперстной и тонкой кишке. Невсосавшаяся часть Fe 3+ выводится с каловыми массами.
После внутримышечного введения попадает в кровоток через лимфатическую систему. Максимальная концентрация наблюдается через 24 часа. В ретикулоэндотелиальной системе комплекс расщепляется на гидроксид Fe 3+ и полимальтозу (метаболизируется путём окисления). В кровотоке железо связывается с трансферрином, в тканях депонируется в составе ферритина, в костном мозге включается в гемоглобин и используется в процессе эритропоэза.
Физиологические потери: эпидермис, волосы, ногти, фекалии, пот, грудное молоко, менструальная кровь, моча — 1,1–1,4 мг в сутки (здоровые мужчины и женщины в постменопаузе — 1 мг в сутки, здоровые женщины репродуктивного периода — 1,5–2 мг в сутки).
Показания
Пероральные формы
Лечение железодефицитной анемии различного генеза и латентного дефицита железа у младенцев и детей младшего возраста; повышенная потребность в железе (беременность, период лактации, донорство, период интенсивного роста, вегетарианство, пожилой возраст).
Раствор для инъекций
Лечение железодефицитной анемии при неэффективности или невозможности приёма пероральных железосодержащих препаратов (в том числе у больных с заболеваниями желудочно-кишечного тракта и страдающих синдромом мальабсорбции).
Противопоказания
Раствор для внутримышечного введения (дополнительно):
Беременность и грудное вскармливание
Применение при беременности
Не следует назначать в течение I триместра беременности.
Во II и III триместрах беременности возможно применение с осторожностью, когда предполагаемая польза для матери превосходит потенциальный риск для плода.
Применение в период грудного вскармливания
Специальных исследований по безопасности применения препарата в период грудного вскармливания не проведено.
Возможно применение только в том случае, когда предполагаемая польза для матери превосходит потенциальный риск для ребёнка.
Способ применения и дозы
Внутрь, во время или сразу после еды. Дозировка и сроки лечения зависят от степени недостатка Fe. Суточная доза может быть разделена на несколько приёмов или принята однократно.
Внутрь.
Таблетки: следует разжёвывать или глотать целиком во время или после еды. Суточную дозу допустимо принимать за 1 раз. Лечение клинически выраженного дефицита: 1 таблетка 1–3 раза в день в течение 3–5 месяцев до нормализации Hb. Затем приём следует продолжить в течение ещё нескольких месяцев для того, чтобы восстановить запасы Fe в организме (1 таблетка в сутки). Беременным женщинам: 1 таблетка 2–3 раза в сутки до нормализации Hb, с последующим приёмом по 1 таблетке в сутки до родов. Для терапии латентного дефицита Fe и для профилактики недостаточности Fe — 1 таблетка в сутки.
Капли допустимо смешивать с фруктовыми и овощными соками или с искусственными питательными смесями, не опасаясь снижения активности препарата. 1 мл (20 капель) содержит 176,5 мг Fe 3+ гидроксид полимальтозного комплекса (50 мг элементарного Fe), 1 капля равна 2,5 мг элементарного Fe.
Дозы для лечения клинически выраженного дефицита Fe: недоношенные дети — 1–2 кап/кг ежедневно в течение 3–5 месяцев; дети до 1 года — 10–20 кап/сут; 1–12 лет — 20–40 кап/сут; дети старше 12 лет и взрослые — 40–120 кап/сут; беременные — 80–120 кап/сут. Длительность лечения — не менее 2 месяцев. В случае клинически выраженного дефицита Fe нормализация Hb достигается лишь через 2–3 месяца после начала лечения. Для восстановления внутренних резервов Fe приём в профилактических дозах должен быть продолжен в течение нескольких месяцев. Дозы для лечения латентного дефицита Fe: дети до 1 года — 6–10 кап/сут; 1–12 лет — 10–20 кап/сут; дети старше 12 лет и взрослые — 20–40 кап/сут; беременные — 40 кап/сут. Профилактика дефицита Fe: дети до 1 года — 2–4 кап/сут; 1–12 лет — 4–6 кап/сут; дети старше 12 лет и взрослые — 4–6 кап/сут; беременные — 6 кап/сут.
Сироп содержит в 1 мл 10 мг Fe3+. Дозы для лечения клинически выраженного дефицита Fe: дети до 1 года — 2,5–5 мл/сут (25–50 мг Fe); 1–12 лет — 5–10 мл/сут; дети старше 12 лет, взрослые и кормящие женщины — 10–30 мл/сут; беременные — 20–30 мл/сут. Дозы для лечения латентного дефицита Fe: дети от 1 до 12 лет — 2,5–5 мл/сут; дети старше 12 лет, взрослые и кормящие женщины — 5–10 мл/сут; беременные — 10 мл/сут. Профилактика дефицита Fe: беременные — 5–10 мл/сут.
Побочные действия
Пероральные лекарственные формы: диспепсия (ощущение переполнения и давления в эпигастральной области, тошнота, запор или диарея), тёмная окраска кала (обусловлена выведением невсосавшегося Fe и не имеет клинического значения).
Раствор для внутримышечного введения: в редких случаях — артралгия, увеличение лимфатических узлов, лихорадка, головная боль, недомогание, диспепсия (тошнота, рвота); крайне редко — аллергические реакции.
Местные реакции (при неправильной технике введения): окрашивание кожи, болезненность, воспаление.
Передозировка
Ранние симптомы (только при приёме внутрь): диарея (иногда с кровью), лихорадка, острые боли и спазмы в желудке, сильная тошнота и рвота (иногда с кровью). Возможно возникновение лейкоцитоза и гипергликемии.
Поздние симптомы: цианоз губ, ладоней и концевых фаланг кисти, сонливость, бледная и липкая кожа, учащение дыхания и сердцебиения, слабость, вялость, судороги, метаболический ацидоз, гипотензия, гипогликемия, токсический гепатит, печёночная недостаточность, коллапс, расстройство желудочно-кишечного тракта.
Лечение: индукция рвоты и промывание желудка (по состоянию), коррекция электролитных нарушений, гемотрансфузия, клизма. Антидот — дефероксамин (противопоказан при почечной недостаточности!). При анурии и олигурии — удаление гемодиализом.
Взаимодействие
Пероральные формы: взаимодействия с другими лекарственными препаратами не обнаружено.
Раствор для инъекций: ингибиторы АПФ усиливают системные эффекты. Не следует применять одновременно с пероральными Fe-содержащими препаратами (уменьшается всасывание Fe из желудочно-кишечного тракта).
Особые указания
Раствор для инъекций: экспериментальное изучение репродукции, а также контролируемые исследования у беременных женщин не проводились. В малых количествах неизменённое железо из полимальтозного комплекса может проникать в грудное молоко, однако маловероятно возникновение нежелательных эффектов у вскармливаемых детей.
Не установлено никаких отрицательных воздействий на плод при назначении пероральных форм в период беременности (в том числе в I триместре).
При назначении препарата пациентам с сахарным диабетом следует учитывать, что 1 мл сиропа содержит 0,04 ХЕ, а 1 мл капель — 0,01 ХЕ.
Приём препаратов железа необходимо продолжать и после нормализации гемоглобина. Не вызывает окрашивания зубной эмали.
Раствор для инъекций предназначен только для внутримышечного введения. Техника инъекции имеет важное значение. В результате неправильного введения препарата могут возникнуть болезненность и окрашивание кожи в месте инъекции. Методика вентро-ягодичной инъекции рекомендована вместо общепринятой — в верхний наружный квадрант большой ягодичной мышцы.
Эффективность и безопасность препаратов трехвалентного железа в лечении железодефицитной анемии
Рассмотрено применение препаратов железа на основе гидроксид-полимальтозного комплекса в лечении железодефицитной анемии. Показано, то они сопоставимы по эффективности с солевыми препаратами железа, но при их использовании значительно реже возникают нежел
Application of iron preparations based on hydroxide-polimaltosis for complex treatment of iron-deficiency anemia is examined. It is stated that in terms of efficiency they can be compared with the salt preparations of iron, but with their use undesirable phenomena appears considerably more rarely.
В настоящее время фармацевтическая промышленность выпускает довольно большое количество препаратов железа для лечения железодефицитной анемии (ЖДА) и продолжается разработка новых препаратов. Возникла необходимость классифицировать препараты железа (рис. 1) и описать их свойства для того, чтобы облегчить выбор. В зависимости от способа введения в организм препараты железа делятся на пероральные и парентеральные (внутривенные, внутримышечные). Пероральные препараты могут содержать различные соли железа (молекулы небольшого размера) или гидроокись железа с полимальтозным комплексом (молекулы большого размера, более 50 кД). Пероральные препараты железа могут быть простыми, т. е. содержащими только соединение железа, или комбинированными с добавлением других веществ (аскорбиновой кислоты, фолиевой кислоты, витамина В12, микроэлементов и других веществ). Комплексы железа для внутривенного введения могут содержать декстран (высокомолекулярный или низкомолекулярный), сахарозу или карбоксимальтозу.
Многие годы «золотым стандартом» среди пероральных препаратов железа являлся сульфат железа. Последний представляет собой солевой препарат железа, который недорог в производстве и, соответственно, имеет невысокую стоимость. Кроме того, оказалось, что сульфат железа обладает высокой всасываемостью в организме, которая выше, чем у глюконата, хлорида или фумарата железа. По этой причине в настоящее время выпускается большое количество препаратов железа, содержащих сульфат железа (Актиферрин, Гемофер пролонгатум, Сорбифер Дурулес, Тардиферон, Ферроплекс, Ферроградумет, Ферро-Фольгамма и др.) [1].
При использовании солевых препаратов железа возможно локальное раздражение слизистой оболочки желудка в месте растворения препарата и слизистой оболочки двенадцатиперстной кишки, где преимущественно происходит всасывание препарата. Процесс всасывания является пассивным, быстрым и дозозависимым. В связи с низкой молекулярной массой солевые препараты железа могут всасываться в большом количестве, приводя к опасным для организма концентрациям, что может вызвать интоксикацию и отравление. Диссоциация солей двухвалентного железа происходит в желудочно-кишечном тракте и сопровождается выделением свободных ионов железа. Следующим процессом метаболизма солевых препаратов железа является окисление, которое осуществляется также в желудочно-кишечном тракте и заключается в переходе двухвалентного железа в трехвалентное. Последнее поступает в кровь и в плазме связывается с транспортным белком — трансферрином и в виде этого комплекса (металлопротеина) направляется в костный мозг и органы депо железа (печень, селезенка). Возврат железа из этих органов осуществляется через лимфатическую систему. Нарушение процесса окисления приводит к высвобождению электронов, образованию свободных радикалов, активации перекисного окисления липидов, повреждению клеток паренхиматозных органов.
В процессе лечения ЖДА солевыми препаратами железа могут возникнуть следующие проблемы:
.jpg)
Препараты железа на основе ГПК обладают следующими свойствами и преимуществами перед солевыми препаратами железа [5]:
На сегодняшний день в арсенале врача имеются современные препараты трехвалентного железа на основе различных полисахаридных комплексов [1]: пероральные препараты железа на основе ГПК (Мальтофер, Мальтофер Фол, Феррум Лек); препараты железа на основе ГПК (Феррум Лек — раствор для внутримышечного введения); препараты железа на основе гидроксид сахарозного комплекса (Венофер — раствор для внутривенного введения); препараты железа на основе карбоксимальтозата (Феринжект) и другие.
Международной тенденцией является смена солевых препаратов железа на препараты железа на основе ГПК [6].
ЖДА — самое «благодарное» гематологическое заболевание и должна вылечиваться сразу и навсегда, что и наблюдается в большинстве случаев. Причинами неуспешного лечения ЖДА препаратами железа являются:
Лечение латентного дефицита железа (ЛДЖ), который рассматривается как предстадия ЖДА и характеризуется снижением запасов железа в депо при нормальной концентрация гемоглобина, проводится пероральными препаратами железа в 50-процентной дозировке в течение 2 мес [9]. Основная задача лечения ЛДЖ — пополнить запасы железа в депо и не дать этому состоянию перейти в ЖДА.
.gif)
Особенностью лечения указанных двух форм дефицита железа (ЛДЖ и ЖДА) является длительное применение пероральных препаратов железа, при котором часто возникают указанные выше нежелательные явления [11].
Показано, что препараты железа на основе ГПК обладают сходной с сульфатом железа биодоступностью [12], обладают стабильной структурой молекулы, имеют контролируемую абсорбцию железа из комплекса [13]. Метаанализ сравнительных исследований [14] подтвердил одинаковую эффективность препаратов железа на основе ГПК и сульфата железа в лечении ЖДА.
В литературе имеется большое количество работ, в которых сравнивается эффективность и переносимость различных солевых препаратов железа и препаратов железа на основе ГПК. Однако лишь недавно были опубликованы результаты рандомизированных исследований, которые являются наиболее доказательными в медицине. Например, в работе B. Yasa и соавт. [15] проведено сравнение эффективности лечения ЖДА и переносимости препаратов железа. Больные были рандомизированы на 2 группы: 1-я группа (52 пациента) получала лечение препаратом железа на основе ГПК в дозе 5 мг/кг в сутки в 1 прием, 2-я группа (51 больной) — сульфат железа в дозе 5 мг/кг в сутки в 2 приема. Эффективность лечения оценивали по приросту концентрации гемоглобина в двух точках — к концу 1-го и к концу 4-го месяцев лечения. Прирост концентрации гемоглобина у пациентов, которые получали препарат железа на основе ГПК, к концу 1-го и 4-го месяца в среднем составил 12 ± 9 и 23 ± 13 г/л соответственно (в обоих случаях р = 0,001 по сравнению с исходной концентрацией гемоглобина), а у пациентов, которые получали сульфат железа, — 18 ± 17 и 30 ± 23 г/л соответственно (в обоих случаях р = 0,001 по сравнению с исходной концентрацией гемоглобина). Статистически значимых различий между группами не получено. Переносимость препаратов оценивали с помощью регистрации нежелательных явлений (боли в животе, тошнота, запоры или сочетание этих симптомов). Нежелательные явления были зарегистрированы у 26,8% пациентов, которые получали препарат железа на основе ГПК, и у 50,8% пациентов, которые получали сульфат железа (р = 0,012).
Таким образом, препараты железа на основе ГПК сопоставимы по эффективности с солевыми препаратами железа, но при их использовании значительно реже возникают нежелательные явления, что обосновывает все возрастающий интерес врачей к препаратам этой группы.
Литература
* ФНКЦ ДГОИ им. Дмитрия Рогачева МЗ РФ,
** ГБОУ ВПО РНИМУ им. Н. И. Пирогова МЗ РФ, Москва
Ферропол (Капли для приема внутрь) (Ferric oxide polymaltose complexes)
Инструкция
Торговое название
Международное непатентное название
Лекарственная форма
Капли для приема внутрь 50 мг/мл, 30 мл
Состав
30 мл препарата содержат
вспомогательные вещества: пропиленгликоль, сахароза, метилпарагидроксибензоат, пропилпарагидроксибензоат, ароматизатор шоколадный, вода очищенная.
Описание
Коричневого цвета раствор с шоколадным вкусом и запахом.
Фармакотерапевтическая группа
Препараты трехвалентного железа для перорального приема.
Фармакологические свойства
Фармакокинетика
Исследования с использованием метода двойных изотопов (55Fe и 59Fe) показали, что абсорбция железа, измеряемая по уровню гемоглобина в эритроцитах, обратно пропорциональна принятой дозе (чем выше доза, тем ниже абсорбция). Установлена также отрицательная корреляция между продолжительностью периода недостаточности железа и уровнем его всасывания (чем дольше сохраняется дефицит железа, тем больше его всасывается).
Железо абсорбируется в двенадцатиперстной и тощей кишках. Выведение железа происходит в основном из желудочно-кишечного тракта и составляет около 1 мг железа в день.
Неабсорбированное железо выводится с калом. У женщин необходимо учитывать потерю железа во время менструации.
Фармакодинамика
Препарат применяют для профилактики и лечения железодефицитных состояний.
Железо является составляющим гемоглобина, миоглобина и некоторых ферментов.
Комплекс не обладает прооксидантными свойствами. Податливость липопротеинов очень низкой плотности и липопротеинов низкой плотности к окислению снижена.
Показания к применению
— профилактика и лечение латентного железодефицита
— железодефицитная анемия в период беременности
Способ применения и дозы
Режим дозирования и продолжительность лечения зависят от степени дефицита железа.
Профилактика и лечение латентного железодефицита:
Дети старше 12 лет, взрослые и матери, кормящие грудью:
Продолжительность лечения составляет около 1-2 месяцев.
Продолжительность лечения составляет около 3-5 месяцев, до нормализации уровня гемоглобина. После этого лечение следует продолжать еще в течение нескольких недель для восполнения запасов железа.
Дети (в возрасте младше 1 года): Начальная доза составляет 10 капель (25 мг железа) в сутки. Затем дозу следует постепенно увеличить до 20 капель (50 мг железа) в сутки.
Беременные:
Режим дозирования и продолжительность лечения зависят от степени дефицита железа.
Профилактика и лечение латентного железодефицита:
Суточные дозы препарата Ферропол, капли для приема внутрь при лечении и профилактике недостаточности железа
Безопасность и эффективность железа (III) гидроксид полимальтозного комплекса
обзор 25-летнего опыта применения
Питер Гейссер (Peter Geisser, PhD), Швейцария
В представленном обзоре применения гидроксид полимальтозного комплекса (ГПК) трёхвалентного железа (Мальтофер®) демонстрируется высокая биодоступность железа после перорального приёма препарата, особенно у лиц с дефицитом железа в организме. Многочисленные клинические исследования у мужчин, женщин, детей грудного и младшего возраста подтвердили высокую эффективность ГПК железа в лечении железодефицитной анемии (ЖДА). В связи с особенностями фармакокинетики, ГПК железа лучше принимать во время еды и в дозе, содержащей несколько большее количество железа, чем в классических препаратах солей железа. Что касается приверженности пациентов к лечению, ГПК железа имеет очевидные преимущества перед другими солями железа. Во многих исследованиях с применением ГПК железа частота прекращения лечения была меньше, чем при назначении других солей железа. В основном это связано с более низкой частотой возникновения нежелательных явлений со стороны желудочно-кишечного тракта.
Ключевые слова: антианемические препараты; железодефицитная анемия; препараты железа; железа (III) гидроксид полимальтозный комплекс, обзор; Мальтофер®.
1. Введение в проблему дефицита железа
Достаточно давно известно, что железо является эссенциальным микроэлементом для человека. 1,2 Кроме того, убедительно доказана потребность в приёме препаратов железа в случае недостаточного поступления и/или избыточного выведения железа из организма, особенно у детей и женщин детородного возраста. Среднее содержание железа в крови у взрослого человека составляет 2100 мг у мужчин и 1350 мг у женщин. Помимо эритроцитов крови, значительная часть железа находится в депонированном состоянии в тканях (в виде ферритина и гемосидерина). В миоглобине, геме и негемовых ферментах содержится всего 200-400 мг железа.
При обычном рационе питания в организм поступает около 10-15 мг железа в сутки, из которого абсорбируется всего 10%. 3 Приблизительно 1 мг железа в сутки человек теряет в результате слущивания рогового слоя эпидермиса и клеток слизистых оболочек. У женщин большую роль в метаболизме железа играют потери железа с менструальной кровью, которые в среднем составляют до 0,7 мг в сутки. Как правило, абсорбция железа и его выведение из организма уравновешены и составляют 1 мг в сутки.
Железодефицитная анемия (ЖДА) имеется более чем у 750 млн человек во всём мире. 4-6 Это заболевание неблагоприятно влияет на психомоторное развитие у детей грудного и младшего возраста и может привести к отдалённым нарушениям когнитивной функции. В исследовании Агаоглу (Agaoglu et al.) было показано, что у детей в возрасте 6-12 лет, имевших ЖДА, средний коэффициент интеллекта (IQ) был значительно меньше (на 12,9 баллов), чем у детей без анемии. 7 Анемия во время беременности ассоциируется с более частым рождением детей с низкой массой тела и недоношенных детей, а также с увеличением перинатальной смертности.
Выделяют три группы, в которых риск развития ЖДА наиболее высокий:
1) маленькие дети (особенно в развивающихся странах, в которых распространённость ЖДА в этой популяции может достигать 63%);
2) молодые женщины в начале детородного периода, среди которых практически у 70% обнаруживается дефицит железа в той или иной степени, даже в популяциях с полноценным питанием;
3) беременные женщины, у которых потребность в поступлении железа возрастает с 0,8 до 7,5 мг в сутки.
Как правило, ЖДА достаточно эффективно лечится путём перорального приёма препаратов железа. В настоящее время имеется множество различных препаратов солей железа, они эффективны и недороги, их побочные эффекты хорошо известны, но часто неприемлемы для пациентов. Соли железа могут вызывать тошноту, рвоту, кишечные колики, запоры и диарею, 6,8 что является основной причиной низкой приверженности пациентов к лечению. Хотя приём препаратов во время еды улучшает их переносимость, биодоступность железа при этом снижается. Другим существенным недостатком солей железа является потенциальная токсичность в случае передозировки. В США ежегодно отмечается несколько летальных исходов на фоне их приёма, обычно среди детей. 9
Идеальный пероральный препарат железа должен обладать высокой терапевтической эффективностью, не вступать во взаимодействие с пищей или лекарствами, иметь широкий диапазон безопасности с минимальным риском случайной передозировки, обладать хорошей переносимостью со стороны желудочно-кишечного тракта и не приводить к нежелательным эффектам, таким как окрашивание зубов или неприятный вкус во рту.
Железистые соли, в частности сульфат железа (СЖ), не подходят под эти критерии. Сульфат железа в высокой степени токсичен, взаимодействует с пищей и другими препаратами, а также вызывает побочные эффекты со стороны желудочно-кишечного тракта практически у 40% пациентов, что часто является причиной прекращения лечения. 8,10,11 Также показано, что СЖ значительно увеличивает уровни железа, не связанного с трансферином, которые ассоциируются с повышенным окислительным стрессом. 13,14
Железа (III) гидроксид полимальтозный комплекс (Мальтофер®) разрабатывался с целью создания перорального препарата железа, обладающего высокой эффективностью в сочетании с хорошей переносимостью. Основанием для его разработки послужило получение вещества с хорошей биодоступностью в широком диапазоне состояний, не вступающего в нежелательные взаимодействия с пищей или другими препаратами и обладающего отличными характеристиками переносимости и долгосрочным профилем безопасности.
2. Химические свойства ГПК железа (Мальтофера®)
Железа (III) гидроксид полимальтозный комплекс (Мальтофер®) представляет собой макромолекулярный комплекс, в котором полициклический гидроксид трёхвалентного железа дополнен полисахаридными группами. Его молекулярная масса составляет 52 300 Дальтон. 11 Вещество хорошо растворяется в воде при широком диапазоне значений pH (от 1 до 14) и, в отличие от простых солей железа, не преципитирует в щелочной среде. 15 По сравнению с другими полимальтозными комплексами железа, препарат Мальтофер® растворим в воде при комнатной температуре и не осаждается при добавлении соляной кислоты. 16 Кроме того, он не вступает во взаимодействия in vitro при pH 3-8 с хелатирующими веществами из пищи (например, фитиновой кислотой) и препаратами, содержащими фенольные группы (например, тетрациклином). Окислительно-восстановительный потенциал ГПК железа составляет 332 мВ; это означает, что вещество не восстанавливается в биологических жидкостях, и следовательно не будет провоцировать окислительный стресс. 14
3. токсикология
По сравнению с солями железа, ГПК железа (Мальтофер®) не токсичен при значениях половинной летальной дозы (ЛД50) у мышей и крыс при введении в концентрации, более чем в 10 раз превышающей концентрацию сульфата железа. В долгосрочных исследованиях на собаках введение ГПК железа в дозах до 270 мг элементарного железа на 1 кг в сутки в течение 52 недель не оказывало какого-либо отрицательного влияния на органы и системы.
4. Клинические данные
4.1. Фармакокинетика и фармакодинамика
По фармакокинетическим характеристикам железо, высвобождающееся из ГПК, достаточно сильно отличается от железа, поступающего в виде препаратов солей. Как у крыс, так и у человека в первые 6 часов после приёма ГПК железа сывороточная концентрация железа либо не меняется, либо увеличивается весьма незначительно. Впоследствии у крыс сывороточные концентрации железа постепенно увеличиваются, достигая максимума через 24 ч. Тем не менее, через 2-3 недели после приёма препарата включение железа в эритроциты достоверно не отличается от такового при назначении солей железа. 17
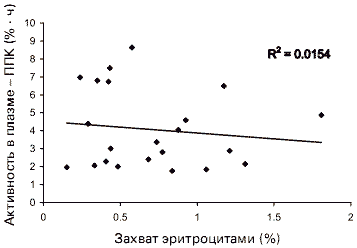
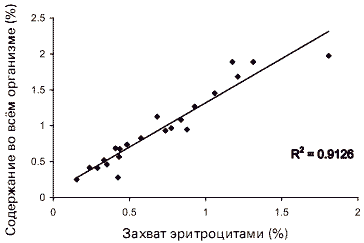
В двух исследованиях у человека, проведённых Потгетером (Potgieter et al.), после применения меченого радиоизотопом оригинального ГПК железа (Мальтофер®) не было выявлено корреляции между площадью под кривой (ППК) сывороточной концентрации железа и отношением утилизации железа (Рисунок 1), однако была обнаружена сильная корреляция между включением железа в эритроциты и содержанием железа во всём организме (Рисунок 2). 18,19 Таким образом, утверждение о том, что низкие значения ППК или максимальной концентрации (Cmax) предопределяют сниженное соотношение абсорбции железа, как предполагалось в работах Диетфельбингер, Хайнрих и Нильсен (Dietzfelbinger, Heinrich, Nielsen et al.), не относится к оригинальному ГПК железа (Мальтофер®). 20-22 Более того, истинная биодоступность определяется скоростью и величиной абсорбции, с которыми активное вещество или активная часть молекулы высвобождаются из лекарственной формы и становятся доступными в месте приложения действия. 23 Что касается препаратов железа, таким местом являются эритроциты, а не сыворотка. Поскольку сыворотка не является местом приложения действия, ППК и Cmax просто отражают соотношение всего количества железа, перенесённого к этому месту. Такие соотношения пропорциональны не значениям ППК, а скорости переноса и/или скорости высвобождения в сыворотку и из сыворотки (Geisser et al.). 24
Рисунок 1. Корреляция между активностью 59 Fe в плазме и значениями ППК (активность в плазме) после приёма Мальтофера и Амфоеля (гидроксид аллюминия) (Potgieter et al.) 18
Рисунок 2. Корреляция между активностью захвата 59 Fe эритроцитами и содержанием железа во всём организме после приёма Мальтофера и Амфоеля (гидроксид аллюминия) (Potgieter et al.) 18
В исследовании, проведённом Якобсом и соавт. (Jacobs et al.), измерялось включение железа в гемоглобин из ГПК или сульфата железа с использованием двойного изотопного метода. 25 Не было обнаружено различий по включению железа между препаратами в дозе, содержащей 50 мг элементарного железа. Назначение этой дозы с пищей было связано с достоверным снижением биодоступности железа в случае применения FeSO4, но не ГПК железа (Таблица 1).
Таблица 1.
Включение железа в гемоглобин через 14 дней применения ГПК железа (Мальтофер®) или сульфата железа во время еды или вне приёмов пищи (адаптировано из работы Jacobs et al., 1979) 25
| Доза | ГПК | % | FeSO4 | % | p |
| 50 мг | 14,5 ± 4,85 | 29,0 | 18,7 ± 3,85 | 37,4 | p > 0,4 |
| 50 мг (во время еды) | 9,0 ± 2,19 | 18,1 | 8,9 ± 2,33 | 17,7 | p > 0,9 |
Как и следовало ожидать, увеличение дозы железа сопровождалось снижением его биодоступности, которую оценивали на основании включения железа в гемоглобин (Таблица 2). Тем не менее, ни в одной из групп не было выявлено статистически значимых различий при назначении ГПК и соответствующих солей железа в одной и той же дозе. Хотя данные по содержанию ферритина в плазме не приводились, авторы отметили отрицательную корреляцию между биодоступностью железа и уровнями ферритина в плазме.
Таблица 2.
Включение железа в гемоглобин через 14 дней перорального приёма ГПК железа (Мальтофер®) или соли железа (адаптировано из работы Jacobs et al., 1984) 26
| Доза, форма | Контроль (соль) | Включение железа в гемоглобин (через 14 дней) | ||
| % ГПК | % соли | p | ||
| 5 мг Fe, жидкая | FeSO4 | 46,6 ± 17,1 | 47,8 ± 14,6 | p > 0,20 |
| 50 мг Fe, жидкая | FeSO4 | 27,1 ± 6,5 | 32,9 ± 13,4 | p > 0,20 |
| 100 мг Fe, твёрдая | Fe фумарат | 10,7 ± 4,7 | 10,3 ± 6,9 | p > 0,20 |
По сравнению с предыдущим исследованием, более высокая биодоступность железа, выявленная для ГПК железа в низкой дозе, могла быть связана с более выраженным истощением запасов железа. Если это так, то полученные данные свидетельствуют о том, что различие по биодоступности между ГПК железа и солями железа, вероятно, менее выражено и может фактически отсутствовать в условиях дефицита железа в организме.
В исследовании Кальтвассера и соавт. (Kaltwasser et al.) изучался синтез гемоглобина и утилизация железа после приёма ГПК железа в каплях, либо препарата соли железа. Оба препарата привели к статистически значимому увеличению концентрации гемоглобина по сравнению с контрольным периодом. Уровни утилизации железа составили 17% для FeSO4 и 12% для ГПК железа. 27
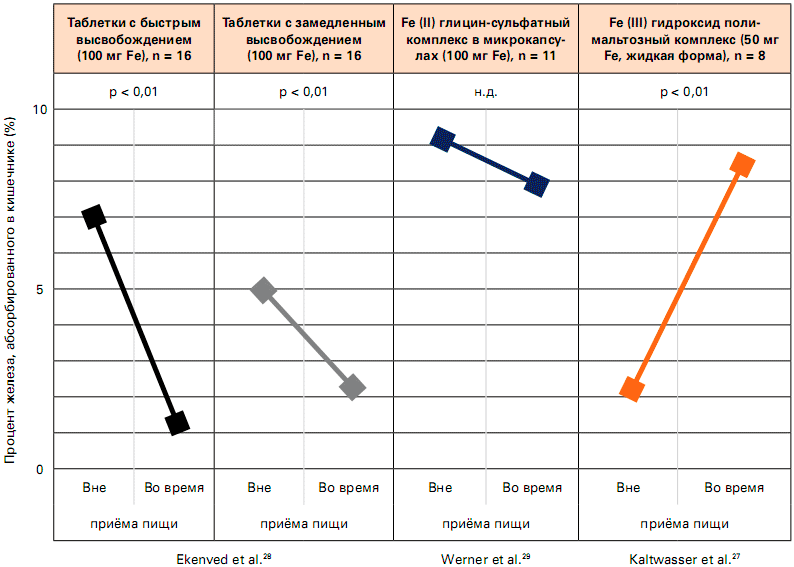
Было обнаружено, что ГПК железа отличается от других препаратов железа тем, что при его приёме во время еды абсорбция железа не уменьшается, а увеличивается, о чём свидетельствуют данные на Рисунке 3.
Рисунок 3. Влияние приёма пищи на абсорбцию препаратов железа (Forth, 1993) 30
4.2. Лекарственные взаимодействия
В исследовании Потгетера и соавт. (Potgieter et al.) сравнивалась биодоступность тетрациклина как при сопутствующем приёме ГПК железа, так и без него. Авторы не выявили клинически значимого уменьшения абсорбции тетрациклина. Плазменные уровни были в пределах обычного диапазона, принятого для биоэквивалентности (80-125%) и отношение для ППК0 всегда находилось в пределах этого окна (79,1-102,0%). 31
В другом исследовании Потгетер и соавт. (Potgieter et al.) изучали влияние одновременного приёма гидроксида алюминия (ГА) на захват железа из покрытых оболочкой таблеток Мальтофера® у пациентов с анемией. Хотя захват железа ( 59 Fe) был меньше, когда препарат назначали вместе с ГА, различия не были значимы ни статистически, ни клинически. К примеру, медиана захвата железа эритроцитами составила 0,607% без сопутствующего приёма ГА и 0,575% на фоне приёма ГА. 18
Лундквист и Сьоберг (Lundqvist, Sjoberg) использовали меченый радиоизотопом 59 Fe ГПК железа с целью изучения влияния приёма пищи на захват железа. Авторы обнаружили пользу одновременного приёма усилителя абсорбции железа (апельсинового сока) у лиц как с дефицитом железа в организме, так и без него. Они также показали, что у пациентов с анемией захват железа был выше при назначении ГПК железа вместе с пищей, тогда как у здоровых лиц, наоборот, был выше в условиях приёма натощак. 32
Исследования у крыс также показали, что захват меченого 59 Fe из ГПК железа достоверно не изменялся при одновременном приёме гидроксида алюминия, тетрациклина, ацетилсалициловой кислоты, сульфасалазина, карбоната кальция, ацетата кальция, кальция/фосфата/витамина D, D-пеницилламина, парацетамола и ауранофина. 33 Исследования in vitro также показали, что у ГПК железа число и диапазон взаимодействий намного меньше, чем у солей железа. 11
Мы можем сделать вывод, что ГПК железа (Мальтофер®), не вступает в значимые взаимодействия с какими-либо продуктами питания, компонентами пищи или лекарствами, за исключением аскорбиновой кислоты, при назначении которой отмечается тенденция к повышению абсорбции железа без измеримого восстановления Fe (III) до Fe 2+ в среде с pH выше 3. Более того, отсутствуют сообщения о реакциях этого препарата с хелатирующими железо средствами, в частности, фенолсодержащими веществами.
4.3. Клинические исследования
Туомаинен и соавт. (Tuomainen et al.) провели 6-месячное плацебо-контролируемое исследование у 48 мужчин с уровнем ферритина в сыворотке ≤30 мкг/л. Пациенты были случайным образом распределены в 3 группы: 1) приём ГПК железа (содержащего 200 мг железа) в комбинации с плацебо, напоминающим FeSO4; 2) приём микрокапсул FeSO4 (180 мг железа) в комбинации с плацебо, напоминающим ГПК железа; 3) приём плацебо для двух препаратов. 34
Через 6 месяцев сывороточные концентрации ферритина увеличились по сравнению с плацебо в 2,2 раза в группе FeSO4 (p 34
Макинтош и Якобс (Mackintosh, Jacobs) провели исследование с участием 46 доноров крови, у 23 из которых уровень железа в организме был снижен (ферритин 35
В группе пациентов с дефицитом железа терапия препаратом железа привела к значительному увеличению уровня гемоглобина (с 14,3 до 15,0 г/дл; p = 0,03) и ферритина в сыворотке (с 16,2 до 43,2 мкг/л; p = 0,002). В группе плацебо не было значимых изменений уровня гемоглобина, однако отмечалось небольшое, но достоверное увеличение уровня ферритина. Это увеличение было достоверно менее выраженным, чем в группе с приёмом ГПК железа. В контрольной группе испытуемых без дефицита железа ни ГПК железа, ни плацебо не привели к значимому изменению уровней гемоглобина или ферритина.
Исследование Якобса и соавт. (Jacobs et al.) с участием 159 доноров крови показывает, что ГПК железа (Мальтофер®) эффективно восполнял сниженные запасы железа в организме и одновременно увеличивал уровни гемоглобина у лиц с дефицитом железа в организме и без клинических признаков анемии (Hb 36
Лангстафф и соавт. (Langstaff et al.) провели исследование в условиях общей практики у 104 пациентов с ЖДА. Сравнивали эффекты приёма железа 200 мг/сут в виде ГПК (Мальтофер®, жевательные таблетки, 2 раза в сутки утром и вечером во время еды) и 180 мг/сут в виде FeSO4 (по 60 мг 3 раза в сутки, приём за 30 минут до еды). Длительность лечения составила 9 недель. При анализе в зависимости от назначенного лечения в обеих группах было выявлено высоко достоверное увеличение уровней гемоглобина в течение первых трёх недель лечения и в периоде с 6-й по 9-ю неделю. Через 3 и 6 недель уровни гемоглобина были достоверно выше в группе FeSO4, однако через 9 недель значимых различий между группами не было. Похожая динамика наблюдалась при оценке показателей гематокрита, концентрации эритроцитов, среднего содержания гемоглобина в эритроцитах, средней концентрации корпускулярного гемоглобина и среднего объёма эритроцита. 37
В данном исследовании пациентов тщательно расспрашивали по поводу возможных нежелательных явлений (НЯ). В связи с развитием НЯ, в основном со стороны желудочно-кишечного тракта, лечение было прекращено у 5 пациентов в группе с приёмом FeSO4 и 3 пациентов в группе с приёмом ГПК железа. Наиболее частыми НЯ были диспепсия, тошнота и диарея, причём первые два вида достоверно чаще возникали в группе с приёмом FeSO4 при оценке на каждом из визитов. После уточнения наиболее распространёнными НЯ (≥10% пациентов в каждой из групп) стали изменение окраски стула (ГПК 43%; FeSO4 48%), боль в животе (10% и 18%), запор (18% и 11%), утомляемость (13% и 13%) и головная боль (7% и 11%).
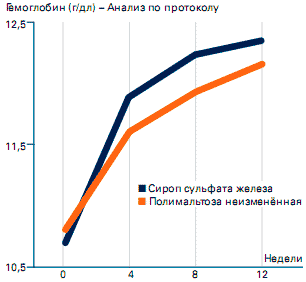
В открытом рандомизированном исследовании Якобс и соавт. (Jacobs et al.) сравнили эффективность ГПК железа и FeSO4 в лечении ЖДА у 143 регулярных доноров крови. 11 Оба препарата назначали в дозе 100 мг 2 раза в сутки. Уровни гемоглобина увеличились в одинаковой степени, без статистически значимых различий между группами через 4 или 8 недель (Рисунок 5). Кроме того, отмечалось похожее увеличение среднего содержания гемоглобина в эритроцитах и среднего объёма эритроцита, а также уменьшение процента гипохромных эритроцитов. Частота выбывания в связи с развитием нежелательных явлений, считавшихся связанными с приёмом препарата, была достоверно выше в группе FeSO4 (15 из 48) по сравнению с группой ГПК (16 из 125; p = 0,007). Основной причиной, указанной в связи с отменой лечения в группе FeSO4, являлась тошнота. Переносимость была расценена как хорошая или удовлетворительная примерно у 80% пациентов в группах с приёмом ГПК железа и 60% пациентов в группе с приёмом сульфата железа. Авторы также отметили, что при лечении солями железа уровни ферритина в сыворотке были выше, что может указывать на появление оксидативного стресса. 12
Рисунок 5. Концентрация гемоглобина в группе для анализа по протоколу через 12 недель лечения ГПК или сульфата железа (модифицировано из работы Jacobs et al., 2000) 12
Шмидт и соавт. (Schmidt et al.) провели рандомизированное двойное слепое исследование у 30 детей в возрасте от 24 до 81 месяца, имевших дефицит железа в организме как с анемией, так и без неё. Дети получали ГПК железа (в виде сиропа Мальтофер®) или сульфат железа в дозе 4 мг/кг в перерывах между приёмами пищи в течение 2 месяцев. В конце исследования в обеих группах уровень гемоглобина был достоверно выше (+1,1 ± 1,14 г/дл при лечении ГПК, +1,8 ± 1,4 г/дл при лечении FeSO4, p 39
Клиническая переносимость была хорошей в обеих группах. В группе сульфата железа окрашивание зубов отмечалось у 30% пациентов, тогда как в группе ГПК железа вообще не обнаруживалось. Жидкий стул был более частым (33%) в группе ГПК железа, чем в группе сульфата железа (10%). Ни один из препаратов не оказывал отрицательного влияния на прибавку массы тела. Частота появления тёмного стула (хорошо известный и клинически незначимый эффект терапии препаратами железа) была одинаковой в обеих группах.
В похожем двойном слепом рандомизированном исследовании Мураховски и соавт. (Murahovschi et al.) наблюдали 49 детей грудного и младшего возраста (6-40 месяцев), случайным образом разделённых на группы, принимавшие ГПК или сульфат железа в течение 60 суток (в суточной дозе 4 мг элементарного железа на 1 кг массы тела). Оба препарата привели к улучшению гематологических показателей, как показано в Таблице 3. В группе с приёмом сульфата железа увеличение происходило несколько быстрее в течение первого месяца, но было менее выраженным в течение второго месяца (Таблица 3). 40
Таблица 3.
Изменения показателей крови у детей с дефицитом железа в организме при лечении ГПК железа или сульфатом железа (из работы Murahovschi et al., 1987) 40
| ГПК (n = 22) | Сульфат железа (n = 19) | |||||
| День 0 | День 30 | День 60 | День 0 | День 30 | День 60 | |
| Эритроциты (10 6 /мм 3 ) | 4,81 ± 0,53 | 4,99 ± 0,85 | 5,08 ± 0,61 | 4,72 ± 0,63 | 4,82 ± 0,39 | 4,97 ± 0,26 |
| Гемоглобин (г/дл) | 10,3 ± 1,4 | 10,6 ± 1,5 | 11,0 ± 1,4 | 9,6 ± 1,3 | 10,3 ± 1,4 | 10,3 ± 1,4 |
| Гематокрит (%) | 33,7 ± 4,3 | 34,7 ± 4,5 | 36,2 ± 4,6 | 32,0 ± 4,3 | 33,4 ± 4,2 | 33,6 ± 4,3 |
Через 2 месяца лечения в этой группе детей с дефицитом железа была продемонстрирована одинаковая эффективность ГПК железа и сульфата железа. Низкая переносимость, приводившая к раннему выбыванию из исследования, отмечалась в 2 случаях (8%) в группе ГПК и 5 случаях (21%) в группе FeSO4. Во всех случаях причинным фактором являлась тяжёлая диарея. В группе с приёмом FeSO4 также отмечались и другие симптомы (рвота и запор, по 1 случаю).
Агаоглу и соавт. (Agaoglu et al.) провели сравнительное исследование у детей в возрасте от 6 до 12 лет (с ЖДА и без) и показали, что в группе детей с ЖДА средний коэффициент интеллекта (IQ) был достоверно меньше на 12,9 пунктов. Приём полимальтозного комплекса железа (5 мг/ кг/сут в составе мультивитаминного препарата в течение 4-6 месяцев сопровождался достоверным увеличением среднего IQ на 4,8 пунктов, в результате чего различия по IQ между двумя группами детей к концу исследования перестали быть значимыми. 7
Деваки и соавт. (Devaki et al.) исследовали влияние дополнительного приёма препарата на иммунную систему у 120 подростков с разными уровнями содержания железа в организме (некоторые с ЖДА, некоторые без). У подростков, получавших ГПК железа (100 мг/сут. 6 дней в неделю в течение 8 месяцев), отмечалось увеличение бактерицидной активности нейтрофилов, улучшение теста на восстановление нитро-синего тетразолия и реакции на фитогеммаглюттинин, чего не наблюдалось в группе плацебо. Побочных эффектов, связанных с приёмом ГПК железа, не отмечалось. 41
Веттер и соавт. (Vetter et al.) сравнили три дозы ГПК железа (200, 400 и 600 мг) у 63 взрослых пациентов с анемией. Средние значения гемоглобина во всех трёх группах возрастали в дозозависимой форме, однако интерпретация этих результатов затрудняется тем фактом, что в группе с приёмом 600 мг препарата было больше пациентов с тяжёлой анемией. Концентрации гемоглобина на момент завершения исследования были одинаковыми во всех группах. Среднее время, необходимое для увеличения уровня Hb до желаемых значений, также зависело от дозы и в группах с приёмом 200, 400 и 600 мг составило 6,6, 8,3 и 11,3 недель, соответственно. Эти данные свидетельствуют о том, что при необходимости более быстрой коррекции дефицита железа суточная доза может быть увеличена до 400 или 600 мг. Все дозы хорошо переносились пациентами; в трёх группах отмечалось всего 6, 7 и 9 нежелательных явлений, связанных с приёмом препарата. 42
Андраде и соавт. (Andrade et al.) сравнили эффекты назначения ГПК детям грудного и младшего возраста с ЖДА с пищей и в перерывах между едой. При сравнении групп значимых различий не отмечалось, что подтверждает тот факт, что приём ГПК железа с пищей не приводит к снижению его эффективности (Таблица 4). 43
Таблица 4.
Эффекты при назначении ГПК железа во время еды или в перерывах между приёмами пищи (из работы Andrade et al., 1992) 43
| ГПК железа (n = 93) | ||||
| Во время еды (n = 50) | В перерывах между приёмами пищи (n = 43) | |||
| День 0 | День 90 | День 0 | День 90 | |
| Эритроциты (10 3 /мм 3 ) | 3903 | 4233 | 3919 | 4344 |
| Гемоглобин (г/дл) | 9,84 | 11,19 | 9,85 | 11,10 |
| Гематокрит (%) | 31,5 | 35,0 | 30,5 | 34,3 |
Нежелательные явления отмечались у 3 пациентов (6%) в группе с приёмом ГПК железа во время еды и у 4 пациентов (8%) в группе с приёмом ГПК в перерывах между едой. Всего 2 пациента в каждой из групп прекратили лечение в связи с желудочно-кишечными событиями (в основном, диареей).
Гюрер и соавт. (Gurer et al.) провели сравнительное исследование у 50 детей в возрасте от 8 месяцев до 9 лет, имевших ЖДА. Пациенты получали 5 мг/кг/сут сиропа Мальтофера® (ГПК железа) или FeSO4. Через 1 месяц лечения в обеих группах отмечалось улучшение уровней гемоглобина, гематокрита, железа сыворотки, общей железо-связывающей способности, насыщения трансферрина железом и ферритина. Исследователи сделали вывод, что различие по эффективности между двумя препаратами не было существенным. Тем не менее, нежелательные явления были более частыми в группе FeSO4, причём это различие в основном было связано с более высокой частотой окрашивания зубов (40% и 18%, соответственно) и развития диареи (20% и 0,4%, соответственно). 45
Халиотис и Папанастасиу (Haliotis, Papanastasiou) провели исследование у 100 детей в возрасте от 12 до 113 месяцев (средний возраст 40 месяцев) с латентной или клинически выраженной ЖДА, которые были случайным образом разделены на группы, принимавшие протеин сукцинилата железа или ГПК железа. Все пациенты получали элементарное железо в дозе 4 мг/кг (максимально 80 мг в сутки) в течение 2 месяцев. Хотя исследование было рандомизированным, в группе с приёмом протеинсукцинилата железа исходные концентрации гемоглобина были достоверно выше. Через 2 месяца лечения прирост концентрации гемоглобина был одинаковым в обеих группах. 46
5. Препараты железа в комбинации с фолиевой кислотой
Препарат ГПК железа назначали в комбинации с фолиевой кислотой беременным женщинам. Гейссер и соавт. (Geisser et al.) в рандомизированном исследовании у беременных женщин с дефицитом железа в организме сравнили три комбинированных препарата железа и фолата. Критериями эффективности служили показатели гемоглобина и гематокрита, а также концентрация эритроцитов, средний объём эритроцита, концентрации ферритина и железа в сыворотке. Значимых различий по каждому из этих показателей между группами и за весь период исследования выявлено не было (Таблица 5). Авторы сделали вывод, что все три комбинации железа и фолата обладают одинаковой эффективностью. 47
Таблица 5.
Сравнение эффективности трёх препаратов железа в комбинации с фолиевой кислотой у беременных женщин с дефицитом железа в организме (из работы Geisser et al. 1987) 47
| Препарат | Мальтофер® Фол | Феррум-H-Фол-B | Ферро-Фолик-500 | |||
| Состав препарата | ГПК железа + фолиевая кислота | Фумарат железа, фолиевая кислота, витамин B12 | Сульфат железа, фолиевая кислота, аскорбиновая кислота | |||
| Неделя | 0 | 8 | 0 | 8 | 0 | 8 |
| Гематокрит (%) | 39,2 ± 3,3 | 38,4 ± 3,2 | 39,4 ± 3,2 | 38,6 ± 2,9 | 39,1 ± 3,4 | 38,1 ± 2,6 |
| Гемоглобин (г/л) | 125,0 ± 10,7 | 121,3 ± 10,1 | 123,0 ± 3,2 | 122,0 ± 8,2 | 124,0 ± 10,4 | 120,7 ± 7,2 |
| Эритроциты (10 12 /л) | 4,38 ± 0,49 | 4,20 ± 0,39 | 4,50 ± 0,77 | 4,20 ± 0,40 | 4,38 ± 0,51 | 4,03 ± 0,38 |
| Средний объём эритроцита (fL) | 89,9 ± 6,1 | 91,5 ± 6,8 | 90,0 ± 6,7 | 92,4 ± 6,2 | 89,6 ± 5,7 | 94,5 ± 5,5 |
| Ферритин (мкг/л) | 34,3 ± 36,6 | 21,2 ± 15,6 | 30,3 ± 21,6 | 19,4 ± 16,0 | 26,3 ± 22,8 | 22,3 ± 14,7 |
| Железо сыворотки (мкмоль/л) | 20,9 ± 7,1 | 21,6 ± 4,9 | 21,0 ± 6,6 | 20,1 ± 6,9 | 20,7 ± 6,3 | 20,7 ± 5,2 |
Это исследование показывает, что ГПК железа сопоставим по своей эффективности в качестве источника железа с такими препаратами как сульфат или фумарат железа, то есть наиболее широко используемыми и хорошо изученными солями железа.
Берути (Beruti) назначал комбинацию ГПК железа и фолиевой кислоты 30 беременным женщинам в третьем триместре, имевшим смешанную железо-фолатную дефицитную анемию (Hb 48
6. Безопасность
Во всех сравнительных исследованиях ГПК железа с солями железа частота развития и, как правило, тяжесть нежелательных явлений при приёме ГПК были либо схожими, либо меньше, чем при назначении солей железа (Таблица 6). Эти различия по частоте и тяжести побочных эффектов были особенно выраженными по таким симптомам, как тошнота, рвота и изжога, и менее выраженными по такому симптому, как диарея, хотя она сравнительно редко отмечалась при всех режимах лечения. Более низкая частота нежелательных явлений со стороны верхних отделов желудочно-кишечного тракта, которые являются основной причиной низкой приверженности пациентов к приёму солей железа, может быть серьезным аргументом в пользу назначения ГПК железа.
Таблица 6.
Нежелательные явления (НЯ), зарегистрированные в исследованиях с использованием железа (III) гидроксид полимальтозного комплекса (Fe-ГПК)
| Автор, год | Популяция | n | лечение; длительность | нежелательные явления в группе Fe-ГПК Примечание |
| Исследования у взрослых людей | ||||
| Jacobs [12], 2000 | Взрослые с ЖДА | 120 | Fe-ГПК, капли; 12 недель | Тошнота 11%, запор 20%, окрашивания зубов 0% В группе FeSO4 тошнота 45%, запор 13%, окрашивание зубов 11% |
| Jacobs [36], 1993 | Взрослые с ЖДА | 108 | Fe-ГПК; 12 недель | Лёгкие побочные эффекты, нет выбываний В группе FeSO4 11 выбыли в связи с НЯ со стороны ЖКТ |
| Langstaff [37], 1993 | Взрослые с ЖДА | 55 | Железо Гаусмана; 9 недель | НЯ со стороны ЖКТ 17%: тошнота/диспепсия (4), диарея (0) В группе FeSO4 НЯ со стороны ЖКТ 24%: тошнота/диспепсия (12), диарея (6), n = 54 |
| Tuomainen [34], 1999 | Взрослые с ЖДА | 15 | Fe-ГПК; 6 месяцев | НЯ со стороны ЖКТ 13% (2) В группе FeSO4 НЯ со стороны ЖКТ 20% (3) |
| Mackintosh [35], 1988 | Доноры крови ± дефицит железа | 22 | Fe-ГПК, таблетки; 8 месяцев | Нет НЯ Fe-ГПК не отличается от плацебо |
| Vetter [42], 1994 | Взрослые с ЖДА | 63 | Мальтофер® 200, 400 или 600 мг; 12 недель | НЯ 52-67%, в основном со стороны ЖКТ; переносимость расценена как хорошая или удовлетворительная у 71-93% |
| Rosenberg [44], 1979 | Женщины с ДЖ | 49 | ПЖГ, сироп; 5-24 дня | Переносимость хорошая или очень хорошая у 92%, 4 случая НЯ Переносимость такая же, как и в группе фумарата железа |
| Исследования у беременных или кормящих женщин | ||||
| Al [52], 2005 | Беременные женщины | 45 | ПЖГ, таблетки + фолиевая кислота; 4 недели | 14 НЯ со стороны ЖКТ, возможно связанных с приёмом препарата |
| Kunz [53], 2003 | Беременные женщины | 60 | М-фолат; 90 дней | Гастроэнтерит (1), запор (3), тошнота/рвота (2), боль в животе (1), окрашивание зубов (1) |
| Beruti [48], 1978 | Беременные женщины | 30 | Fe-ГПК + фолиевая кислота + цианокобаламин; 30 дней | Превосходная переносимость 90% (27); тошнота/боль в эпигастрии (3) |
| Sas [38], 1984 | Женщины (5 беременных) с ЖДА | 20 | ПЖГ, сироп; 12 недель | Несколько НЯ, диарея (1) В группе FeSO4 гастралгия (1), рвота (1), n = 20 |
| Malikova [54], 2005 | Кормящие женщины | 50 | Мальтофер, таблетки; 12 недель | Не было НЯ у матерей и детей |
| Исследования у детей грудного, младшего и старшего возраста, подростков | ||||
| Soboleva [55], 2003 | Дети 6 мес.-4 года | 127 | Мальтофер®, капли | Лечение завершено во всех случаях; 10% запоры (6% прекратили лечение) |
| Agaoglu [7], 2007 | Дети 6-12 лет | 30 | Fe-ГПК | Нет НЯ |
| Kavakli [56], 2004 | Дети 6 мес.-15 лет с ЖДА | 33 | Fe-ГПК; 6 месяцев | Боль в животе (2); запор (2); диарея (2), тошнота (2) В группе FeSO4 боль в животе (1), запор (1), диарея (1), тошнота (2), окрашивание зубов (1), n = 39 |
| Gurer [45], 1998 | Дети с ЖДА | 25 | ПЖГ; 4 недели | Окрашивание зубов (4), тошнота (6), диарея (1), запор (1) В группе глицин-сульфата железа окрашивание зубов (10), тошнота (5), диарея (5), запор (0), n = 25 |
| Haliotis [46], 1998 | Дети с ДЖА | 50 | Fe-ГПК; 8 недель | НЯ 12% (6): боль в животе (2), диарея (3), тошнота (4), рвота (2) Протеин-суккцинилат железа: боль в животе (2), диарея (1), тошнота (3), рвота (1), n = 50 |
| Murahovchi [40] | Дети | 25 | Fe-ГПК; 8 недель | Хорошая переносимость 88%; тяжёлая диарея 8% (2) В группе FeSO4 хорошая переносимость 66%; тяжёлая диарея 21% (5), рвота (1), запор (1), n = 17 |
| Schmidt [39] | Дети с ДЖ или ЖДА | 15 | Fe-ГПК; 8 недель | Хорошая переносимость (нет окрашивания зубов) В группе FeSO4 окрашивание зубов у 3 из 10 |
| Soboleva [57] | Дети | 72 | Fe-ГПК ± фолиевая кислота (вариабельно) | 2 случая запора, других НЯ не было |
| Kazyolova [58] | Дети с ЖДА | 69 | Мальтофер, капли; 4-9 недель | Нет НЯ |
| Andrade [43] | Дети | 97 | Fe-ГПК с едой или в перерывах между; 90 дней | НЯ у 7; 3 выбывания, связанных с лекарством: диарея (2), тошнота/рвота (1) |
| Soboleva [59] | Подростки 15-18 лет | 170 | Мальтофер, капли или сироп, либо Феррум-лек жидкий (вариабельно) | Запоры 6-8% Препараты Fe-ГПК были лучше, чем три препарата Fe (II) |
| Devaki [41] | Подростки | Fe-ГПК; 8 месяцев | Нет НЯ | |
В ряде клинических исследований ранняя отмена лечения в связи с нежелательными явлениями отмечалась реже при лечении ГПК, чем препаратами железа в виде железистых солей. В связи с этим можно сделать вывод, что назначение ГПК железа (Мальтофера®) позволяет достичь более высокой приверженности к лечению, чем назначение препаратов солей железа.
За последние годы повышенное внимание уделялось изучению тонких механизмов поддержания окислительно-восстановительного баланса клетки, и постепенно были получены доказательства того, что железо может обладать проокислительным действием. 14 Утверждалось также, что приём солей железа может служить потенциальным фактором риска развития целого ряда хронических заболеваний.
Туомаинен и соавт. (Tuomainen et al.) продемонстрировали, что при назначении сульфата железа способность липопротеинов очень низкой (ЛОНП) и низкой плотности (ЛНП) к окислению увеличена на 8,8% (p 34
Якобс и соавт. (Jacobs et al.) сообщили о более выраженном увеличении уровня ферритина сыворотки по сравнению с ферритином эритроцитов при лечении сульфатом железа в сравнении с ГПК железа. 12 Как известно, ферритин выступает в роли «позитивного» реагента острой фазы и таким образом не может служить надёжным показателем для оценки запасов железа при заболеваниях, характеризующихся острой реакцией. 50 Авторы утверждают, что увеличение уровня ферритина в сыворотке, наблюдающееся при лечении различными солями железа, частично связано с влиянием железа на клеточном уровне.
7. различные формы полимальтозного комплекса железа
Во всех представленных выше исследованиях в качестве препарата ГПК железа использовали Мальтофер®. Однако в некоторых странах существуют и другие препараты полимальтозного комплекса железа или углеводных соединений железа. Они отличаются по своим физико-химическим свойствам (Таблица 7), что влияет на их биодоступность и переносимость. К примеру, вещества, нерастворимые при значениях pH желудочного сока равных 1,2 не будут обладать одинаковой эффективностью, поскольку они с большей вероятностью образуют агрегаты или преципитаты, имеющие меньшую площадь поверхности для высвобождения железа по сравнению с раствором того же вещества. Комплексы с более высокой молекулярной массой, как правило, характеризуются замедленным высвобождения железа, что определяет менее приемлемую степень абсорбции и низкую эффективность. 11,16
Таблица 7.
Физико-химические свойства различных препаратов ГПК железа (из работы Geisser 2004) 16
Прямое сравнение Мальтофера® с гематином у детей в возрасте от 6 до 24 месяцев с анемией показало, что в группе Мальтофера® процент пациентов с ответом на лечение (то есть достижением уровня гемоглобина не менее 11 г/дл) был выше, к тому же Мальтофер лучше переносился и вызывал меньшее число нежелательных эффектов, чем гематин.
8. Выводы
В ряде исследований было продемонстрировано, что ГПК железа достоверно улучшает первичные конечные точки лечения препаратами железа (то есть синтез гемоглобина и/или восстановление запасов железа) как у детей грудного и младшего возраста, так и у взрослых (Таблица 8).
Таблица 8.
Общий анализ эффективности: динамика концентрации гемоглобина, среднего объёма эритроцита, концентраций ферритина сыворотки и ферритина эритроцитов на фоне лечения препаратами ГПК железа
| n | Форма препарата, доза | Длительность терапии | результаты | Сравнение с контролем | Ссылка | ||
| До лечения | Среднее изменение | До лечения | Среднее изменение | ||||
| Гемоглобин | |||||||
| 24 | Капли, 100 мг 2 р./сут. | 12 недель | 107,8 г/л | +13,5 г/л | FeSO4 107,1 г/л | + 16,1 г/л | [12] |
| 23 | 108,9 г/л | +13,7 г/л | |||||
| 24 | 107,8 г/л | +9,6 г/л | |||||
| 93 | Капли, 2,5 мг/кг | 90 дней | 98,4 г/л | +13,5 г/л | Нет контроля | [43] | |
| 98,5 г/л | +12,5 г/л | ||||||
| 50 | Капли, 4 мг/кг/сут., max 80 мг/сут. | 2 месяца | 107,0 г/л | +14,0 г/л | Протеин сукцинилат железа 111 г/л | + 14,0 г/л | [46] |
| 12 | Сироп, 2 мг/кг 2 р./сут. | 60 дней | 115,0 г/л | +10,8 г/л | FeSO4 106,0 г/л | + 18,5 г/л | [39] |
| 22 | Сироп, 2 мг/кг 2 р./сут. | 60 дней | 103,2 г/л | +7,0 г/л | FeSO4 96,4 г/л | +6,7 г/л | [40] |
| 20 | Сироп, 100 мг/сут. | 12 недель | 104,3 г/л | +13,4 г/л | FeSO4 108,3 г/л | + 13,0 г/л | [38] |
| Фумарат 104,2 г/л | + 12,5 г/л | ||||||
| 49 | Сироп, 100 мг/сут. | 5-24 дня | 109,0 г/л | +6,7 г/л | Фумарат 108,0 г/л | +8,7 г/л | [44] |
| 15 | Таблетки, 100 мг 2 р./сут. | 6 месяцев | 145 г/л | +3,0 г/л | FeSO4 145,0 г/л | +1,5 г/л | [34] |
| Плацебо 144,0 г/л | -3,6 г/л | ||||||
| 22 | Таблетки, 100 мг 2 р./сут. | 8 недель | 143,1 г/л | +7,1 г/л | Плацебо 142,5 г/л | +6,2 г/л | [35] |
| 146,1 г/л | +4,1 г/л | Плацебо 146,0 г/л | +6,0 г/л | ||||
| 53 | Таблетки, 100 мг/сут. | 12 недель | 116,3 г/л | +9,6 г/л | FeSO4 114,0 г/л | +18,1 г/л | [36] |
| 55 | Таблетки, 100 мг 2 р./сут. | 114,3 г/л | +16,6 г/л | ||||
| 22 | Таблетки, 100 мг 2 р./сут. | 3 недели | 107,4 г/л | +6,0 г/л | 109,3 г/л | +8,3 г/л | [37] |
| 6 недель | 107,4 г/л | +9,3 г/л | + 12,8 г/л | ||||
| 9 недель | 107,4 г/л | +12,9 г/л | + 14,6 г/л | ||||
| 15 | Таблетки, 100 мг 2 р./сут. | 12 недель | 110,0 г/л | +10,8 г/л | Нет контроля | [42] | |
| 13 | Таблетки, 200 мг 2 р./сут. | 107,0 г/л | +10,0 г/л | ||||
| 17 | Таблетки, 200 мг 3 р./сут. | 100,0 г/л | +22,7 г/л | ||||
| 15 | 3 мг/кг 3 р./сут. | 60 дней | 85,0 г/л | +34,0 г/л | 86,0 г/л | +35,0 г/л | [60] |
| 14 | 3-6 мг/сут. | 6 месяцев | 100,0 г/л | +16,0 г/л | 96,0 г/л | +29,0 г/л | [61] |
| Средний объём эритроцита | |||||||
| 24 | Капли, 100 мг 2 р./сут. | 12 недель | 73,9 мкм 3 | +5,7 мкм 3 | FeSO4 73,7 мкм 3 | +6,9 мкм 3 | [12] |
| 23 | 71,6 мкм 3 | +6,3 мкм 3 | |||||
| 24 | 72,8 мкм 3 | +5,5 мкм 3 | |||||
| 93 | Капли, 2,5 мг/кг | 90 дней | 76,7 мкм 3 | +2,68 мкм 3 | Нет контроля | [43] | |
| 76,5 мкм 3 | + 1,90 мкм 3 | ||||||
| 50 | Капли, 4 мг/кг/сут., max 80 мг/сут. | 2 месяца | 70,5 мкм 3 | +4,2 мкм 3 | 72,9 мкм 3 | +4,9 мкм 3 | [46] |
| 22 | Сироп, 2 мг/кг 2 р./сут. | 60 дней | 70,2 мкм 3 | +1,2 мкм 3 | 65,3 мкм 3 | +2,4 мкм 3 | [40] |
| 15 | Таблетки, 100 мг 2 р./сут. | 6 месяцев | 88,0 мкм 3 | +3,0 мкм 3 | FeSO4 88,0 мкм 3 | +3,0 мкм 3 | [34] |
| Плацебо 89,0 мкм 3 | + 1,0 мкм 3 | ||||||
| 22 | Таблетки, 100 мг 2 р./сут. | 3 недели | 83,6 мкм 3 | +2,1 мкм 3 | 82,2 мкм 3 | +3,2 мкм 3 | [37] |
| 6 недель | +2,6 мкм 3 | +5,0 мкм 3 | |||||
| 9 недель | +3,0 мкм 3 | +4,4 мкм 3 | |||||
| 15 | Таблетки, 100 мг 2 р./сут. | 12 недель | 81,8 мкм 3 | +2,8 мкм 3 | Нет контроля | [42] | |
| 13 | Таблетки, 200 мг 2 р./сут. | 80,5 мкм 3 | +3,7 мкм 3 | ||||
| 17 | Таблетки, 200 мг 3 р./сут. | 76,6 мкм 3 | +7,0 мкм 3 | ||||
| Ферритин | |||||||
| 24 | Капли, 100 мг 2 р./сут. | 12 недель | 2,94 мкг/л | +2,58 мкг/л | FeSO4 3,50 мкг/л | +8,55 мкг/л | [12] |
| 23 | 3,20 мкг/л | +2,72 мкг/л | |||||
| 24 | 3,81 мкг/л | +5,50 мкг/л | |||||
| 50 | Капли, 4 мг/кг/сут., max 80 мг/сут | 2 месяца | 11,1 мкг/л | +20,2 мкг/л | Протеин сукцинилат железа 12,7 мкг/л | +25,1 мкг/л | [46] |
| 12 | Сироп, 2 мг/кг 2 р./сут | 60 дней | 12,3 мкг/л | +20,3 мкг/л | FeSO4 12,3 мкг/л | +53,7 мкг/л | [39] |
| 22 | Сироп, 2 мг/кг 2 р./сут | 60 дней | 30,5 мкг/л | -19,2 мкг/л | FeSO4 16,5 мкг/л | -3,2 мкг/л | [40] |
| 15 | Таблетки, 100 мг 2 р./сут. | 6 месяцев | 20,5 мкг/л | +27,4 мкг/л | FeSO4 22,0 мкг/л | +47,0 мкг/л | [34] |
| Плацебо 20,0 мкг/л | +5,0 мкг/л | ||||||
| 22 | Таблетки, 100 мг 2 р./сут. | 8 недель | 16,2 мкг/л | +27,0 мкг/л | Плацебо 16,7 мкг/л | +10,6 мкг/л | [35] |
| 71,1 мкг/л | + 10,7 мкг/л | Плацебо 68,6 мкг/л | -10,8 мкг/л | ||||
| 53 | Таблетки, 100 мг/сут. | 12 недель | 13,5 мкг/л | +3,0 мкг/л | FeSO4 18,5 мкг/л | +17,8 мкг/л | [36] |
| 55 | Таблетки, 100 мг 2 р./сут. | 14,8 мкг/л | +7,2 мкг/л | ||||
| 15 | Таблетки, 100 мг 2 р./сут. | 12 недель | 6,6 мкг/л | +7,8 мкг/л | Нет контроля | [42] | |
| 13 | Таблетки, 200 мг 2 р./сут. | 5,0 мкг/л | +3,2 мкг/л | ||||
| 17 | Таблетки, 200 мг 3 р./сут. | 5,3 мкг/л | +5,8 мкг/л | ||||
| 15 | 3 мг/кг 3 р./сут | 60 дней | 19,6 мкг/л | + 15,7 мкг/л | 15,9 мкг/л | +25,7 мкг/л | [60]* |
| 14 | 3-6 мг/сут | 6 месяцев | 22,6 мкг/л | -10,8 мкг/л | 20,2 мкг/л | +36,4 мкг/л | [61]** |
| Ферритин эритроцитов | |||||||
| 15 | Таблетки, 100 мг 2 р./сут. | 6 месяцев | 16,9 | +4,6 | FeSO4 15,9 | +5,8 | [34] |
| Плацебо 17,7 | -2,9 | ||||||
| 24 | Таблетки, 100 мг 2 р./сут. | 12 недель | 1,3 фг/1000 | +0,86 фг/1000 | FeSO4 1,40 фг/1000 | +0,80 фг/1000 | [12] |
| 23 | 1,1 фг/1000 | +0,31 фг/1000 | |||||
| 24 | 0,83 фг/1000 | +0,43 фг/1000 | |||||
Было обнаружено, что для ГПК железа характерно более медленное развитие терапевтического эффекта, чем при назначении классических солей железа. Однако в дальнейшем в исследовании Якобса и соавт. (Jacobs et al.), проведённом в соответствии с принципами надлежащей клинической практики (GCP), не было обнаружено каких-либо различий по всем контрольным точкам. 12 Более того, примерно через 3 месяца терапии эффекты были одинаковыми. Исследования с ранжированием доз свидетельствуют о том, что суточная доза 2 х 100 мг более эффективна, чем 100 мг, и не приводит к увеличению частоты нежелательных явлений. В другом исследовании также были получены обоснования для применения препарата железа в суточной дозе до 600 мг.
Важное различие между ГПК железа и солями железа заключается в том, что биодоступность первого возрастает, если его принимать во время еды, в связи с чем данный режим приёма является рекомендуемым.
Показаниями к назначению ГПК железа в виде перорального препарата является лечение любого рода дефицита железа в организме, например, железодефицитной анемии или латентного дефицита железа (уменьшение запасов железа), а также профилактика возникновения дефицита железа во время беременности и кормления грудью.
Более того, ГПК железа успешно используют для восстановления запасов железа у регулярных доноров крови и коррекции дефицита железа (как с анемией, так и без неё) у детей грудного и младшего возраста.
Препарат ГПК железа хорошо переносится и гораздо реже приводит к желудочно-кишечным расстройствам, чем препараты солей железа. Как частота развития, так и тяжесть нежелательных явлений были меньше в группе с приёмом ГПК железа, чем в группе с приёмом сульфата железа. Кроме того, препарат ГПК железа более безопасен в плане возможной случайной передозировки, так как для него не было зарегистрировано ни одного случая летального исхода.
Недавно проведённые исследования свидетельствуют о том, что сульфат железа может повышать активность окислительного стресса, в то время как имеются данные о том, что это опасение не имеет оснований в случае использования ГПК железа.
Принимая во внимание критерии определения терапевтической эффективности, согласно которым две формы эквивалентны, если они демонстрируют одинаковую эффективность, можно сделать вывод, что ГПК железа превосходит соли железа, так как демонстрирует сходную эффективность, но имеет более высокий профиль безопасности.
_500.gif)