Дилатация левого предсердия что это такое и как
Дилатация предсердий
Дилатация предсердий – это расширение полости левого и (или) правого предсердий с сохранением нормальной толщины образующих их стенок. Данное состояние не является самостоятельным заболеванием и рассматривается как один из симптомов, характерных для целого ряда врожденных либо приобретенных патологий сердечно-сосудистой или дыхательной системы.
Причины
В основе патологического механизма развития дилатации предсердий лежит затруднение кровотока через атриовентрикулярные отверстия, посредством которых происходит сообщение полостей желудочков и предсердий.
Причиной расширения полости левого предсердия чаще всего является длительно сохраняющееся повышенное давление в большом круге кровообращения, обусловленное систематическими значительными физическими нагрузками. Еще одной причиной дилатации правого предсердия может стать мерцательная аритмия, хотя во многих случаях она развивается уже как осложнение патологического расширения камеры сердца.
К дилатации правого предсердия приводит повышение давления крови в малом круге кровообращения, что может быть обусловлено следующими факторами:
Формы
В зависимости от особенностей патогенеза выделяют две формы дилатации предсердий:
Диагноз «дилатация» ставится в случае увеличение объема одной или нескольких камер сердца более чем на 5%.
Признаки
Незначительная или умеренная дилатация предсердий протекает без каких-либо клинических симптомов и обычно выявляется случайно, при проведении обследования по другому поводу, и по своей сути является диагностической находкой.
Значительное расширение предсердий сопровождается ухудшением их насосной функции, что приводит к появлению аритмии, развитию хронической сердечной недостаточности. Симптомы:
Диагностика
Основным методом диагностики дилатации предсердий является ультразвуковое исследование сердца. Оно позволяет оценить объем сердечных камер, толщину стенок миокарда и особенности их сокращения, выявить возможную патологию перикарда, тромбы в полостях сердца, признаки поражения клапанного аппарата. Полученные в ходе исследования данные сравниваются с нормой с учетом роста и веса пациента. Диагноз «дилатация» ставится в случае увеличение объема одной или нескольких камер сердца более чем на 5%.
В диагностике дилатации предсердий используются и другие инструментальные методы:
Дилатация предсердий требует дифференциальной диагностики с наследственными кардиомиопатиями, миокардитами, ишемической болезнью, врожденными и приобретенными пороками сердца, расслаивающей аневризмой.
Лечение
Во многих случаях выявить причину, вызвавшую развитие дилатации предсердий, не удается, и потому лечение направлено на борьбу с хронической сердечной недостаточностью. С этой целью пациентам назначают:
Если удается устранить причину дилатации предсердий, то их объем может постепенно уменьшиться и вернуться к нормальным значениям.
При неэффективности консервативной терапии дилатации предсердий и нарастании симптомов хронической сердечной недостаточности решается вопрос о хирургическом лечении. Оно заключается в установке кардиостимулятора, обеспечивающего улучшение гемодинамических процессов.
При тяжелой сердечной недостаточности единственный метод лечения – трансплантация сердца. Однако эта операция выполняется крайне редко ввиду высокой стоимости и сложности.
Профилактика
Профилактика развития дилатации предсердий заключается в мерах, направленных на предотвращение развития заболеваний сердечно-сосудистой и дыхательной систем. К ним относятся:
Последствия и осложнения
Если удается устранить причину дилатации предсердий, то их объем может постепенно уменьшиться и вернуться к нормальным значениям. Во всех остальных случаях камеры сердца постепенно увеличиваются в объеме, что приводит к нарастающей сердечной недостаточности.
Об авторе
Опыт работы: врач анестезиолог-реаниматолог городского родильного комплекса, врач реаниматолог отделения гемодиализа.
Информация является обобщенной и предоставляется в ознакомительных целях. При первых признаках болезни обратитесь к врачу. Самолечение опасно для здоровья!
В стремлении вытащить больного, доктора часто перегибают палку. Так, например, некий Чарльз Йенсен в период с 1954 по 1994 гг. пережил более 900 операций по удалению новообразований.
Даже если сердце человека не бьется, то он все равно может жить в течение долгого промежутка времени, что и продемонстрировал нам норвежский рыбак Ян Ревсдал. Его «мотор» остановился на 4 часа после того как рыбак заблудился и заснул в снегу.
Раньше считалось, что зевота обогащает организм кислородом. Однако это мнение было опровергнуто. Ученые доказали, что зевая, человек охлаждает мозг и улучшает его работоспособность.
При регулярном посещении солярия шанс заболеть раком кожи увеличивается на 60%.
Кроме людей, от простатита страдает всего одно живое существо на планете Земля – собаки. Вот уж действительно наши самые верные друзья.
В нашем кишечнике рождаются, живут и умирают миллионы бактерий. Их можно увидеть только при сильном увеличении, но, если бы они собрались вместе, то поместились бы в обычной кофейной чашке.
Для того чтобы сказать даже самые короткие и простые слова, мы задействуем 72 мышцы.
Существуют очень любопытные медицинские синдромы, например, навязчивое заглатывание предметов. В желудке одной пациентки, страдающей от этой мании, было обнаружено 2500 инородных предметов.
Если улыбаться всего два раза в день – можно понизить кровяное давление и снизить риск возникновения инфарктов и инсультов.
Ученые из Оксфордского университета провели ряд исследований, в ходе которых пришли к выводу, что вегетарианство может быть вредно для человеческого мозга, так как приводит к снижению его массы. Поэтому ученые рекомендуют не исключать полностью из своего рациона рыбу и мясо.
Согласно исследованиям, женщины, выпивающие несколько стаканов пива или вина в неделю, имеют повышенный риск заболеть раком груди.
Печень – это самый тяжелый орган в нашем теле. Ее средний вес составляет 1,5 кг.
Общеизвестный препарат «Виагра» изначально разрабатывался для лечения артериальной гипертонии.
Каждый из нас слышал истории о людях, которые никогда не чистили зубы и не имели при этом проблем. Так вот, скорее всего, эти люди либо не знали о наличии у себ.
Фибрилляция предсердий (мерцательная аритмия) – что должен знать пациент
Фибрилляция предсердий (ФП), или мерцательная аритмия (многие врачи до сих пор называют ее так), – одно из самых частых нарушений ритма. У пожилых людей встречается чаще, чем у молодых. Давайте вместе разберемся, почему она возникает – причины мерцательной аритмии – и чем может быть опасна для человека.
Что такое фибрилляция предсердий?
Формы
Мерцательная аритмия (фибрилляция предсердий) может быть приступообразной или хронической. Если приступы аритмии (пароксизмы) длятся недолго (от нескольких минут до 7 дней) и нормальный ритм восстанавливается самопроизвольно, такая форма фибрилляции предсердий называется пароксизмальной.
Может ли фибрилляция предсердий быть опасной для здоровья?
Симптомы фибрилляции предсердий (мерцательной аритмии)
Причины мерцательной аритмии (фибрилляции предсердий)
Причины, которые приводят к фибрилляции предсердий (мерцательной аритмии), могут быть разные. Фибрилляция предсердий может быть самостоятельным заболеванием (идиопатическая форма), однако гораздо чаще мерцательная аритмия ритма появляется у людей, страдающих сердечно-сосудистыми заболеваниями: пороки клапанов сердца, ишемическая болезнь сердца, гипертония, кардиомиопатии, перикардит и миокардит, операции на сердце. Также в группу риска заполучить мерцательную аритмию входят люди, страдающие патологией щитовидной железы (гиперфункция щитовидной железы – тиреотоксикоз, или «токсический зоб»). Иногда нарушение ритма – первое проявление заболевания щитовидной железы, поэтому при первом пароксизме фибрилляции предсердий врачи всегда проводят ее обследование.
Очень подробно и наглядно о фибрилляции предсердий рассказывает следующий ролик (на английском языке):
Также частой причиной фибриляции предсердий является злоупотребление алкоголем. Частый прием алкоголя нарушает уровень и баланс электролитов в крови (ионы калия, натрия и магния очень важны при работе любых мышц, но в первую очередь – сердечной) и оказывает прямое токсическое действие на сердце, приводя к расширению предсердий и желудочков, снижению сократительной функции. Возможно появление мерцательной аритмии у пациентов с хроническими заболеваниями легких, на фоне общих тяжелых заболеваний, патологии желудочно-кишечного тракта (рефлюкс-эзофагит, грыжа пищеводного отверстия диафрагмы) – это тоже одна из причин фибрилляции предсердий, или мерцательной аритмии.
Фибрилляция предсердий: что делать, как лечить?
Диагностика мерцательной аритмии (фибрилляции предсердий) основывается на записи электрокардиограммы (ЭКГ). Иногда фибрилляция предсердий протекает бессимптомно и выявляется случайно, например, когда ЭКГ записывают при проф. осмотре или во время стационарного лечения по поводу другого заболевания. Однако чаще всего пациент обращается к врачу с жалобами на перебои в работе сердца, приступы учащенного неровного сердцебиения, которые могут сопровождаться слабостью, одышкой, потливостью, головокружением, чувством «внутренней дрожи», болями в области сердца и снижением артериального давления. Когда приступ случается внезапно, следует обязательно обратиться к врачу или вызвать бригаду «скорой помощи». Очень важно, чтобы запись ЭКГ была сделана именно в время приступа – врач сможет точно определить характер аритмии, поставить диагноз и назначить правильное лечение.
Если приступы случаются достаточно часто, но их не удается «поймать» на обычной ЭКГ, пациента направляют на суточное мониторирование ЭКГ (холтер, холтеровское мониторирование). В течение 24 часов (и более, в зависимости от аппарата) регистрируется ЭКГ больного и в электронном виде записывается специальным прибором размером с ладонь, который пациент носит с собой. Запись обрабатывается на компьютере, и если за время проведения обследования у пациента случались приступы аритмии, они будут зафиксированы и документально подтверждены. Врач получит всю необходимую информацию.
Может случиться, что во время проведения холтеровского мониторирования приступ не возникнет. Потребуется повторное исследование, и так до тех пор, пока аритмию не «поймают». Если приступы случаются редко, это сделать очень сложно. В таких случаях врач может рекомендовать исследование, позволяющее спровоцировать появление приступа – чреспищеводную стимуляцию предсердий (ЧПСП). При проведении ЧПСП через нос пациента в пищевод вводится тонкий электрод, который устанавливается на уровне предсердий и с помощью специального прибора позволяет наносить на сердце электрические импульсы. При возникновении пароксизма ФП проводится запись ЭКГ, затем синусовый ритм восстанавливается. ЧПСП проводится только в стационаре, в специальных отделениях, специализирующихся на лечении нарушений сердечного ритма.
Пароксизм фибрилляции предсердий – что делать?
Если приступ неровного учащенного сердцебиения возник у вас впервые, необходимо сразу же обратиться к врачу или вызвать бригаду «скорой помощи». Даже если вы хорошо себя чувствуете. Помните – очень важно зафиксировать приступ на ЭКГ. Приступ может закончиться самостоятельно через некоторое время, но восстанавливать правильный ритм необходимо в течение первых двух суток. Чем больше времени пройдет от начала пароксизма, тем сложнее сердцу восстановить нормальную работу и выше риск образования тромбов в камерах сердца. Если от начала приступа прошло больше двух суток или вы точно не знаете время его возникновения, восстанавливать сердечный ритм необходимо только под наблюдением врача после обследования камер сердца на эхокардиографии, ЭхоКГ (для исключения уже сформировавшихся тромбов) и специальной подготовки препаратами, разжижающими кровь (для предотвращения тромбообразования).
Если пароксизмы мерцательной аритмии (фибрилляции предсердий) возникают часто, необходимо вместе с врачом разработать план ваших действий во время приступа. При хорошей переносимости аритмии и при коротких (не более 24 часов) приступах аритмии, которые часто заканчиваются самостоятельно, можно не предпринимать специальных действий. Необходимо продолжать прием препаратов, рекомендованных врачом, не изменяя дозы. Ваш врач может рекомендовать при возникновении приступа разовый прием антиаритмического препарата в дополнение к базовой терапии или временное увеличение дозы уже принимаемых медикаментов. Если во время пароксизма фибрилляции предсердий самочувствие значительно ухудшается, или аритмия продолжается больше суток, обращение к врачу обязательно.
Что «лучше» – приступы или постоянная мерцательная аритмия (фибрилляция предсердий)?
Долгое время врачи считали, что единственным оптимальным результатом лечения является восстановление правильного, синусового ритма. И сейчас в большинстве случаев врач посоветует вам всеми способами восстанавливать и удерживать синусовый ритм. Однако не во всех случаях. Исследования показали, что в случае невозможности эффективного сохранения восстановленного синусового ритма (когда сердце постоянно «срывается» в фибрилляцию предсердий), постоянная фибрилляция предсердий (мерцательная аритмия) с медикаментозным контролем частоты сердечных сокращений около 60 ударов в минуту – безопаснее, чем частые пароксизмы мерцательной аритмии (особенно затяжные, требующие введения высоких доз антиаритмических препаратов или проведения электроимпульсной терапии).
Решение о целесообразности восстановления синусового ритма или сохранения постоянной формы фибрилляции предсердий принимает врач. В каждом случае такое решение индивидуально и зависит от причины развития аритмии, заболевания, на фоне которого она возникла, от ее переносимости и эффективности проводимого для удержания правильного ритма лечения мерцательной аритмии.
Затянувшийся более двух суток приступ необходимо лечить только под наблюдением врача, после специальной подготовки. В случае удачного восстановления синусового ритма врач проведет коррекцию постоянной антиаритмической терапии и посоветует прием препаратов, разжижающих кровь, как минимум в течение месяца после кардиоверсии.
Лечение фибрилляции предсердий (мерцательной аритмии)
Существует несколько способов лечения фибрилляции предсердий (мерцательной аритмии) – восстановления синусового ритма. Это прием антиаритмических препаратов внутрь, введение антиаритмических препаратов внутривенно и кардиоверсия (электроимпульсная терапия, ЭИТ). Если восстановление ритма врач проводит в поликлинике или на дому у пациента, чаще всего начинают с внутривенных препаратов, затем – прием таблеток. Процедура проводится под контролем ЭКГ, врач наблюдает пациента 1-2 часа. Если восстановления синусового ритма не произошло, пациента госпитализируют в стационар. В стационаре также могут вводить препараты внутривенно, но если время ограничено (длительность приступа приближается к концу вторых суток) или пациент плохо переносит пароксизм (наблюдается снижение АД, т.д.), чаще применяется ЭИТ.
Кардиоверсия проводится под внутривенным наркозом, поэтому электрический разряд безболезненный для пациента. Успешность восстановления ритма зависит от многих факторов: длительность приступа, размеры полостей сердца (в частности, левого предсердия), достаточное насыщение организма антиаритмическим препаратом), и т.д. Эффективность ЭИТ приближается к 90-95%.
Если пароксизм фибрилляции предсердий длится более двух суток, восстанавливать ритм возможно только после специальной подготовки. Основные этапы – это прием препаратов, разжижающих кровь, под контролем специального анализа (МНО) и проведение чреспищеводной эхокардиографии (ЧПЭхоКГ) перед ЭИТ для исключения тромбов в полостях сердца.
Приступы мерцательной аритмии – как предотвратить?
Для того чтобы пароксизмы мерцательной аритмии не возобновлялись, пациент должен постоянно принимать антиаритмический препарат. С целью профилактики. На сегодняшний день существует немало антиаритмиков, выбор препарата должен сделать врач. Пациенту с мерцательной аритмией необходимо наблюдение кардиолога, при котором проводится регулярное обследование (например, ЭхоКГ раз в год, или суточное холтеровское мониторирование при необходимости, для оценки эффективности лечения), коррекция лечения. Подбор медикаментозной терапии всегда, при любом заболевании, очень кропотливое занятие, которое требует грамотности и упорства со стороны врача и понимания и исполнительности со стороны пациента. Индивидуальной может быть не только эффективность, но и переносимость лечения.
Неэффективность медикаментозной терапии фибрилляции предсердий может быть показанием к хирургическому лечению. В левом предсердии (около впадения легочных вен) располагаются зоны, в которых формируются электрические импульсы, способные запускать фибрилляцию предсердий. Повышенная электрическая активность этих зон может быть выявлена с помощью специального электрофизиологического обследования (ЭФИ). Специальный катетер вводится в полость сердца, полученная информация позволяет составить электрическую «карту» и определить триггерные («пусковые») участки. Исследование проводится под местной анестезией и достаточно безопасно для больного. После определения «пусковых» участков проводится операция – радиочастотная аблация триггерных зон (РЧА). Катетер с помощью высокочастотного тока разрушает эти участки и нарушает запуск аритмии. В четырех случаях из пяти мерцательная аритмия больше не возобновляется. В анимированном виде процесс РЧА триггерных зон при фибрилляции предсердий представлен в ролике.
Фибрилляция предсердий стала постоянной
У определенной части пациентов, страдающих приступами фибрилляции предсердий, рано или поздно наступает время, когда восстановить синусовый ритм уже не удается. Мерцательная аритмия переходит в постоянную форму. Как правило, это случается у больных со значительно увеличенными размерами левого предсердия (4,5 см и более). Такое расширенное предсердие просто не в состоянии удерживать синусовый ритм. При постоянной форме пациенту также необходимо наблюдение врача.
Цели лечения – удержание частоты сердечных сокращений в пределах 60-70 ударов в минуту в состоянии покоя, профилактика образования тромбов в полостях сердца и снижение риска тромбоэмболических осложнений.
Контроль частоты сердечных сокращений проводят бета-блокаторами, дигоксином или антагонистами кальция (группа верапамила), подбирая индивидуальную дозу препарата по принципу «чем выше доза, тем реже ЧСС». На оптимальной дозе титрование заканчивают, и пациент получает ее ежедневно. Оценить эффективность контроля над ЧСС можно с помощью суточного холтеровского мониторирования ЭКГ. Если снижения частоты ритма не удается достичь таблетками, врачи прибегают к хирургическим методам. Хирург-аритмолог изолирует предсердия от желудочков и имплантирует электрокардиостимулятор, который программируется на определенное число сердечных сокращений в покое и адаптируется к нагрузкам.
Для предотвращения тромбообразования применяют препараты, «разжижающие» кровь, то есть замедляющие процессы свертывания крови. С этой целью используют аспирин и антикоагулянты (чаще всего варфарин). На сегодняшний день подход к тактике антикоагулянтной терапии определен на основании оценки риска тромбоэмболических осложнений и риска кровотечений на фоне приема этих препаратов, и утвержден в Национальных Российских рекомендациях ВНОК.
Многие пациенты боятся начать прием препаратов, так как в инструкции указаны такие осложнения, как кровотечение. Вы должны знать, что перед назначением антикоагулянтов врач всегда взвешивает пользу и риск лечения препаратом, и назначает только тогда, когда полностью уверен, что польза значительно превышает риск. Четкое соблюдение рекомендаций и регулярный контроль анализов крови (международное нормализованное отношение (МНО) для пациентов, получающих варфарин) плюс Ваша информированность об основных механизмах действия препарата и тактике Ваших действий при первых признаках кровоточивости делают такое лечение полностью предсказуемым и максимально безопасным.
Предварительно анализируются данные компьютерной томографии. Для доступа производится пункция и катетеризация бедренной вены. По проводнику инструменты проводят в правое предсердие, после выполнения позиционирования производится пункция межпредсердной перегородки и через этот прокол проводник попадает в левое предсердие. Затем производится выбор места имплантации и подбор размера окклюдера. Окклюдер устанавливается в устье ушка левого предсердия, прекращая кровоток в нем и, таким образом, исключается появление тромбов в этом анатомическом образовании. В Красноярске такие операции выполняются в Краевой клинической больнице.
Кардиологи «Центра Современной Кардиологии» обладают не только всеми современными функциональными и лабораторными методами диагностики заболеваний, вызывающих фибрилляцию предсердий, но и огромным опытом диагностики и лечения различных форм мерцательной аритмии.
Дилатация левого предсердия что это такое и как
Предполагается, что в развитии ФП участвуют два основных механизма, которые могут сосуществовать изолированно и одновременно: 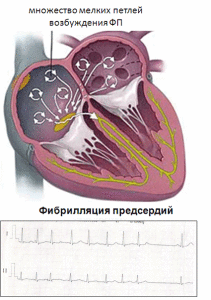
1. Наличие одного или нескольких фокусов с быстрой импульсацией. (Фокус – участок миокарда, способный инициировать аритмию.) Фокусы чаще всего расположены в области верхних легочных вен, впадающих в левое предсердие. Также фокусы встречаются в области мышечных муфт легочных вен, в правом предсердии и редко в верхней полой вене или венечном синусе, а также в связке Маршала.
Дилатация (расширение) легочных вен – один из важных анатомических факторов возникновения ФП.
2. Наличие одной или множества мелких волн (петлей) возбуждения по типу re-entry (ре-ентри – повторный вход возбуждения). В отличие от других аритмий, при которых обычно определяется одна петля re-entry, в основе ФП могут участвовать несколько петель, поскольку рассеивание фронта волн по мере их продвижения по предсердиям приводит к возникновению самоподдерживающихся “дочерних волн”.
Электрическое ремоделирование предсердий. Если длительность ФП составляет менее 24 часов, то восстановление синусового ритма, как правило, завершается успешно, тогда как большая длительность ФП снижает вероятность восстановления и поддержания синусового ритма. Эти наблюдения дали основание для появления крылатого выражения “фибрилляция предсердий порождает фибрилляцию предсердий”. Повышенная склонность к ФП связана с постепенным укорочением эффективного рефрактерного периода по мере увеличения продолжительности приступа. Такое явление получило название “электрическое ремоделирование”.
Атриовентрикулярное проведение. Предсердно-желудочковый узел ограничивает проведение импульса при ФП (в отсутствие дополнительного проводящего пути). Частота сокращений желудочков при ФП зависит от свойств узла, а также воздействующих на него лекарственных препаратов и активность симпатической и парасимпатической нервной системы.
Предрасполагающие к ФП клинические состояния
ФП ассоциирована с целым рядом сердечно-сосудистых состояний, которые могут поддерживать аритмию.
Артериальная гипертензия – наиболее частое фоновое состояние у пациентов с ФП; обнаруживается примерно у 2/3 всех пациентов с ФП по данным различных обследований. Недостаточный контроль АД – фактор риска возникновения (первого обнаружения) ФП у пациентов с гипертензией и фактор риска осложнений ФП: инсульта и системных тромбоэмболий, даже у пациентов на антикоагулянтной терапии.
Хроническая сердечная недостаточность, определенная как СН с одышкой при физической нагрузке (II-IV ФК по HYHA), выявляется у 30% пациентов с ФП. В свою очередь, ФП обнаруживается у 5-50% пациентов с СН. Распространенность ФП увеличивается при клиническом прогрессировании ХСН: у пациентов с ХСН IV ФК по NYHA ФП выявляется почти в 50% случаев.
Клапанная патология сердца, особенно пороки митрального клапана (стеноз и недостаточнсть), которые вызывают перегрузку ЛП давлением или объемом и, таким образом, провоцируют ФП.
Кардиомиопатии (гипертрофическая, дилатационная, правожелудочковая), включая первичные электрические болезни сердца (синдром удлиненного интервала Q-T, укороченного интервала Q-T, синдром Бругада и катехоламинэргическая ЖТ), привносят высокий индивидуальный риск развития ФП.
Врожденный порок сердца (ВПС), дефект межпредсердной перегородки (ДМПП) по данным исследований ассоциированы с ФП у 10-15% пациентов.
Другие врожденные пороки сердца часто связаны с ФП. Пациенты с одиночным желудочком, пациенты после перенесенной операции восстановления предсердий (операция Мастерда) при транспозиции магистральных артерий или после операции Фонтена имеют повышенный риск развития ФП. Измененная анатомия предсердий вследствие первичных нарушений, хирургической операции или по причине последующих гемодинамических нарушений может быть одним из главных предрасполагающих факторов развития ФП. У таких пациентов ФП может иметь выраженные симптомы и зачастую трудна для лечения.
ИБС представлена в 20% случаев среди пациентов с ФП. Предрасполагает ли ИБС сама по себе к возникновению ФП – неизвестно. Но необходимо принимать во внимание, что ФП при ИБС может быть обусловлена ХСН после перенесенного инфаркта миокарда (ИМ), артериальная гипертензия. ФП редко встречается у пациентов со стабильным течением ИБС и сохраненной функцией ЛЖ, но ее наличие указывает на плохой прогноз после перенесенного ИМ.
Нарушение функции щитовидной железы – важная причина возникновения ФП. В исследованиях показана взаимосвязь ФП, как при гипо- и гиперфункции щитовидной железы, так и при субклинических гипертиреозах. Концентрация Т4 свободного была независимо ассоциирована с ФП.
Ожирение выявляют у 25% пациентов с ФП. По результатам метаанализа популяционных когортных исследований, лица с ожирением имеют на 49% выше риск развития ФП по сравнению с лицами без ожирения. Среди других факторов ожирение ассоциировано с артериальной гипертензией, сонным апноэ, ХОБЛ и сахарным диабетом. Ожирение служит наиболее вероятным маркером сердечно-сосудистого риска, связанным, помимо прочего, с ФП.
У многих пациентов с метаболическим синдромом развивается ФП, с другой стороны, данная связь зависит от состояний, предрасполагающих к ФП (артериальная гипертензия, ожирение).
Ночное апноэ ассоциировано с повышением внутрипредсердного давления и дилатацией и может предрасполагать к развитию ФП.
Высокий рост ассоциирован с ФП. Механизм данного явления неясен, но предполагается, что вклад в развитие аритмии могут вносить механическое растяжение легочных вен (ЛВ) и дилатация ЛП.
Хроническая обструктивная болезнь легких (ХОБЛ) выявляется у 10-15% пациентов с ФП. У некоторых пациентов заболевание легких может быть в большей степени маркером сердечно-сосудистого риска в целом, чем специфическим фактором, предрасполагающим к ФП. Рак бронха может также протекать с ФП.
Хроническая почечная недостаточность (ХПН) представлены у 10-15% пациентов с ФП. ХПН может повышать риск осложнений, связанных с ФП, особенно сердечно-сосудистых осложнений. ХПН, сахарный диабет и ХОБЛ встречаются еще чаще у пациентов с постоянной ФП.
Последствия ФП
Гемодинамические последствия ФП. При ФП на гемодинамику могут влиять 3 фактора: отсутствие синхронности сокращений предсердий, беспорядочность ответа желудочков и чрезмерно высокая частота сердечных сокращений. В связи с ухудшением сократительной функции предсердий может наблюдаться значительное снижение сердечного выброса, особенно у больных со снижением диастолического наполнения желудочков, артериальной гипертензией, митральным стенозом, гипертрофической или рестриктивной кардиомиопатией. Помимо влияния на функцию предсердий, постоянно ускоренная частота желудочковых сокращений при ФП может вызывать дилатационную кардиомиопатию (аритмогенная кардиомиопатия, вызванная тахикардией).
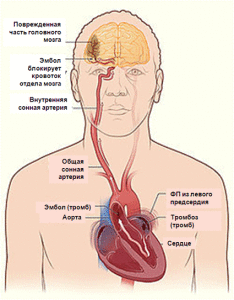
Тромбоэмболические последствия ФП. Инсульт – наиболее ужасающее последствие ФП. Примерно каждый 5-6-й инсульт возникает вследствие ФП. Основным источником инвалидизирующих ишемических инсультов кардиоэмболической этиологии у пациентов с ФП считаются тромбы, формирующиеся в ушке левого предсердия в результате застоя крови. До 25% инсультов, связанных с ФП, могут быть последствиями уже существующих цереброваскулярных заболеваний и развиваться за счет тромбоэмболий из других сердечных источников или атеросклеротических бляшек аорты.
Качество жизни. По имеющимся данным качество жизни пациентов с ФП существенно хуже, чем у лиц из той же возрастной группы, не страдающих ФП. Восстановление и поддержание синусового ритма ассоциируется с улучшением качества жизни и лучшей переносимостью нагрузки по данным некоторых исследований, но не всех. В типичных исследованиях большинство пациентов с пароксизмальной ФП считали, что аритмия нарушает их стиль жизни, но это ощущение не ассоциировалось ни с продолжительностью, ни с частотой приступов, сопровождавшихся клиническими проявлениями.


