Дистресс плода что это
Дистресс плода-как контролируется ваш ребенок во время родов?
Иногда в последний момент беременности случаются неприятные вещи,которые могут оказаться очень печальными. Дистресс плода, является одним из таких осложнений, которое, если не будет решаться, может привести к проблемам как для матери, так и для ребенка.
Дистресс плода
Дистресс плода подразделяется на внутриутробный, и возникающий при родах. Дистресс, как правило, определяется путем мониторинга сердечного ритма ребенка. Наличие мекония (первого стула ребенка) может также указывать на недомогание плода в утробе матери.
Дистресс плода часто заменяют термином гипоксия или угроза асфиксии, это происходит когда младенец не получает достаточно кислорода в утробе матери или во время родов.
Для мониторинга, врачи также могут использовать устройство которое прикладывается к коже головы ребенка.
Каким должен быть идеальный сердечный ритм плода?
Результаты электронного фетального монитора показаны на мониторе в диаграммной форме. Врач и медсестры постоянно отслеживают цифры на графиках и проверяют, находится ли частота сердечных сокращений в пределах адекватных параметров. Идеальный диапазон должен составлять от 110 до 160 ударов в минуту.
Слишком высокая температура может указывать на то, что ребенок находится в плохом положении или лихорадке. В то время как слишком низкая температура «говорит» о недостатке кислорода. Мониторинг подразделяет показания на 2-е категории: ускоренное сердцебиение и замедленное.
Ускоренное сердцебиение
Это означает кратковременное повышение частоты сердечных сокращений, скажем, 15 ударов в минуту, которые могут длиться 15 секунд или более. Ускоренное, вполне нормально, оно говорит о достатке кислорода. У большинства младенцев в течение всего процесса рождения сердцебиение может ускоряться несколько раз.
Если у врача возникаю какие-либо подозрения о ухудшенном состоянии плода, он может вызвать увеличения сердцебиения плода. Подозрение могут возникнуть в результате:
Перед родами, обязательно проконсультируйтесь с ваши врачом, задайте ему все необходимые и интересующие вас вопросы. Получите вашу медицинскую карту. И вперед на роды.
И помните, бдительность-это Ключ к успешному рождению вашего малыша.
Что такое антенатальная гибель плода? Причины возникновения, диагностику и методы лечения разберем в статье доктора Кондратенко Юлии Николаевны, гинеколога со стажем в 16 лет.
Определение болезни. Причины заболевания
Опосредованные причины антенатальной гибели плода :
Инфекция может быть вирусной (цитомегаловирусы, вирусы простого герпеса, краснухи, Коксаки, ВИЧ), бактериальной (хламидии, микоплазмы, уреаплазмы, стрептококки группы В, энтеробактерии, кишечная палочка) и грибковой (кандидоз).
Симптомы антенатальной гибели плода
В течение первых трёх дней гибели малыша пациентка может обратить внимание на изменения своего состояния:
Если с момента гибели плода в утробе матери прошло несколько недель, могут присоединяться признаки воспалительной реакции:
Патогенез антенатальной гибели плода
Суть патогенеза заключается в нарушении функции плаценты, развитии хронической плацентарной недостаточности, нарушении кровоснабжения плода, его росте и развитии. Поражаются внутренние органы плода — развивается внутриутробная пневмония, менингит и др. В какой-то момент происходит нарушение нормального функционирования плаценты, развивается острая плацентарная недостаточность и плод погибает.
Профессором И. В. Бариновой в 2015 году были представлены два типа плодовых потерь при внутриутробной гипоксии. Каждому из них характерно своеобразное сочетание патогенетических факторов, связанных с матерью, плацентой и плодом.
Патогенез второго типа обусловлен нарушением циркуляции в плодовой части плаценты, незрелостью ворсин относительно срока беременности, а также васкулопатией сосудов плода и тромбозом ворсин.
Классификация и стадии развития антенатальной гибели плода
Пока не существует общепринятой классификации внутриутробной гибели плода. Однако изучение причин перинатальной смертности привело к появлению двух понятий:
Осложнения антенатальной гибели плода
При своевременном обращении к доктору антенатальная гибель плода не приводит к осложнениям. Если же пациентка обратилась за медицинской помощью спустя больше двух недель после смерти ребёнка, то у неё с большой вероятностью могут развиваться такие осложнения, как:
Чтобы избежать их, необходимо тщательно наблюдать за состоянием пациентки и выполнять профилактические мероприятия:
Диагностика антенатальной гибели плода
После того как женщина обращается к врачу с жалобами на недомогание и отсутствие шевеления плода, врач направляет пациентку на диагностическое обследование. Оно позволяет поставить точный диагноз.
Постановка диагноза внутриутробной гибели плода включает следующие этапы обследования:
Анализы для диагностики внутриутробной гибели плода на позднем сроке беременности не так важны. Отсутствия шевелений плода в течение нескольких дней и сердцебиения по данным УЗИ достаточно для правильной постановки диагноза.
Лечение антенатальной гибели плода
При подтверждённом диагнозе антенатальной гибели плода показана экстренная госпитализация и принятие решения о методе и сроке родоразрешения. Чем меньше интервал между установленным диагнозом и родоразрешением, тем меньше риск возникновения осложнений во время и после родов.
Выбор метода определяется индивидуально, на основании клинических данных и особенностей акушерской ситуации. Оптимальным вариантом родоразрешения при антенатальной гибели плода являются роды через родовые пути. Но иногда выполняется кесарево сечение, например при раннем отделении плаценты от стенок матки, обильном или продолжающемся кровотечении из половых путей.
При родоразрешении беременных с антенатальной гибелью плода, осложнившейся септическим состоянием, показано экстренное оперативное вмешательство. Объём операции решается индивидуально, возможна удаление матки с плодом (экстирпация).
После родов важно тщательно наблюдать за состоянием роженицы, провести профилактику послеродового кровотечения и гнойно-септических осложнений. Необходимо обратить внимание на выделения из половых путей (гнойные или кровянистые ), температуру тела, появление озноба, слабости, тянущих болей внизу живота.
Прогноз. Профилактика
Потеря беременности является показанием к проведению медицинской, психологической и социальной реабилитации пациенток. Необходим полный комплекс диагностических исследований для выяснения причины гибели плода. Выбор алгоритма обследования базируется на данных анамнеза, особенностях течения беременности и результатах патологоанатомического исследования плода и последа.
При неустановленной причине гибели плода в анамнезе необходимо учитывать данный факт при выработке тактики родоразрешения последующих беременностей.
Профилактика антенатальной гибели плода предполагает:
Дистресс плода что это
Сотрудниками Перинатального центра Воронежской области «Воронежская областная клиническая больница № 1» и «Воронежского государственного медицинского университета имени Н.Н. Бурденко» было проведено исследование на тему использования оценки лицевых движений плода в качестве дополнительного критерия развития возможного дистресса. Данное исследование является одним из перспективных направлений в современной неонатологии, что связано с тем фактом, что плоды с 20–22-й по 28-ю неделю гестации являются уязвимой группой по развитию дистрессовых состояний ввиду невозможности использования у них кардиотокографии (КТГ).
Исторически термин «дистресс» в акушерстве и неонатологии использовался для описания случаев, когда плод не получал достаточного количества кислорода во время беременности или родов. Особое внимание к данному состоянию в современной практике врачей не случайно: оно связано с последствиями и физиологическими перестройками внутри организма плода, которые могут привести к негативным последствиям.
Известно, что при снижении уровня кислорода плод испытывает 3 стадии: преходящую гипоксию без метаболического ацидоза, тканевую гипоксию с риском метаболического ацидоза и гипоксию с развившимся метаболическим ацидозом. Все эти реакции на кислородную недостаточность регулируются автономной нервной системой, опосредованной каскадными парасимпатическими и симпатическими механизмами. Компенсаторные механизмы, направленные на поддержание плода во время родов, к сожалению, не могут помочь в случае длительной непрерывной гипоксии плода.
Таким образом, последнее состояние приводит к снижению частоты сердечных сокращений, перераспределению сердечного выброса преимущественно перфузирующим органам, таким как сердце, мозг и надпочечники, и переходу к анаэробному клеточному метаболизму. Все эти каскадные реакции связаны со значительной перинатальной заболеваемостью и смертностью, при этом особое внимание уделяется краткосрочным и долгосрочным осложнениям, включая энцефалопатию, судороги, церебральный паралич и нарушения психоречевого и моторного развития.
Тот факт, что частота сердечных сокращений плода заметно изменяется в ответ на длительную кислородную недостаточность, делал мониторинг данного параметра ценным и широко используемым инструментом для диагностики дистресса плода в течение многих лет. С развитием методов диагностики и новейших подходов перед врачами разных специальностей открылись новые возможности ранней диагностики фетального дистресса, к которым относится кардиотокография (КТГ), что существенно увеличило раннюю диагностику и своевременную коррекцию данного состояния.
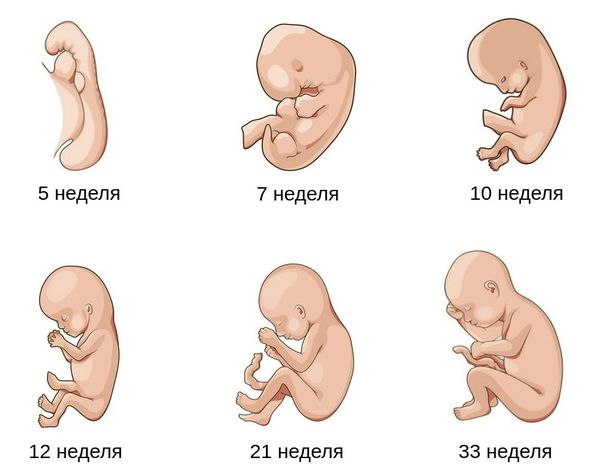
Несмотря на то что КТГ является «золотым стандартом» в диагностике дистресса у плода во внутриутробном периоде, использование данного метода ограничено гестационным возраст ом исследуемых: плоды с 20–22-й по 28-ю неделю гестации являются уязвимой группой по угрозе развития дистрессовых состояний вследствие невозможности применения у них метода КТГ. Учитывая данный факт, одним из перспективнейших и развивающихся направлений в ранней диагностике дистресса плода можно смело считать оценку лицевых моделей поведения, что имеет под собой анатомические и пренатальные обоснования. Доказано, что лицо плода опосредует собой реакции мозга на изменения, касающиеся центральной нервной системы и организма в целом. Лицевой и тройничный нервы, иннервирующие мышцы мимики лица, появляются на сроке 10–11 нед гестации, а иннервируемые мышцы – к 16-й неделе. Несмотря на раннее появление нервов и иннервируемых ими мышц в онтогенезе, полная оценка их совместной неврологической деятельности во внутриутробном периоде разумна только с 22–24-й недели гестации, что связано с развитием жировой ткани на лице плода, которое продолжается вплоть до 36-й недели беременности. Таким образом, использование оценки лицевых движений плода в качестве дополнительного критерия развития возможного дистресса является одним из перспективных направлений в современных неонатологии, акушерстве и гинекологии.
В исследование были включены 313 плодов в сроке гестации не менее 22–24 нед проходивших консультацию и УЗ-диагностику на базе БУЗ ВО «Воронежская областная клиническая больница № 1 “Перинатальный центр”» с 2017 по 2019 г.
Исследователями было получено добровольное информированное согласие на участие в исследовании у законных представителей. Все исследуемые плоды были разделены на 2 группы: 1-я группа – с диагностированными случаями дистресса в акушерском анамнезе (n=98), 2-я группа – с отсутствием клинических признаков дистресса (n=215). Для верификации диагноза дистресса КТГ проводили с 32-й недели гестации всем исследуемым. КТГ оценивали согласно критериям FIGO (2015): базальная частота сердечных сокращений (ЧСС) плода, вариабельность базального ритма и децелерации. В соответствие с полученными результатами лента КТГ расценивалась специалистом как нормальная, подозрительная или патологическая.
Основными критериями включения плодов в 1-ю группу исследования являлось наличие одного или нескольких критериев, согласно данным КТГ: тахикардия/брадикардия; стойкая монотонность ритма (генерация записи 5 уд/мин и меньше); ранние, вариабельные и поздние децелерации с амплитудой >30 уд/мин. Допплерометрия проводилась с 24-й недели гестации всем плодам, принимавшим участие в исследовании. В качестве проявлений дистресса специалисты рассматривали следующие параметры: снижение скорости в диастолу (ниже нормативных показателей), повышение пульсационного индекса в маточной артерии, регистрация дикротической выемки (в одной/обеих маточных артериях). Все плоды, имеющие клинические признаки дистресса согласно вышеперечисленным критериям, сразу после проведения КТГ и допплерометрии были обследованы с помощью аппарата УЗ-диагностики, при проведении которой с разрешения законных представителей получено согласие на фото- и видеофиксацию материалов. При проведении УЗ-диагностики использовали аппарат GE Healthcare Voluson 730 и брюшной датчик 5 МГц. Критерием выбора данного аппарата в исследовании являлась его техническая возможность съемки от 15 до 24 фотограмм в секунду (в зависимости от заданного диапазона углов). При исследовании минимальных мимических единиц на GE Healthcare Voluson 730 датчик был расположен специалистом таким образом, чтобы на экран выводилась сагиттальная часть лица плода, включающая лоб, нос и рот – это было необходимо для оценки анализа поведения плода. Окончательная верификация диагноза основывалась на оценке по шкале Апгар на 1-й и 5-й минутах жизни (баллы) и среднем уровне лактата (ммоль/л).
Подходя к оценке дистресса у плодов и новорожденных, стоит понимать, что данное состояние охватывает не только физическую, но и психологическую стороны боли и страдания, что неоднократно подтверждено исследованиями.
При оценке лицевых движений плодов сложность ранней диагностики неразрывно связана с тем, что выражения лица и минимальные мимические единицы не всегда могут соответствовать стереотипным выражениям отрицательных эмоций, представляя собой группу лицевых конфигураций, которые довольно многообразны и изменчивы по своей морфологии.
Cогласно исследованиям, корковые зоны у недоношенных детей активируются болевыми раздражителями и различаются при сравнении ответов на внутриутробные раздражения. Термин «боль/дистресс гештальт» применим к эмоциональным выражениям, которые становятся координированными со временем в ответ на дистрессовые состояния по мере «созревания» ноцицептивной нервной системы, что нашло отражение в зарубежных исследованиях.
В ходе исследования особое внимание было уделено не наличию отдельных известных лицевых движений плода, а их последовательной совокупности, где важными диагностическим (и в последующем прогностическим) признаком являлись опускание брови, поднятие внутренней и внешней части брови и сближение внутренних углов бровей. Данная последовательность в момент дистресса была оценена нами как фундаментальная комбинация действий на лице плода.
Выделение нами опускания брови как пускового и обязательного предиктора возможного дистресса неслучайно: данное лицевое движение отдельно (или в сочетании с другими известными двигательными лицевыми единицами) является обязательным компонентом отрицательных эмоций у детей и никогда не встречается при положительных эмоциях.
В дополнение к опусканию брови (при вовлечении musculus procerus, musculus depressor supercilii и musculus corrugator supercilii) нами были оценены и детально проанализированы другие паттерны лица, которые связаны с негативной эмоциональной реакцией у новорожденных, следующей друг за другом: поднятие внутренней части брови (при вовлечении медиальной части musculus epicranius), поднятие внешней части брови (при вовлечении латеральной части musculus epicranius) и сближение внутренних углов бровей.
Для подтверждения достоверности наличия выделенных лицевых движений у плодов в состоянии дистресс-синдрома была оценена встречаемость последовательности мимических единиц у плодов в сроке гестации от 28 до 37 нед с наличием подтвержденного дистресс-синдрома и без него по данным КТГ. КТГ проводилась всем исследуемым в непрерывном режиме при участии специалиста, владеющего данной процедурой. При оценке комбинации действий на лице плодов, имеющих подтвержденный дистресс-синдром, было выявлено, что отдельно такая лицевая двигательная единица, как опускание брови, встречалась в 98,9% случаев, поднятие внутренней части брови – в 96,9%, поднятие внешней части брови – в 96,9%, сближение внутренних углов бровей – в 97,9%. Комбинация 4 представленных показателей в единицу времени встречалась в 96,9% у плодов с подтвержденным дистресс-синдромом по данным КТГ. При анализе оценки по шкале Апгар на 1-й и 5-й минутах жизни было выявлено, что в группе обследуемых с диагностированным дистрессом средние значения составляли на 1-й минуте 4,06±0,59 балла, на 5-й минуте 5,78±0,47 балла, средний уровень лактата – 6,3±1,7 ммоль/л (рН 7,28–7,23, ВЕ –10–5,6). При оценке комбинации действий на лице плодов, не имеющих подтвержденного дистресс-синдрома, было выявлено, что отдельно такая лицевая двигательная единица, как опускание брови, встречалась в 2,3% случаев, поднятие внутренней части брови – в 1,39%, поднятие внешней части брови – в 1,39%, сближение внутренних углов бровей – в 2,79%. Комбинация 4 представленных показателей в единицу времени не встречалась ни у одного из плодов, не имеющих дистресс-синдром по данным КТГ.
Полученные сравнительные данные демонстрируют тот факт, что развивающееся направление «чтение эмоций» перспективно в ранней диагностике дистресса плода и может быть использовано для применения в уязвимой группе плодов с 20–22-й по 28-ю неделю гестации. Авторы понимают, что оценка лицевых движений плода, позволяющих выявить дистрессовое состояние, требует дальнейшего изучения и исследований в данной области.
Коротаева Н.В., Ипполитова Л.И., Федотова Т.В., Чибисова Н.А., Першина Е.С.
Журнал для непрерывного медицинского образования врачей. Неонатология: новости, мнения, обучение. Том 8, № 2, 2020
Перинатальные и отдаленные исходы у детей с синдромом задержки роста плода
В. Е. Радзинский, А. А. Оразмурадов, Е. А. Девятова
Кафедра акушерства и гинекологии с курсом перинатологии Российского Университета Дружбы Народов
ул. Миклухо – Маклая, 8, Медицинский факультет, 117198, Москва, Россия
Т. В. Златовратская, Н. М. Старцева
ГБУЗ «Городская клиническая больница № 29 им. Н.Э. Баумана» ДЗМ
Госпитальная площадь, д. 2, 111020 Москва, Россия
Актуальность: в статье представлен широкий обзор литературы по проблеме хронической плацентарной недостаточности (ПН), и освещены взгляды, сложившихся на рубеже XX–XXI веков. ПН остается одной из наиболее актуальных проблем современного акушерства и перинатологии, так как перинатальная заболеваемость и смертность в большой мере определяются степенью тяжести ПН, а малый вес при рождении – фактор риска повышенной заболеваемости на протяжении всей последующей жизни ребенка и формирует перинатальную заболеваемость и смертность.
Перинатальные поражения центральной нервной системы приводят к возникновению неврологических осложнений различной степени тяжести, что существенно ухудшает качество жизни таких детей.
При изучении отдаленных исходов у детей с синдромом задержки роста плода (ЗРП) в анамнезе обращает на себя внимание не только большой удельный вес неврологических осложнений, но и высокая частота болезней органов дыхания и болезней крови.
Хроническая ПН остаётся ключевой проблемой акушерства, неонатологии, патологии анте- и перинатального периодов, поскольку функциональная недостаточность плаценты приводит к угрозе прерывания беременности, гипоксии, отставанию роста и развития плода, либо к его гибели ( Савельева Г. М., 1991; Бунин А. Т., 1993; Башмакова Н. В. и др., 1996; Макаров И. О., 1998; Радзинский В. Е., Милованов А. П. и др., 2004). Плацентарная недостаточность – это клинический синдром, отражающий патологическое состояние материнской (маточно – плацентарной) и плодной (плацентарно – плодной) частей плаценты, приводящее к замедлению развития и роста плода (Савельева Г. М. и др., 1991). Милованов А. П., (1999) предложил определение ПН: это клинико – морфологический симптомокомплекс, возникающий как результат сочетанной реакции плода и плаценты на различные нарушения состояния материнского организма. Клинически обоснована терминология и классификация ПН предложенная Радзинским В. Е. (1983, 2001): это поликаузальный синдром, возникающий как результат сочетанной реакции плода и плаценты на различные изменения в материнском организме, характеризующийся нарушением молекулярных, клеточных, тканевых и органных адаптационно – гомеостатических реакций фетоплацентарной системы и реализующийся в компенсированной, субкомпенсированной и декомпенсированной формах. Частота плацентарной недостаточности составляет 17 – 26%, не имеет тенденции к снижению и обусловливает до 47% перинатальных потерь (Колгушкина Т. Н., 2004). По данным Барашнева Ю. И. и др. (1997), частота ее колеблется от 3 – 4 % до 45 %, перинатальная заболеваемость достигает 700 %о, а смертность 24,2 – 177,4%о. По данным других исследователей, ПН составляет более 20% в структуре причин перинатальной смертности (Мурашко Л.Е., Бадоева Ф.С., Асымбекова Г.У., Павлович С.В., 1997).
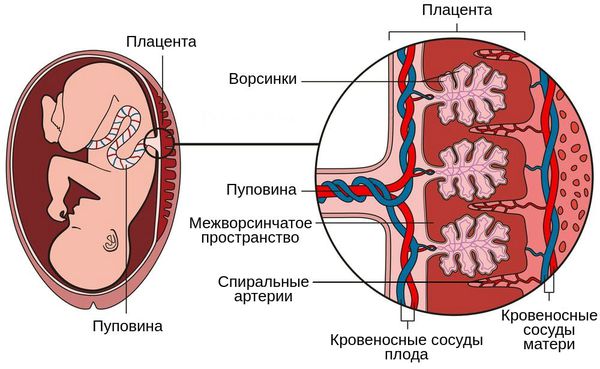
К основным звеньям многогранного патогенеза ПН относят нарушения маточно – плацентарного и плодово – плацентарного кровотока, метаболизма, синтетической функции и состояния клеточных мембран плаценты, изменения иммунного статуса плода. Патология маточно – плацентарного кровообращения в свою очередь характеризуется тремя важнейшими моментами: нарушением притока крови в межворсинчатое пространство, затруднением оттока из него и локальными изменениями реологических и коагуляционных свойств крови.
Функциональная недостаточность плаценты оказывает прямое отрицательное воздействие на развитие плода и новорожденного, что проявляется характерной клинической симптоматикой, в частности синдромом ЗРП, который занимает важное место в структуре перинатальной смертности и оказывает отрицательное влияние на последующее развитие ребенка. (Борзова Н. Ю., Гагаева Ю. В. и др., 2004). Синдром ЗРП – одно из наиболее часто встречающихся состояний новорожденного (Афанасьева Н. В., Игнатко И. В., 2003). В акушерской практике, по данным Медведева Н. В., Юдиной Е. В. (1998), данная патология встречается в 5 – 31 % случаев.
Учитывая важность своевременной профилактики и диагностики ПН, необходима адекватная оценка степени риска ее развития. По данным Сидельниковой В. М. (2002), хроническая ПН наблюдается у каждой третьей женщины из группы высокого перинатального риска. Легко оцениваемым фактором риска является возраст матери до 18 и старше 35 лет. По данным Стрижакова А. Н. (2003), у 26 – 30 % беременных в возрасте до 20 лет выявляются признаки ПН, что создает угрозу развития ЗРП у данной группы беременных. При наличии экстрагенитальной патологии риск развития ПН составляет 24 – 45%. Важная роль в формировании ПН отведена заболеваниям сердечно – сосудистой и эндокринной систем, а болезни почек составляют до 9,5% среди факторов риска ее развития. Среди эндокринных заболеваний особого внимания заслуживает сахарный диабет. Популяционная частота сахарного диабета у беременных составляет 0,2 – 3,0%, однако среди беременных с ПН он встречается в 2 – 3 раза чаще. При этом частота гипотрофии плода составляет 35,5%, а отставание в росте плода, по данным ряда исследователей, отмечается уже в начале II триместра гестации.
В последние годы все больше внимания уделяется изучению внутриутробного инфицирования как этиологического фактора развития ПН. Так, при хронических неспецифических заболеваниях легких отмечается увеличение процента рождения детей с низкими весо – ростовыми показателями. При этом у 30,8% детей выявляются признаки внутриутробной инфекции. У беременных с ПН на фоне генитальных инфекций в 1,6 раза чаще наблюдается ЗРП, при этом в 2 раза чаще возникает ее симметричная форма.
Среди осложнений беременности, наиболее часто приводящих к развитию ПН, первое место занимает гестоз. При наличии ПН на фоне гестоза, частота ЗРП составляет 22,7 – 44%. Частота клинических проявлений ПН прямо пропорциональна тяжести гестоза и составляет при легкой, среднетяжелой и тяжелой степени 16, 22 и 62% для ЗРП соответственно (Федорова М. В. и др., 1997).
Существенную роль в патогенезе плацентарной недостаточности играет неполноценное питание беременных, прежде всего недостаток белков, жиров, витаминов. При отсутствии рациональной диеты частота ЗРП может достигать 16,2%.
Из данных акушерского анамнеза статистически достоверную связь с развитием плацентарной недостаточности имеют перенесенные ранее самопроизвольные аборты, антенатальная гибель плода и рождение детей с низкой массой тела.
Ранняя диагностика ПН и профилактическое лечение беременных групп высокого риска по развитию синдрома ЗРП позволяет предупредить декомпенсированные формы маточно – плацентарной дисфункции и прогнозировать благополучный исход беременности с высокой степенью вероятности (Афанасьева Н. В., Стрижаков А. П., 2004).
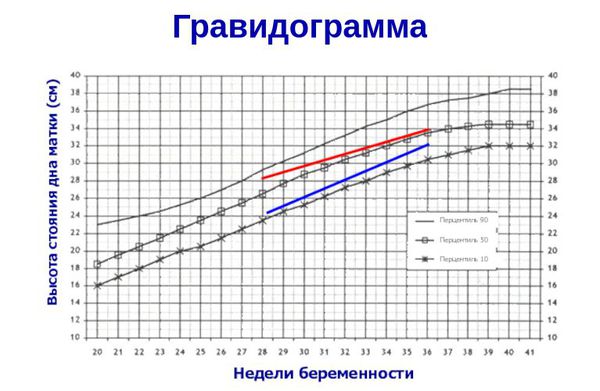
Выявление синдрома ЗРП и определение его формы является основной задачей эхографии при диагностике хронической ПН. ЗРП диагностируется при выявлении параметров фетометрии ниже 10 – го перцентиля или более чем на 2 стандартных отклонения ниже среднего значения для данного гестационного возраста. Некоторые исследователи допускают прогнозирование развития ЗРП по отклонению фетометрических показателей ниже 25 – го перцентиля (Федорова и др., 2001). Однако в этом случае вероятность подтверждения прогноза составляет только 70%.
При ультразвуковой (УЗИ) диагностике ЗРП, говоря о I степени тяжести, наблюдается отставание фетометрических параметров до 2 недель (34,2%), при II степени – в пределах 2 – 4 недель (56,6%), при III степени – более 4 недель (9,2%) от должных значений для данного гестационного срока. Клинически принято выделять симметричную, ассиметричную и смешанную формы данного синдрома. Ассиметричная форма встречается чаще симметричной, но развивается обычно позднее (в 30 – 34 недели гестации). Смешанная форма синдрома ЗРП характеризуется непропорциональным отставанием всех фетометрических показателей при наиболее выраженном отставании размеров живота и считается наиболее неблагоприятной. При обнаружении несоответствия одного или нескольких показателей показано произведение расширенной фетометрии. В то же время отставание фетометрических параметров не всегда позволяет уверенно диагностировать ЗРП. До настоящего времени остаются недостаточно разработанными вопросы тактики ведения беременных с симметричным отставанием размеров плода от срока гестации при отсутствии остальных проявлений ПН, поскольку имеются данные о том, что в этих случаях (генетически детерминированная малая масса, плод «small for date») перинатальные исходы не отличаются от таковых в популяции.
Экстрагенитальные заболевания матери в сочетании с акушерской патологией, реализуясь посредством различных патогенетических механизмов, приводят к единому результату – прогрессирующей ЗРП (Радзинский В. Е., Милованов А. П. и др.,2004). Многолетние наблюдения за развитием детей, родившихся у пациенток с диагностированной ПН, позволили сделать вывод, что акушерская патология обусловливает значительное увеличение перинатальной заболеваемости и является субстратом для возникновения многочисленных патологических изменений в организме ребенка, которые в течение первых лет жизни становятся основной причиной нарушения его физического, умственного развития и повышенной заболеваемости.
По данным Л. О. Бадаляна и др. (1983), более 60% всех заболеваний центральной нервной системы детского возраста связано с перинатальной гипоксией плода. Многие авторы (Paneth N., Stark R., 1983; Seidman D.S., Paz G., 1991 и др.) отмечают, что более половины энцефалопатий обусловлено не острой гипоксией при родах, а длительной, хронической гипоксией плода и новорожденного, нередко связанной с внутриутробной инфекцией. Дети, перенесшие острую гипоксию в родах, чаще имеют совершенно нормальное развитие в дальнейшем (Самсыгина Г.А. и др., 1995).
По данным А. Н. Стрижова и др. (1995), при декомпенсированной форме ПН перинатальная смертность достигает 50%, а заболеваемость новорожденных 100%. ЗРП формирует перинатальную заболеваемость и смертность, а также является фактором риска повышения заболеваемости на протяжении предстоящей жизни. Кроме того, у детей, родившихся маловесными, сокращается средняя продолжительность предстоящей жизни, в сравнении с детьми, не имевшими дефицита веса при рождении (Lithell., 1999). Частота ЗРП по данным многих авторов колеблется от 3% до 22% у доношенных, от 18 до 24% у недоношенных, и не имеет тенденции к снижению (Белоусова В. Б., 1988, Ахмадеева Н. Э. и др., 1989; Радзинский В. Е. и др., 1990).
В структуре перинатальной смертности 23% – 25% занимает ЗРП и связанные с этой патологией осложнения. У 32,5% детей, родившихся с гипотрофией, в возрасте одного года сохраняются отклонения в физическом развитии.
Перинатальные поражения центральной нервной системы занимают одно из важнейших мест в структуре перинатальной заболеваемости по частоте и значимости и составляют 60 – 80% всех заболеваний нервной системы детского возраста ( Студеникин М. Я., Халлман Н., 1984; Яцык Г. В., 1989; Бадалян Л. О., 1989, Барашнев Ю. И., 1993). Перинатальные повреждения головного мозга характеризуются многофакторным генезом, но гипоксия является центральным патогенетическим фактором, приводящим к различным структурным и функциональным повреждениям и порокам развития центральной нервной системы. Характер церебральных изменений зависит от гестационного возраста в период развития патологии, времени действия гипоксии и её интенсивности (Студеникин М.Я. и др., 1993).
Серьёзные неврологические осложнения: такие как детский церебральный паралич, ретинопатиия недоношенных, глухота, грубая задержка темпов психомоторного развития, приводят к неполноценному развитию и снижению качества жизни у таких детей. Неврологические осложнения наиболее распространены у недоношенных детей. Частота неврологических нарушений легкой степени у этих детей составляет 10% – 45 %, тяжелой степени 7% – 9 % (Савельева Г. М., Федорова М. В., Клименко П. А., Сичинава Л. Г., 1991).
Снижение уровня смертности в последние годы сопровождается повышением процента инвалидизации (Cano A., Fons F., Brines J., 2001). Ведущее место среди причин детской инвалидности занимают болезни нервной системы, врождённая и наследственная патология, состояния перинатального периода (Емельянова А. С. 1999).
При снижении летальности новорожденных с массой тела при рождении 1500 г и менее до 49—57%, число выживших детей достигает 43—51%. Однако из выживших детей здоровыми оказываются не более 10—25%. Причем количество детей с тяжелыми психоневрологическими расстройствами может достигать 12—19% (Michelsson K., Lindahl E., Parre M.,1984; Lloyd B. W., 1984; Vohr B.R., Coll C., 1985).
Риск развития психоневрологических расстройств разной степени тяжести у новорожденных с очень низкой массой тела при рождении в 3 раза выше, чем у детей с нормальной массой тела при рождении. Для новорожденных с экстремально низкой массой тела (ЭНМТ) при рождении 1000 г и менее перинатальная смертность может достигать 64—85%, а число выживших детей — не более 15—36%. У выживших детей тяжелые инвалидизирующие расстройства могут превышать 28%, а менее грубые психоневрологические нарушения до 44%. Причем, из выживших детей здоровые составляют не более 8—15% ( HirataT., Epcar J.R., Walsh A.,1983; Fleischman A.R.,1986). При сравнении перинатальных исходов в группах новорожденных с ЭНМТ, 1001 – 1500, 1501 – 2000 и 2001 – 2500 гр. Шалина Р. И. и др., 1999, пришли к заключению, что абдоминальное родоразрешение не позволяет полностью избежать развития мозговых дисфункций, но тем не менее способствует уменьшению числа детей с умеренно выраженными и тяжелыми нарушениями центральной нервной системы.
Изучение отдаленного катамнеза у детей группы высокого инфекционного риска от матерей с внутриутробным инфицированием также представляет большой интерес, поскольку имеются сведения, что у таких детей отмечаются симптомы поражения центральной нервной системы: отставание в психомоторном развитии, прогрессирующие нарушения зрения и слуха (Веденеева Г. Н. и др., 1997; Тареева Т.Г. и др., 1999; Hess D.,1993; Couvreus J. Et al., 1996).
По данным Волгиной С. Я. (2000), в структуре заболеваемости недоношенных детей с ЗРП, в различные периоды жизни выявлялись свои особенности. Доминирующее положение занимают болезни органов дыхания. У детей раннего возраста второе и третье места занимали болезни нервной системы и крови. К 7 годам жизни у значительного количества детей, родившихся с признаками ЗРП, сохраняются изменения неврологического статуса. Развитие этой патологии соотносится со степенью отставания фетометрических показателей и выраженностью признаков внутриутробного страдания плода.
Вывод: состояние здоровья маловесных детей в перинатальном и отдаленном периоде не позволяет приуменьшить значимость проблемы плацентарной недостаточности в настоящее время, а лишь еще раз указывает на необходимость ее детального изучения, своевременной профилактики и лечения.
Вся информация носит ознакомительный характер. Если у вас возникли проблемы со здоровьем, то необходима консультация специалиста.