Для чего нужно изучать тепловые явления
Общие сведения
В обычной жизни человечество постоянно становится свидетелем тепловых явлений, происходящих в природе. Например, выпадение снега, дождя, образование росы. Все эти процессы связаны с температурой, а именно изменением тепловых движений. Любое вещество состоит из молекул или атомов, взаимодействующих между собой. Эти частицы находятся в постоянном беспорядочном колебании и движении. Характеризуется этот процесс кинетической энергией, которая содержится внутри тела.
Как показали исследования, насколько уменьшается механическая энергия, настолько увеличивается внутренняя. Это правило назвали законом сохранения. То есть значение существующей энергии в природе — всегда постоянная величина. Именно поэтому тепловые колебания никогда не прекращаются. Количество внутренней энергии зависит от многих факторов, но особо значимым из них является температура. Если её значение изменяется без совершения работы, то говорят о прохождении теплопередачи.
Существует несколько типов процессов, сопровождающихся изменением температуры или переходом из одного агрегатного состояния в другое. В зависимости от происходящего действия к тепловым явлениям относятся:
Эти явления могут изучаться не только на уроках физики, но и на химии, металловедении. Они используются при разработке различных устройств, учитываются при проведении строительных работ. Так, при прокладке трубопроводов делается изгиб п-образной формы. Это позволяет избежать деформации и разрушения. Рельсы устанавливаются с зазором, а провода на столбах навешивают так, чтобы они свисали. Все эти мероприятия позволяют бороться с тепловыми явлениями, которые обязательно необходимо знать и учитывать.
Тепловой баланс
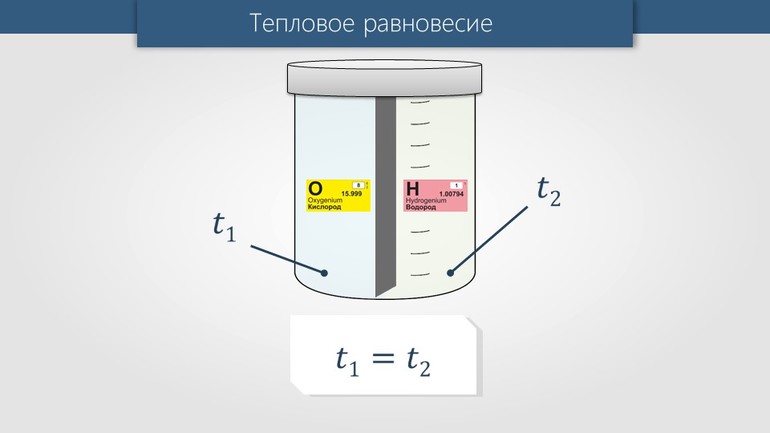
Равновесие — это термин, довольно часто используемый в физике. Под ним понимают состояние, в котором тело может находиться сколь угодно долгое время при условии, что на него не воздействуют внешние силы. Чтобы разобраться в тепловом равновесии, нужно рассмотреть пример.
Пусть есть два бруска, находящихся на некотором расстоянии друг от друга. Один из них нагрет, а второй, наоборот — охлаждён. Эти два тела можно привести в соприкосновение. При этом будет происходить одновременно два явления:
Через некоторое время под действием этих явлений установится устойчивое состояние. Горячий и холодный объектыпримут одинаковую температуру, то есть станут тёплым. Это состояние может сохраняться в замкнутой системе продолжительное время. Другими словами, наступит явление теплового равенства. Это один из важнейших законов природы, определение которого звучит так: в состоянии равновесия физическая система имеет одинаковую температуру в любой точке.
Степень нагрева или охлаждения характеризуется температурой. Определить её можно различными способами. Самый простой из них — использовать тактильные ощущения. Но это приблизительный метод — субъективный. При изменении температуры происходит хаотичное движение молекул, которое в конце концов приводит к диффузии.
При взаимном проникновении молекул веществ происходит заполнение ими промежутков в структуре тела. Можно провести простой эксперимент. Например, взять колбу и налить на её дно подкрашенную воду, а сверху — чистую. Через некоторое время граница между средами станет размытой. Это и есть простой пример произошедшей диффузии. Теперь если эту колбу нагреть или охладить, то можно будет заметить, что процесс смешивания происходит с разной скоростью. Так, при низкой температуре скорость движения молекул становится меньше по сравнению с высокой. Другими словами, снижается энергия движения.
Следовательно, чем выше температура тела, тем больше средняя кинетическая энергия (СКЭ) хаотичного перемещения его молекул. Таким образом, чтобы определить нагрев или охлаждение, нужно измерить СКЭ. Сделать это на опыте невозможно. Но как оказалось, от температуры зависят многих характеристики вещества. Одна из них — объём. На этом явлении и основана работа термометра, устройства, способного количественно определить температуру вещества.
Расширение тел, газов, жидкостей
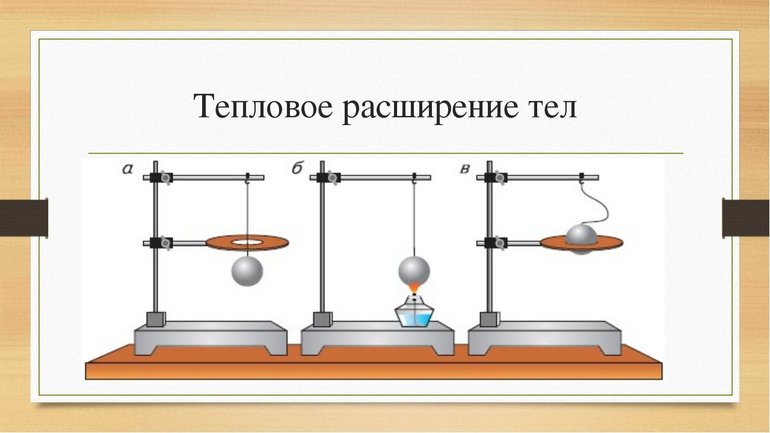
Явление, характеризующее изменение геометрических размеров тела или объёма, получило название тепловое расширение. Большинство веществ при нагревании увеличивают свои размеры, но встречаются и исключения. Например, вода при температуре от 0 до 4 градусов Цельсия уменьшает свой объём. Как оказалось, тепловому расширению подвержены тела, находящиеся в любом агрегатном состоянии:
Твёрдые тела относятся к веществам, у которых явление расширения или сжатия имеет небольшую степень. Для того чтобы зарегистрировать изменения длины, используют специальный прибор. Но наглядно увидеть эффект можно и самостоятельно. Например, пусть имеется медная трубка, закреплённая одним концом в тиски, а второй лежит на подставке. Чтобы наблюдать изменение длины при нагреве, можно положить на подставку стекло, а на него — иголку. Если при нагревании трубка будет удлиняться, то игла начнёт катиться. Это и произойдёт при опыте.
Почему это происходит, объяснить довольно просто. Стержень удлиняется из-за увеличения расстояния между молекулами. То есть сначала частицы колеблются в состоянии равновесия с установившейся амплитудой. Когда происходит нагрев, то размах увеличивается. При этом размеры молекул остаются неизменным. Следовательно, возрастает расстояние между частицами — твёрдое тело удлиняется.
Увидеть, как будет изменяться от температуры жидкость, можно, поместив колбу с водой в кипящий раствор. При этом водяной столб сначала опустится на некоторую величину, а потом будет набирать высоту. Происходит это явление из-за того, что первоначально нагрелась колба, а затем уже вода. В результате сначала объём сосуда увеличился, и вода как бы провалилась. Затем начинает прогреваться жидкость, и водяной столб возрастает. Из эксперимента можно сделать важный вывод — текучие вещества расширяются сильнее, чем твёрдые.
Аналогичный опыт можно провести для колбы, наполненной газом. Внизу неё налита подкрашенная жидкость, в которую вставлена трубочка, выходящая наружу через пробку. Если сосуд начать нагревать, то станет довольно заметно, как под влиянием тепла будет подниматься жидкость. То есть под действием увеличивающего давления газа происходит вытеснение воды из-за расширения.
Количественное описание расширения
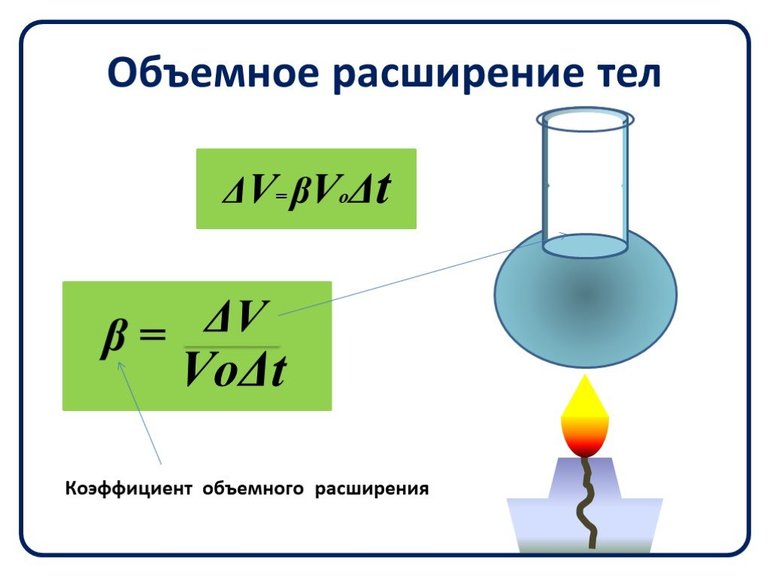
Изменение линейных размеров тела с учётом температурной зависимости характеризуется коэффициентом теплового расширения. Это физическая величина, показывающая, как меняется объём при росте температуры на один градус по кельвину. При этом давление должно оставаться неизменным.
Каждое вещество в зависимости от своего строения характеризуется собственным значением коэффициента линейного расширения. Обозначают его с помощью буквы α, а для вычисления его значения используют формулу: α = ΔL / L * ΔT, где: ΔT — увеличение температуры, ΔL — изменение длины вещества, L — первоначальный размер. Это табличная величина.
Таким образом, если необходимо узнать, какое значение примет линейное расширение, нужно воспользоваться выражением: ΔL = α * L * ΔT. Аналогичные формулы используют и для расчёта изменения объёма или площади тела. В простом случае, при котором коэффициент теплового расширения не зависит ни от температуры, ни от направления расширения, материал будет равномерно расширяться во все стороны.
Но, как показывает практика, не все вещества, особенно твёрдые тела, равномерно расширяются по всем направлениям. Причём не все материалы удлиняются одинаково. Самый яркий пример — вода. В интервале от 0 °C до +4 °C коэффициент α принимает отрицательное значение. Из-за этого природного эффекта моря и океаны никогда не промерзают до дна. Ещё одно аномальное свойство воды в том, что при превращении в лёд её удельная плотность уменьшается.
Изучаемые в 8 классе на физике тепловые явления жизненно важны для человечества. Так, любой инженер, составляя проект металлоконструкций, не может не учитывать возможного перепада температур в течение года. Например, при постройке мостов используется секционное строительство со специальными буферными зонами. Иначе зимой его может просто разорвать, а летом — вздыбить.
Проект по физике на тему: «Тепловые явления»
Министерство образования РД
на тему: «Тепловые явления»
Подготовил: учитель физики и информатики
- Введение. 3
- Цели и задачи 4
- Тепловое движение молекул 5
- Тепловые процессы 7
- Заключение 15
В природе мы являемся свидетелями тепловых явлений, но порой, не обращаем внимания на их сущность. Например, летом идёт дождь, а зимой снег. Образуется роса на листьях. Появляется туман. Зимой моря и реки покрываются льдом, а весной этот лед тает. Можно привести множество подобных примеров
Значение тепловых явлений в жизни человека очень велико. К примеру, незначительное изменение температуры организма означает заболевание. Температура внешней среды в любом точке Земли меняется как в течение суток, так и в течение года. Организма сам по себе не может компенсировать изменение температуры при теплообмене со средой, и нужно принимать какие-то дополнительные меры: т. е. надеть соответствующую одежду, строить жильё с учетом условий местности, где живут люди, ограничивать пребывание человека в среде, температура которой отличается от температуры организма.
Благодаря научным знаниям и достижениям созданы легкие, прочные малотеплопроводные материалы для одежды и защиты жилища, кондиционеры, вентиляторы и прочие приспособления. Это позволяет нам преодолевать трудности и многие проблемы, связанные с теплом. Но все же изучать тепловые явления необходимо, так как они имеют исключительно большое влияние на нашу жизнь.
1. Рассказать о тепловых явлениях и тепловых процессах.
2. Показать важность тепловых процессов в жизни человека.
Изучить теорию тепловых явлений. На практике рассмотреть существование тепловых процессов. Показать на опыте проявление этих опытов.
ТЕПЛОВОЕ ДВИЖЕНИЕ МОЛЕКУЛ.
Молекулы или атомы вещества всегда находятся в постоянном беспорядочном движении. Это движение обусловливает собой наличие в любом веществе внутренней кинетической энергии, которая, связана с температурой вещества. Поэтому, то беспорядочное движение, в котором всегда находятся молекулы или атомы, называется тепловым.
Тепловое движение частиц твердого тела носит колебательный характер: частицы колеблются около среднего положения с различными амплитудами в разных плоскостях.
Такой характер теплового движения частиц твердого тела обусловливается тем, что между ними имеются прочные связи, делающие твердое тело способным самостоятельно сохранять свой объем и форму.
Тепловое движение молекул жидкости носит в основном уже поступательный характер с различными скоростями, в разных направлениях; это объясняется меньшей прочностью связей между молекулами жидкости; жидкость способна сохранять самостоятельно только объем, но не форму.
Тепловое движение молекул газообразного вещества имеет только поступательный характер с очень слабым взаимодействием между молекулами, особенно при низких давлениях.
Свойства вещества в различных агрегатных состояниях.
Твёрдые тела в обычных условиях трудно сжать или растянуть. В отсутствии внешних воздействий оно сохраняют и форму и объём.
Жидкости легко меняют свою форму. В обычных условиях она принимает форму сосуда, в котором она находиться. Итак, жидкости не имеют форму, но сохраняют объём.
Газы не имеют ни форму, ни объём.
Тепловоме движемние — процесс хаотичного (беспорядочного) движения частиц, образующих вещество. Чем выше температура, тем больше скорость движения частиц. Чаще всего рассматривается тепловое движение атомов и молекул.
Хаотичность — важнейшая черта теплового движения. Важнейшими доказательствами существования движения молекул является Броуновское движение и диффузия.
Изучение тепловых явлений показывает, что насколько в них уменьшается механическая энергия тел, настолько же увеличивается их механической и внутренней энергий, при любых процессах остаётся неизменной. В этом заключается закон сохранения энергии. Энергия не возникает из ничего и не исчезает ни куда. Она может лишь переходит из одного вида в другой, сохраняя своё полное значение.
Тепловое движение молекул никогда не прекращается. Поэтому любое тело всегда обладает какой-то внутренней энергией.
Кинетическая энергия всех молекул, из которых состоит тело, и потенциальная энергия их взаимодействия составляют внутреннюю энергию тела. 
где Еk – кинетическая энергия, Еp – потенциальная энергия.
Внутренняя энергия зависит от температуры тела, агрегатного состояния вещества и других факторов и не зависит от механического положения тела и его механического движения. При повышении температуры внутренняя энергия тела увеличивается.
Внутренняя энергия тела изменяется в процессе теплопередачи и при совершении работы.
Изменение внутренней энергии тела без совершения работы называется теплопередачей. Теплопередача всегда происходит в направлении от тела с большей температурой к телу с меньшей температурой.
Существует три вида теплопередачи.
Теплопроводность – это вид теплообмена, при котором происходит непосредственная передача энергии от частиц более нагретой части тела к частицам его менее нагретой части. Гвоздики, прикреплённые к штативу, по мере нагревания штатива выпадают (рис1). Теплопроводность зависит от рода вещества. Скорость передачи энергии пропорциональна разности температур.
Конвекция – это теплообмен в жидких и газообразных средах, осуществляемый потоками вещества. Вещество, нагретое сильнее, имеет меньшую плотность и перемещается под действием этой силы относительно менее нагретого вещества. Поэтом тёплый воздух поднимается на верх (рис2)
Излучение – это теплообмен, при котором энергия переносится различными лучами. Это могут быть солнечные лучи, а также лучи, испускаемые нагретыми телами, находящимися вокруг нас. Чем выше температура, тем сильнее тепловое излучение.
Энергия, которую получает или теряет тело при теплопередаче, называется количеством теплоты Q. Количество теплоты зависит от массы тела, рода вещества и изменения температуры тела. Количество теплоты измеряется в джоулях (Дж).
Приёмник тепла нагревается и тепло переходит по шлангу к термометру (рис3)
Физическая величина, равная количеству теплоты, которое необходимо передать телу массой 1 кг для того, чтобы его температура увеличилась на 1 єC, называется удельной теплоемкостью вещества c. Таким образом:
Тепловые процессы – разновидность тепловых явлений; процессы, при которых меняется температура тел и веществ, а также возможно изменение их агрегатных состояний.
К тепловым процессам относятся:
Нагревание Охлаждение Парообразование Кипение Испарение Кристаллизация Плавление Конденсация Сгорание Сублимация Десублимация
Нагревание – процесс повышения температуры тела или вещества. Нагревание сопровождается поглощением теплоты из окружающей среды. При нагревании агрегатное состояние вещества не изменяется.
Формула для вычисления количества теплоты при нагревании:
Q = cm(t2 – t1), где Q – количество теплоты,
с – удельная теплоемкость вещества, m – масса вещества,
t1 – начальная температура, t2 – конечная температура,
Давайте покажем нагревание на опыте.
Наберём воду из крана в стакан и измерим её температуру (25°C), затем поставим стакан на теплое место, и через некоторое время измерим температуру воды (30°C).
Подождав ещё некоторое время, я еще раз измерил температуру (35°C).
Вывод: термометр показывает увеличение температуры сначала на 5°C, а потом и на 10°C.
Охлаждение – процесс, понижения температуры вещества или тела; Охлаждение сопровождается выделением теплоты в окружающую среду. При охлаждении агрегатное состояние вещества не изменяется.
Q = cm(t2 – t1), где Q – количество теплоты,
с – удельная теплоемкость вещества, m – масса вещества,
t1 – начальная температура, t2 – конечная температура,
При охлаждении Q становиться отрицательным, так как конечная температура становиться меньше, чем начальная.
Посмотрим как происходит охлаждение на опыте.
Из крана в стакан наберём горячую воду и измерим её температуру (60°C) затем этот стакан на некоторое время поставим на подоконнике, после чего измерим температуру воды и она стала равной (20°C).
Вывод: вода охлаждается и термометр показывает понижение температуры.
Парообразование – процесс перехода вещества из жидкого состояния в газообразное. При парообразовании энергия (теплота) из окружающей среды поглощается.
Количество теплоты, поглощаемой из окружающей среды при парообразовании, вычисляется по формуле:
Q = rm, где Q – количество теплоты, m – масса вещества,
r – удельная теплота парообразования.
Парообразование может осуществляться двумя способами:
испарением и кипением.
Кипение – процесс интенсивного парообразования, при котором внутри жидкости растут и поднимаются вверх пузырьки пара.
Температура кипения – температура, при которой то или иное вещество начинает закипать. Для разных веществ эта температура различна.
Во время процесса кипения температура жидкости не меняется, то есть остается постоянной.
Температура кипения зависит от давления оказываемого на свободную поверхность жидкости. При увеличении этого давления рост и подъём пузырьков внутри жидкости начинается при большей температуре, при уменьшении давления – при меньшей температуре. При понижении давлении температура кипения воды становится меньше 1000С. Например в горных районах (на высоте 3км, где давление атмосферы составляет 70кПа вода кипит при 900С
С кипением мы каждый день сталкиваемся дома.
Нальём в чайник воду и поставим его на плиту. С начала вода нагревается, а затем происходит кипения воды. Об этом свидетельствует пар, выходящий из носика чайника.
Вывод: при кипении воды, пар из горлышка чайника выходит через маленькое отверстие и свистит и мы выключаем плиту.
Испарение – это парообразование, происходящее со свободной поверхности жидкости.
Испарение может происходить как с закрытой, так и с открытой поверхности жидкости.
Испарение зависит от:
- Температуры вещества
- (чем выше температура, тем интенсивнее испарение);
Площади поверхности жидкости
- (чем больше площадь, тем больше испарение);
Рода вещества
- (разные вещества испаряются с разной скоростью).
Наличия ветра
- (при наличии ветра испарение происходит быстрее);
Мы понаблюдаем за испарением на опыте.
Если Вы когда-нибудь лужайками после дождя, то Вы, несомненно, замечали, что лужи становятся меньше и меньше. Что произошло с водой?
Вывод: она испарилась!
Кристаллизация (отвердевание) – это переход вещества из жидкого агрегатного состояния в твердое. Кристаллизация сопровождается выделением энергии (теплоты) в окружающую среду.
Количество выделяемой теплоты вычисляется по формуле:
Жидкие вещества начинают свою кристаллизацию при той температуре, при которой аналогичные им твердые вещества начинают плавиться. Это температура называется температурой кристаллизации (отвердевания).
Во время кристаллизации температура также остается постоянной.
Опыт 5: Кристаллизация.
Чтобы обнаружить кристаллизацию, проведём опыт.
Наберём воду из крана в стакан и поставим в морозильную камеру холодильника. Через некоторое время происходит процесс отвердевания вещества, т. е. на поверхности воды появляется корка. Затем вся вода в стакане полностью превратилась в лед, то есть кристаллизуется.
Рис 13 Рис 14 Рис 15
Вывод: сначала вода охлаждается до 0 градусов, затем замерзает.
Плавление – переход вещества из твердого состояния в жидкое. Этот процесс сопровождается поглощением теплоты из окружающей среды. Чтобы расплавить твёрдое кристаллическое тело ему необходимо передать некоторое количество теплоты.
Количество теплоты, затрачиваемой на плавление тела, вычисляется по формуле:
Q = лm, где Q – количество теплоты, m – масса тела.
л – удельная теплота плавления.
Для каждого вещества существует своя определенная температура плавления – температура, при которой начинается процесс перехода вещества из твердого состояния в жидкое. Во время плавления температура остается постоянной.
Плавление легко обнаруживается на опыте.
Достаём из морозильной камеры холодильника стакан с замёрзшей водой, который поставили мы. Через некоторое время в стакане появилась вода – лед начал таять. Спустя некоторое время весь лед растаял, то есть полностью перешел из твердого в жидкое.
Рис 16 Рис 17 Рис 18
Вывод: лёд с течением времени получает тепло от окружающей среды и со временем растает.
Конденсация –переход вещества из газообразного состояния в жидкое.
Конденсация сопровождается выделением теплоты в окружающую среду.
Количество выделяемой теплоты при конденсации вычисляется формуле:
Q = rm, где Q – количество теплоты, m – масса вещества,
r – удельная теплота парообразования.
Опыт 7: Конденсация.
Давайте обнаружим на опыте конденсацию.
Мы вскипятили воду и поднесли к носику чайника холодное зеркало.
Через несколько минут на зеркале четко видны капли конденсировавшегося водяного пара.
Вывод: пар оседая на зеркале превращается в воду.
Явление конденсации можно наблюдать летом, ранним прохладным утром. Капельки воды на траве и цветах – роса – свидетельствуют о том, что водяной пар, содержавшийся в воздухе, конденсировался.
Сгорание – процесс сжигания топлива, сопровождающийся выделением энергии. Эта энергия используется в различных сферах нашей жизни.
Выделение энергии при сжигании объясняется тем, что атомы соединяются в молекулы, не совершая при этом работы по преодолению сил притяжения между ними.
Количество теплоты, выделяемой при сгорании, вычисляется по формуле:
Q = qm, где Q – количество выделяемой теплоты, q – удельная теплота сгорания топлива,
Каждый день мы можем наблюдать, как сгорает природный газ в горелке плиты. Это и есть процесс сгорания топлива. Также процессом сгорания топлива является процесс сжигания дров.
Поэтому, чтобы провести опыт по сгоранию топлива, достаточно только зажечь газовую горелку или спичку.
Вывод: при сгорании топлива выделяется тепло, может появиться специфический запах.
Сублимация – переход вещества из твёрдого состояния в газообразное (минуя жидкое) от латинского слова «сублимо»- возношу.
Например, графит можно нагреть до двух тысяч градусов, тем не менее в жидкость он не превратится: он из твёрдого состояния сразу переходит в газообразное.
Десублимация – переход вещества из газообразного состояния в твёрдое.
Например: образование на окнах зимой узоров из кристаллического льда. Эти красивые узоры являются результатом десублимации водяного пара, находящегося в воздухе.
В своей проектной работе я изучал наиболее распространенные тепловые процессы: нагревание, охлаждение, парообразование, кипение, испарение, плавление, кристаллизация, конденсация, сгорание, сублимации и десублимации.
Кроме того, в работе были затронуты такие темы, как теплообмен, способы теплообмена, тепловое движение, агрегатные состояния веществ, а также общая теория по тепловым явлениям и тепловым процессам.
Были изучены основные формулы вычисления количества теплоты в различных тепловых процессах
На основе простейших опытов рассматривалось то или иное тепловое явление. Опыты сопровождаются демонстрационными картинками.
ВЫВОДЫ:
- Теория по теме «Тепловые явления» изучена полностью;
- На основе одиннадцати опытов рассмотрено существование различных тепловых процессов;
- Доказана актуальность тепловых процессов в жизни человека.
- Поставленная мною цель и задачи проектной работы выполнены.