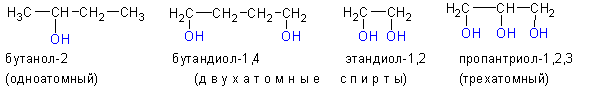
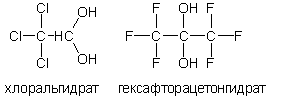
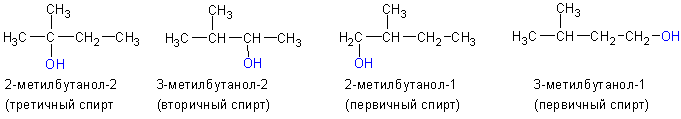
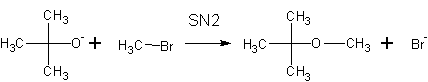
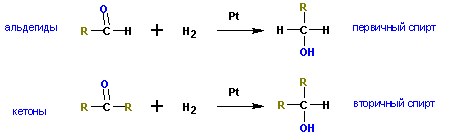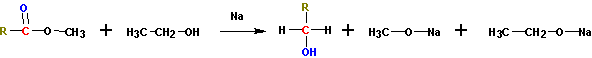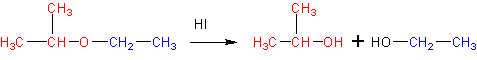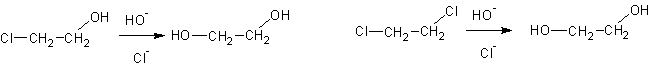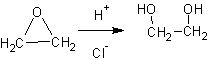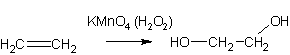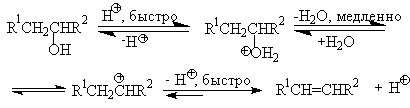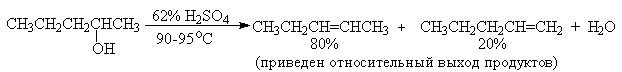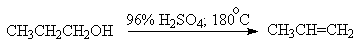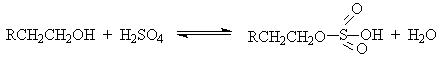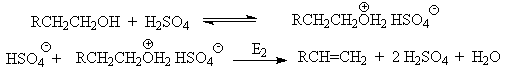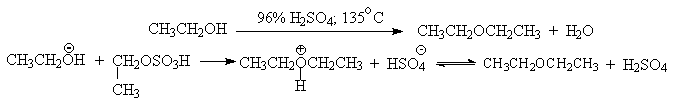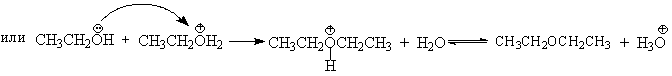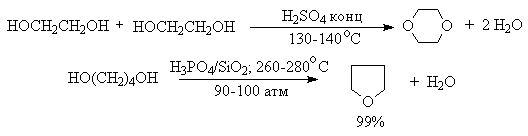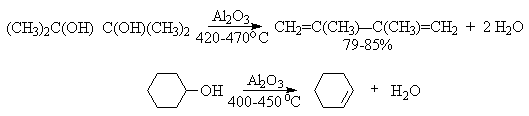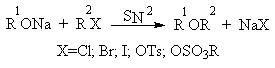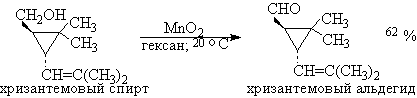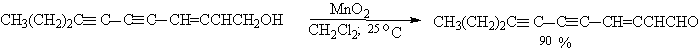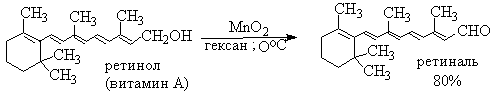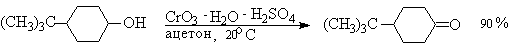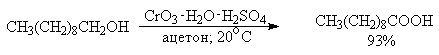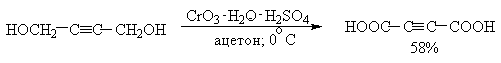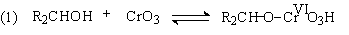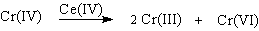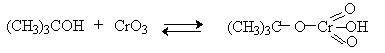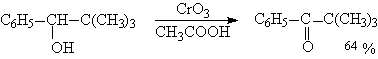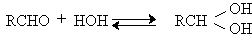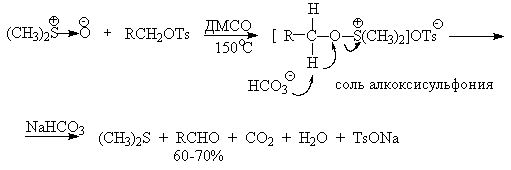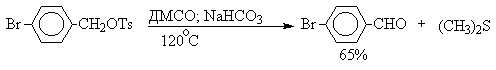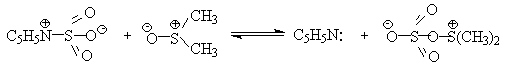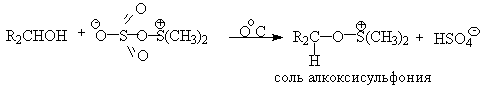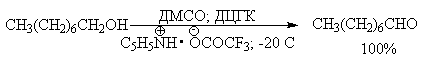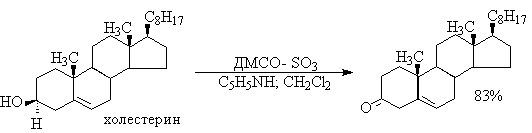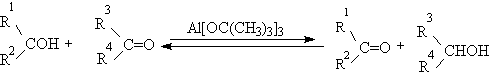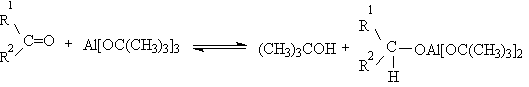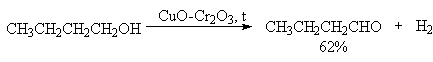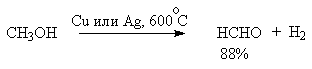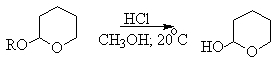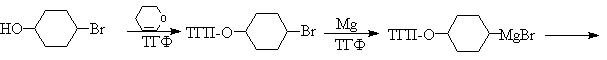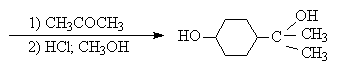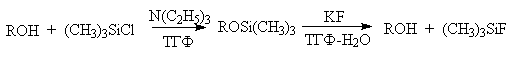До чего окисляются спирты вторичные
Окисление вторичных спиртов
Вы будете перенаправлены на Автор24
Общим методом получения кетонов из вторичных спиртов является окисление их оксидом хрома (VI) в воде или разведенной уксусной кислоте. Хромовый ангидрид в ацетоне и дихроматы пиридиния можно использовать для окисления ненасыщенных вторичных спиртов, не нарушая двойных и тройных связей:
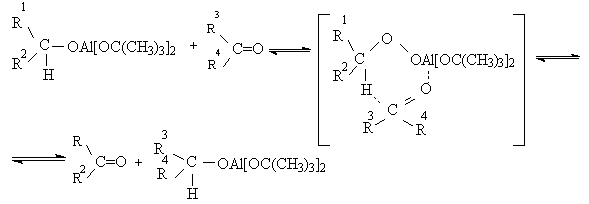
Вторичные спирты сложного строения, содержащие чувствительные к действию окислителей группы, можно с хорошими выходами окиснюваты в соответствующие кетонов, используя метод Оппенауера. В системе, содержащей вторичный спирт и кетоны (как правило ацетон) в присутствии алкоголятов алюминия устанавливается равновесие:
Готовые работы на аналогичную тему
Окисление ароматических спиртов
Окисление фенолов является сложным, многостадийным процессом, механизм которого мало изучен. Сам фенол окислением производными шестивалентного хрома, четырех и семи валентного марганца в серной кислоте образует с удовлетворительным выходом пара-хинон.
Вторичную гидроксильную группу ароматических спиртов можно окислять в карбонильную и при наличии в молекуле других заместителей, например, первичной спиртовой группы. Для этого, первичную гидроксильную группу защищают превращением в трифенилметиловий эфир (третичная защита) обработкой диола трифенил-хлорометаном в присутствии основания (пиридина) при комнатной температуре. Эфир, который образуеться, устойчивый в нейтральной и щелочной среде, а незащищенную вторичную спиртовую группу можно окислять диоксидом марганца. Третичную защиту снимают при нагревании с разбавленной уксусной или соляной кислотой:
Окислители для окисления вторичных спиртов
Расщепление α-гликолей
Механизм этой реакции полностью еще не выяснен. Как правило, цис-гликоли расщепляются значительно быстрее, чем транс- гликоли. Йодатная кислота, в отличие от тетраацетата свинца, растворима в воде и поэтому может быть использована в качестве реагента для расщепления нерастворимых в органических растворителях сахаров. Она используется для определения размеров колец гликозидов.
Спирты
Классификация спиртов
Одноатомные спирты также подразделяются в зависимости от положения OH-группы: первичные (OH-группа у первичного атома углерода), вторичные (OH-группа у вторичного атома углерода) и третичные (OH-группа у третичного атома углерода).
Номенклатура и изомерия спиртов
Названия спиртов формируются путем добавления суффикса «ол» к названию алкана с соответствующим числом атомов углерода: метанол, этанол, пропанол, бутанол, пентанол и т.д.
Для спиртов характерна изомерия углеродного скелета (начиная с бутанола), положения функциональной группы и межклассовая изомерия с простыми эфирами, которых мы также коснемся в данной статье.
Получение спиртов
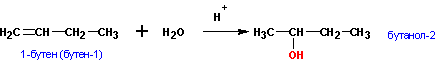
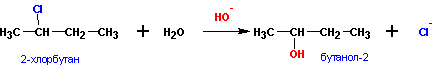
Присоединения молекулы воды (HOH) протекает по правилу Марковникова. Атом водорода направляется к наиболее гидрированному атому углерода, а гидроксогруппа идет к соседнему, наименее гидрированному, атому углерода.
В результате восстановления альдегидов и кетонов получаются соответственно первичные и вторичные спирты.
Синтез газом в промышленности называют смесь угарного газа и водорода, которая используется для синтеза различных химических соединений, в том числе и метанола.
В ходе брожения глюкозы выделяется углекислый газ и образуется этанол.
Химические свойства спиртов
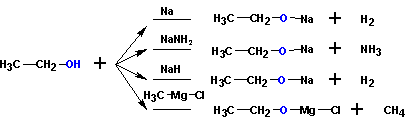
Щелочные металлы (Li, Na, K) способны вытеснять водород из спиртов с образованием солей: метилатов, этилатов, пропилатов и т.д.
Необходимо особо заметить, что реакция с щелочами (NaOH, KOH, LiOH) для предельных одноатомных спиртов невозможна, так как образующиеся алкоголяты (соли спиртов) сразу же подвергаются гидролизу.
Реакция с галогеноводородами протекают как реакции обмена: атом галогена замещает гидроксогруппу, образуется молекула воды.
В результате реакций спиртов с кислотами образуются различные эфиры.
Дегидратация спиртов (отщепление воды) идет при повышенной температуре в присутствии серной кислоты (водоотнимающего) компонента.
Качественной реакцией на спирты является взаимодействие с оксидом меди II. В ходе такой реакции раствор приобретает характерное фиолетовое окрашивание.
Замечу, что в обычных условиях третичные спирты окислению не подвергаются. Для них необходимы очень жесткие условия, при которых углеродный скелет подвергается деструкции.
Вторичные и третичные спирты определяются другой качественной реакцией с хлоридом цинка II и соляной кислотой. В результате такой реакции выпадает маслянистый осадок.
Такой реакцией является взаимодействие многоатомного спирта со свежеприготовленным гидроксидом меди II. В результате реакции раствор окрашивается в характерный синий цвет.
Важным отличием многоатомных спиртов от одноатомных является их способность реагировать со щелочами (что невозможно для одноатомных спиртов). Это говорит об их более выраженных кислотных свойствах.
© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
До чего окисляются спирты вторичные
Tомский государственный университет
кафедра органической химии
Кислородсодержащие соединения. Спирты
Строение и классификация спиртов
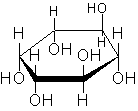
Среди многоатомных спиртов наиболее известен шестиатомный циклический спирт инозит :
3. По положению гидроксильной группы в цепи различают первичные, вторичные и третичные спирты:
При наименовании спиртов по номенклатуре IUPAC находят самую длинную цепь атомов углерода, содержащую гидрокисльную группу, и нумеруют ее с края, к которому ближе гидроксильная группа. После перечисления заместителей добавляется название, соответствующее углеводороду главной цепи с добавлением окончания –о л и цифры, показывающей место гидроксильной группы в цепи (см. примеры выше).
Химические свойства спиртов
1. Реакции дегидратации спиртов (внутри- и межмолекулярная дегидратация)
При кипячении с кислотами спирты могут образовывать алкены и простые эфиры.
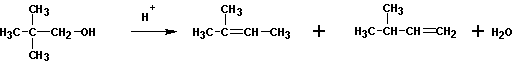
Как правило, получаются смеси продуктов. Преобладание того или иного соединения связано с условиями проведения реакции. Так, при повышении температуры выход алкенов увеличивается. Выходы алкенов также возрастают при переходе от первичных к третичным спиртам. Очень часто перечисленные реакции сопровождаются перестройками в углеродном скелете:
Образование простых эфиров (межмолекулярная дегидратация спиртов).
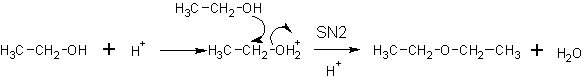
В присутствии серной кислоты:
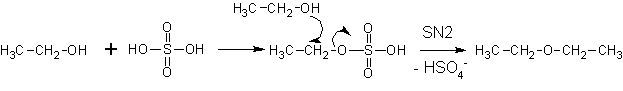
Пример получения метил-третбутилового эфира (МТБЭ) реакциями:
2. Образование галоидных алкилов из спиртов происходит при реакции с различными реагентами:
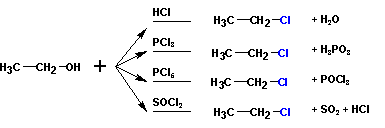
Во всех случаях наиболее гладко протекают реакции с первичными спиртами, третичные спирты чаще дают различные побочные продукты.
Механизмы галогенирования спиртов тионилхлоридом ( SOCl 2 ) и галогенидами фосфора
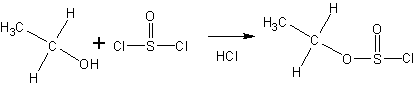
Тионилхлорид образует со спиртами эфиры хлорсернистой кислоты (хлорсульфиты ):
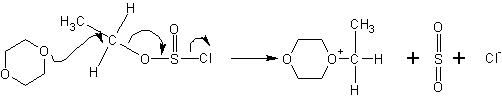
При этом генерируется некоторое (заметное) количество анионов хлора.
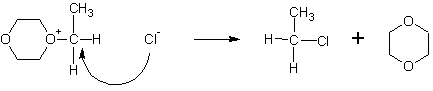
Полученное промежуточное соединение атакуется повторно анионами Cl- с противоположной стороны, в результате чего не происходит обращения оптической конфигурации (если сравнивать с исходным спиртом):
Однако, в таких растворителях, как пиридин или гексаметилфосфотриамид (НМРТ), концентрация свободных ионов хлора достаточно велика, чтобы атаковать эфиры хлорсульфита с образованием галогенпроизводных спирта с обращенной конфигурацией:
Реакции с галогенидами фосфора протекают с обращением конфигурации согласно ниже приведенной схеме;
После чего хлорид ио н- замещает группировку с атомом фосфора:
3. Кислотные свойства спиртов
При взаимодействии с сильными основаниями и щелочными металлами спирты ведут себя как кислоты:
4. Окисление спиртов
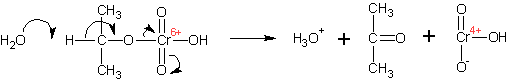
Спирты окисляются различными окислителями до альдегидов (первичные спирты) и кетонов (вторичные спирты). Механизм окисления спиртов хромовой кислотой:
Образующиеся вначале эфиры хромовой кислоты претерпевают отщепление протона от атома углерода, при котором стояла гидроксильная группа (вследствие повышения его кислотности в результате образования эфира, он отщепляется даже таким слабым основанием, как вода):
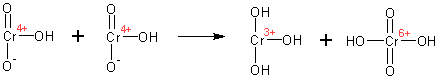
Образуется продукт окисления и хромистая кислота ( Cr IV ). Хромистая кислота быстро диспропорционирует до гидроокиси хрома ( Cr III ) и хромовой кислоты ( Cr VI ):
Если таким образом окисляются вторичные спирты, то образующиеся кетоны сравнительно устойчивы, однако, при окислении первичных спиртов образуются альдегиды, которые легко окисляются дальш е- до карбоновых кислот (если не предпринимать меры предосторожности). Альдегиды с небольшим числом атомов углерода можно выделить из реакционной смеси отгонкой в процессе получения, однако, для более тяжелых альдегидов такой способ не помогает.
Окисление спиртов реагентом Саретта ( Sarett )- смесью хромового ангидрида и пиридина позволяет выделять альдегиды.
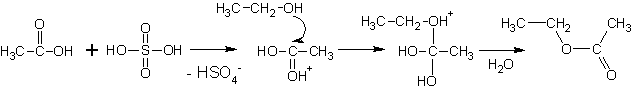
5. Образование сложных эфиров
Сложные эфиры образуются при реакции спиртов с минеральными и органическими кислотами.
(Реакции протекают при умеренном нагревании, кислотный катализ).
6. Образование ацеталей и полуацеталей
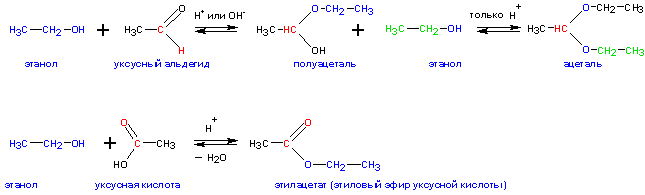
Спирты взаимодействуют с альдегидами и кетонами— с образованием полуацеталей и ацеталей (альдегиды) и полукеталей и кеталей (кетоны):
Ацетали представляют собой жидкости с приятным эфирным запахом.
Способы получения спиртов
1. Гидратация алкенов (правило Марковникова):
2. Гидролиз галоидных алкилов :
а) обратимый гидролиз в кислой среде;
б) необратимый гидролиз в щелочной среде:
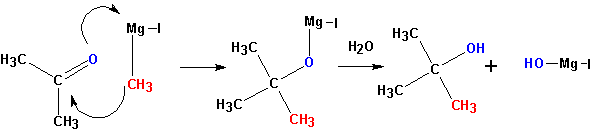
3. Взаимодействие металлорганических соединений (реактивы Гриньяра ) с карбонильными группами (нуклеофильное присоединение по кратной связи С =О):
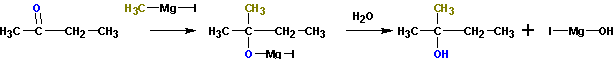
Из кетонов получаются третичные спирты. Так, из метилэтилкетона (бутанон-2) получается 2-метилбутанол-2. Альдегиды в подобной реакции дают вторичные спирты. Из пропионового альдегида (пропаналь ) получается бутанол-2:
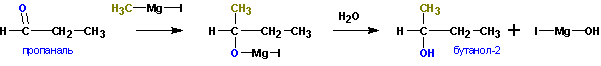
Из формальдегида образуются первичные спирты.
Взаимодействие реактивов Гриньяра со сложными эфирами карбоновых и муравьиной кислот ы- приводит к получению третичных и вторичных спиртов, соответственно.
Менее распространены способы получения спиртов восстановлением альдегидов и кетонов.
5. Восстановление сложных эфиров ( каталитические и некаталитические).
Получение спиртов восстановлением сложных эфиров по Буво-Блану (кипячение с натрием).
6. Расщепление простых эфиров HJ и HBr
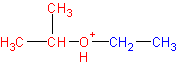
Реакция представляет собой нуклеофильное замещение в алкил оксонии :
Реакции двухатомных спиртов (отличные от первичных спиртов реакции).
1. внутримолекулярная дегидратация :
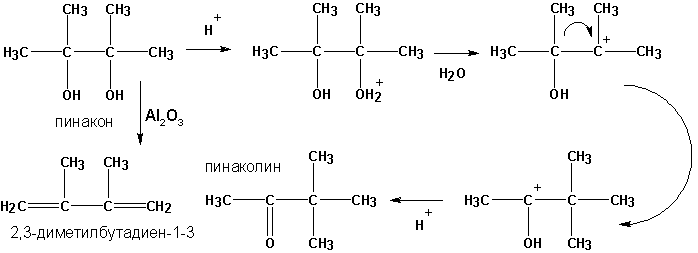
г) пинакон-пинаколиновая перегруппировка
д ) дегидратация пинаконов в присутствии окиси алюминия приводит к диенам:
а) образование спиртоэфиров
б) образование циклических эфиров:
Получение двухатомных спиртов
1. Гидролиз дигалогенпроизводных или хлоргидринов :
2. Гидратация альфа-окисей (эпоксидов ):
3. Окисление олефинов перекисью водорода или перманганатом (холодные растворы):
4. Каталитическое восстановление сложных эфиров дикарбоновых кислот:
Окисление спиртов
Вы будете перенаправлены на Автор24
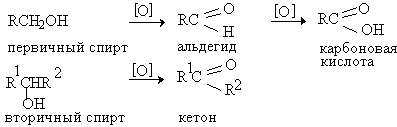
Окисление первичных спиртов в альдегиды и вторичных спиртов в кетоны является одним из важнейших превращений функциональных групп и оценкой избирательного действия окислительного агента:
Третичные спирты в обычных условиях не окисляются, а в очень жестких условиях их окисление сопровождается деструкцией углеродного скелета.
Окисление первичных спиртов до карбоновых кислот
Окисление первичных спиртов в соответствующие карбоновые кислоты легко осуществить действием большинства известных окислителей. Так, концентрированная азотная кислота быстро превращает спирты в соответствующие карбоновые кислоты. Этот метод можно применить ко всем первичным спиртам, при условии, что они не содержат групп, чувствительных к действию азотной кислоты:
Карбоновые кислоты также образуются при окислении первичных спиртов щелочным раствором перманганата калия. Надо отметить, что в этих условиях не разрушаются группы, чувствительные к кислой среде. Это обстоятельство может быть использована для окисления первичных спиртовых групп в присутствии альдегидных. Для этого из альдегидоспиртов получают ацетали, затем окисляют первичную спиртовую группу в карбоксильную и кислотным гидролизом снимают защиту, освобождая альдегидную группу. Например, таким путем можно превратить гликолевый альдегид в глиоксиловую кислоту:
Готовые работы на аналогичную тему
Окисления щелочным раствором перманганата калия ароматических первичных спиртов является удобным методом синтеза ароматических кислот:
Окисление спиртов до карбонильных соединений
Для окисления первичных и вторичных спиртов в соответствующие альдегиды или кетоны используют смесь бихромата с серной кислотой, хромовый ангидрид, перманганат калия, диоксид марганца, а также каталитическое дегидрирование.
Получение альдегидов
Принципиальной проблемой, которая возникает при окислении спиртов до альдегидов, является то, что альдегиды очень легко подвергаются дальнейшему окислению по сравнению с исходными спиртами. По сути альдегиды являются активными органическими восстановителями. Так, при окислении первичных спиртов бихроматом натрия в серной кислоте (смесь Бекмана), альдегид, который образуется, необходимо защитить от дальнейшего окисления до карбоновой кислоты. Можно, например, удалять альдегид из реакционной смеси. И это широко применяется, так как температура кипения альдегида как правило ниже, чем температура кипения исходного спирта. Таким путем могут быть получении, в первую очередь, низкокипящие альдегиды, например, уксусный, пропионовый, изомасляный:
Лучшие результаты можно получить, если вместо серной кислоты использовать ледяную уксусную кислоту.
Для получения высококипящих альдегидов из соответствующих первичных спиртов в качестве окислителя используют трет-бутиловый эфир хроматных кислоты:
При окислении трет-бутилхроматом ненасыщенных спиртов (в апротонных неполярных растворителях) кратные связи не занимаются, и ненасыщенные альдегиды образуются с высокими выходами.
Достаточно селективным является метод окисления, в котором используют диоксид марганца в органическом растворителе, пентан или хлористый метилен. Например, алил- и бензил- спирты таким образом можно окислять в соответствующие альдегиды. Выходные спирты мало растворимые в неполярных растворителях, а альдегиды, которые образуются в результате окисления, значительно лучше растворимые в пентан или хлористый метилен. Поэтому карбонильные соединения переходят в слой растворителя и таким образом можно предотвратить контакт с окислителем и дальнейшем окислению:
Проводить окисление вторичных спиртов в кетоны значительно проще, чем первичных спиртов в альдегиды. Выходы здесь выше, так как, во-первых, реакционная способность вторичных спиртов выше, чем первичных, а во-вторых, кетоны, которые образуются значительно более стойки к действию окислителей чем альдегиды.
Получение кетонов
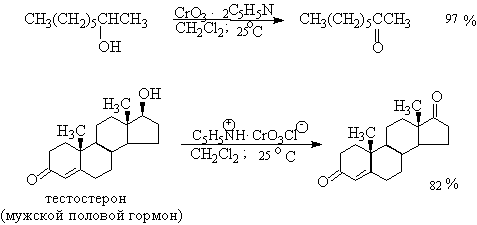
Общим методом является окисление оксидом хрома ($VI$) в воде или разведенной уксусной кислоте. Хромовый ангидрид в ацетоне и дихроматы пиридиния можно использовать для окисления ненасыщенных вторичных спиртов, не нарушая двойных и тройных связей:
Вторичные спирты сложного строения, содержащие чувствительные к действию окислителей группы, можно с хорошими выходами окиснюваты в соответствующие кетонов, используя метод Оппенауера. В системе, содержащей вторичный спирт и кетоны (как правило ацетон) в присутствии алкоголятов алюминия устанавливается равновесие:
До чего окисляются спирты вторичные
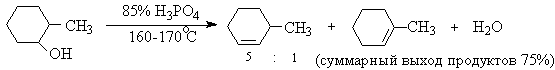
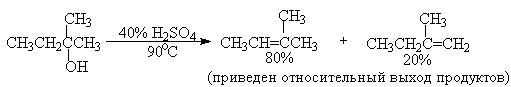
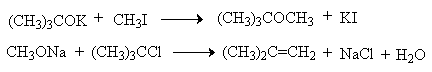
Приведенная последовательность превращений типична для реакций мономолекулярного элиминирования Е1, продукты которого определяются правилом Зайцева, т.е. преобладает наиболее разветвленный при двойной связи алкен. Вторичные спирты подвергаются дегидратациии при нагревании с 85%-ной
Фосфорной кислотой при 160-170 о С или с 60-70%-ной серной кислотой при 90-100 о С и направление дегидратации соответствует правилу Зайцева.
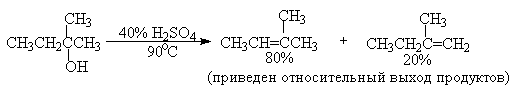
Дегидратацию третичных спиртов можно проводить уже в 20-50%-ной серной кислоте при 85-100 o С.
Третичные спирты дегидратируются так легко, что возможна избирательная дегидратация диола, содержащего третичную и первичную гидроксильные группы.
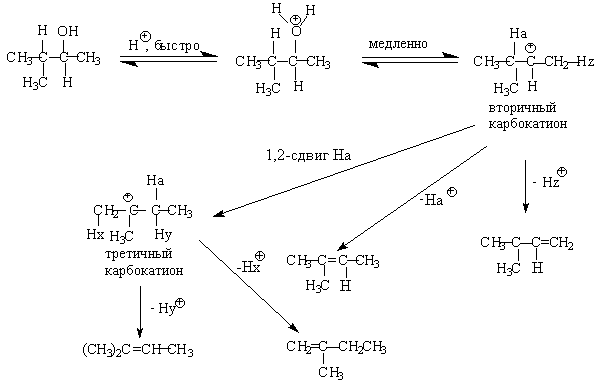
Для El-элиминирования, также как и для других процессов с образованием карбокатиона в качестве интермедиата, характерны перегруппировки, включающие анионотропную 1,2-миграцию гидрид-иона или алкильной группы. В качестве примера можно привести кислотно-катализируемую дегидратацию 3-метилбутанола-2 в 80%-ной серной кислоте.
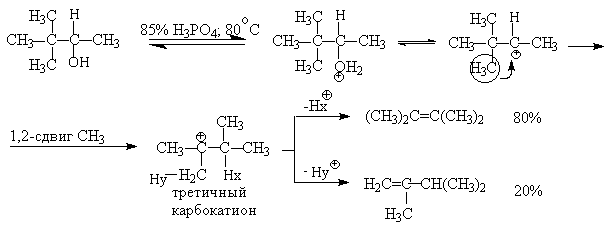
Примером скелетной изомеризации карбокатиона в Е1-элиминировании может служить дегидратация 3,3-диметилбутанола-2.
Для первичных спиртов, вероятно, реализуется иной, Е2 механизм дегидратации в концентрированной серной кислоте, они дегидратируются в гораздо более жестких условиях. Так, пропан ол-1 дает пропилен при нагревании с 96%-ной серной кислотой при 170-190 o С, этанол в этих же условиях дает этилен.
Первичные спирты при взаимодействии с серной кислотой легко образуют полуэфиры серной кислоты. Е2-Элиминированию в этом случае, по-видимому, подвергается полуэфир, а роль основания выполняет гидросульфат-ион или вода.
Возможен и другой механизм дегидратации первичных спиртов, в котором субстратом является катион алкоксония, а основанием гидросульфат-ион.
В более мягких условиях при нагревании простейших первичных спиртов с 96%-ной серной кислотой при 130-140 o С преимущественно получаются простые эфиры. При этом первичный спирт алкилируется либо под действием полуэфира серной кислоты, либо при взаимодействии с катионом алкоксония.
Этот способ неприемлем для получение несимметричных эфиров из двух спиртов, так как при этом образуется смесь трех возможных продуктов ROR, R’OR, R’OR’.
В промышленности для внутри- или межмолекулярной дегидратации вместо серной кислоты в качестве дегидратирующего средства используют безводную окись алюминия. Гетерогенная каталитическая дегидратация первичных, вторичных и третичных спиртов над окисью алюминия при 350-450 o С приводит к алкенам.
4. Получение простых эфиров по Вильямсону
Наиболее простым методом получения простых эфиров является реакция алкоголятов щелочных металлов с алкилгалогенидами или алкилсульфонатами (реакция Вильямсона, 1852 г.).
В отличие от межмолекулярной дегидратации спиртов реакция Вильямсона пригодна для синтеза как симметричных, так и несимметричных простых эфиров.
Получение простых эфиров по Вильямсону представляет собой обычную реакцию бимолекулярного нуклеофильного замещения у насыщенного атома углерода с помощью алкоксид- или феноксид-ионов. Если простой эфир содержит вторичную или третичную алкильные группы, ее следует вводить с помощью алкоголята, но не алкилгалогенида или алкилсульфоната, поскольку в противном случае преимущественно или исключительно будет происходить Е2-элиминирование.
Наилучшие результаты достигаются в том случае, когда в качестве алкилирующего агента используются первичные алкил-, аллил- и бензилгалогениды и сульфонаты.
Окисление первичных спиртов в альдегиды и вторичных спиртов в кетоны является одним из важнейших превращений функциональных групп и оценкой избирательного действия реагента, используемого в качестве окислителя.
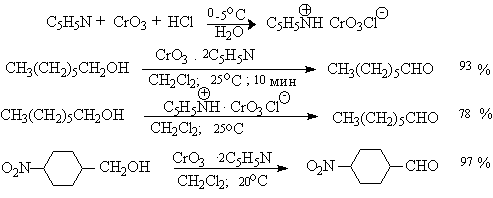
Ниже приведены некоторые наиболее типичные примеры окисления первичных спиртов до альгедигов комплексами оксида хрома VI.
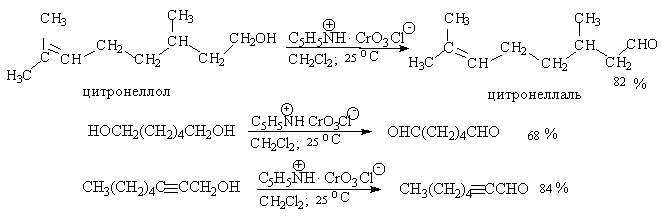
Оба окислителя обеспечивают очень высокие выходы альдегидов, однако хлорхромат пиридиния имеет важное преимущество, так как он не затрагивает двойную и тройную связи и может быть использован для получения ненасыщенных альдегидов.
Для получения a,b-ненасыщенных альдегидов окислением замещенных аллиловых спиртов универсальным окислителем является оксид марганца (IV) MnO2. Этот реагент окисляет в петролейном эфире или хлористом метилене ненасыщенные спирты с одной или несколькими двойными или тройными связями без изомеризации и перегруппировки, что с успехом используется в синтезе природных соединений.
Комплексы хромового ангидрида с пиридином окисляют и вторичные спирты до кетонов с почти количественными выходами.
Первичные спирты окисляются реактивом Джонса до карбоновых кислот.
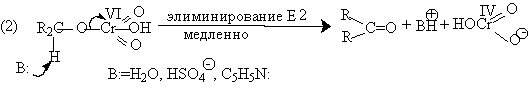
Механизм оксиления спиртов под действием хромового ангидрида подробно изучен. Эта реакция включает несколько стадий. Сначала из спирта и CrO3 образуется сложный эфир хромовой кислоты. Во второй, ключевой, стадии имеет место окислительно-восстановительное элиминирование, приводящее к образованию альдегида или кетона и частицы, содержащей Cr(IV). При окислении дейтерированного CH3CD(OH)CH3 и недейтерированного пропанола-2 наблюдается кинетический изотопный эффект КН/KD=7. Столь значительный первичный кинетический изотопный эффект показывает, что элиминирование является наиболее медленной стадией, определяющей скорость всего процесса.
Установлено, что частицы, содержащие хром (IV), также принимают участие в окислении спирта.
Окисление под действием соединений Cr (IV) можно полностью подавить с помощью солей, содержащих ионы Mn (II) или Ce (III), которые окисляются Cr (IV). Каталитические количества Ce (IV) также подавляют эту побочную реакцию, поскольку Ce (IV) катализируют диспропорционирование Cr(IV) на Cr(III) и Cr (VI).
Для третичных спиртов, не содержащих атомов водорода при карбонильном углероде, эфиры хромовой кислоты могут быть выделены.
Раствор хромового ангидрида в трет-бутиловом спирте также используется для окисления первичных и вторичных спиртов. Раствор хромового ангидрида в уксусной кислоте нередко употребляется в качестве окислителя вторичных спиртов до кетонов.
Поэтому для того, чтобы избежать дальнейшего окисления альдегида, окисление первичных спиртов следует проводить в апротонной среде при полном отсутствии влаги. Этому условию в полной мере удовлетворяют реагенты Коллинза и Кори, для которых в качестве растворителей используют тщательно обезвоженный хлористый метилен.
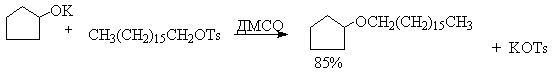
В последние тридцать лет разработано несколько эффективных способов окисления первичных и вторичных спиртов с помощью ДМСО или комплексов ДМСО с электрофильными агентами. Тозилаты первичных спиртов, также как и бензилтозилаты, окисляются в альдегиды при нагревании в ДМСО в течение 10-30 минут при 120-150 о С в присутствии гидрокарбоната натрия как слабого основания.
ДМСО в этой реакции выполняет роль нуклеофильного агента, который замещает тозилоксигруппу по обычному SN2 механизму с образованием алкоксисульфониевой соли. Катион алкоксисульфониевой соли далее подвергается окислительно-восстановительному элиминированию по механизму, аналогичному для окислительно-восстановительного элиминирования из сложных эфиров хромовой кислоты. Гидрокарбонат-ион является основанием в этой Е2 реакции элиминирования, приводящей к диметилсульфиду и альдегиду. В качестве примера приведем получение гептаналя и и-бромбензальдегида.
Слабый нуклеофильный агент ДМСО легко превращается в сильный электрофильный агент, который реагирует со спиртами уже ниже 0 o С в мягких условиях. Необходимую активацию ДМСО проводят с помощью серного ангидрида, трифторуксусного ангидрида, N-хлорсукцинимиджа или N,N-дициклогексилкарбодиимида C6H11N=C=NC6H11 (ДЦГК). Во всех случаях в качестве реакционноспособного интермедиата образуется активированная алкоксисульфониевая соль, которая далее подвергается внутримолекулярной окислительно-восстановительной фрагментации.
Для окисления первичных и вторичных спиртов до альдегидов и кетонов в мягких условиях эффективен комплекс ДМСО с SOs, образующийся при взаимодействии пиридинсульфотриоксида с ДМСО.
SO3 в качестве электрофильной частицы может быть заменен трифторуксусным ангидридом или ДЦГК (реактив Пфитцера-Моффата). Этот реагент в настоящее время употребляется наиболее часто.
Приведем для иллюстрации два примера окисления спиртов комплексами ДМСО.
Окисление спиртов по Оппенауэру в теоретическом отношении представляет собой пример окислительного процесса с переносом гидрид-иона от восстановителя к окислителю в одну стадию, в то время, как в выше описанных процессах окисление спиртов осуществляется в несколько стадий с последовательным переносом одного или нескольких электронов.
6. Защитные группы для гидроксильной группы
При осуществлении многостадийных синтезов сложных органических молекул часто необходимо защитить гидроксильную группу, чтобы провести требуемую реакцию по другой функциональной группе. Введение «защиты» включает три стадии: 1) образование инертного производного; 2) выполнение требуемого превращения с другой функциональной группой и 3) снятие защитной группы. Для гидроксильной группы хорошо зарекомендовавшим себя методом является образование ацеталя в результате кислотно-катализируемого присоединения спирта к 2,3-дигидропирану.
Подобно простым эфирам, тетрагидропиральные (ТГП) эфиры инертны по отношению к нуклеофильным агентам, сильным основаниям (RMgX, RLi, NaH, NaNHz, RONa и др.), а также окислителям и восстановителям. Однако ТГП-группа чувствительна к кислотному расщеплению и легко удаляется в растворе хлористого водорода в метаноле.
Ниже приведен типичный пример использования защитной ТГП-группы.
Другой защитной группой является триметилсилильная группа, которая вводится с помощью (СНз)зSiС1. Эта группа легко удаляется под действием фторид-иона.