Жидкость в матке на узи что это пожилом возрасте
Диагностика патологии эндометрия в постменопаузе: применение 2D и 3D технологий
Журнал «SonoAce Ultrasound»
Содержит актуальную клиническую информацию по ультрасонографии и ориентирован на врачей ультразвуковой диагностики, выходит с 1996 года.
Введение
Трехмерное УЗИ в последние годы чаще используется в работе как врачей ультразвуковой диагностики, так и врачей акушеров-гинекологов, несмотря на то, что остается ряд дискуссионных вопросов, роль которых в диагностике гинекологической патологии еще предстоит определить 1.
В большей мере освещены вопросы патологии эндометрия в постменопаузальном возрасте. Так, S. Kupesic и соавт. определили, что трехмерная энергетическая допплерография может использоваться для раннего выявления рака эндометрия, особенно у женщин в постменопаузальном возрасте без клинической симптоматики заболевания, а также для уточнения инвазии опухоли в миометрий [4].
При обследовании пациенток постменопаузального возраста с аденокарциномой, гиперплазией, атрофией эндометрия и субмукозной миомой матки, J.L. Alcazar и R. Galv n установили, что 3D энергетическая допплерография может быть полезна в диагностике рака эндометрия, так как у этих пациенток статистически значимо повышены индекс васкуляризации (ИВ) и васкуляризационно-потоковый индекс (ВПИ) эндометрия в сравнении с пациентками других групп [5].
В свою очередь R. Galv n и соавт. при изучении стадийности эндометриального рака у пациенток в постменопаузе определили, что ИВ в малигнизированном эндометрии коррелирует с некоторыми гистологическими характеристиками опухоли [6].
G. Opolskiene и соавт. определили, что у женщин с кровотечением в постменопаузальном возрасте ИВ и ВПИ не отличались как при доброкачественных, так и при злокачественных изменениях в эндометрии [7]. К противоположным выводам пришли A.K. Makled и соавт., которые в своих исследованиях доказали, что значение ИВ является достоверным диагностическим критерием рака эндометрия в постменопаузе [8].
Как видно из изложенного выше, в последние годы увеличивается интерес к проблемам постменопаузы, что связано в первую очередь с тенденцией населения развитых стран к старению. Поэтому так актуальны вопросы патологии эндометрия в постменопаузальном периоде [9].
Кроме того, заболеваемость раком эндометрия увеличилась во всех экономически развитых странах [10, 11].
В постменопаузальном возрасте у ряда пациенток происходит полная облитерация цервикального канала, и показанием для проведения раздельного диагностического выскабливания становится расширение полости матки за счет жидкости, выявленное при УЗИ в 2D режиме. Между тем у врачей ультразвуковой диагностики нет четких критериев, позволяющих исключить злокачественную трансформацию эндометрия у таких пациенток. Следовательно, поиск путей улучшения диагностики патологических состояний эндометрия у пациенток в постменопаузальном возрасте с использованием трехмерной эхографии с опцией энергетического допплера побудил нас к исследованиям в этой области.
Целью настоящего исследования стало проведение анализа совпадений результатов рутинного двухмерного трансвагинального УЗИ у пациенток постменопаузального возраста с окончательным патоморфологическим заключением исследования биоптата эндометрия, определение возможности использования трехмерной энергетической допплерографии у пациенток с облитерацией цервикального канала в постменопаузе.
Материал и методы
Для достижения поставленной цели нами ретроспективно оценено 50 историй болезни женщин постменопаузального возраста, госпитализированных в гинекологическое отделение для проведения раздельного диагностического выскабливания и гистероскопии в плановом порядке. Показанием для госпитализации явились данные рутинного трансвагинального УЗИ (ультразвуковое заключение: патология эндометрия). Данные ультразвуковых заключений, послужившие поводом для госпитализации в стационар, были оценены ретроспективно и сопоставлены с данными гистологических заключений после раздельного диагностического выскабливания.
Пациентке с атрезией цервикального канала и скоплением жидкости в полости матки проведено трансвагинальное сканирование с использованием объемного ректовагинального датчика 4-9 МГц на стационарном ультразвуковом сканере Accuvix-V10 компании Samsung Medison в режиме 3D реконструкции с опцией энергетического допплера по методике И.А. Озерской [12], с последующим автоматическим получением ИВ, индекса потока (кровотока) (ИП), ВПИ реконструированной матки в программе Virtual Organ Computeraided AnaLysis (VOCAL).
Статистическая обработка данных осуществлялась с применением прикладного программного пакета «Statistica 6.0», адаптированного для медико-биологических исследований. Производилось вычисление относительных частот признака (%) в группе.
Результаты и обсуждение
Анализ приведенных результатов побуждает к поиску дополнительных ультразвуковых методик, которые можно применить в постменопаузальном возрасте, особенно в ситуации с атрезией цервикального канала и последующим скоплением жидкости в полости матки. Именно это состояние занимает высокий удельный вес в постменопаузальном возрасте и, не представляя трудностей в диагностике при рутинном трансвагинальном УЗИ, ведет к проведению раздельного диагностического выскабливания.
Мы попытались применить у такой категории пациенток 3D энергетическую допплерографию и приводим клинический пример.
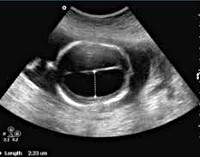
Пациентка К., 60 лет, поступила в гинекологическое отделение для проведения раздельного диагностического выскабливания под контролем гистероскопии с диагнозом: подозрение на рак тела матки. Данные трансвагинального УЗИ, проведенного амбулаторно: тело матки нормальных размеров, контур матки ровный, миометрий однородный, полость матки расширена до 6 мм, заполнена анэхогенным содержимым. Яичники обычных размеров и эхоструктуры, свободная жидкость в позадиматочном пространстве не визуализируется. Ультразвуковое заключение: серозометра.
Анамнестические данные: постменопауз 5 лет, из гинекологических заболеваний в анамнезе пациентка отмечает эктопию шейки матки, по поводу чего была произведена диатермоэлектрокоагуляция шейки матки. В анамнезе 2 родов, в срок, без осложнений и один медицинский аборт в срок 8-9 нед, без осложнений.
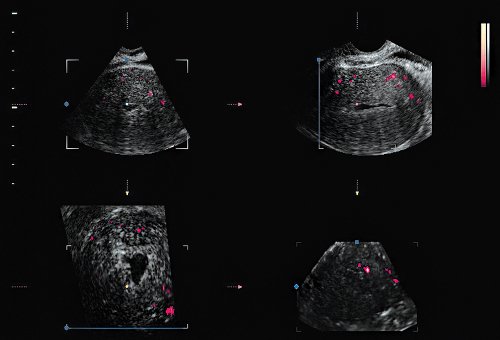
До проведения раздельного диагностического выскабливания, на стационарном ультразвуковом сканере Accuvix-V10 компании Samsung Medison после опорожнения мочевого пузыря мы провели трансвагинальное сканирование с использованием объемного ректовагинального датчика 4-9 МГц в режиме 3D реконструкции с опцией энергетического допплера и получили объемное изображение (рис. 1).
Рис. 1. Объемное изображение в режиме энергетического допплера.
Серозометра
Серозометра — накопление серозной жидкости в полости матки из-за наличия механических препятствий на пути ее оттока во влагалище или повышенной секреции. На начальных этапах клинически не проявляется и выявляется случайно во время гинекологического обследования. При накоплении больших объемов жидкости пациентку беспокоит тупая боль в надлобковой области, учащенное мочеиспускание, запоры и другие нарушения функции тазовых органов. Для диагностики используют бимануальное обследование, УЗИ, эндоскопические, томографические, цитологические и микробиологические методы. Лечение направлено на устранение заболевания, вызвавшего серозометру.
Общие сведения
Накопление серозной жидкости в матке является неспецифическим проявлением ряда заболеваний, сопровождающихся повышенной секрецией или нарушением оттока экссудата во влагалище. Серозометра чаще возникает во время постменопаузы на фоне инволютивных процессов в женских половых органах и в ходе гинекологического УЗИ диагностируется у 40% пациенток этой группы. При этом наиболее часто подобное нарушение выявляют у женщин с длительностью постменопаузы от 15 до 25 лет. Появление внутриматочной жидкости у пациенток репродуктивного возраста, как правило, имеет другие причины, чем серозометра в постменопаузе, и требует быстрой тщательной дифференциальной диагностики.
Причины серозометры
Скопление серозной жидкости в полости матки может быть обусловлено механическим нарушением проходимости путей оттока во влагалище или повышенной секрецией на фоне неадекватной резорбции и выведения. Основными причинами органической несостоятельности служат:
К возникновению серозометры также приводит избыточная секреция экссудата эндометрием или его поступление из фаллопиевых труб. Гиперпродукция серозной жидкости наблюдается при таких патологических состояниях, как:
Важную роль в формировании серозометры играют факторы, которые снижают местный или общий иммунитет, вызывают гормональные сбои и преждевременное старение репродуктивной системы. Ключевыми из них являются:
Дополнительными факторами риска возникновения серозометры служат малоподвижный образ жизни, нерациональное питание с употреблением жирных и других продуктов, усугубляющих обменные нарушения.
Патогенез
Симптомы серозометры
На начальных этапах присутствие серозной жидкости в полости матки не проявляется клинически и в подавляющем большинстве случаев становится случайной находкой при плановом гинекологическом УЗИ. Если серозометра сочетается с увеличением матки, пациентку беспокоят тупые или ноющие боли в надлобковой области, иногда возникает учащенное мочеиспускание, ощущение давления на мочевой пузырь или прямую кишку, появляются запоры или, наоборот, более частые позывы к дефекации. Боли могут усиливаться во время полового акта или при значительных физических нагрузках.
При сохранении проходимости цервикального канала женщина обычно отмечает увеличение количества влагалищных выделений. Зачастую они имеют водянистую консистенцию, выглядят прозрачными или светло-серыми. Когда к серозометре присоединяются гнойно-воспалительные процессы, характер выделений изменяется: они становятся более густыми, желто-зелеными с неприятным запахом. При этом усиливаются боли, может повышаться температура, беспокоить общее недомогание, слабость, разбитость, усталость, головокружение.
Осложнения
Наиболее грозным осложнением серозометры является присоединение воспалительного процесса с нагноением, выраженными местными и общими проявлениями интоксикации, инфекционным поражением других органов женской половой сферы. Давление увеличенной матки приводит к нарушению функций органов малого таза, а также нарушению оттока крови из нижних конечностей с формированием отеков. Кроме того, поскольку серозометра — не заболевание, а состояние, спровоцированное другой патологией, при несвоевременной диагностике основных причин накопления жидкости в матке могут быть пропущены опухоли и воспалительные заболевания.
Диагностика
Основная задача диагностики при обнаружении серозометры — выявление причин, вызвавших накопление жидкости. С этой целью пациентке рекомендовано комплексное гинекологическое обследование, в которое входят:
В репродуктивном возрасте особенно важна дифференциальная диагностика серозометры от других состояний, при которых в полости матки выявляется жидкость, — лохиометры, гематометры, пиометры. В сомнительных случаях к постановке диагноза привлекают онкогинекологов и хирургов.
Лечение серозометры
Схема лечения зависит от объема серозной жидкости, выявленной в полости матки, динамики ее накопления и причин, приведших к возникновению патологического состояния. При небольшом объеме жидкости (до 5 мл) и отсутствии признаков инфекционных процессов рекомендовано динамическое наблюдение с проведением УЗ-контроля и назначение препаратов, которые стимулируют маточное кровообращение, улучшают тонус сосудов и регенерацию эпителия. В таких случаях эффективно дополнительное назначение физиотерапевтических процедур.
Если объем серозной жидкости превышает 5 мл, ее количество увеличивается в динамике, отсутствуют механические препятствия на пути оттока во влагалище, выявлены воспалительные изменения, рекомендована комплексная терапия серозометры. Как правило, пациентке назначают:
При наличии органической патологии, препятствующей оттоку серозной жидкости, показаны специальные методы лечения основной патологии — бужирование цервикального канала, удаление полипа, миомэктомия, терапевтическое и хирургическое лечение объемных новообразований и т. п.
Прогноз и профилактика
Патологии эндометрия, полости матки и цервикального канала
1. Паталогии эндометрия
Полость матки выстлана эндометрием – пронизанной кровеносными сосудами слизистой оболочкой (мукозный слой), ткань которой постоянно меняется и обновляется в зависимости от фазы менструального цикла.
Природное предназначение эндометрия – обеспечить надежное прикрепление и кровоснабжение (питание) оплодотворенной яйцеклетки. В эндометрии, как и в любом другом структурно сложном образовании живого организма, обнаруживаются многочисленные заболевания, функциональные расстройства и аномалии развития. К наиболее распространенным относятся следующие.
2. Гиперплазия и полипы
Гиперплазия
Увеличение, разрастание эндометрия, зачастую неравномерное, очаговое, полипообразное, железисто-кистовое и т.д. Согласно статистическим данным, гиперплазия эндометрия наблюдается примерно у 40% всех гинекологических пациенток, причем частота встречаемости не зависит от возраста. Основными этиопатогенетическими факторами считаются эндокринные нарушения, инфекционные заболевания, генетические сбои; однако, пусковые механизмы остаются неясными. Как правило, больные жалуются на патологически обильные менструации, выделения или маточные кровотечения, не связанные с циклом. Основными диагностическими методами являются УЗИ (трансвагинальный вариант наиболее информативен), гистероскопия (при необходимости отбирается материал для гистологического исследования). Терапия гиперплазии эндометрия включает гормональные препараты и/или малоинвазивное вмешательство: хирургическую гистероскопию, аблацию, гистерорезектоскопию.
Полипы
Очаговая доброкачественная пролиферация (разрастание) клеток эндометрия матки и/или цервикального канала (участка между маткой и влагалищем). Обнаруживаются более чем у половины пациенток после менопаузы; проявляются, в основном, кровянистыми выделениями. К главным причинам образования полипов относят неоднократные и неполные выскабливания. Различают несколько видов полипов (аденоматозные, железистые и пр.). Диагностика и лечение (удаление) полипов осуществляется, как правило, гистероскопическим методом.
3. Перегородка полости матки
4. Синехии и серозометра
Синехии
Внутриматочные синехии (спайки, сращения – синдром Ашермана) могут быть обусловлены рядом причин: травмы (в т.ч. хирургические), инфекции, нарушения нейровисцеральной регуляции. По охвату внутриматочного пространства выделяют три степени синехий. Основным клиническим симптомом является неспособность забеременеть либо выносить беременность. Диагностируется аппаратными методами. Единственным лечением является хирургическая коррекция (в настоящее время подавляющее большинство вмешательств производится малоинвазивными методами).
Серозометра
Скопление серозной жидкости (т.е. секрета слизистой оболочки) в полости матки. Серозометра не является самостоятельным диагнозом – это всегда симптом иного заболевания или состояния (в частности, послеродовое скопление носит название лохиометра, наличие жидкой крови – гематометра). Часто встречается в раннем климактерическом периоде на фоне гормональной перестройки. Провоцирующими факторами считают также вредные привычки и гиподинамический образ жизни. Проявляется ноющей болью, при большом объеме жидкости – видимым увеличением живота, водянистыми выделениями, при инфицировании – симптоматикой острого воспаления. Терапией выбора обычно является расширение цервикального канала с отводом жидкости; обязательно проводится гистологическое исследование, при необходимости – бактериальный посев и лечение инфекции.
Заболевания 
Жалобы и симптомы 
Диагностика 
Наши цены 
Мы стараемся оперативно обновлять данные по ценам, но, во избежание недоразумений, просьба уточнять цены в клинике.
Данный прайс-лист не является офертой. Медицинские услуги предоставляются на основании договора.
Оптимизация тактики ведения пациенток пожилого и старческого возраста с внутриматочными патологическими процессами
Клиническая больница Управления делами Президента РФ, г. Москва
Московский государственный медико-стоматологический университет имени А.И. Евдокимова
Введение. Согласно демографическим прогнозам к 2030 г. каждый пятый человек в мире будет старше 65 лет. Как и многие государства Европы, Россия относится к странам с высоким уровнем «демографической старости». В связи с этим большое значение приобретает изучение особенностей возникновения, течения, лечения и профилактики заболеваний у лиц пожилого возраста.
Уровень заболеваемости населения в пожилом возрасте (60-74 года) в 2 раза выше, а в старческом (старше 75 лет) – почти в 6 раз выше, чем у людей молодого возраста. В результате возникает высокая потребность в оказании амбулаторной и стационарной помощи лицам пожилого и старческого возраста [7]. В настоящее время считается необоснованным отказ пациентам старших возрастных групп в адекватной медицинской помощи, щадящая консервативная тактика, например, не отвечающая современным принципам онкопрофилактики [9,10].
Очевидна актуальность изучения особенностей патологических процессов постменопаузального периода жизни женщины. Постменопауза представляет собой закономерное физиологическое состояние, сопровождающееся гормональными сдвигами, которые, в свою очередь, часто являются предвестниками различных проблем со здоровьем и могут влиять не только на качество жизни, но и на ее продолжительность [12]. В структуре гинекологической заболеваемости женщин пожилого и старческого возраста наиболее часто встречается патология эндометрия [11,13].
По данным разных авторов частота встречаемости различной внутриматочной патологии в постменопаузе следующая: полипы эндометрия –39,2-69,3%; атрофия эндометрия –16,7-47,4%; гиперплазия эндометрия без атипии –3,3-4,9%; гиперплазия эндометрия с атипией –0,5-5,2%; аденокарцинома –0,5-14%; субмукозная миома матки – 3,6-8,5%; синехии 4,8-7,9%. Процент выявляемой патологии зависит от методики исследования, длительности постменопаузы и наличия маточного кровотечения (наиболее частый симптом в постменопаузе, заставляющий пациентку обратиться к врачу) [2, 6, 9, 14, 17, 21, 22].
Ведущим методом диагностики патологии органов репродуктивной системы, в том числе эндометрия, признано ультрасонографическое исследование [1,4,5]. Многие зарубежные и отечественные авторы в своих работах указывают на высокую эффективность, простоту выполнения, неинвазивность, низкую стоимость данного метода исследования, позволяющего в ряде случаев избежать использование агрессивных инвазивных процедур. Он считается скрининговым методом диагностики внутриматочной патологии [2, 9, 15, 18]. Одним из значимых критериев является симметричность и толщина эндометрия (показатель М-эха). За норму, в зависимости от длительности постменопаузы, принято считать показатель М-эха, равный 3-5 мм [15,17]. По мнению большинства авторов, толщина эндометрия в постменопаузе, превышающая 5 мм, рассматривается как ведущий эхографический признак патологии эндометрия [18,20].
Для дальнейшей верификации диагноза необходимо получить материал для патоморфологического исследования [3]. Это достигается прицельной биопсией или раздельным выскабливанием цервикального канала и полости матки с последующим гистологическим исследованием соскоба. Но при выскабливании слизистой оболочки матки «вслепую» часто пропускаются или удаляются не полностью полипы эндометрия, узлы миомы, участки гиперплазированного эндометрия и т.д. Поэтому на сегодняшний день «золотым стандартом» в диагностике и лечении внутриматочной патологии гинекологами всего мира признается гистероскопия с последующим патогистологическим исследованием биопсии эндометрия [2,6,9,10,14,19]. Однако выполнение данного вида вмешательства у пациенток пожилого и старческого возраста имеет свои особенности, возможно развитие как анестезиологических, так и хирургических осложнений.
У данной группы больных отмечается изменение основного обмена, снижение компенсаторных возможностей сердечно-сосудистой и дыхательной систем, а также функции печени и почек. Изменяется фармакокинетика препаратов: снижается метаболизм, повышается чувствительность к опиоидам, гипнотикам, ингаляционным анестетикам и мышечным релаксантам, замедляется выведение препаратов из организма. Таким образом, необходимо крайне осторожно титровать внутривенные гипнотики при «малых» гинекологических операциях до получения необходимого эффекта [8].
Процессы старения в организме женщины характеризуются атрофическими изменениями органов генитального тракта. Матка уменьшается в размерах, истончаются ее мышечный слой и эндометрий, ткани теряют эластичность. Наиболее частой проблемой, с которой сталкиваются гинекологи при лечении возрастных пациенток, является частичная или полная атрезия цервикального канала. Наличие всех этих факторов влечет за собой увеличение риска хирургических осложнений, таких как перфорация матки, «ложный ход», кровотечения [16,19].
Несмотря на актуальность проблемы, имеется лишь ограниченное число публикаций, посвященных правилам проведения анестезиологического пособия и хирургических методик «малых» гинекологических вмешательств у пациенток пожилого и старческого возраста.
Цель исследования. Анализ особенностей клинических проявлений внутриматочных патологических процессов в пожилом и старческом возрасте и определение оптимальной тактики ведения пациенток с данным видом патологии.
Материал исследования включал 288 женщин в периоде стойкой постменопаузы, поступивших в гинекологическое отделение ФГБУ «Клиническая больница» Управления делами Президента РФ с подозрением на внутриматочную патологию.
Все пациентки, поступившие в гинекологическое отделение с подозрением на внутриматочную патологию в плановом порядке, были полностью обследованы в прикрепленных поликлиниках. На амбулаторном этапе они проходили общеклиническое и лабораторное исследование, при экстренной госпитализации пациентки полностью обследовались в стационарных условиях. Учитывая наличие сопутствующей экстрагенитальной патологии, пациенткам проводились консультации профильных специалистов.
Цервикальный канал выскабливали кюреткой №1, затем выскабливали полость матки кюретками № 2,4,6. Соскобы помещали в отдельные пластиковые контейнеры для последующего гистологического исследования. Для гистерорезектоскопии использовали гистерорезектоскоп KARL STORZ, Germany, 26050 SL.
Средами для расширение полости матки с целью адекватной интраоперационной визуализации являлись 0,9%-й раствор натрия хлорида при гистероскопии и 5%-й раствор глюкозы при гистерорезектоскопии.
Возраст наступления менопаузы варьировал от 38 до 56 лет (в среднем – 44,9±6,8 лет). При изучении социального статуса было установлено, что около половины обследованного контингента больных в постменопаузе являются служащими (145 пациенток, 50,35%), остальные (143 пациентки, 49,66%) – неработающими пенсионерами. Таким образом, очевидна важность обследования и лечения пациенток с внутриматочной патологией в постменопаузальном периоде как с медицинских, так и с социально-экономических позиций. Изучение анамнестических данных основывалось на анализе особенностей менструальной и репродуктивной функций (сроки наступления менархе и постменопаузы, начало половой жизни, число беременностей и их исход) перенесенных и сопутствующих гинекологических и экстрагенитальных заболеваний в различные периоды жизни.
При анализе репродуктивной функции обследованных больных были получены следующие данные: беременность не наступала у 28 пациенток, живущих половой жизнью, остальные (260 пациенток) имели однократные роды –120 женщин, двое родов – 116, трое – 11, четверо – 2 пациентки. Наиболее часто в анамнезе встречались миома матки (21,53%), патология эндометрия (16,32%), псевдоэрозия шейки матки (16,67%) с последующей диатермокоагуляцией ввиду неэффективности консервативной терапии, а также воспалительные заболевания гениталий (16,67%). Реже диагностировались в прошлом кисты яичников (2,43%), полип цервикального канала (1,05%), неполное выпадение матки (2,78%) и эктопическая беременность (4,17%). У многих пациенток отмечалось сочетание различных гинекологических заболеваний.
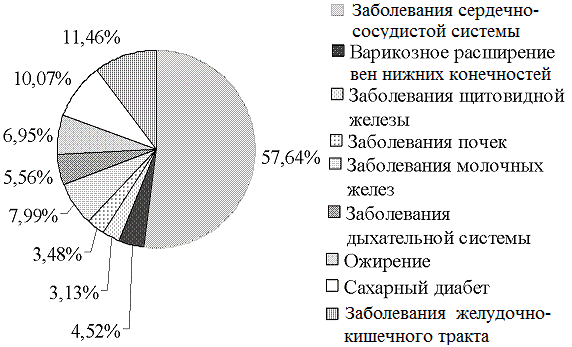
При анализе сопутствующих заболеваний было отмечено, что наиболее часто встречается патология сердечно-сосудистой системы – у 166 пациенток (57,64%), представленная ишемической болезнью сердца (ИБС), гипертонической болезнью в сочетании с другими заболеваниями или изолированно.
Варикозное расширение вен нижних конечной, в том числе с оперативным лечением, встретилось в 4,52% случаев, патология щитовидной железы – в 3,13%, мочекаменная болезнь – в 3,48%, патология молочных желез, в том числе рак молочной железы – в 7,99%. Патология органов дыхания была представлена бронхиальной астмой (3,13%) и хронической обструктивной болезнью легких (ХОБЛ) в стадии ремиссии (2,43%). У многих пациенток имелись эндокринные нарушения: ожирение 2-4 степени у 6,95%, сахарный диабет 2 типа –у 10,07% больных. Патология желудочно-кишечного тракта отмечена у 11,46% обследованных пациенток (рис. 1).
Рис. 1. Частота экстрагенитальной патологии у пациенток пожилого и старческого возраста
Не подлежит сомнению тот факт, что пожилому и старческому возрасту свойственна компелляция хронических заболеваний. У большинства больных отмечалось сочетание различной экстрагенитальной патологии. У многих больных в анамнезе были оперативные вмешательства по поводу различных заболеваний.
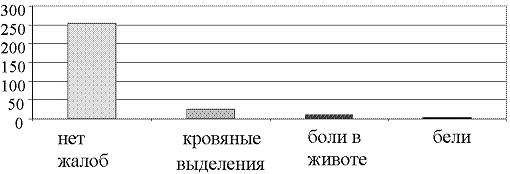
Рис. 2. Структура жалоб у госпитализированных женщин пожилого и старческого возраста с подозрением на внутриматочную патологию
Следует отметить, что у 237 пациенток каких-либо особенностей при гинекологическом осмотре не отмечено. У 38 больных выявлена атрезия наружного зева на фоне длительной постменопаузы, у 13 –при осмотре шейки матки в зеркалах обнаружен полип цервикального канала, в 18 случаях отмечено увеличение матки до 8-9 недель беременности в связи с наличием миомы матки, у 22 больных выявлено опущение стенок влагалища.
Всем пациенткам (n=288), поступившим в гинекологическое отделение с подозрением на внутриматочную патологию в пожилом и старческом возрасте, выполнено раздельное диагностическое выскабливание матки под контролем гистероскопии с последующим патоморфологическим исследованием полученного материала.
У 38 пациенток при гинекологическом осмотре отмечалась атрезия наружного зева, еще у 23 – атрезия внутреннего зева, выявленная при зондировании матки во время оперативного вмешательства. Таким образом, затруднения при расширении цервикального канала были отмечены у 61 пациентки (21,2%). С целью прохождения цервикального канала и определения длины полости матки выполняли форсированное зондирование по предполагаемому ходу цервикального канала, исходя из результатов гинекологического осмотра и ультразвукового сканирования. Также применяли водную диссекцию при цервикоскопии. В 17 случаях (5,9%) при невозможности прохождения цервикального канала зондом расширение проводили эндоскопическими щипцами или ножницами под гистероскопическим контролем. У одной пациентки инструментально не удалось пройти цервикальный канал. У двух пациенток сделан «ложный ход» (диагностика этого осложнения основана на данных гистероскопии и УЗИ малого таза). В 3-х описанных случаях вмешательство прекращено ввиду высокого риска перфорации матки. Пациентки выписаны из стационара под наблюдение гинеколога поликлиники с динамическим ультразвуковым скринингом. При отрицательной динамике планировалась повторная госпитализация в стационар.
285 пациенткам выполнено раздельное диагностическое выскабливание с предварительной диагностической гистероскопией. Гистероскопическая картина полости матки характеризовалась наличием полипов различной величины и локализации, неоднородным локальным утолщением эндометрия, наличием субмукозных или интерстициально-субмукозных узлов миомы, синехий в полости матки, признаков атрофии эндометрия и хронического эндометрита. Затем, при необходимости, была выполнена оперативная гистероскопия с использованием эндоскопических щипцов и ножниц (38) – в том числе для удаления небольших полипов из трубных углов, гистерорезектоскопия (7) –удаление миоматозных узлов, а также аблация эндометрия (3). Заметим, что дополнительную деструкцию эндометрия проводили пациенткам, у которых в анамнезе были указания на внутриматочные вмешательства в период постменопаузы.
При патогистологическом исследовании патологические изменения эндометрия были обнаружены у 200 из 283 пациенток (70,7%). Их структура представлена в табл. 1.
Таблица 1. Структура внутриматочной патологии у женщин пожилого и старческого возраста
У 69 пациенток из 285 (24,2%) гистологически была выявлена лишь атрофия эндометрия, а у 16 (5,6%) – субмукозные миомы матки.
Таким образом, наиболее частая патология эндометрия у пациенток пожилого и старческого возраста – железисто-фиброзные полипы (92%). Обращает на себя внимание высокий процент атрофических процессов эндометрия, что обусловлено постменопаузальными изменениями, а также высокая частота злокачественных новообразований эндометрия в пожилом и старческом возрасте. Представляет интерес и отсутствие гиперплазии эндометрия в изученной группе наблюдений.
Интраоперационно, а также в ранний и поздний послеоперационный периоды маточных кровотечений не отмечалось. Перфорации матки не было ни у одной пациентки из наблюдаемой группы.
32 пациенткам (11,1%) отложено оперативное лечение ввиду повышенных цифр артериального давления, выявленных при осмотре анестезиологом. Эта группа пациенток консультирована кардиологом, проведена коррекция гипотензивной терапии, к лечению добавлены седативные препараты. Через 1-2 суток у 28 пациенток цифры артериального давления не превышали 140/90 мм рт. ст., им было выполнено оперативное лечение под внутривенным наркозом.
Четверым пациенткам потребовался перевод в кардиологическое отделение для детального дообследования и подбора гипотензивных препаратов, после чего больные возвращались снова в гинекологическое отделение на оперативное лечение без выписки из стационара.
Особое внимание при ведении пациенток пожилого и старческого возраста с различной внутриматочной патологией уделялось анестезиологическому пособию при «малых» гинекологических операциях.
Для внутривенной анестезии использовали комбинацию препаратов пропофол + кетамин в сочетании 4:1 (Пропофол 200 мг + Кетамин 50 мг).
Индукция в/в анестезии методом титрования по 3 мл смеси до исчезновения ресничных рефлексов при сохранении спонтанного дыхания. На фоне ингаляции увлажненного кислорода через носовой катетер, сатурация кислорода не опускалась ниже 90%.
Во время проведения анестезии регургитация выявлена в 43 случаях (18,9%), аспирации не отмечалось ни у одной пациентки. Данное осложнение связано как со скоплением желудочного сока при длительном ожидании операции, так и несоблюдением режима голода пациентками.
Более половины наблюдаемых пациенток (57,6%) страдали гипертонической болезнью, что объясняет высокие цифры артериального давления перед анестезией, обусловленные волнением (32 пациенткам отложено оперативное лечение ввиду необходимости медикаментозной коррекции), а также отмечались низкие цифры АД после индукции анестезии.
Интраоперационное снижение артериального давления у лиц, страдающих гипертонической болезнью, связано с сочетанным применением препаратов для внутривенного наркоза и постоянного приема гипотензивных препаратов.
В течение раннего послеоперационного периода следует отметить замедленный выход из анестезии по сравнению с пациентками более ранних возрастов, а также в 5% случаев наличие кратковременной спутанности сознания, как индивидуальной реакции на применение кетамина.
В позднем послеоперационном периоде осложнений, связанных с наркозом, не наблюдали.
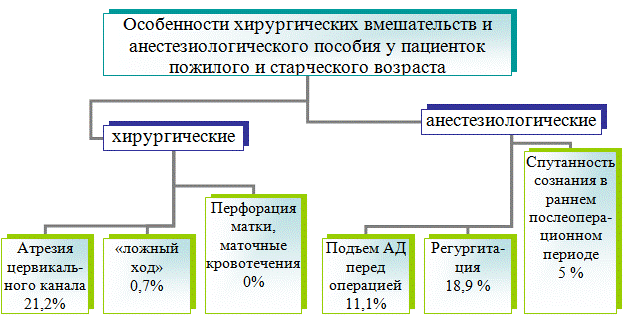
Особенности хирургических вмешательств и анестезиологического пособия у пациенток пожилого и старческого возраста по результатам исследования представлены на рис. 3.
Все пациентки в послеоперационном периоде получали антибактериальную терапию с целью профилактики воспалительных осложнений: ципрофлоксацин 500 мг 2 раза в день, метронидазол 500 мг 3 раза в день. Курс лечения составлял 5-7 дней, зачастую пациентки начинали прием препаратов в гинекологическом отделении и продолжали в амбулаторных условиях после выписки из стационара. Также больным проводили физиотерапетические процедуры в противоспалительном и сокращающем режимах (амплипульс-терапия, магнитотерапия, электрофорез с йодидом калия и антибиотиками). Тепловые факторы лечения не использовали до получения результатов гистологического исследования ввиду онконастороженности.
Результаты патоморфологического исследования материала, полученного при выскабливании цервикального канала и полости матки, направляли в поликлинику с целью коррекции дальнейшей тактики ведения пациенток.
Так как все пациентки, поступившие в плановом порядке в гинекологическое отделение из поликлиник для раздельного диагностического выскабливания матки и гистероскопии, были полностью обследованы амбулаторно, предоперационный период был непродолжительным: сроки оперативного лечения составили от 1 до 5 суток, в среднем 1,64±0,67 суток. Средний койко-день пребывания пациенток в стационаре составил 3,45±1,62. Данная система преемственности амбулаторного и стационарного звена позволяет значительно снизить медико-экономические затраты и повысить эффективность лечения пациенток с внутриматочной патологией.
Рис. 3. Особенности хирургических вмешательств и анестезиологического пособия у пациенток пожилого и старческого возраста
Выводы. Особенностью внутриматочных патологических процессов у больных пожилого и старческого возраста является их преимущественно бессимптомное течение, и диагноз может быть поставлен на основании ультразвукового скрининга.
Анатомическими особенностями матки у больных пожилого и старческого возраста, создающими сложности при операции, являются ее малые размеры, атрофические изменения тканей и частичная или полная атрезия цервикального канала.
Наиболее частой патологией эндометрия у женщин пожилого и старческого возраста являются железисто-фиброзные полипы эндометрия, повышена частота эндометриальных аденокарцином.
Учитывая возрастные изменения органов малого таза, наличие сопутствующей экстрагенитальной патологии, часто выраженную эмоциональную лабильность, высокий риск осложнений, целесообразно
1. Тщательно корректировать сопутствующую патологию на догоспитальном этапе.
2. Для исключения аспирации желудочного содержимого более ответственно отслеживать соблюдение пищевого режима.
3. Проводить операцию с применением седативной премедикации для исключения повышения артериального давления.
4. В связи с высоким риском перфорации матки операция должна выполняться только высококвалифицированным хирургом.
5. Для снижения риска травматизации шейки матки использовать гистероскопические щипцы и ножницы для расширения цервикального канала при полных и частичных атрезиях последнего.
6. Крайне важная роль для поддержания здоровья женщин должна быть отведена преемственной работе системы поликлиника-стационар, а также диспансерному обследованию наблюдаемого контингента.
Список использованных источников:
1. Ашрафян Л.А., Киселев В.И. Опухоли репродуктивных органов (этиология и патогенез). – М.: Компания «Димитрейд График Групп», 2008. –216 с.
2. Бреусенко В.Г., Голова Ю.А., Каппушева Л.М., Шилина Е.А., Климова И.В. Внутриматочная патология в постменопаузе: диагностика и лечение// Акушерство и гинекология. – 2003. – № 2. – С. 36-40.
3. Горных О.А., Самойленко В.В., Биштави А.Х., Каниболоцкий А.А., Манухин И.Б., Табакман Ю.Ю. Гиперплазия и предрак эндометрия// Опухоли женской репродуктивной системы. –2011. –№4. –С. 59-63.
4. Девятовская А.Г. Применение трехмерной эхографии в мониторинге лечения гиперпластических процессов эндометрия: Дис. … канд. мед. наук.- М., 2009, 117 с.
5. Демидов В.Н., Гус А.И. Патология полости матки и эндометрия. ВМК. Эхография органов малого таза у женщин. Практическое пособие. – М., 2001. – 138 с.
7. Журавлева Т.П. Основы гериатрии: учебное пособие. – М.: ФОРУМ: ИНФРА-М, 2007. – 288 с.
9. Мартиросян К.А. Пролиферативные процессы эндометрия у пациенток старше 60 лет. Современные технологии в диагностике и хирургическом лечении: Автореф. дис. … канд. мед. наук. – М., 2012. – 26 с.
11. Стрижова Н.В., Сухих Г.Т., Соболева Г.М., Холодова Ж.Л., Рейснер Е.А. Сравнение сывороточной активности матриксной металлопротеиназы-2 у больных с железистой и железисто-кистозной гиперплазиями эндометрия в перименопаузе// Проблемы репродукции. – Спец. выпуск. –2008. –С. 312-313.
12. Сухих Г.Т., Адамян Л.В. Репродуктивное здоровье семьи// Проблемы репродукции. –2008. – Спец. выпуск. –С. 5-10.
13. Торчинов А.М., Умаханова М.М., Фидарова Т.В., Габараева М.Р. Пролиферативная активность железистого эпителия полипов эндометрия в период пери- и постменопаузы// Матер. IX Всеросс. науч. форума «Мать и дитя». – 2007. – С. 540-541.
14. Хитрых О.В. Отдаленные результаты и оптимизация тактики лечения полипов эндометрия в постменопаузе: Автореф. дис. … канд. мед. наук. – М., 2009. – 18 с.
15. Щеглова Е.А. Ультразвуковая диагностика гиперпластических процессов эндометрия у женщин различных возрастных периодов: Автореф. дис. … канд. мед. наук. – М., 2009. – 26 с.
16. Brand A.H. The woman with postmenopausal bleeding// Aust. Fam. Physician. 2007; 36 (3): 116-20.
17. Dreisler E., Sorensen S.S., Ibsen PH. Prevalence of endometrial polyps and abnormal uterine bleeding in a Danish population aged 20-74 years// ultrasound Obstet Gynecol. 2009; 33 (1): 102-108.
18. Goldstein S.R. Significance of incidentally thick endometrial echo on transvaginal ultrasound in postmenopausal women// Menopause. 2011; 18 (4): 434-6.
19. Hefler L.L. The intraoperative complication rate of nonobstetrics dilation and curettage// Obstetrics & Gynecology 2009; 113 (6): 1268-71.
20. Kasraeian M., Asadi N., Ghaffarpasand F., Karimi A.A. Value of transvaginal ultrasonography in endometrial evaluation of non-bleeding postmenopausal women// Climacteric. 2011; 14 (1): 126-31.
21. Mossa B., Torcia F., Avenoso F. Occurrence of malignancy in endometrial polyps during postmenopause// Eur J Gynaecol Oncol. 2010; 31 (2): 165-8.
22. Raouf S.A., Gupta P., Papaioannou S., Pradhan P. Endometrial thickness for invasive investigations in women with postmenopausal bleeding// Climacteric. 2011; 14 (1): 117-20.
23. Svirsky R., Smorgick N., Rozovski U. Can we rely on blind endometrial biopsy for detection of focal intrauterine pathology?// Am J Obstet Gynecol. 2008; 199 (2): 115. e 1-3.
24. Wethington S.L., Herzog T.J., Burke W.M. Risk and predictors of malignancy in women with endometrial polyps// Ann Surg Oncol. 2011; 18 (13): 3819-23.
25. Wolfman W., Leyland N., Heywood M. Asymptomatic endometrial thickening// J. Obstet Gynaecol Can. 2010; 32 (10): 990-9.